

Eine Reise durch die Physiologie - Wie der Körper des Menschen funktioniert

Respirationssystem
und Atemgastransport

 Atemmechanik
Atemmechanik
© H. Hinghofer-Szalkay
 Atelektase: ἀτελής = unvollständig, ἔκτασις = Ausdehnung
Atelektase: ἀτελής = unvollständig, ἔκτασις = Ausdehnung
Boyle-Mariotte-Gesetz: Robert Boyle, Edme Mariotte
Donders'scher Druck: Franciscus Donders
Phrenikusnerv: φρήν = Seele, Geist, Gemüt (im Plural: Zwerchfell)
Pleura: πλευρά = Flanke, Seite; seit dem Mittelalter: Brustfell
Pneumothorax: πνευμα = Luft, Geist, Atem, θώραξ = Brustkorb
Surfactant: surface active agent
Valsalva-Versuch: Antonio Valsalva
Die Lunge zieht sich wie ein angespanntes Gummiband zusammen (Retraktion), wenn sie dazu Gelegenheit hat. Das hat zwei Gründe: Ein Netzwerk elastischer Fasern,
die umso stärker gedehnt sind, je tiefer die Einatmung ist;
zweitens die Oberflächenspannung
an der Grenzfläche zwischen Luft und Flüssigkeit an der
Innenwand der Alveolen. Auch diese Kraft wirkt in Richtung
Verkleinerung der Lunge; wäre diese nicht im Thorax "aufgespannt",
würde sie kollabieren.
Zwei entgegengesetzte Kräfte halten die Lunge in ihrer Position: Pulmonale elastische
Retraktion (nach innen) und eine - bei Atemruhe gleich starke - Haltekraft des Thorax
(nach außen). Im ausgeatmeten Ruhezustand ergibt sich so ein passives
Kräftgleichgewicht (ausgeatmete Ruhelage).
Bei der
Einatmung kommt eine aktive Komponente dazu (Kontraktion von Zwerchfell und Zwischenrippenmuskeln), die
Position des Systems verschiebt sich - die Lunge wird entfaltet und stärker
gedehnt. - Ausatmung erfolgt, wenn die Muskelkomponente wieder wegfällt (Relaxation).
Nachdem die Lunge nach innen und der Thorax nach außen ziehen, ergibt
sich zwischen ihnen eine Zugkraft im Pleuraspalt (mittels Ösophagussonde bestimmbar): Der intrathorakale (Donders'sche) Unterdruck.
Die Mechanik des Systems hat eine Lungen- und eine
Thoraxkomponente. Letztere ist im Zustand der Atemruhe
passiv-elastisch, bei Einatmung kommt die Kraft der
Inspirationsmuskeln dazu. Aus der Lungencompliance und der Thoraxcompliance ergibt sich die Dehnbarkeit des gesamten Respirationsapparates. Darüber geben verschiedene Methoden Aufschluss: Die Spirometrie misst (atembare) Volumina, die Pneumotachographie Strömungsgeschwindigkeiten, die Ganzkörperplethysmographie (indirekt) den Alveolardruck.
Forcierte Aus- oder Einatmung hat Auswirkungen auf Kreislaufgrößen (Valsalva-, Müller-Versuch) - der Zeitverlauf der Effekte erlaubt Rückschlüsse über die Regulation von Blutdruck und Herzfrequenz.
|
Luft
bewegt sich durch die Atemwege, wenn ein Druckunterschied zwischen
"außen" (Umgebungsatmosphäre, Maske, Tubus) und "innen"
(Alveolarsystem) auftritt - entsprechend den Strömungsgesetzen (Boyle-Mariotte: Volumen und Druck verändern sich wechselseitig, das Produkt aus beiden bleibt konstant). Normalerweise erfolgen solche Druckunterschiede durch Kontraktion der Inspirationsmuskeln (Einatmung: das Volumen des Alveolarraums nimmt zu, der Alveolardruck ab) oder durch Retraktion der Lunge (Ausatmung: das Volumen des Alveolarraums nimmt ab, der Alveolardruck zu).
Die Lunge zieht nach innen, die Brustwand nach außen
Voraussetzung
für jede Strömung durch die Luftwege - Einatmung (Inspiration), Ausatmung (Exspiration) - ist ein Druckunterschied zwischen Alveolen und
Außenluft: Je größer dieser ist, und je kleiner der Strömungswiderstand (je weiter die Bronchien), desto leichter bewegt sich die Luft
(Strömungsgesetz).
Die Veränderung der Atemvolumina erfolgt durch die Tätigkeit der
Atemmuskulatur (hauptsächlich Zwerchfell und Interkostalmuskulatur). Der äußere Luftdruck (pB) ist im Regelfall konstant; der Luftdruck im Alveolarraum (pA) ändert sich bei Vergrößerung (Inspiration) oder Verringerung des Lungenvolumens (Expiration, Pressen).

 Abbildung: Zwerchfell und Atmung
Abbildung: Zwerchfell und Atmung
Nach einer Vorlage bei Silverthorn, Human Physiology - an integrated approach, 4th ed. Pearson International 2007
Im ausgeatmeten Ruhezustand
(1)
besteht ein passives Kräftegleichgewicht zwischen Lunge
(Zug nach innen) und Thoraxwand (Zug nach außen), Alveolar- und
Außendruck sind gleich groß; der Druck im Pleuraspalt liegt 2 mmHg unter dem
äußeren Luftdruck.
Bei der Einatmung (2)
kommt die Kraft der Inspirationsmuskeln dazu, welche den Thorax
erweitert (schwarze Pfeile) - insbesondere rückt das Zwerchfell nach
kaudal. Der Druck in Pleuraspalt und Alveolarraum nimmt ab, Luft strömt
in die Lunge ein (blaue Pfeile). Im eingeatmeten Ruhezustand
besteht wiederum ein Kräftegleichgewicht, Alveolardruck und Außendruck
sind gleich groß, der Pleuradruck ist erniedrigt (z.B. um 4 mmHg).
Bei
der Ausatmung (3)
läßt die entfaltende Kraft der Inspirationsmuskeln nach,
Retraktionskräfte der Lunge ziehen diese nach innen (schwarze Pfeile),
der Druck in Pleuraspalt und Alveolen steigt an, folglich strömt Luft
aus der Lunge (blaue Pfeile)
Die Gleitbewegungen der Lunge an der Brustwand erfolgen mit geringem Widerstand, dafür sorgt der - mit einer geringen Menge Flüssigkeit
gefüllte - Pleuraspalt  . Dieser enthält einige Milliliter Pleuraflüssigkeit. Diese transzelluläre Flüssigkeit ist
isoton und hat normalerweise einen niedrigen Eiweißgehalt (weniger als
50% des Plasmaproteinspiegels bzw. <1,2 g/dl Albumin).
. Dieser enthält einige Milliliter Pleuraflüssigkeit. Diese transzelluläre Flüssigkeit ist
isoton und hat normalerweise einen niedrigen Eiweißgehalt (weniger als
50% des Plasmaproteinspiegels bzw. <1,2 g/dl Albumin).
Der elastische Lungenzug senkt den Druck im Pleuraspalt sowie im Brustraumgewebe unter den Betrag des Umgebungsdrucks (pleuraler und intrathorakaler "Unterdruck", auch als Donders'scher Druck bezeichnet; der intrathorakale Raum heißt auch Donders'scher Raum). Der intrathorakale "Unterdruck" ist einer Messung mittels Speiseröhrensonde zugänglich (intraösophagealer
Druck).
Druck bezeichnet; der intrathorakale Raum heißt auch Donders'scher Raum). Der intrathorakale "Unterdruck" ist einer Messung mittels Speiseröhrensonde zugänglich (intraösophagealer
Druck).
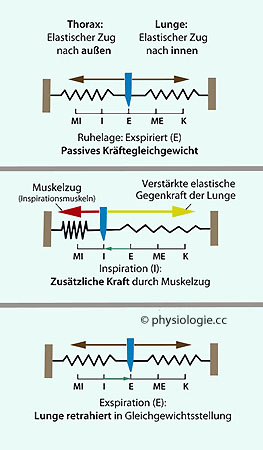
 Abbildung: Mechanik des Thorax-Lungen-Systems
Abbildung: Mechanik des Thorax-Lungen-Systems
NNach einer Vorlage in H. Hinghofer-Szalkay: Praktische Physiologie, 3. Aufl. Blackwell Berlin 1994
Oben: Ausgeatmete Ruhelage, Mitte: Einatmung, unten: ausgeatmete Ruhelage.
Die
Atemmuskulatur verändert das
Gleichgewicht hin zur Inspirationsstellung (I). Dies erhöht die
elastische Retraktionskraft der Lunge. Verschwindet die aktive
Komponente
des Muskelzugs, stellt sich das passive Kräftegleichgewicht
wieder ein
MI = maximale Inspiration  I = normale Inspirationsstellung
I = normale Inspirationsstellung  E =
ausgeatmete Ruhelage
E =
ausgeatmete Ruhelage  ME = maximale Exspiration
ME = maximale Exspiration  K = pulmonale Kollapsposition
K = pulmonale Kollapsposition


Zu
diesem durch den elastischen Lungenzug bedingten Druck kommen bei der
Atmung Druckschankungen in den Alveolen. Auch diese wirken sich auf den
Pleuradruck aus:
 Der Druck im Pleuraraum
(pIP) - und damit der intrathorakale Druck - ist die Summe aus dehnungsbedingtem (Gewebe) und Alveolardruck (Luft). Er ergibt sich aus
Der Druck im Pleuraraum
(pIP) - und damit der intrathorakale Druck - ist die Summe aus dehnungsbedingtem (Gewebe) und Alveolardruck (Luft). Er ergibt sich aus
 lungenseitigen
Komponenten (Luftdruck im Alveolarraum, Retraktionskräfte durch
elastische Fasern und Oberflächenspannung) und
lungenseitigen
Komponenten (Luftdruck im Alveolarraum, Retraktionskräfte durch
elastische Fasern und Oberflächenspannung) und
 thoraxseitigen Kräften
(Retraktionskraft in Richtung passive Ruhelage des Thorax, Kräfte aus
der Atemmuskulatur).
thoraxseitigen Kräften
(Retraktionskraft in Richtung passive Ruhelage des Thorax, Kräfte aus
der Atemmuskulatur).
In Atemruhelage (Lungeninhalt: FRC, funktionelle Residualkapazität) beträgt der Pleuradruck minus 3 cm H2O (-0,3 kPa), im
eingeatmeten Zustand (Lungeninhalt: FRC + Atemzugvolumen) und ruhiger Atmung minus 6-8 cm H2O (-0,6 bis -0,8 kPa), bei maximaler Einatmung (Lungeninhalt: Totalkapazität) bis zu -30 cm H2O (-3 kPa).
Atemlage (Glottis offen)
|
Pleuradruck
|
exspiriert
|
-0,3 kPa
|
inspiriert
|
~ -0,7 kPa
|
maximal inspiriert
|
bis -3 kPa
|
Dazu kommt - lageabhängig - der Einfluss der Schwerkraft:
So beträgt der intrapleurale Druck bei aufrechter Körperhaltung (in
Sitzen oder Stehen) apikal (im Bereich der Lungenspitze) - hier erhöht
das Gewicht der Lunge den Sog auf den Pleuraspalt - typischerweise -10
cm H2O (-1 kPa), an der Lungenbasis (auf der bei dieser Position das Gewicht der Lunge ruht) hingegen -3 H2O (-0,3 kPa) - der Druckunterschied beträgt also rund 7 cm H2O.
(Der hydrostatische Druckunterschied alleine wäre größer, zusätzliche
Kräfte reduzieren diesen Effekt.) Analog ist bei Linkslagerung der
Pleuradruck im rechten Pleuraspalt stärker negativ als im linken, und
vice versa.
Bei maximaler Aktivierung der Exspirationsmuskulatur und gleichzeitigem Verschluss der Glottis (Pressen) kann der Pleuradruck vorübergehend bis über +100 cm H2O (10 kPa) steigen und damit im Bereich des arteriellen Blutdrucks
liegen. Arterielle Gefäße im Brustraum können partiell komprimiert
werden und der Zufluß von Blut aus dem extrathorakalen Raum (Nachschub
von venösem Blut für die Herztätigkeit) wird unmöglich ( s. unten).
s. unten).
Retraktionskraft und Oberflächenspannung
Retraktionskraft.
Die Lunge zieht sich, wenn möglich, zusammen (sie retrahiert).
Je tiefer eingeatmet wird, desto größer wird diese
Retraktionskraft (wie beim Anspannen eines Gummibandes). Die Retraktionskräfte wirken einer Inspiration entgegen.
Die Komponenten der Retraktionskraft sind
die folgenden:
 Elastische Fasern tragen zu 30-50% zum Widerstand bei, der bei Einatmung zu überwinden ist.
Diese gut dehnbaren Strukturelemente sind netzförmig im Lungengewebe
eingelagert und bewirken eine Retraktionskraft, die mit der Zahl der
Fasern und ihrer Dehnung (Inspiration) zunimmt. Verringerung
ihrer Zahl oder strukturelle Zerstörung (Lungenemphysem) führt zu abnehmender Retraktionskraft der Lunge. (Über Elastin s. auch dort)
Elastische Fasern tragen zu 30-50% zum Widerstand bei, der bei Einatmung zu überwinden ist.
Diese gut dehnbaren Strukturelemente sind netzförmig im Lungengewebe
eingelagert und bewirken eine Retraktionskraft, die mit der Zahl der
Fasern und ihrer Dehnung (Inspiration) zunimmt. Verringerung
ihrer Zahl oder strukturelle Zerstörung (Lungenemphysem) führt zu abnehmender Retraktionskraft der Lunge. (Über Elastin s. auch dort)
 Kollagenfasern. Auch
diese rigideren - weniger dehnbaren - Fasern wirken der
Ausdehnung der Lunge entgegen; auch ihr Widerstand gegen Erweiterung
der Lunge nimmt mit der Inspiration und ihrer Zahl zu. Verringerung
ihrer Zahl führt zu abnehmender Retraktionskraft der Lunge.
Kollagenfasern. Auch
diese rigideren - weniger dehnbaren - Fasern wirken der
Ausdehnung der Lunge entgegen; auch ihr Widerstand gegen Erweiterung
der Lunge nimmt mit der Inspiration und ihrer Zahl zu. Verringerung
ihrer Zahl führt zu abnehmender Retraktionskraft der Lunge.

Abbildung: Druck- Volumen- Dynamik bei normaler Atmung
Nach einer Vorlage bei Silverthorn, Human Physiology, an integrated approach, 4th Int'l ed. 2007, Pearson / Benjamin Cummings
Der
Druck im Pleuraspalt (intrapleuraler Druck) ergibt sich aus
lungenseitigen und thoraxseitigen Kräften. Im ausgeatmeten Ruhezustand
besteht ein passives Kräftegleichgewicht zwischen Lunge
(Retraktionskraft, Zug nach innen) und Thoraxwand (reaktiv-elastischer
Zug nach außen).
Dazu kommt z.B. bei der Einatmung
Muskelkraft (Inspirationsmuskeln: Zwerchfell, mm. intercostales
externi), welche den Thorax nach außen aufspannt (vergrößert). Das
erzeugt den für die Einatmung nötigen Unterdruck im Alveolarraum
(subatmosphärischer intrapulmonaler Druck), das Atemzugvolumen strömt
in die Lunge ein.
Bei der Ausatmung
zieht die Lunge den Thorax in die Ausgangslage zurück, der Alveolarraum
wird kleiner und der intrapulmonale Druck vorübergehend positiv, was
die Ausatmung verursacht. Der intrapleurale Druck bewegt sich
normalerweise im subatmosphärischen Bereich (Donders'scher Unterdruck),
kann aber auch positive Werte annehmen, z.B. beim Pressen

 Oberflächenspannung: Durch
die alveolären Grenzflächen (Luft / Wasser) ergibt sich eine
Oberflächenspannung. Diese versucht, die Grenzfläche in den Alveolen
kleiner zu machen, wirkt also im Sinne einer Exspiration. Dieser Effekt wäre um ein Vielfaches größer,
wären die Alveolen nicht mit dem oberflächenspannungsvermindernden Surfactant
Oberflächenspannung: Durch
die alveolären Grenzflächen (Luft / Wasser) ergibt sich eine
Oberflächenspannung. Diese versucht, die Grenzfläche in den Alveolen
kleiner zu machen, wirkt also im Sinne einer Exspiration. Dieser Effekt wäre um ein Vielfaches größer,
wären die Alveolen nicht mit dem oberflächenspannungsvermindernden Surfactant  ausgekleidet (Problem bei Frühgeburten, RDS s. unten). Der verbleibende (reale) Betrag ist etwas größer als
die durch das elastische Fasergerüst der Lunge bewirkte Retraktionskraft.
ausgekleidet (Problem bei Frühgeburten, RDS s. unten). Der verbleibende (reale) Betrag ist etwas größer als
die durch das elastische Fasergerüst der Lunge bewirkte Retraktionskraft.
Füllt
man im experimentellen Modell eine Lunge mit physiologischer
Kochsalzlösung, dann entfällt der Effekt der Oberflächenspannung und
die Retraktionskraft der Lunge beträgt höchstens nur noch die Hälfte des
Normalbetrags. Das demonstriert den bedeutenden Anteil (bis ~70%) der Oberflächenspannung an der Retraktion der Lunge.

 Abbildung: Wirkungsmechanismus des Surfactant
Abbildung: Wirkungsmechanismus des Surfactant
Nach einer Vorlage in Boron / Boulpaep: Concise Medical Physiology, Elsevier 2021
Die
Ausrichtung der Surfactantmoleküle (hydrophobe Anteile gelb dargestellt) in der Grenzfläche (Alveolarluft - feuchte Alveolaroberfläche) minimiert
deren Tendenz, in die Wasserphase einzutauchen (bei Wassermolekülen: rote Pfeile) und ergibt eine in die Luftphase gerichtete Kraft (grüne Pfeile).
Je geringer die Anzahl der Wassermoleküle in der Grenzfläche, desto niedriger ist der Betrag der Oberflächenspannung, umso leichter kann sich die Lunge entfalten und umso geringer ist die Atelektaseneigung

Die Oberflächenspannung im Alveolarbereich wird durch
Surfactant
(oberflächenaktive Phospholipide) in den Alveolen auf ~1/3 des sonst
herrschenden Wertes gesenkt (abhängig von Schichtdicke des
Flüssigkeitsfilms und damit von der Atemtiefe). Surfactant erhöht
dadurch die Compliance (Dehnungsfähigkeit) der Lunge, verhindert
Atelektasen und erleichtert die Entfaltung
allfällig atelektatischer Alveolen.
 Als Atelektase
Als Atelektase  bezeichnet
man den Kollaps von Lungenbläschen bzw. einem Lungenabschnitt. Sie kann
im Rahmen eines
Pneumothorax (Entspannungsatelektase), durch Verlegung von Bronchien
(Obstruktionsatelektase), Einengung z.B. infolge eines Pleuraergusses
(Kompressionsatelektase), Fehlen des Luftstickstoffs bei Beatmung mit
reinem Sauerstoff (Resorptionsatelektase) auftreten. Atelektasen reduzieren den Atemgasaustausch mit der Umgebung, treten
(je nach Ursache) partiell oder komplett auf und können spontan
wieder verschwinden.
bezeichnet
man den Kollaps von Lungenbläschen bzw. einem Lungenabschnitt. Sie kann
im Rahmen eines
Pneumothorax (Entspannungsatelektase), durch Verlegung von Bronchien
(Obstruktionsatelektase), Einengung z.B. infolge eines Pleuraergusses
(Kompressionsatelektase), Fehlen des Luftstickstoffs bei Beatmung mit
reinem Sauerstoff (Resorptionsatelektase) auftreten. Atelektasen reduzieren den Atemgasaustausch mit der Umgebung, treten
(je nach Ursache) partiell oder komplett auf und können spontan
wieder verschwinden.
Durch die Wirkung des Surfactant (reduzierte Oberflächenspannung)
unterstützt, entfalten sich die betroffenen Alveolen in der Mehzahl der
Fälle von selbst wieder - vorausgesetzt, es herrscht an der
betreffenden Stelle ein positiver transmuraler bzw. transpulmonaler Druck (=intraalveolärer
minus intrapleuraler Druck), der die Alveole sich wieder entfalten
lässt (der "negative" Druck im Pleuraspalt ist eine wesentliche
Komponente).
Alveolarepithelzellen
(Typ II) produzieren Surfactant als phospholipidhältige Lamellenkörper (lamellar bodies)
und geben diese an den Flüssigkeitsfilm ab, der die Alveolen überzieht.
Die Freisetzung wird durch Dehnung angeregt, wie sie bei tiefen
Atemzügen auftritt.

Mehr zu
Oberflächenspannung und
Surfactant s.
dort
Surfactant ist für die Entfaltung der Lunge nach
der Geburt von entscheidender Bedeutung:
Neugeborene
mit mangelnder Bildung von Surfactant leiden
unter dem idiopathischen Atemnotsyndrom (Membransyndrom, infant respiratory
distress syndrome, RDS): Die Lungen entfalten sich nur unzulänglich,
Alveolen füllen sich nicht mit Luft, es kommt zu Sauerstoffmangel
(Hypoxie).
"Autoregulation" der Alveolenweite: Der Betrag der Oberflächenspannung nimmt mit der Alveolenweite zu,
da das Surfactant auf eine größere Fläche "ausgespreizt" wird und seine
oberflächenspannungsreduzierende Wirkung abnimmt. Dadurch werden
"überblähte" Alveolen automatisch verkleinert, die einzelnen Alveolen
auf einen mittleren Durchmesser eingestellt.
Einatmung erfolgt aktiv, Ausatmung meist passiv

In Atemruhelage (ausgeatmete Position) balancieren sich nach innen
(Lunge) und nach außen gerichtete nicht-muskuläre (elastische) Kräfte (Thorax, Gewicht des Bauchraums) aus. Bei einer Einatmung kommen aktive
Komponenten dazu (Inspirationsmuskeln): Der Thorax öffnet sich in
seinen oberen Partien vor allem nach vorne, weiter unten vorwiegend
zurn Seite ( Abbildung).
Abbildung).
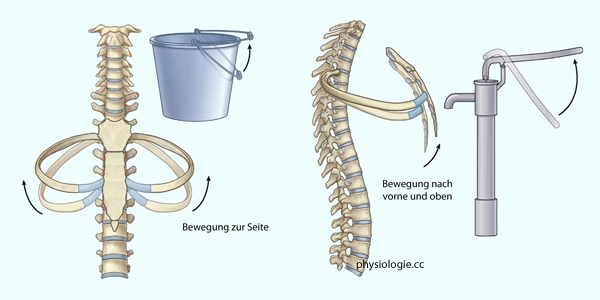

Abbildung: Rippenbewegung
Nach einer Vorlage bei Thibodeau / Patton, Anatomy & Physiology (6th ed), Mosby Elsevier 2007
Die Rotationsachsen der unteren Rippen ergeben eine inspiratorische Erweiterung des Thorax vor allem seitwärts (links), diejenige der oberen Rippen vor allem nach vorne (rechts).
Man
kann die laterale Erweiterung unterer Thoraxpartien mit der Bewegung
eines Kübelgriffes (links) und die sagittale mit der eines
Pumpenschwengels vergleichen (rechts) - "bucket-handle, water-pump-handle effect"

Einatmung (inspiration)
Bei der Atmung verändern sich Volumen und dadurch Druck
(Boyle-Mariotte-Gesetz  :
Bei unveränderter Temperatur - hier: Körpertemperatur - bleibt für eine
umschriebene Gasmenge das Produkt aus Druck und Volumen konstant).
Die Einatmung ist Folge der Kontraktion mehrerer Inspirationsmuskeln; der wichtigste ist das Zwerchfell. Die primäre Inspirationsmuskulatur wird bei jeder Atmung aktiviert (Zwerchfell, zahlreiche Interkostalmuskeln), die sekundäre oder akzessorische nur bei forcierter Atmung (mm. scaleni, m. sternocleidomastoideus, Hals- und Rückenmuskeln).
:
Bei unveränderter Temperatur - hier: Körpertemperatur - bleibt für eine
umschriebene Gasmenge das Produkt aus Druck und Volumen konstant).
Die Einatmung ist Folge der Kontraktion mehrerer Inspirationsmuskeln; der wichtigste ist das Zwerchfell. Die primäre Inspirationsmuskulatur wird bei jeder Atmung aktiviert (Zwerchfell, zahlreiche Interkostalmuskeln), die sekundäre oder akzessorische nur bei forcierter Atmung (mm. scaleni, m. sternocleidomastoideus, Hals- und Rückenmuskeln).
Die Inspirationsmuskulatur ist bei ausgeatmeter Position gut vorgedehnt und
funktioniert effizienter als in eingeatmeter Position, wo die Muskelfasern
verkürzt sind (Selbstlimitierung der
Inspirationsstärke).
Die
Inspirationsmuskeln erhöhen die Rückstellkräfte wie bei stärkerem
Spannen eines Gummibandes. Diese Kräfte werden bei der Ausatmung genützt.
Das
Zwerchfell (Diaphragma) wird vom Phrenikusnerven  aus dem Halsbereich des Rückenmarks
gesteuert. Es kontrahiert sich und flacht ab, d.h. seine
Kuppel rückt nach unten ("Bauchatmung") - bei ruhiger Atmung um etwa einen Zentimeter. Die Zwischenrippenmuskeln (mm. intercostales) helfen bei der Erweiterung des Brustraumes mit, indem sie die Rippen
anheben.
aus dem Halsbereich des Rückenmarks
gesteuert. Es kontrahiert sich und flacht ab, d.h. seine
Kuppel rückt nach unten ("Bauchatmung") - bei ruhiger Atmung um etwa einen Zentimeter. Die Zwischenrippenmuskeln (mm. intercostales) helfen bei der Erweiterung des Brustraumes mit, indem sie die Rippen
anheben.
Die schrägen Zugrichtungen machen die meisten Anteile der äußeren Interkostalmuskeln zu Einatemmuskeln ( Abbildung), insbesondere ihre oberen und dorsalen Anteile. Sie heben den Brustkorb, zusammen mit parasternalen Anteilen der inneren Interkostalmuskeln.
Abbildung), insbesondere ihre oberen und dorsalen Anteile. Sie heben den Brustkorb, zusammen mit parasternalen Anteilen der inneren Interkostalmuskeln.
 Zum
Brustkorb zählt man Rippen und Interkostalmuskeln, Wirbelsäule und
Zwerchfell (Diaphragma). Er enthält die Lungen (mit Pleura), das Herz
(mit Perikard), die Speiseröhre sowie Gefäße und Nerven.
Zum
Brustkorb zählt man Rippen und Interkostalmuskeln, Wirbelsäule und
Zwerchfell (Diaphragma). Er enthält die Lungen (mit Pleura), das Herz
(mit Perikard), die Speiseröhre sowie Gefäße und Nerven.
Der abnehmende Druck im Alveolarraum erzeugt einen Druckgradienten, und Luft strömt in die Lunge (Einatmung, Inspiration).
 Bei einem Schluckauf (Singultus, hiccup)
führt die Kombination einer unwillkürlichen Kontraktion des Zwerchfells
(Reizung des nervus phrenicus) und - einen Sekundenbruchteil später -
Verschluss der Epiglottis zu ruckartiger Reduktion des intrapulomonalen
und intrapleuralen Drucks (Inspirationsbewegung bei verschlossenem Kehlkopf). Das erzeugt das für Schluckauf charakteristische "Hicks"-Geräusch.
Bei einem Schluckauf (Singultus, hiccup)
führt die Kombination einer unwillkürlichen Kontraktion des Zwerchfells
(Reizung des nervus phrenicus) und - einen Sekundenbruchteil später -
Verschluss der Epiglottis zu ruckartiger Reduktion des intrapulomonalen
und intrapleuralen Drucks (Inspirationsbewegung bei verschlossenem Kehlkopf). Das erzeugt das für Schluckauf charakteristische "Hicks"-Geräusch.
Bei der Einatmung flacht das Zwerchfell ab, die Lungenränder weiten
sich und rücken nach kaudal, und die Pleurablätter im Bereich der Appositionszone
(recessus costodiaphragmatici) entfernen sich voneinander. Die dabei
auftretende Tangentialbewegung zwischen Pleura parietalis und Lunge
(pleura visceralis) wäre nicht möglich, wenn die Pleurablätter nicht
frei gegeneinander verschiebbar sind (was bei Pleuritis geschehen kann - in diesem Fall ist die Atmung extrem behindert und schmerzhaft).
Der Thorax erweitert sich nach vorne
und zur Seite, die Lunge vergrößert sich nach allen Richtungen. Das
Lungenvolumen nimmt dadurch zu, der Druck in den Alveolen ab
(Boyle-Mariotte).
Bei hoher (unterhalb C5)
Querschnittslähmung mit Tetraplegie bleibt das Zwerchfell
(innerviert aus C3-C5) funktionsfähig und ermöglicht die Atemtätigkeit
über “Bauchatmung”. Die
Inspirationsmuskulatur des Thorax (mm. intercostales externi &
interni intercartilaginei - innerviert aus Thorakalsegmenten) ist in
diesem Zustand gelähmt. Bedingt durch den inspiratorisch stärker
negativen intrathorakalen Druck sinkt während der Einatmung das Sternum
dorsalwärts ein, weil die aktive Abstützung (Expansion) durch die
Interkostalmuskeln wegfällt.
Forcierte Einatmung.
Bei starker körperlicher Belastung oder bei Ventilationsstörungen -
wenn also der Beitrag der primären Inspirationsmuskeln für adäquate
Ventilation nicht ausreicht - wird die Einatmung durch Inspirationshilfsmuskeln unterstützt: Die mm. scaleni heben die ersten beiden Rippen an, der m. sternocleidomastoideus bewegt das Brustbein nach vorne-oben, die Hals- und Rückenmuskulatur hebt den Schultergürtel an. Zusätzlich senkt die Aktivierung von Muskeln im oberen Respirationstrakt den Atemwegwiderstand.
In einer sitzenden, leicht nach vorne gebeugten Position, mit den Händen auf den Knien und damit fixierten Armen ("tripod position"), werden die Brustmuskeln
(mm. pectorales) ebenfalls zu Hilfsmuskeln der Inspiration, weil sie in
dieser Position den Brustkorb anheben. (Normalerweise dienen sie der
Armbewegung.)
 Abbildung: Wirkung der führenden Respirationsmuskulatur
Abbildung: Wirkung der führenden Respirationsmuskulatur
Nach einer Vorlage in Boron / Boulpaep: Concise Medical Physiology, Elsevier 2021
Die Hauptzugrichtung der mm. intercostales externi ist ventrokaudal (nach vorne-unten), die der mm. intercostales interni dorsokaudal (nach hinten-unten).
Der wichtigste Inspirationsmuskel
ist das Diaphragma, weiters obere und dorsale Anteile der mm.
intercostales externi sowie parasternale Anteile der mm. intercostales
interni. Bei forcierter Einatmung werden auch akzessorische
Inspirationsmuskeln aktiv (scaleni, sternocleidomastoideus).
Ruhige Ausatmung
erfolgt ohne Muskelbeteiligung. Bei forcierter Exspiration helfen
Bauchdeckenmuskulatur sowie einige Anteile der Interkostalmuskeln, den
Druck im Thoraxraum zu erhöhen

Volumenabnahme und Druckanstieg. Erschlaffen die
Inspirationsmuskeln, stellt sich das ursprüngliche Kräftegleichgewicht
ein: Die Lunge rückt in die Ausgangsstellung zurück. Mit zunehmender
Ausatmung steigen die nach außen wirkenden Rückstellkräfte des Thorax,
während der elastische Lungenzug immer geringer wird,
der Thorax zieht das System in die Ausgangslage zurück.
Die elastische
Retraktion der Lunge reicht für eine ruhige Ausatembewegung aus (Druckgradient ~0,2 kPa).
Bei starker körperlicher Belastung oder bei Ventilationsstörungen wird die Ausatmung
durch Exspirationshilfsmuskeln unterstützt. Die Bauchmuskulatur (m. rectus
abdominis, mm. obliqui und m. transversus abdominis) sowie die mm. intercostales interni erhöhen den
intraabdominellen Druck bzw. ziehen die Rippen nach kaudal.
Vordehnung der Muskeln: Auch für die Exspirationshilfsmuskeln gilt, dass ihre Kraft mit der Vordehnung - und damit zunehmender Inspiration - zunimmt: Bei eingeatmeter Position arbeiten sie effizienter als wenn man schon ausgeatmet hat (und die Muskelfasern
verkürzt sind).
Pressen: Bei
forcierter oder tiefer Exspiration hingegen werden die Bauchdecken
angespannt (z.B. bei Husten, Pressen, Niesen, Singen, Schreien),
wodurch im Bauchraum ein Überdruck entsteht (bis zur Höhe des arteriellen Blutdrucks oder darüber hinaus: Valsalva-Versuch),
der das Zwerchfell nach
oben schiebt. Beteiligt sind die mm. obliquus internus und externus,
rectus, transversus abdominis. Kollektiv erhöhen sie den Druck im
Bauchraum, drängen die Zwerchfellkuppel nach kranial und erhöhen
dadurch den intrathorakalen Druck.
Auch ziehen die kaudalen Anteile der inneren sowie kaudal-ventrale der äußeren Zwischenrippenmuskeln die Rippen nach unten und innen, was den Brustkorb komprimiert und den intrathorakalen Druck erhöht. Schließlich können Anteile der Hals- und Rückenmuskulatur den Schultergürtel senken und dadurch das Volumen des Thraxraumes senken.
Bei ruhiger Atmung
betragen die Druckschwankungen in den Alveolen einige cm H2O (=Zehntel kPa). Die Luftströmung
erreicht bei ruhiger Atmung einen Höchstwert von <1 Liter pro Sekunde, bei forcierter
Exspiration oder Inspiration (intensives Luftschnappen) ein Vielfaches
davon (Strömungsgeschwindigkeiten beim Niesen oder Husten bis zu mehreren hundert Stundenkilometer - dies löst Schleim
und Fremdkörper von der Wand der Luftwege und reißt sie mundwärts).
Wiederholtes starkes Husten kann das Herzzeitvolumen senken, was bis zu
Bewußtlosigkeit (Synkope) führen kann (Valsalva-Manöver, s. unten).
Wie dehnbar ist der Atemapparat?
Die Dehnbarkeit (Compliance
= ΔV/Δp, Volumenänderung / Druckänderung) ist ein mitbestimmender
Faktor für den Energieaufwand, der bei der Atmung aufgebracht werden
muss:
 Abbildung: Compliancekurven des respiratorischen Systems im passiven Zustand (Atemmuskeln entspannt)
Modifiziert nach einer Vorlage bei Beachey W: Respiratory care anatomy and physiology, 2nd ed, Mosby St. Louis 2007
Abbildung: Compliancekurven des respiratorischen Systems im passiven Zustand (Atemmuskeln entspannt)
Modifiziert nach einer Vorlage bei Beachey W: Respiratory care anatomy and physiology, 2nd ed, Mosby St. Louis 2007
Passives Druck-Volumen-Verhalten (Compliance) ohne Muskelbeteiligung.
Die Compliance (ΔV/Δp) des Thorax nimmt mit zunehmender Inspiration zu, diejenige der Lunge ab. Ordinate: Lungenvolumen, Abszisse: transmuraler Druck (jeweils Innendruck minus Außendruck).
Grüner Pfeilkopf: Totalkapazität (TC); blauer Pfeilkopf: Residualvolumen (RV).
"Thorax" (magenta) und "Lunge" (blaugrün) sind die Ruhedehnungskurven der Thoraxwand einerseits, der Lunge andererseits (unabhängig voneinander). R-T: Relaxationsvolumen des isolierten Thorax; R-L: Relaxationsvolumen der isolierten Lunge.
A: Stark ausgeatmeter Zustand,
Rückstellkraft des Thorax nach außen stärker als Zug der Lunge nach innen (→ Einatmung ohne Muskulatur); B: Gleichgewichtspunkt (Atemruhe); C: Thoraxwand entspannt, nur Retraktionskraft der Lunge wirksam; D: Stark eingeatmeter Zustand,
sowohl Thorax als auch Lunge wirken in Richtung Retraktion (→ Ausatmung ohne Muskulatur).
Auf eine isolierte Lunge
muss ein positiver transmuraler Druck einwirken (Abszisse), um Luft in
sie zu bekommen (Ordinate) - entweder durch Aufblasen über die
Luftwege, oder durch Aufdehnen mittels Unterdrucks im Pleuraspalt
(physiologisch). Ohne Einwirken eines transmuralen Drucks verbleibt nur
ein Minimalvolumen (Relaxationsvolumen: Alveolardruck - Pleuradruck = 0) in der (kollabierten) Lunge.
Ein isolierter Thorax würde
- bei entspannter Atemmuskulatur - die Form annehmen, die
einer Inspirationsstellung von ungefähr 75% der Totalkapazität (das
abgebildete Beispiel zeigt mit 50% VC einen niedrigeren Wert)
entspricht (Relaxationsvolumen R-T). Um ihn
zu verkleinern oder zu vergrößern, bedarf es entsprechender Änderungen des transmuralen Drucks. (Oder die Atemmuskulatur wird
aktiviert.)
Sind
Lunge und Thoraxwand zu einem Gesamtsystem gekoppelt - über den
luftdichten Pleuraspalt (physiologischer Normalfall) -, ergibt sich die S-förmige Ruhedehnungskurve des Gesamtsystems (schwarz dargestellt).
Zustand
B (roter Punkt): Relaxationsvolumen des Lunge-Thorax-Systems. Thorax zieht nach außen, Lunge nach innen - passive Gleichgewichtslage des respiratorischen Systems (grüne Doppelpfeile). FRC
= funktionelle Residualkapazität (Luftmenge, die sich bei ausgeameter
Ruhelage in der Lunge befindet).
Ausgehend vom ausgeatmeten Ruhezustand würde ein vollständiger Pneumothorax den Zustandspunkt für Thorax (Erweiterung) und Lunge (Kollaps) entsprechend den blauen Pfeilen nach oben und unten verändern, weil diese dann mechanisch entkoppelt sind.
Bei der Atmung kommen aktive
Kräfte dazu, welche die Druck-Volumen-Beziehung des Thorax entsprechend
verändern. Beispielsweise würde bei normaler Einatmung die Thoraxkurve
so verschoben, dass im inspirierten Zustand der erforderliche
transmurale Druck für das Gesamtsystem Null beträgt (d.h. das System
strebt diesen Punkt an)

Thoraxwand und Lunge sind durch den Pleuraraum mechanisch (druckmäßig)
zu einem Gesamtsystem verknüpft. Die Kurve des Gesamtsystems ist S-förmig, die Compliance (Volumen / Druck) ist in
Mittellage am größten (beste Dehnbarkeit).
Der Atemapparat (Lunge + Thorax) hat in Atemruhelage die höchste Compliance (~1 l/kPa)
|
Compliance (C) bedeutet Dehnbarkeit, definiert als Volumenänderung ∂V pro Druckänderung ∂p. Die Compliance der Lunge entspricht dem Kehrwert ihrer Eigenelastizität (Druck / Volumen). Die
Compliance kann (auch ohne Kenntnis des absoluten Füllungsvolumens) aus
der aktuellen Volumen- und Druckänderung während eines Atemzuges
ermittelt werden:
Die Compliancekurve der Lunge
( Abbildung oben) beginnt bei 0% Vitalkapazität bereits bei einem transmuralen Druck von ~5 cm H2O
(0,5 kPa), d.h. die Lunge ist auch schon bei dieser niedrigen
Füllung
bestrebt, sich zusammenzuziehen. Je größer das Volumen (je mehr die
Lunge gedehnt wird), desto mehr nimmt die elastische Gegenkraft zu, der
Zug nach innen wird zusehends stärker, die Dehnbarkeit der Lunge (ihre Compliance) nimmt immer mehr ab.
Abbildung oben) beginnt bei 0% Vitalkapazität bereits bei einem transmuralen Druck von ~5 cm H2O
(0,5 kPa), d.h. die Lunge ist auch schon bei dieser niedrigen
Füllung
bestrebt, sich zusammenzuziehen. Je größer das Volumen (je mehr die
Lunge gedehnt wird), desto mehr nimmt die elastische Gegenkraft zu, der
Zug nach innen wird zusehends stärker, die Dehnbarkeit der Lunge (ihre Compliance) nimmt immer mehr ab.
Die Tabelle zeigt typische Compliancewerte für den mittleren Dehnungsbereich (die Compliance ändert sich mit dem Dehnungsgrad, s. oben):
Compliance Lunge (L)
|
Compliance Thoraxwand (TC)
|
Respiratorische Compliance (L+TC)
|
2,6 l/kPa
(260 ml/cm H2O)
|
2,6 l/kPa
(260 ml/cm H2O)
|
1,3 l/kPa
(130 ml/cm H2O)
|
Als Elastanz (Dehnungswiderstand oder Volumenelastizität, elastance) bezeichnet man den Reziprokwert (E = Δp/ΔV) der Compliance. Sie ist ein Maß für die Steifigkeit des Gewebes (der Betrag ist umso höher, je niedriger die Compliance ist).
 Zur
Überwindung der Gewebesteifigkeit (Brustwand plus Lunge) muss bei
normaler Atmung mehr Arbeit aufgebracht werden als zur Überwindung des
Strömungswiderstandes in den Luftwegen.
Zur
Überwindung der Gewebesteifigkeit (Brustwand plus Lunge) muss bei
normaler Atmung mehr Arbeit aufgebracht werden als zur Überwindung des
Strömungswiderstandes in den Luftwegen.
Starke Belastung mit
staubhältiger Luft (z.B. bei Kohlearbeitern) führt zu narbigen
Veränderungen der Alveolaroberfläche. Das vermindert die Dehnbarkeit
(Compliance) der Lunge (restriktive Ventilationsstörung) und erhöht
folglich die Atemarbeit.
Da sich die Gesamtelastanz eines Systems als die Summe der Elastanzen
seiner Komponenten berechnen lässt, ergibt die Summe der Kehrwerte der
Compliance der Einzelkomponenten des Systems (hier: Thoraxwand TC: thoracic cage, L: Lunge) den Kehrwert der Compliance des Gesamtsystems:
1/RC = 1/LC + 1/TCC
wobei RC = respiratorische Compliance
(Gesamtsystem Lunge + Thorax), LC = Compliance der Lunge, TCC =
Compliance des Brustkorbs (in der obenstehenden Tabelle: 1/1,3 = 1/2,6
+ 1/2,6).
 Rechenbeispiel: Die Compliance der Lunge eines Patienten beträgt 2
l/kPa. Wie stark muss sich der transpulmonale Druck ändern, damit ein
Volumen von 500 ml geatmet werden kann?
Antwort: Um 0,25 kPa (0,5 / 2)
Rechenbeispiel: Die Compliance der Lunge eines Patienten beträgt 2
l/kPa. Wie stark muss sich der transpulmonale Druck ändern, damit ein
Volumen von 500 ml geatmet werden kann?
Antwort: Um 0,25 kPa (0,5 / 2)
 Physiologische Einflüsse auf Compliancewerte:
Der Wert der Compliance des Brustkorbs (TCC) hängt ab vom Muskeltonus
und der Form des Brustkorbes (Wirbelsäule, Rippenbögen); derjenige der
Lunge (LC) von der Oberflächenspannung in den Alveolen sowie dem
elastischen Zug des pulmonalen Bindegewebes.
Physiologische Einflüsse auf Compliancewerte:
Der Wert der Compliance des Brustkorbs (TCC) hängt ab vom Muskeltonus
und der Form des Brustkorbes (Wirbelsäule, Rippenbögen); derjenige der
Lunge (LC) von der Oberflächenspannung in den Alveolen sowie dem
elastischen Zug des pulmonalen Bindegewebes.
Zwerchfellhochstand engt den Bewegungsspielraum der Lunge ein und senkt
die respiratorische Compliance. Beispiele: Liegende Körperposition;
fortschreitende Schwangerschaft; Blähungen; Adipositas.
In höheren
Lebensalter nimmt die Menge an elastischem Gewebe ab, die
respiratorische Compliance nimmt leicht zu (wie bei milden
Emphysemformen).
In der Atemruhelage ist die Compliance des Atemsystems am höchsten (steilster Verlauf der ∂V / ∂p-Kurve, Abbildung oben); bei tiefer Aus- oder Einatmung ist das System weniger gut dehnbar.
|
Bei tiefer Aus- oder Einatmung verringert sich die Compliance des Atemapparats |
Die Thoraxwand
ist bei demjenigen Zustand entspannt, der einem transmuralen Druck von
Null ergibt. Dies entspricht ungefähr einer Inspirationsstallung von 75% der Totalkapazität.
 Ist das Volumen kleiner,
ist der Thorax nach innen gezogen worden (in Richtung Exspiration,
gewöhnlich durch den elastischen Lungenzug), und er strebt nach Erweiterung,
um wieder in seine Gleichgewichtslage zurückzukehren (negativer
transmuraler Druck zur Aufrechterhaltung dieser Position nötig).
Ist das Volumen kleiner,
ist der Thorax nach innen gezogen worden (in Richtung Exspiration,
gewöhnlich durch den elastischen Lungenzug), und er strebt nach Erweiterung,
um wieder in seine Gleichgewichtslage zurückzukehren (negativer
transmuraler Druck zur Aufrechterhaltung dieser Position nötig).
 Ist das Volumen größer, ist der Thorax nach außen gezogen worden (durch tiefe Inspiration der Einatemmuskulatur), und er strebt nach Verkleinerung (positiver transmuraler Druck zur Aufrechterhaltung dieser Position nötig).
Ist das Volumen größer, ist der Thorax nach außen gezogen worden (durch tiefe Inspiration der Einatemmuskulatur), und er strebt nach Verkleinerung (positiver transmuraler Druck zur Aufrechterhaltung dieser Position nötig).
Eine Bestimmung der Compliance kann klinisch wichtig sein: Abnahme der
Volumendehnbarkeit erzwingt gesteigerte Atemarbeit (z.B. bei
Lungenentzündung, restriktiven Lungenerkrankungen, Lungenödem). Die
Compliance kann bei Lungenemphysem hingegen erhöht sein, weil in diesem
Fall das Gewebe "ausgedünnt" und leichter dehnbar ist.

Der
Thorax (ohne Muskelaktivität) hat
eine Ruhelage, die er (für sich alleine) spontan einnimmt (Abb.: Inset C),
entsprechend einer mäßigen Inspirationslage (Compliancekurve bei null
transmuralem Druck). Wird er verkleinert, hat er das Bestreben, sich zu
erweitern (nach außen gerichtete Pfeile in A und B), wird er weiter
expandiert, hat er das Bestreben, kleiner zu werden (nach innen
gerichteter Pfeil in D)

Die
Lunge
hat ein Druck-Verhalten wie ein elastischer Ball; ihr Inhalt nimmt
mit steigendem Füllungsdruck zu. Auf sich alleine
gestellt würde sie sich praktisch vollständig zusammenziehen
(kollabieren); das geschieht bei einem
Pneumothorax 
(s. ganz
unten)

Das
Gesamtsystem
(Abb.: durchgezogene Kurve) ist in Atemruhelage im Kräftegleichgewicht und
enthält definitionsgemäß die funktionelle Residualkapazität (
FRC,
roter Punkt): Hier sind die nach außen (Thorax) und innen (Lunge)
gerichteten Kräfte im Gleichgewicht: Strichlierte und punktierte
Compliancekurven weisen denselben transmuralen Druckbetrag auf - Thorax
negativ, Lunge positiv, die Druckbeträge kompensieren einander, Pfeile
im Zustand "B" (gleicher Abstand des roten Punkts zu Thorax- und Lungenkurve)
Bei guter (hoher) Compliance der Lunge ist der Unterdruck im Pleuraspalt gering
|
 Man unterscheidet statische und dynamische Compliance:
Man unterscheidet statische und dynamische Compliance:
 Die statische Compliance wird bei Atemruhe
ermittelt, wenn also keine Luft durch die Atemwege strömt. Methode: Die
Einatmung erfolgt stufenweise (z.B. in 500-ml-Schritten), jeweils in
den Atempausen wird der intrapleurale Druck ermittelt
(Oesophagus-Ballonkatheter).
Die statische Compliance wird bei Atemruhe
ermittelt, wenn also keine Luft durch die Atemwege strömt. Methode: Die
Einatmung erfolgt stufenweise (z.B. in 500-ml-Schritten), jeweils in
den Atempausen wird der intrapleurale Druck ermittelt
(Oesophagus-Ballonkatheter).
Die Lunge
expandiert mit zunehmendem Unterdruck im Pleuraspalt nicht gleichmäßig,
die statische Dehnungskurve des Gesamtsystems ist S-förmig ( Abbildung, links):
Abbildung, links):
 Bei niedrigem Volumen ist die Druck-Volumen-Charakteristik flach (geringe Compliance)
Bei niedrigem Volumen ist die Druck-Volumen-Charakteristik flach (geringe Compliance)
 Im normalen "Ruhebereich" ist die Kurve steil (hohe Compliance, System gut dehnbar)
Im normalen "Ruhebereich" ist die Kurve steil (hohe Compliance, System gut dehnbar)
 Bei hohen Druck- und Volumenwerten verflacht die Charakteristik wieder (geringe Compliance)
Bei hohen Druck- und Volumenwerten verflacht die Charakteristik wieder (geringe Compliance)
 Eine dynamische Compliance lässt sich aus Druck- und Volumenverläufen während kontinuierlicher Atmung
ableiten, wenn also die fortlaufenden Messungen nicht durch Ruhepunkte
unterbrochen werden (
Eine dynamische Compliance lässt sich aus Druck- und Volumenverläufen während kontinuierlicher Atmung
ableiten, wenn also die fortlaufenden Messungen nicht durch Ruhepunkte
unterbrochen werden ( Abbildung, rechts).
Abbildung, rechts).
Es gibt zwei Umkehrpunkte - end-inspiratorisch und
end-exspiratorisch. Zwischen diesen beiden Punkten kann in der Druck /
Volumen- Darstellung eine gerade Linie gezogen werden; der Gradient ist
dann weniger steil als für die statische Compliance, d.h. die
dynamische Compliance ist geringer als die statische.
Ursache dafür ist der Beitrag des Strömungswiderstandes der Luftwege.
Daher kann auch die Differenz zwischen statischer und dynamischer
Compliance als Maß für den Atemwegwiderstand verwendet werden.
Quantifizierung der Compliance erfordert Volumen- (Spirometrie) und Druckmessungen:
 Der intrathorakale (Donders'sche)
- und damit intrapleurale - Druck kann mittels Ösophagussonde ermittelt werden (
Der intrathorakale (Donders'sche)
- und damit intrapleurale - Druck kann mittels Ösophagussonde ermittelt werden ( Abbildung - die Speiseröhre
durchzieht den Donders'schen Raum):
Abbildung - die Speiseröhre
durchzieht den Donders'schen Raum):
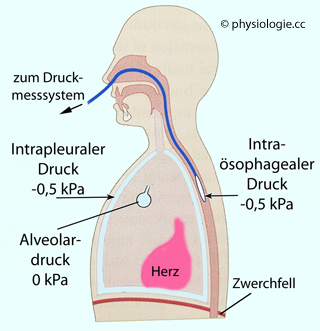
 Abbildung: Messung des intrapleuralen Drucks
Nach einer Vorlage bei Ward / Ward / Leach, The Respiratory System at a Glance, 4th ed. Wiley 2015
Abbildung: Messung des intrapleuralen Drucks
Nach einer Vorlage bei Ward / Ward / Leach, The Respiratory System at a Glance, 4th ed. Wiley 2015
Eine
Druckmessung im engen Pleuralspalt wäre zu riskant (Gefahr einer
Punktion der Lunge). Die Speiseröhre ist normalerweise sowohl an ihrem
Eingang als auch am Ausgang verschlossen, der Innendruck entspricht dem
Pleuradruck auf derselben Höhe (im gezeigten Beispiel 0,5 kPa unter dem
Außendruck) und kann mit einer Ösophagussonde gefahrlos ermittelt werden

Der
intrathorakale Druck liegt
normalerweise unter dem Umgebungsdruck, da die Lungen einen Sog am
Pleuraspalt ausüben. Bei forcierter Exspiration kann er positive Werte
annehmen, insbesondere bei verschlossener Glottis, z.B. beim Niesen
oder Husten bis auf etwa 8 kPa (60 mmHg).
 Der Alveolardruck kann u.a. mittels Ganzkörperplethysmographie ermittelt werden.
Der Alveolardruck kann u.a. mittels Ganzkörperplethysmographie ermittelt werden.
Die Compliance (Dehnbarkeit) des Atemapparates ist erhöht bei Emphysem (Abbau von Gewebe macht die Lunge dehnbarer) und erniedrigt bei Fibrose (versteifte Lunge durch Bindegewebsvermehrung), Skoliose oder Obesitas (eingeschränkte Bewegungsfreiheit des Atemapparates).
Atemwege können durch die Atmung verengt werden
Strömt Luft mit erhöhter Geschwindigkeit
durch einen Luftweg (z.B. bei körperlicher Belastung), kann der
sinkende Lateraldruck den transmuralen Druck so ändern, dass die Wand -
trotz der expandierenden Wirkung elastischer Kräfte - zur Mitte
"gesaugt" wird und den Luftstrom erschwert:

Abbildung: Dynamische Atemwegskompression (schematisch)
Nach einer Vorlage bei Pryor JA (ed) Respiratory care. Elsevier Edinburgh 1991
"Momentaufnahme"
des Ablaufs während einer forcierten Exspiration, wie z.B. während
eines Hustenstosses. Der pleurale Druck beträgt in diesem Beispiel 20
cmH2O - bedingt durch die Kraft der Exspirationsmuskeln
(auch höhere Beträge sind möglich) -, die elastische Retraktionskraft
der Lunge 5 cmH2O. Damit beträgt der periphere (Alveolar-) Druck 25 cmH2O, und der Druckgradient bis zum Mundraum (0 cmH2O) 25 cmH2O.
Ab einer Zone, wo der Außen- und Innendruck der Luftwege gleich groß ist (hier 20 cmH2O),
ist der transmurale Druck nach innen gerichtet und die Wand der
Atemwege wird nach innen komprimiert. Die Verengung erhöht den
Strömungswiderstand, je enger die Luftwege, desto stärker (dynamischer
Kollaps, Kompression). Das hat zur Folge, dass die Atemstromstärke mit
zunehmendem Alveolardruck (wie bei einem Starling-Resistor) nicht weiter zunimmt

Dynamische Atemwegskompression: Wie in der  Abbildung
dargelegt, werden bei forcierter Ausatmung durch den Anstieg des
Donders'schen Drucks über den Betrag des atmosphärischen Drucks hinaus
die Atemwege komprimiert - der Atemwegwiderstand steigt. Erklärbar ist dieses Phänomen durch den Bernoulli-Effekt: Strömt ein Gas oder eine Flüssigkeit entlang einer Struktur (z.B. der
Wand eines Bronchus), nimmt mit zunehmender Geschwindigkeit der Druck
senkrecht zur Strömungsrichtung ab (
Abbildung
dargelegt, werden bei forcierter Ausatmung durch den Anstieg des
Donders'schen Drucks über den Betrag des atmosphärischen Drucks hinaus
die Atemwege komprimiert - der Atemwegwiderstand steigt. Erklärbar ist dieses Phänomen durch den Bernoulli-Effekt: Strömt ein Gas oder eine Flüssigkeit entlang einer Struktur (z.B. der
Wand eines Bronchus), nimmt mit zunehmender Geschwindigkeit der Druck
senkrecht zur Strömungsrichtung ab ( vgl. dort).
vgl. dort).
Im Alveolarbereich kommt zu diesem positiven
Druck die elastische Retraktionskraft des Lungengewebes dazu, die
Alveolen bleiben geöffnet (in diesem Beispiel: +25 cmH2O in den Alveolen, 20 cmH2O außen).
Forcierte Exspiration erhöht den Atemwegwiderstand
|
Auf der Strecke zwischen Alveolen und Trachea bzw. Pharynx besteht ein
Druckgradient; der Innendruck wird proximalwärts immer geringer, bis
ein Punkt mit gleichem Druck erreicht ist (EPP: equal pressure point), und ab dieser Stelle sinkt der intrabronchiale Druck unter den Betrag des Donders'schen ab - der transmurale Druck
wird also negativ -, und die Luftwege kollabieren (teilweise).
 Als Equal pressure point (EPP)
bezeichnet man den Druck, bei dem während der Ausatmung der transmurale
Druck der Luftwege 0 beträgt, d.h. der Druck in den Bronchien gleich
hoch ist wie der intrapleurale Druck. Flow limitation ist ein EPP-Zustand in peripheren Atemwegen, bei dem die Strömung trotz Anstieg des Druckgradienten nicht ansteigt.
Als Equal pressure point (EPP)
bezeichnet man den Druck, bei dem während der Ausatmung der transmurale
Druck der Luftwege 0 beträgt, d.h. der Druck in den Bronchien gleich
hoch ist wie der intrapleurale Druck. Flow limitation ist ein EPP-Zustand in peripheren Atemwegen, bei dem die Strömung trotz Anstieg des Druckgradienten nicht ansteigt.
Bronchien sind kollapsible Luftwege. Der
Kollaps erhöht den Strömungswiderstand, und die
Strömungsgeschwindigkeit kann auch bei zunehmendem Pressdruck nicht
weiter ansteigen (flow limitation). Bronchiolen sind wegen ihrer Knorpelringe und glatten Muskulatur, teilweise auch der Anwesenheit von Surfactant nicht kollapsibel.
Welche Auswirkungen hat das Pressen auf den Kreislauf?
Bei
forcierter Atmung ändern sich die Druckwerte wesentlich stärker als bei Spontanatmung:
 Abbildung: Valsalva-Versuch
Nach einer Vorlage in answers.com / blood pressure
Abbildung: Valsalva-Versuch
Nach einer Vorlage in answers.com / blood pressure
Violettes Feld: Während
des Pressens (Druckmessung an Mundstück) nehmen venöser Rückstrom und
kardiale Vorlast ab, Schlagvolumen und arterieller
Blutdruck sinken. Der Baroreflex
hebt die Herzfrequenz, was den weiteren Blutdruckverlauf normalerweise
stabilisiert (kreislauflabile Patienten können in dieser Phase das Bewußtsein verlieren
und kollabieren).
Bei Beendigung des Pressens steigt zunächst das
venöse Blutangebot an das rechte Herz, was sich auf den
Blutdruck kaum auswirkt.
Rotes Feld: Erreicht das erhöhte Blutangebot
aus dem Pulmonalkeislauf das rechte Herz, nehmen Schlagvolumen
und arterieller Druck stark zu, die Herzfrequenz nimmt wieder auf den Ausgangswert ab

 Versucht man - Nase und Mund
geschlossen - mit größter Kraft einzuatmen,
so kann der Druck in Lunge und Pleuraspalt bis auf -120 cm H2O
absinken (Müller-Versuch).
Klinisch kann dieses Verfahren Aufschluss über allfällige Schwächen im
Bereich der oberen Luftwege geben, der Versuch dient u.a. zur
Aufklärung von Ursachen einer Schlafapnoe.
Versucht man - Nase und Mund
geschlossen - mit größter Kraft einzuatmen,
so kann der Druck in Lunge und Pleuraspalt bis auf -120 cm H2O
absinken (Müller-Versuch).
Klinisch kann dieses Verfahren Aufschluss über allfällige Schwächen im
Bereich der oberen Luftwege geben, der Versuch dient u.a. zur
Aufklärung von Ursachen einer Schlafapnoe.

Beim Pressen kann der Druck bis auf +180 cm H
2O (fast 1/5
Atmosphäre) steigen (
Valsalva-Pressversuch 
,

Abbildung
).
Das bedeutet, dass man beim Pressen im Bauch-und Brustraum einen Druck
ausüben kann, der über dem arteriellen Blutdruckwert liegt.
Man kann mehrere Phasen dieses Tests unterscheiden:

Phase 1 - Die Pulmonalgefäße werden durch den erhöhten Pressdruck
Richtung linkes Herz entleert, das Schlagvolumen steigt an, der
arterielle Blutdruck steigt vorübergehend kurz an, reflektorisch kann
die Herzfrequenz leicht absinken

Phase 2 - Der hohe intrathorakale Druck behindert den venösen
Rückstrom, Schlagvolumen und arterieller Druck nehmen ab, reflektorisch
steigt die Herzfrequenz

Phase 3 - Nach 10 Sekunden wird abgebrochen. Die Venen im Brustraum
füllen sich, Schlagvolumen und Blutdruck sinken, die Herzfrequenz
steigt reflektorisch an

Phase 4 - Die linksventrikuläre Vorlast normalisiert sich. Da die
Herzfrequenz noch erhöht ist, steigt der Blutdruck vorübergehend an.
Reflektorisch erhöhte parasympathische Aktivität bringt dann Blutdruck
und Herzfrequenz zu Normalwerten zurück.
Dieses Verfahren
(Valsalva maneuver) hat zahlreiche Anwendungen, u.a. dient er

der
Kreislauftestung: Während des
Pressens verringert sich die Vorlast des Herzens, das Schlagvolumen -
das zunächst durch die direkte Druckwirkung für kurze Zeit ansteigt
(oft mit durch den Baroreflex bedingtem kurzem Abfall der Herzfrequenz)
- sinkt kontinuierlich, und die Herzfrequenz nimmt zu. Nachher dreht
sich das Muster entsprechend um

dem Druckausgleich im Mittelohr über die tuba Eustachii bei
zunehmendem Außendruck (sinkende Meereshöhe, Landeanflug mit dem
Flugzeug)

der Untersuchung von Extremitätenvenen (halten die Venenklappen bei zentralem Druckanstieg dicht?)

einer Beendigung supraventrikulärer Tachykardie

 Die
von Antonio Vaslsalva (1666-1723) beschriebene Methode zur Erhöhung des
Luftdrucks im Rachenraum diente ursprünglich u.a. zum Test der
Tubendichtigkeit und zum Austreiben von Eiter aus dem Mittelohr.
Die
von Antonio Vaslsalva (1666-1723) beschriebene Methode zur Erhöhung des
Luftdrucks im Rachenraum diente ursprünglich u.a. zum Test der
Tubendichtigkeit und zum Austreiben von Eiter aus dem Mittelohr.
Die Compliance der Lunge ist bei einem Emphysem erhöht.
Bei diesem Krankheitsbild (oft durch Rauchen bedingt) ist die Lunge
leicht dehnbar, weil Wandelemente und extrazelluläre Matrix (u.a.
Elastin) zerstört wurden. Die Fläche für den Gasaustausch nimmt ab,
Bronchiolen kollabieren leicht, die Ausatmung ist erschwert, und es
kann zum Tod durch Ersticken kommen.
Lungenfibrose (z.B. Asbestlunge) führt zu erniedrigter Dehnbarkeit der Lunge; bindegewebige Strukturen sind vermehrt, die Atmung erschwert, die körperliche Belastbarkeit reduziert.
 Das
Auftreten einer offenen äußeren Verbindung zum Pleuraspalt (z.B. Stichverletzung) führt zu einem äußeren, zwischen
Pleuraspalt und Alveolen (z.B. Platzen einer
Emphysemblase) zu einem inneren Pneumothorax. In beiden
Fällen strömt Luft in den Pleuraraum, so dass sich die Lunge von der
Brustwand löst und retrahiert.
Das
Auftreten einer offenen äußeren Verbindung zum Pleuraspalt (z.B. Stichverletzung) führt zu einem äußeren, zwischen
Pleuraspalt und Alveolen (z.B. Platzen einer
Emphysemblase) zu einem inneren Pneumothorax. In beiden
Fällen strömt Luft in den Pleuraraum, so dass sich die Lunge von der
Brustwand löst und retrahiert.
Kollabiert die Lunge vollständig, so
verbleibt in ihr nur die Minimalluft (~0,2 Liter), das ist wesentlich weniger als das
Residualvolumen (~1 Liter).
Das Lungenfell kann Luft rasch resorbieren, daher kann
ein Pneumothorax spontan abheilen, sofern Luft nicht weiter in den Pleuraspalt eindringt.
 Beim Pressen zum Stuhl können kreislauflabile Menschen
(Frischoperierte!) das Bewußtsein verlieren und kollabieren (s.
Valsalva-Versuch oben).
Beim Pressen zum Stuhl können kreislauflabile Menschen
(Frischoperierte!) das Bewußtsein verlieren und kollabieren (s.
Valsalva-Versuch oben).
 Als Pneumothorax bezeichnet man eine Luftansammlung im Pleuraraum. Dieser kann
Als Pneumothorax bezeichnet man eine Luftansammlung im Pleuraraum. Dieser kann
 offen sein: Hier besteht eine Verbindung mit der Außenluft, entweder
offen sein: Hier besteht eine Verbindung mit der Außenluft, entweder
 durch eine Öffnung in der Thoraxwand (äußeres Trauma, z.B. Stichverletzung), oder
durch eine Öffnung in der Thoraxwand (äußeres Trauma, z.B. Stichverletzung), oder
 über die Luftwege, z.B. bei Rippenbruch (inneres Trauma); oder
über die Luftwege, z.B. bei Rippenbruch (inneres Trauma); oder
 geschlossen (ohne Verbindung mit der Außenluft).
geschlossen (ohne Verbindung mit der Außenluft).
Ein Spontanpneumothorax kann
bei Lungenerkrankungen (Emphysem, Tuberkulose, Astma, COPD..)
auftreten, indem bei Belastungen (Pressen, Husten) Gewebedefekte zu
einem inneren Pneumothorax führen.
Ein Spannungspneumothorax liegt
vor, wenn sich durch einen Ventilmechanismus inspiratorisch ein
Zugang zum Pleuraspalt auftut (das Loch wird gedehnt und dadurch geöffnet), der sich exspiratorisch wieder schließt (Gewebeteile legen sich über die Öffnung und verschließen sie).
Dann strömt bei jeder Einatmung Luft in den Pleuraspalt ein, die bei
der Ausatmung nicht wieder entweichen kann.
Luft sammelt sich an, der
Druck steigt, das Mediastinum wird von der betroffenen auf die
(gesunde) Gegenseite verlagert.Das belastet den Kreislauf, es kann
Blutdruckabfall, Tachykardie und Sauerstoffmangel auftreten (Notfall: Entlastungspunktion erforderlich).


 Der mit einigen ml isotoner Pleuraflüssigkeit gefüllte Pleuraspalt ermöglicht Gleitbewegungen der Lunge an der Brustwand mit geringem Widerstand. Der pleurale Druck
entspricht etwa dem intrathorakalen "Unterdruck" (Donders'scher Druck),
verursacht durch die elastische Retraktionskraft der Lunge (exspiriert -0,3 kPa, inspiriert Der mit einigen ml isotoner Pleuraflüssigkeit gefüllte Pleuraspalt ermöglicht Gleitbewegungen der Lunge an der Brustwand mit geringem Widerstand. Der pleurale Druck
entspricht etwa dem intrathorakalen "Unterdruck" (Donders'scher Druck),
verursacht durch die elastische Retraktionskraft der Lunge (exspiriert -0,3 kPa, inspiriert
~ -0,7 kPa) plus atmungsbedingte Druckschankungen in den Alveolen:
Der Druck im Pleuraraum ist die Summe aus dehnungsbedingtem (Gewebe)
und Alveolardruck
 Elastische Fasern und Kollagenfasern bewirken eine Retraktionskraft, die mit der Inspiration zunimmt. Die Oberflächenspannung der alveolären Grenzflächen (Luft / Wasser) wirkt im Sinne einer Exspiration (bis ~70% Anteil an der Retraktionskraft). Ohne dem von Alveolarepithelzellen (Typ II) produzierten Surfactant (oberflächenaktive Phospholipide) wäre die Retraktionskraft durch Oberflächenspannung um ein Mehrfaches höher, abhängig von Schichtdicke des Flüssigkeitsfilms und damit von der Atemtiefe. Die
Oberflächenspannung nimmt mit der Alveolenweite zu (Surfactant
auf größere Fläche verdünnt), überblähte Alveolen werden automatisch verkleinert (Autoregulation der Alveolenweite, "Surfactant-Bremse") Elastische Fasern und Kollagenfasern bewirken eine Retraktionskraft, die mit der Inspiration zunimmt. Die Oberflächenspannung der alveolären Grenzflächen (Luft / Wasser) wirkt im Sinne einer Exspiration (bis ~70% Anteil an der Retraktionskraft). Ohne dem von Alveolarepithelzellen (Typ II) produzierten Surfactant (oberflächenaktive Phospholipide) wäre die Retraktionskraft durch Oberflächenspannung um ein Mehrfaches höher, abhängig von Schichtdicke des Flüssigkeitsfilms und damit von der Atemtiefe. Die
Oberflächenspannung nimmt mit der Alveolenweite zu (Surfactant
auf größere Fläche verdünnt), überblähte Alveolen werden automatisch verkleinert (Autoregulation der Alveolenweite, "Surfactant-Bremse")
 Das vom N. phrenicus (C3-C5) gesteuerte Zwerchfell (Diaphragma) ist der wichtigste Inspirationsmuskel. Zusammen mit den mm. intercostales externi bewirkt es die Einatmung. Zusätzlich können Inspirationshilfsmuskeln (m. sternocleidomastoideus, mm. scaleni) wirken (starke körperliche Belastung, Ventilationsstörungen). Der
Thorax erweitert sich nach vorne und zur Seite, das Lungenvolumen
steigt, der Alveolardruck sinkt (Boyle-Mariotte), Luft strömt ein. Die Inspirationsmuskeln erhöhen die pulmonalen Rückstellkräfte, diese werden zur Ausatmung genützt Das vom N. phrenicus (C3-C5) gesteuerte Zwerchfell (Diaphragma) ist der wichtigste Inspirationsmuskel. Zusammen mit den mm. intercostales externi bewirkt es die Einatmung. Zusätzlich können Inspirationshilfsmuskeln (m. sternocleidomastoideus, mm. scaleni) wirken (starke körperliche Belastung, Ventilationsstörungen). Der
Thorax erweitert sich nach vorne und zur Seite, das Lungenvolumen
steigt, der Alveolardruck sinkt (Boyle-Mariotte), Luft strömt ein. Die Inspirationsmuskeln erhöhen die pulmonalen Rückstellkräfte, diese werden zur Ausatmung genützt
 Erschlaffen die
Inspirationsmuskeln, rückt die Lunge in die ausgeatmete Ruhelage
zurück. Bei starker körperlicher Belastung oder bei
Ventilationsstörungen unterstützen Exspirationshilfsmuskeln
die Ausatmung. Bauchmuskulatur und mm. intercostales interni erhöhen
den intraabdominellen Druck (forcierte Exspiration). Bei ruhiger Atmung
betragen die Druckschwankungen in den Alveolen einige Zehntel kPa, die
Luftströmung erreicht einen Höchstwert von <1 l/s (bei forcierter
Atmung ein Vielfaches davon - beim Niesen oder Husten bis zu mehrere
hundert km/h) Erschlaffen die
Inspirationsmuskeln, rückt die Lunge in die ausgeatmete Ruhelage
zurück. Bei starker körperlicher Belastung oder bei
Ventilationsstörungen unterstützen Exspirationshilfsmuskeln
die Ausatmung. Bauchmuskulatur und mm. intercostales interni erhöhen
den intraabdominellen Druck (forcierte Exspiration). Bei ruhiger Atmung
betragen die Druckschwankungen in den Alveolen einige Zehntel kPa, die
Luftströmung erreicht einen Höchstwert von <1 l/s (bei forcierter
Atmung ein Vielfaches davon - beim Niesen oder Husten bis zu mehrere
hundert km/h)
 Thoraxwand (entspannt bei ~75% der Totalkapazität, entsprechend mäßiger Inspiration) und Lunge (entspannt im kollabierten Zustand) sind über die Pleurablätter mechanisch verknüpft. Die
Compliance (ΔV/Δp) des Thorax nimmt mit zunehmender Inspiration zu,
diejenige der Lunge ab. Das Gesamtsystem (Lunge + Thorax) ist in
Atemruhelage (FRC) am dehnbarsten (Compliance ~1,3 l/kPa); die
Compliance der Lunge und des Thorax alleine beträgt jeweils 2-3 l/kPa. Der Kehrwert (Elastance,
Dehnungswiderstand, Volumenelastizität Δp/ΔV) ist ein Maß für die
Steifigkeit des Gewebes. Quantifizierung der Compliance erfordert
Volumen- (Spirometrie) und Druckmessungen: Der intrathorakale
(Donders'sche) Druck wird mittels Ösophagussonde ermittelt, der
Alveolardruck mittels Ganzkörperplethysmographie Thoraxwand (entspannt bei ~75% der Totalkapazität, entsprechend mäßiger Inspiration) und Lunge (entspannt im kollabierten Zustand) sind über die Pleurablätter mechanisch verknüpft. Die
Compliance (ΔV/Δp) des Thorax nimmt mit zunehmender Inspiration zu,
diejenige der Lunge ab. Das Gesamtsystem (Lunge + Thorax) ist in
Atemruhelage (FRC) am dehnbarsten (Compliance ~1,3 l/kPa); die
Compliance der Lunge und des Thorax alleine beträgt jeweils 2-3 l/kPa. Der Kehrwert (Elastance,
Dehnungswiderstand, Volumenelastizität Δp/ΔV) ist ein Maß für die
Steifigkeit des Gewebes. Quantifizierung der Compliance erfordert
Volumen- (Spirometrie) und Druckmessungen: Der intrathorakale
(Donders'sche) Druck wird mittels Ösophagussonde ermittelt, der
Alveolardruck mittels Ganzkörperplethysmographie
 Zwischen
Alveolen und Trachea nimmt der Innendruck bei forcierter Exspiration
proximalwärts ab, bis ein Punkt erreicht ist, ab dem der
intrabronchiale Druck unter den Donders'schen absinkt (negativer
transmuraler Druck) und die Luftwege kollabieren (dynamische Atemwegskompression durch Bernoulli-Effekt).
Der Kollaps erhöht den Strömungswiderstand, die
Strömungsgeschwindigkeit kann auch bei zunehmendem Pressdruck nicht
weiter ansteigen Zwischen
Alveolen und Trachea nimmt der Innendruck bei forcierter Exspiration
proximalwärts ab, bis ein Punkt erreicht ist, ab dem der
intrabronchiale Druck unter den Donders'schen absinkt (negativer
transmuraler Druck) und die Luftwege kollabieren (dynamische Atemwegskompression durch Bernoulli-Effekt).
Der Kollaps erhöht den Strömungswiderstand, die
Strömungsgeschwindigkeit kann auch bei zunehmendem Pressdruck nicht
weiter ansteigen
 Beim Pressen
kann der Alveolar- und Pleuradruck vorübergehend bis über 10 kPa ansteigen (Bereich
des arteriellen Blutdrucks: Arterien im Brustraum werden komprimiert,
der Zufluß von venösem Blut aus dem extrathorakalen Raum unterbrochen (Valsalva-Versuch: Ist die Kreislaufregulation stabil? Halten die Klappen der Extremitätenvenen dicht?).
Während des Pressens verringert sich die Vorlast des Herzens, das
Schlagvolumen (das zunächst ansteigt, oft mit kurzem Abfall der
Herzfrequenz) sinkt (die Herzfrequenz steigt). Beendet man das Pressen,
dreht sich das Muster entsprechend um Beim Pressen
kann der Alveolar- und Pleuradruck vorübergehend bis über 10 kPa ansteigen (Bereich
des arteriellen Blutdrucks: Arterien im Brustraum werden komprimiert,
der Zufluß von venösem Blut aus dem extrathorakalen Raum unterbrochen (Valsalva-Versuch: Ist die Kreislaufregulation stabil? Halten die Klappen der Extremitätenvenen dicht?).
Während des Pressens verringert sich die Vorlast des Herzens, das
Schlagvolumen (das zunächst ansteigt, oft mit kurzem Abfall der
Herzfrequenz) sinkt (die Herzfrequenz steigt). Beendet man das Pressen,
dreht sich das Muster entsprechend um
|

 Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.
Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.





 Atemmechanik
Atemmechanik
 Atelektase: ἀτελής = unvollständig, ἔκτασις = Ausdehnung
Atelektase: ἀτελής = unvollständig, ἔκτασις = Ausdehnung Retraktionskraft, Oberflächenspannung
Retraktionskraft, Oberflächenspannung  Einatmung
Einatmung  Ausatmung
Ausatmung  Pulmonale Compliance
Pulmonale Compliance  Dynamische Atemwegskompression
Dynamische Atemwegskompression  Valsalva- und Müller-Test
Valsalva- und Müller-Test
 Atelektase
Atelektase  Equal pressure point, flow limitation
Equal pressure point, flow limitation
 Core messages
Core messages
 Abbildung: Zwerchfell und Atmung
Abbildung: Zwerchfell und Atmung
 . Dieser enthält einige Milliliter Pleuraflüssigkeit. Diese transzelluläre Flüssigkeit ist
isoton und hat normalerweise einen niedrigen Eiweißgehalt (weniger als
50% des Plasmaproteinspiegels bzw. <1,2 g/dl Albumin).
. Dieser enthält einige Milliliter Pleuraflüssigkeit. Diese transzelluläre Flüssigkeit ist
isoton und hat normalerweise einen niedrigen Eiweißgehalt (weniger als
50% des Plasmaproteinspiegels bzw. <1,2 g/dl Albumin). Druck bezeichnet; der intrathorakale Raum heißt auch Donders'scher Raum). Der intrathorakale "Unterdruck" ist einer Messung mittels Speiseröhrensonde zugänglich (intraösophagealer
Druck).
Druck bezeichnet; der intrathorakale Raum heißt auch Donders'scher Raum). Der intrathorakale "Unterdruck" ist einer Messung mittels Speiseröhrensonde zugänglich (intraösophagealer
Druck).
 Abbildung: Mechanik des Thorax-Lungen-Systems
Abbildung: Mechanik des Thorax-Lungen-Systems I = normale Inspirationsstellung
I = normale Inspirationsstellung  E =
ausgeatmete Ruhelage
E =
ausgeatmete Ruhelage  ME = maximale Exspiration
ME = maximale Exspiration  K = pulmonale Kollapsposition
K = pulmonale Kollapsposition

 Der Druck im Pleuraraum
(pIP) - und damit der intrathorakale Druck - ist die Summe aus dehnungsbedingtem (Gewebe) und Alveolardruck (Luft). Er ergibt sich aus
Der Druck im Pleuraraum
(pIP) - und damit der intrathorakale Druck - ist die Summe aus dehnungsbedingtem (Gewebe) und Alveolardruck (Luft). Er ergibt sich aus  lungenseitigen
Komponenten (Luftdruck im Alveolarraum, Retraktionskräfte durch
elastische Fasern und Oberflächenspannung) und
lungenseitigen
Komponenten (Luftdruck im Alveolarraum, Retraktionskräfte durch
elastische Fasern und Oberflächenspannung) und thoraxseitigen Kräften
(Retraktionskraft in Richtung passive Ruhelage des Thorax, Kräfte aus
der Atemmuskulatur).
thoraxseitigen Kräften
(Retraktionskraft in Richtung passive Ruhelage des Thorax, Kräfte aus
der Atemmuskulatur). s. unten).
s. unten).
 Elastische Fasern tragen zu 30-50% zum Widerstand bei, der bei Einatmung zu überwinden ist.
Diese gut dehnbaren Strukturelemente sind netzförmig im Lungengewebe
eingelagert und bewirken eine Retraktionskraft, die mit der Zahl der
Fasern und ihrer Dehnung (Inspiration) zunimmt. Verringerung
ihrer Zahl oder strukturelle Zerstörung (Lungenemphysem) führt zu abnehmender Retraktionskraft der Lunge. (Über Elastin s. auch dort)
Elastische Fasern tragen zu 30-50% zum Widerstand bei, der bei Einatmung zu überwinden ist.
Diese gut dehnbaren Strukturelemente sind netzförmig im Lungengewebe
eingelagert und bewirken eine Retraktionskraft, die mit der Zahl der
Fasern und ihrer Dehnung (Inspiration) zunimmt. Verringerung
ihrer Zahl oder strukturelle Zerstörung (Lungenemphysem) führt zu abnehmender Retraktionskraft der Lunge. (Über Elastin s. auch dort) Kollagenfasern. Auch
diese rigideren - weniger dehnbaren - Fasern wirken der
Ausdehnung der Lunge entgegen; auch ihr Widerstand gegen Erweiterung
der Lunge nimmt mit der Inspiration und ihrer Zahl zu. Verringerung
ihrer Zahl führt zu abnehmender Retraktionskraft der Lunge.
Kollagenfasern. Auch
diese rigideren - weniger dehnbaren - Fasern wirken der
Ausdehnung der Lunge entgegen; auch ihr Widerstand gegen Erweiterung
der Lunge nimmt mit der Inspiration und ihrer Zahl zu. Verringerung
ihrer Zahl führt zu abnehmender Retraktionskraft der Lunge. 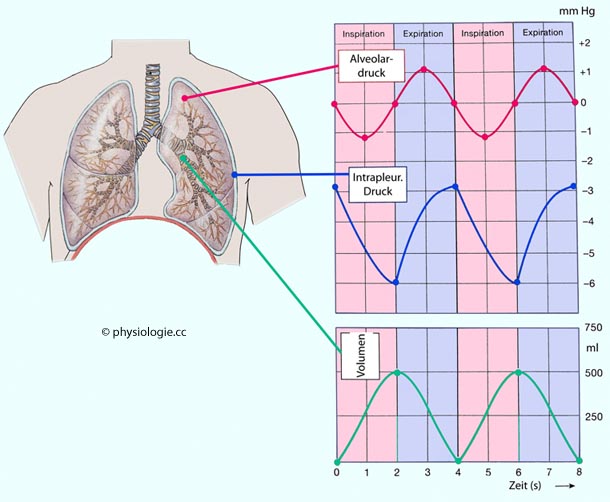
 Abbildung: Druck- Volumen- Dynamik bei normaler Atmung
Abbildung: Druck- Volumen- Dynamik bei normaler Atmung
 Oberflächenspannung: Durch
die alveolären Grenzflächen (Luft / Wasser) ergibt sich eine
Oberflächenspannung. Diese versucht, die Grenzfläche in den Alveolen
kleiner zu machen, wirkt also im Sinne einer Exspiration. Dieser Effekt wäre um ein Vielfaches größer,
wären die Alveolen nicht mit dem oberflächenspannungsvermindernden Surfactant
Oberflächenspannung: Durch
die alveolären Grenzflächen (Luft / Wasser) ergibt sich eine
Oberflächenspannung. Diese versucht, die Grenzfläche in den Alveolen
kleiner zu machen, wirkt also im Sinne einer Exspiration. Dieser Effekt wäre um ein Vielfaches größer,
wären die Alveolen nicht mit dem oberflächenspannungsvermindernden Surfactant  ausgekleidet (Problem bei Frühgeburten, RDS s. unten). Der verbleibende (reale) Betrag ist etwas größer als
die durch das elastische Fasergerüst der Lunge bewirkte Retraktionskraft.
ausgekleidet (Problem bei Frühgeburten, RDS s. unten). Der verbleibende (reale) Betrag ist etwas größer als
die durch das elastische Fasergerüst der Lunge bewirkte Retraktionskraft.
 Abbildung: Wirkungsmechanismus des Surfactant
Abbildung: Wirkungsmechanismus des Surfactant
 Als Atelektase
Als Atelektase  bezeichnet
man den Kollaps von Lungenbläschen bzw. einem Lungenabschnitt. Sie kann
im Rahmen eines
Pneumothorax (Entspannungsatelektase), durch Verlegung von Bronchien
(Obstruktionsatelektase), Einengung z.B. infolge eines Pleuraergusses
(Kompressionsatelektase), Fehlen des Luftstickstoffs bei Beatmung mit
reinem Sauerstoff (Resorptionsatelektase) auftreten. Atelektasen reduzieren den Atemgasaustausch mit der Umgebung, treten
(je nach Ursache) partiell oder komplett auf und können spontan
wieder verschwinden.
bezeichnet
man den Kollaps von Lungenbläschen bzw. einem Lungenabschnitt. Sie kann
im Rahmen eines
Pneumothorax (Entspannungsatelektase), durch Verlegung von Bronchien
(Obstruktionsatelektase), Einengung z.B. infolge eines Pleuraergusses
(Kompressionsatelektase), Fehlen des Luftstickstoffs bei Beatmung mit
reinem Sauerstoff (Resorptionsatelektase) auftreten. Atelektasen reduzieren den Atemgasaustausch mit der Umgebung, treten
(je nach Ursache) partiell oder komplett auf und können spontan
wieder verschwinden.  Abbildung).
Abbildung).
 Abbildung: Rippenbewegung
Abbildung: Rippenbewegung
 :
Bei unveränderter Temperatur - hier: Körpertemperatur - bleibt für eine
umschriebene Gasmenge das Produkt aus Druck und Volumen konstant).
Die Einatmung ist Folge der Kontraktion mehrerer Inspirationsmuskeln; der wichtigste ist das Zwerchfell. Die primäre Inspirationsmuskulatur wird bei jeder Atmung aktiviert (Zwerchfell, zahlreiche Interkostalmuskeln), die sekundäre oder akzessorische nur bei forcierter Atmung (mm. scaleni, m. sternocleidomastoideus, Hals- und Rückenmuskeln).
:
Bei unveränderter Temperatur - hier: Körpertemperatur - bleibt für eine
umschriebene Gasmenge das Produkt aus Druck und Volumen konstant).
Die Einatmung ist Folge der Kontraktion mehrerer Inspirationsmuskeln; der wichtigste ist das Zwerchfell. Die primäre Inspirationsmuskulatur wird bei jeder Atmung aktiviert (Zwerchfell, zahlreiche Interkostalmuskeln), die sekundäre oder akzessorische nur bei forcierter Atmung (mm. scaleni, m. sternocleidomastoideus, Hals- und Rückenmuskeln). aus dem Halsbereich des Rückenmarks
gesteuert. Es kontrahiert sich und flacht ab, d.h. seine
Kuppel rückt nach unten ("Bauchatmung") - bei ruhiger Atmung um etwa einen Zentimeter. Die Zwischenrippenmuskeln (mm. intercostales) helfen bei der Erweiterung des Brustraumes mit, indem sie die Rippen
anheben.
aus dem Halsbereich des Rückenmarks
gesteuert. Es kontrahiert sich und flacht ab, d.h. seine
Kuppel rückt nach unten ("Bauchatmung") - bei ruhiger Atmung um etwa einen Zentimeter. Die Zwischenrippenmuskeln (mm. intercostales) helfen bei der Erweiterung des Brustraumes mit, indem sie die Rippen
anheben.  Abbildung), insbesondere ihre oberen und dorsalen Anteile. Sie heben den Brustkorb, zusammen mit parasternalen Anteilen der inneren Interkostalmuskeln.
Abbildung), insbesondere ihre oberen und dorsalen Anteile. Sie heben den Brustkorb, zusammen mit parasternalen Anteilen der inneren Interkostalmuskeln. Zum
Brustkorb zählt man Rippen und Interkostalmuskeln, Wirbelsäule und
Zwerchfell (Diaphragma). Er enthält die Lungen (mit Pleura), das Herz
(mit Perikard), die Speiseröhre sowie Gefäße und Nerven.
Zum
Brustkorb zählt man Rippen und Interkostalmuskeln, Wirbelsäule und
Zwerchfell (Diaphragma). Er enthält die Lungen (mit Pleura), das Herz
(mit Perikard), die Speiseröhre sowie Gefäße und Nerven. Bei einem Schluckauf (Singultus, hiccup)
führt die Kombination einer unwillkürlichen Kontraktion des Zwerchfells
(Reizung des nervus phrenicus) und - einen Sekundenbruchteil später -
Verschluss der Epiglottis zu ruckartiger Reduktion des intrapulomonalen
und intrapleuralen Drucks (Inspirationsbewegung bei verschlossenem Kehlkopf). Das erzeugt das für Schluckauf charakteristische "Hicks"-Geräusch.
Bei einem Schluckauf (Singultus, hiccup)
führt die Kombination einer unwillkürlichen Kontraktion des Zwerchfells
(Reizung des nervus phrenicus) und - einen Sekundenbruchteil später -
Verschluss der Epiglottis zu ruckartiger Reduktion des intrapulomonalen
und intrapleuralen Drucks (Inspirationsbewegung bei verschlossenem Kehlkopf). Das erzeugt das für Schluckauf charakteristische "Hicks"-Geräusch.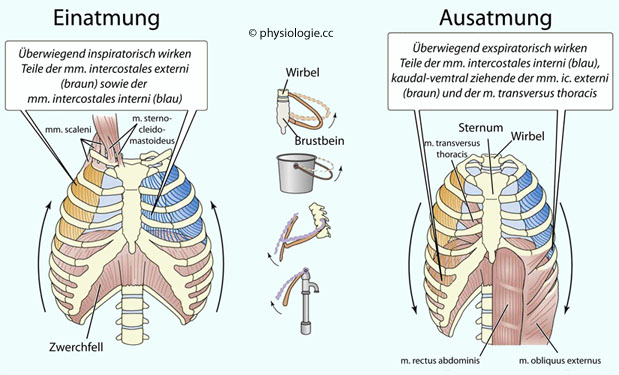
 Abbildung: Wirkung der führenden Respirationsmuskulatur
Abbildung: Wirkung der führenden Respirationsmuskulatur
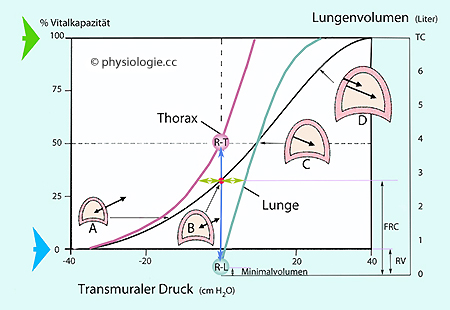
 Abbildung: Compliancekurven des respiratorischen Systems im passiven Zustand (Atemmuskeln entspannt)
Abbildung: Compliancekurven des respiratorischen Systems im passiven Zustand (Atemmuskeln entspannt)

 Abbildung oben) beginnt bei 0% Vitalkapazität bereits bei einem transmuralen Druck von ~5 cm H2O
(0,5 kPa), d.h. die Lunge ist auch schon bei dieser niedrigen
Füllung
bestrebt, sich zusammenzuziehen. Je größer das Volumen (je mehr die
Lunge gedehnt wird), desto mehr nimmt die elastische Gegenkraft zu, der
Zug nach innen wird zusehends stärker, die Dehnbarkeit der Lunge (ihre Compliance) nimmt immer mehr ab.
Abbildung oben) beginnt bei 0% Vitalkapazität bereits bei einem transmuralen Druck von ~5 cm H2O
(0,5 kPa), d.h. die Lunge ist auch schon bei dieser niedrigen
Füllung
bestrebt, sich zusammenzuziehen. Je größer das Volumen (je mehr die
Lunge gedehnt wird), desto mehr nimmt die elastische Gegenkraft zu, der
Zug nach innen wird zusehends stärker, die Dehnbarkeit der Lunge (ihre Compliance) nimmt immer mehr ab.  Zur
Überwindung der Gewebesteifigkeit (Brustwand plus Lunge) muss bei
normaler Atmung mehr Arbeit aufgebracht werden als zur Überwindung des
Strömungswiderstandes in den Luftwegen.
Zur
Überwindung der Gewebesteifigkeit (Brustwand plus Lunge) muss bei
normaler Atmung mehr Arbeit aufgebracht werden als zur Überwindung des
Strömungswiderstandes in den Luftwegen. Rechenbeispiel: Die Compliance der Lunge eines Patienten beträgt 2
l/kPa. Wie stark muss sich der transpulmonale Druck ändern, damit ein
Volumen von 500 ml geatmet werden kann?
Rechenbeispiel: Die Compliance der Lunge eines Patienten beträgt 2
l/kPa. Wie stark muss sich der transpulmonale Druck ändern, damit ein
Volumen von 500 ml geatmet werden kann? Physiologische Einflüsse auf Compliancewerte:
Der Wert der Compliance des Brustkorbs (TCC) hängt ab vom Muskeltonus
und der Form des Brustkorbes (Wirbelsäule, Rippenbögen); derjenige der
Lunge (LC) von der Oberflächenspannung in den Alveolen sowie dem
elastischen Zug des pulmonalen Bindegewebes.
Physiologische Einflüsse auf Compliancewerte:
Der Wert der Compliance des Brustkorbs (TCC) hängt ab vom Muskeltonus
und der Form des Brustkorbes (Wirbelsäule, Rippenbögen); derjenige der
Lunge (LC) von der Oberflächenspannung in den Alveolen sowie dem
elastischen Zug des pulmonalen Bindegewebes.  Ist das Volumen kleiner,
ist der Thorax nach innen gezogen worden (in Richtung Exspiration,
gewöhnlich durch den elastischen Lungenzug), und er strebt nach Erweiterung,
um wieder in seine Gleichgewichtslage zurückzukehren (negativer
transmuraler Druck zur Aufrechterhaltung dieser Position nötig).
Ist das Volumen kleiner,
ist der Thorax nach innen gezogen worden (in Richtung Exspiration,
gewöhnlich durch den elastischen Lungenzug), und er strebt nach Erweiterung,
um wieder in seine Gleichgewichtslage zurückzukehren (negativer
transmuraler Druck zur Aufrechterhaltung dieser Position nötig). Ist das Volumen größer, ist der Thorax nach außen gezogen worden (durch tiefe Inspiration der Einatemmuskulatur), und er strebt nach Verkleinerung (positiver transmuraler Druck zur Aufrechterhaltung dieser Position nötig).
Ist das Volumen größer, ist der Thorax nach außen gezogen worden (durch tiefe Inspiration der Einatemmuskulatur), und er strebt nach Verkleinerung (positiver transmuraler Druck zur Aufrechterhaltung dieser Position nötig). Der Thorax (ohne Muskelaktivität) hat
eine Ruhelage, die er (für sich alleine) spontan einnimmt (Abb.: Inset C),
entsprechend einer mäßigen Inspirationslage (Compliancekurve bei null
transmuralem Druck). Wird er verkleinert, hat er das Bestreben, sich zu
erweitern (nach außen gerichtete Pfeile in A und B), wird er weiter
expandiert, hat er das Bestreben, kleiner zu werden (nach innen
gerichteter Pfeil in D)
Der Thorax (ohne Muskelaktivität) hat
eine Ruhelage, die er (für sich alleine) spontan einnimmt (Abb.: Inset C),
entsprechend einer mäßigen Inspirationslage (Compliancekurve bei null
transmuralem Druck). Wird er verkleinert, hat er das Bestreben, sich zu
erweitern (nach außen gerichtete Pfeile in A und B), wird er weiter
expandiert, hat er das Bestreben, kleiner zu werden (nach innen
gerichteter Pfeil in D) Die Lunge
hat ein Druck-Verhalten wie ein elastischer Ball; ihr Inhalt nimmt
mit steigendem Füllungsdruck zu. Auf sich alleine
gestellt würde sie sich praktisch vollständig zusammenziehen
(kollabieren); das geschieht bei einem Pneumothorax
Die Lunge
hat ein Druck-Verhalten wie ein elastischer Ball; ihr Inhalt nimmt
mit steigendem Füllungsdruck zu. Auf sich alleine
gestellt würde sie sich praktisch vollständig zusammenziehen
(kollabieren); das geschieht bei einem Pneumothorax  (s. ganz unten)
(s. ganz unten) Das Gesamtsystem
(Abb.: durchgezogene Kurve) ist in Atemruhelage im Kräftegleichgewicht und
enthält definitionsgemäß die funktionelle Residualkapazität (FRC,
roter Punkt): Hier sind die nach außen (Thorax) und innen (Lunge)
gerichteten Kräfte im Gleichgewicht: Strichlierte und punktierte
Compliancekurven weisen denselben transmuralen Druckbetrag auf - Thorax
negativ, Lunge positiv, die Druckbeträge kompensieren einander, Pfeile
im Zustand "B" (gleicher Abstand des roten Punkts zu Thorax- und Lungenkurve)
Das Gesamtsystem
(Abb.: durchgezogene Kurve) ist in Atemruhelage im Kräftegleichgewicht und
enthält definitionsgemäß die funktionelle Residualkapazität (FRC,
roter Punkt): Hier sind die nach außen (Thorax) und innen (Lunge)
gerichteten Kräfte im Gleichgewicht: Strichlierte und punktierte
Compliancekurven weisen denselben transmuralen Druckbetrag auf - Thorax
negativ, Lunge positiv, die Druckbeträge kompensieren einander, Pfeile
im Zustand "B" (gleicher Abstand des roten Punkts zu Thorax- und Lungenkurve) Man unterscheidet statische und dynamische Compliance:
Man unterscheidet statische und dynamische Compliance:  Die statische Compliance wird bei Atemruhe
ermittelt, wenn also keine Luft durch die Atemwege strömt. Methode: Die
Einatmung erfolgt stufenweise (z.B. in 500-ml-Schritten), jeweils in
den Atempausen wird der intrapleurale Druck ermittelt
(Oesophagus-Ballonkatheter).
Die statische Compliance wird bei Atemruhe
ermittelt, wenn also keine Luft durch die Atemwege strömt. Methode: Die
Einatmung erfolgt stufenweise (z.B. in 500-ml-Schritten), jeweils in
den Atempausen wird der intrapleurale Druck ermittelt
(Oesophagus-Ballonkatheter).  Abbildung, links):
Abbildung, links): Bei niedrigem Volumen ist die Druck-Volumen-Charakteristik flach (geringe Compliance)
Bei niedrigem Volumen ist die Druck-Volumen-Charakteristik flach (geringe Compliance) Im normalen "Ruhebereich" ist die Kurve steil (hohe Compliance, System gut dehnbar)
Im normalen "Ruhebereich" ist die Kurve steil (hohe Compliance, System gut dehnbar)  Bei hohen Druck- und Volumenwerten verflacht die Charakteristik wieder (geringe Compliance)
Bei hohen Druck- und Volumenwerten verflacht die Charakteristik wieder (geringe Compliance) Eine dynamische Compliance lässt sich aus Druck- und Volumenverläufen während kontinuierlicher Atmung
ableiten, wenn also die fortlaufenden Messungen nicht durch Ruhepunkte
unterbrochen werden (
Eine dynamische Compliance lässt sich aus Druck- und Volumenverläufen während kontinuierlicher Atmung
ableiten, wenn also die fortlaufenden Messungen nicht durch Ruhepunkte
unterbrochen werden ( Abbildung, rechts).
Abbildung, rechts). 
 Abbildung: Druck-Volumen- Diagramme normaler Atemzyklen
Abbildung: Druck-Volumen- Diagramme normaler Atemzyklen
 Der intrathorakale (Donders'sche)
- und damit intrapleurale - Druck kann mittels Ösophagussonde ermittelt werden (
Der intrathorakale (Donders'sche)
- und damit intrapleurale - Druck kann mittels Ösophagussonde ermittelt werden ( Abbildung - die Speiseröhre
durchzieht den Donders'schen Raum):
Abbildung - die Speiseröhre
durchzieht den Donders'schen Raum): 
 Abbildung: Messung des intrapleuralen Drucks
Abbildung: Messung des intrapleuralen Drucks
 Der Alveolardruck kann u.a. mittels Ganzkörperplethysmographie ermittelt werden.
Der Alveolardruck kann u.a. mittels Ganzkörperplethysmographie ermittelt werden.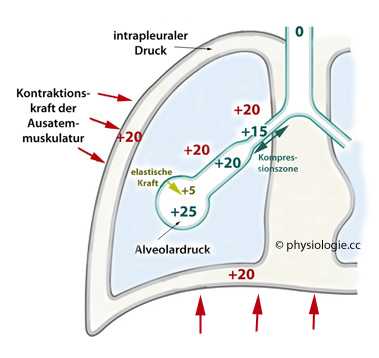
 Abbildung: Dynamische Atemwegskompression (schematisch)
Abbildung: Dynamische Atemwegskompression (schematisch)
 Abbildung
dargelegt, werden bei forcierter Ausatmung durch den Anstieg des
Donders'schen Drucks über den Betrag des atmosphärischen Drucks hinaus
die Atemwege komprimiert - der Atemwegwiderstand steigt. Erklärbar ist dieses Phänomen durch den Bernoulli-Effekt: Strömt ein Gas oder eine Flüssigkeit entlang einer Struktur (z.B. der
Wand eines Bronchus), nimmt mit zunehmender Geschwindigkeit der Druck
senkrecht zur Strömungsrichtung ab (
Abbildung
dargelegt, werden bei forcierter Ausatmung durch den Anstieg des
Donders'schen Drucks über den Betrag des atmosphärischen Drucks hinaus
die Atemwege komprimiert - der Atemwegwiderstand steigt. Erklärbar ist dieses Phänomen durch den Bernoulli-Effekt: Strömt ein Gas oder eine Flüssigkeit entlang einer Struktur (z.B. der
Wand eines Bronchus), nimmt mit zunehmender Geschwindigkeit der Druck
senkrecht zur Strömungsrichtung ab ( vgl. dort).
vgl. dort). Als Equal pressure point (EPP)
bezeichnet man den Druck, bei dem während der Ausatmung der transmurale
Druck der Luftwege 0 beträgt, d.h. der Druck in den Bronchien gleich
hoch ist wie der intrapleurale Druck. Flow limitation ist ein EPP-Zustand in peripheren Atemwegen, bei dem die Strömung trotz Anstieg des Druckgradienten nicht ansteigt.
Als Equal pressure point (EPP)
bezeichnet man den Druck, bei dem während der Ausatmung der transmurale
Druck der Luftwege 0 beträgt, d.h. der Druck in den Bronchien gleich
hoch ist wie der intrapleurale Druck. Flow limitation ist ein EPP-Zustand in peripheren Atemwegen, bei dem die Strömung trotz Anstieg des Druckgradienten nicht ansteigt.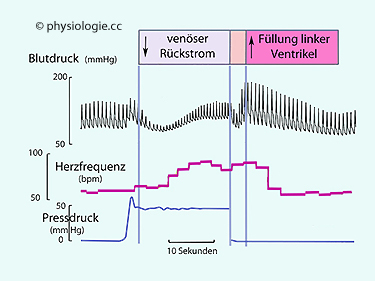
 Abbildung: Valsalva-Versuch
Abbildung: Valsalva-Versuch
 Versucht man - Nase und Mund
geschlossen - mit größter Kraft einzuatmen,
so kann der Druck in Lunge und Pleuraspalt bis auf -120 cm H2O
absinken (Müller-Versuch).
Klinisch kann dieses Verfahren Aufschluss über allfällige Schwächen im
Bereich der oberen Luftwege geben, der Versuch dient u.a. zur
Aufklärung von Ursachen einer Schlafapnoe.
Versucht man - Nase und Mund
geschlossen - mit größter Kraft einzuatmen,
so kann der Druck in Lunge und Pleuraspalt bis auf -120 cm H2O
absinken (Müller-Versuch).
Klinisch kann dieses Verfahren Aufschluss über allfällige Schwächen im
Bereich der oberen Luftwege geben, der Versuch dient u.a. zur
Aufklärung von Ursachen einer Schlafapnoe. Beim Pressen kann der Druck bis auf +180 cm H2O (fast 1/5
Atmosphäre) steigen (Valsalva-Pressversuch
Beim Pressen kann der Druck bis auf +180 cm H2O (fast 1/5
Atmosphäre) steigen (Valsalva-Pressversuch  ,
,  Abbildung).
Das bedeutet, dass man beim Pressen im Bauch-und Brustraum einen Druck
ausüben kann, der über dem arteriellen Blutdruckwert liegt.
Abbildung).
Das bedeutet, dass man beim Pressen im Bauch-und Brustraum einen Druck
ausüben kann, der über dem arteriellen Blutdruckwert liegt.  Phase 1 - Die Pulmonalgefäße werden durch den erhöhten Pressdruck
Richtung linkes Herz entleert, das Schlagvolumen steigt an, der
arterielle Blutdruck steigt vorübergehend kurz an, reflektorisch kann
die Herzfrequenz leicht absinken
Phase 1 - Die Pulmonalgefäße werden durch den erhöhten Pressdruck
Richtung linkes Herz entleert, das Schlagvolumen steigt an, der
arterielle Blutdruck steigt vorübergehend kurz an, reflektorisch kann
die Herzfrequenz leicht absinken Phase 2 - Der hohe intrathorakale Druck behindert den venösen
Rückstrom, Schlagvolumen und arterieller Druck nehmen ab, reflektorisch
steigt die Herzfrequenz
Phase 2 - Der hohe intrathorakale Druck behindert den venösen
Rückstrom, Schlagvolumen und arterieller Druck nehmen ab, reflektorisch
steigt die Herzfrequenz Phase 3 - Nach 10 Sekunden wird abgebrochen. Die Venen im Brustraum
füllen sich, Schlagvolumen und Blutdruck sinken, die Herzfrequenz
steigt reflektorisch an
Phase 3 - Nach 10 Sekunden wird abgebrochen. Die Venen im Brustraum
füllen sich, Schlagvolumen und Blutdruck sinken, die Herzfrequenz
steigt reflektorisch an Phase 4 - Die linksventrikuläre Vorlast normalisiert sich. Da die
Herzfrequenz noch erhöht ist, steigt der Blutdruck vorübergehend an.
Reflektorisch erhöhte parasympathische Aktivität bringt dann Blutdruck
und Herzfrequenz zu Normalwerten zurück.
Phase 4 - Die linksventrikuläre Vorlast normalisiert sich. Da die
Herzfrequenz noch erhöht ist, steigt der Blutdruck vorübergehend an.
Reflektorisch erhöhte parasympathische Aktivität bringt dann Blutdruck
und Herzfrequenz zu Normalwerten zurück. der Kreislauftestung: Während des
Pressens verringert sich die Vorlast des Herzens, das Schlagvolumen -
das zunächst durch die direkte Druckwirkung für kurze Zeit ansteigt
(oft mit durch den Baroreflex bedingtem kurzem Abfall der Herzfrequenz)
- sinkt kontinuierlich, und die Herzfrequenz nimmt zu. Nachher dreht
sich das Muster entsprechend um
der Kreislauftestung: Während des
Pressens verringert sich die Vorlast des Herzens, das Schlagvolumen -
das zunächst durch die direkte Druckwirkung für kurze Zeit ansteigt
(oft mit durch den Baroreflex bedingtem kurzem Abfall der Herzfrequenz)
- sinkt kontinuierlich, und die Herzfrequenz nimmt zu. Nachher dreht
sich das Muster entsprechend um dem Druckausgleich im Mittelohr über die tuba Eustachii bei
zunehmendem Außendruck (sinkende Meereshöhe, Landeanflug mit dem
Flugzeug)
dem Druckausgleich im Mittelohr über die tuba Eustachii bei
zunehmendem Außendruck (sinkende Meereshöhe, Landeanflug mit dem
Flugzeug) der Untersuchung von Extremitätenvenen (halten die Venenklappen bei zentralem Druckanstieg dicht?)
der Untersuchung von Extremitätenvenen (halten die Venenklappen bei zentralem Druckanstieg dicht?) einer Beendigung supraventrikulärer Tachykardie
einer Beendigung supraventrikulärer Tachykardie
 Die
von Antonio Vaslsalva (1666-1723) beschriebene Methode zur Erhöhung des
Luftdrucks im Rachenraum diente ursprünglich u.a. zum Test der
Tubendichtigkeit und zum Austreiben von Eiter aus dem Mittelohr.
Die
von Antonio Vaslsalva (1666-1723) beschriebene Methode zur Erhöhung des
Luftdrucks im Rachenraum diente ursprünglich u.a. zum Test der
Tubendichtigkeit und zum Austreiben von Eiter aus dem Mittelohr.
 Das
Auftreten einer offenen äußeren Verbindung zum Pleuraspalt (z.B. Stichverletzung) führt zu einem äußeren, zwischen
Pleuraspalt und Alveolen (z.B. Platzen einer
Emphysemblase) zu einem inneren Pneumothorax. In beiden
Fällen strömt Luft in den Pleuraraum, so dass sich die Lunge von der
Brustwand löst und retrahiert.
Das
Auftreten einer offenen äußeren Verbindung zum Pleuraspalt (z.B. Stichverletzung) führt zu einem äußeren, zwischen
Pleuraspalt und Alveolen (z.B. Platzen einer
Emphysemblase) zu einem inneren Pneumothorax. In beiden
Fällen strömt Luft in den Pleuraraum, so dass sich die Lunge von der
Brustwand löst und retrahiert.  Beim Pressen zum Stuhl können kreislauflabile Menschen
(Frischoperierte!) das Bewußtsein verlieren und kollabieren (s.
Valsalva-Versuch oben).
Beim Pressen zum Stuhl können kreislauflabile Menschen
(Frischoperierte!) das Bewußtsein verlieren und kollabieren (s.
Valsalva-Versuch oben). Als Pneumothorax bezeichnet man eine Luftansammlung im Pleuraraum. Dieser kann
Als Pneumothorax bezeichnet man eine Luftansammlung im Pleuraraum. Dieser kann  offen sein: Hier besteht eine Verbindung mit der Außenluft, entweder
offen sein: Hier besteht eine Verbindung mit der Außenluft, entweder  durch eine Öffnung in der Thoraxwand (äußeres Trauma, z.B. Stichverletzung), oder
durch eine Öffnung in der Thoraxwand (äußeres Trauma, z.B. Stichverletzung), oder über die Luftwege, z.B. bei Rippenbruch (inneres Trauma); oder
über die Luftwege, z.B. bei Rippenbruch (inneres Trauma); oder geschlossen (ohne Verbindung mit der Außenluft).
geschlossen (ohne Verbindung mit der Außenluft).
 Der mit einigen ml isotoner Pleuraflüssigkeit gefüllte Pleuraspalt ermöglicht Gleitbewegungen der Lunge an der Brustwand mit geringem Widerstand. Der pleurale Druck
entspricht etwa dem intrathorakalen "Unterdruck" (Donders'scher Druck),
verursacht durch die elastische Retraktionskraft der Lunge (exspiriert -0,3 kPa, inspiriert
Der mit einigen ml isotoner Pleuraflüssigkeit gefüllte Pleuraspalt ermöglicht Gleitbewegungen der Lunge an der Brustwand mit geringem Widerstand. Der pleurale Druck
entspricht etwa dem intrathorakalen "Unterdruck" (Donders'scher Druck),
verursacht durch die elastische Retraktionskraft der Lunge (exspiriert -0,3 kPa, inspiriert Elastische Fasern und Kollagenfasern bewirken eine Retraktionskraft, die mit der Inspiration zunimmt. Die Oberflächenspannung der alveolären Grenzflächen (Luft / Wasser) wirkt im Sinne einer Exspiration (bis ~70% Anteil an der Retraktionskraft). Ohne dem von Alveolarepithelzellen (Typ II) produzierten Surfactant (oberflächenaktive Phospholipide) wäre die Retraktionskraft durch Oberflächenspannung um ein Mehrfaches höher, abhängig von Schichtdicke des Flüssigkeitsfilms und damit von der Atemtiefe. Die
Oberflächenspannung nimmt mit der Alveolenweite zu (Surfactant
auf größere Fläche verdünnt), überblähte Alveolen werden automatisch verkleinert (Autoregulation der Alveolenweite, "Surfactant-Bremse")
Elastische Fasern und Kollagenfasern bewirken eine Retraktionskraft, die mit der Inspiration zunimmt. Die Oberflächenspannung der alveolären Grenzflächen (Luft / Wasser) wirkt im Sinne einer Exspiration (bis ~70% Anteil an der Retraktionskraft). Ohne dem von Alveolarepithelzellen (Typ II) produzierten Surfactant (oberflächenaktive Phospholipide) wäre die Retraktionskraft durch Oberflächenspannung um ein Mehrfaches höher, abhängig von Schichtdicke des Flüssigkeitsfilms und damit von der Atemtiefe. Die
Oberflächenspannung nimmt mit der Alveolenweite zu (Surfactant
auf größere Fläche verdünnt), überblähte Alveolen werden automatisch verkleinert (Autoregulation der Alveolenweite, "Surfactant-Bremse") Das vom N. phrenicus (C3-C5) gesteuerte Zwerchfell (Diaphragma) ist der wichtigste Inspirationsmuskel. Zusammen mit den mm. intercostales externi bewirkt es die Einatmung. Zusätzlich können Inspirationshilfsmuskeln (m. sternocleidomastoideus, mm. scaleni) wirken (starke körperliche Belastung, Ventilationsstörungen). Der
Thorax erweitert sich nach vorne und zur Seite, das Lungenvolumen
steigt, der Alveolardruck sinkt (Boyle-Mariotte), Luft strömt ein. Die Inspirationsmuskeln erhöhen die pulmonalen Rückstellkräfte, diese werden zur Ausatmung genützt
Das vom N. phrenicus (C3-C5) gesteuerte Zwerchfell (Diaphragma) ist der wichtigste Inspirationsmuskel. Zusammen mit den mm. intercostales externi bewirkt es die Einatmung. Zusätzlich können Inspirationshilfsmuskeln (m. sternocleidomastoideus, mm. scaleni) wirken (starke körperliche Belastung, Ventilationsstörungen). Der
Thorax erweitert sich nach vorne und zur Seite, das Lungenvolumen
steigt, der Alveolardruck sinkt (Boyle-Mariotte), Luft strömt ein. Die Inspirationsmuskeln erhöhen die pulmonalen Rückstellkräfte, diese werden zur Ausatmung genützt  Erschlaffen die
Inspirationsmuskeln, rückt die Lunge in die ausgeatmete Ruhelage
zurück. Bei starker körperlicher Belastung oder bei
Ventilationsstörungen unterstützen Exspirationshilfsmuskeln
die Ausatmung. Bauchmuskulatur und mm. intercostales interni erhöhen
den intraabdominellen Druck (forcierte Exspiration). Bei ruhiger Atmung
betragen die Druckschwankungen in den Alveolen einige Zehntel kPa, die
Luftströmung erreicht einen Höchstwert von <1 l/s (bei forcierter
Atmung ein Vielfaches davon - beim Niesen oder Husten bis zu mehrere
hundert km/h)
Erschlaffen die
Inspirationsmuskeln, rückt die Lunge in die ausgeatmete Ruhelage
zurück. Bei starker körperlicher Belastung oder bei
Ventilationsstörungen unterstützen Exspirationshilfsmuskeln
die Ausatmung. Bauchmuskulatur und mm. intercostales interni erhöhen
den intraabdominellen Druck (forcierte Exspiration). Bei ruhiger Atmung
betragen die Druckschwankungen in den Alveolen einige Zehntel kPa, die
Luftströmung erreicht einen Höchstwert von <1 l/s (bei forcierter
Atmung ein Vielfaches davon - beim Niesen oder Husten bis zu mehrere
hundert km/h) Thoraxwand (entspannt bei ~75% der Totalkapazität, entsprechend mäßiger Inspiration) und Lunge (entspannt im kollabierten Zustand) sind über die Pleurablätter mechanisch verknüpft. Die
Compliance (ΔV/Δp) des Thorax nimmt mit zunehmender Inspiration zu,
diejenige der Lunge ab. Das Gesamtsystem (Lunge + Thorax) ist in
Atemruhelage (FRC) am dehnbarsten (Compliance ~1,3 l/kPa); die
Compliance der Lunge und des Thorax alleine beträgt jeweils 2-3 l/kPa. Der Kehrwert (Elastance,
Dehnungswiderstand, Volumenelastizität Δp/ΔV) ist ein Maß für die
Steifigkeit des Gewebes. Quantifizierung der Compliance erfordert
Volumen- (Spirometrie) und Druckmessungen: Der intrathorakale
(Donders'sche) Druck wird mittels Ösophagussonde ermittelt, der
Alveolardruck mittels Ganzkörperplethysmographie
Thoraxwand (entspannt bei ~75% der Totalkapazität, entsprechend mäßiger Inspiration) und Lunge (entspannt im kollabierten Zustand) sind über die Pleurablätter mechanisch verknüpft. Die
Compliance (ΔV/Δp) des Thorax nimmt mit zunehmender Inspiration zu,
diejenige der Lunge ab. Das Gesamtsystem (Lunge + Thorax) ist in
Atemruhelage (FRC) am dehnbarsten (Compliance ~1,3 l/kPa); die
Compliance der Lunge und des Thorax alleine beträgt jeweils 2-3 l/kPa. Der Kehrwert (Elastance,
Dehnungswiderstand, Volumenelastizität Δp/ΔV) ist ein Maß für die
Steifigkeit des Gewebes. Quantifizierung der Compliance erfordert
Volumen- (Spirometrie) und Druckmessungen: Der intrathorakale
(Donders'sche) Druck wird mittels Ösophagussonde ermittelt, der
Alveolardruck mittels Ganzkörperplethysmographie Zwischen
Alveolen und Trachea nimmt der Innendruck bei forcierter Exspiration
proximalwärts ab, bis ein Punkt erreicht ist, ab dem der
intrabronchiale Druck unter den Donders'schen absinkt (negativer
transmuraler Druck) und die Luftwege kollabieren (dynamische Atemwegskompression durch Bernoulli-Effekt).
Der Kollaps erhöht den Strömungswiderstand, die
Strömungsgeschwindigkeit kann auch bei zunehmendem Pressdruck nicht
weiter ansteigen
Zwischen
Alveolen und Trachea nimmt der Innendruck bei forcierter Exspiration
proximalwärts ab, bis ein Punkt erreicht ist, ab dem der
intrabronchiale Druck unter den Donders'schen absinkt (negativer
transmuraler Druck) und die Luftwege kollabieren (dynamische Atemwegskompression durch Bernoulli-Effekt).
Der Kollaps erhöht den Strömungswiderstand, die
Strömungsgeschwindigkeit kann auch bei zunehmendem Pressdruck nicht
weiter ansteigen Beim Pressen
kann der Alveolar- und Pleuradruck vorübergehend bis über 10 kPa ansteigen (Bereich
des arteriellen Blutdrucks: Arterien im Brustraum werden komprimiert,
der Zufluß von venösem Blut aus dem extrathorakalen Raum unterbrochen (Valsalva-Versuch: Ist die Kreislaufregulation stabil? Halten die Klappen der Extremitätenvenen dicht?).
Während des Pressens verringert sich die Vorlast des Herzens, das
Schlagvolumen (das zunächst ansteigt, oft mit kurzem Abfall der
Herzfrequenz) sinkt (die Herzfrequenz steigt). Beendet man das Pressen,
dreht sich das Muster entsprechend um
Beim Pressen
kann der Alveolar- und Pleuradruck vorübergehend bis über 10 kPa ansteigen (Bereich
des arteriellen Blutdrucks: Arterien im Brustraum werden komprimiert,
der Zufluß von venösem Blut aus dem extrathorakalen Raum unterbrochen (Valsalva-Versuch: Ist die Kreislaufregulation stabil? Halten die Klappen der Extremitätenvenen dicht?).
Während des Pressens verringert sich die Vorlast des Herzens, das
Schlagvolumen (das zunächst ansteigt, oft mit kurzem Abfall der
Herzfrequenz) sinkt (die Herzfrequenz steigt). Beendet man das Pressen,
dreht sich das Muster entsprechend um 