

Eine Reise durch die Physiologie - Wie der Körper des Menschen funktioniert


 Leistungsfähigkeit der Muskulatur
Leistungsfähigkeit der Muskulatur
© H. Hinghofer-Szalkay

Calsequestrin: calx = Kreide, Kalkstein (Calcium), sequester = Vermittler (von sequere = folgen)
isometrisch: ἴσος = gleich, μέτρον = Maß
isotonisch: ἴσος = gleich, τόνος = Spannung
Phospholamban: "Phosphor-Rezeptor" (λαμβἀνειν = erhalten)
plyometrisch: πλειων = mehr, μέτρον = Maß, Länge
Skelettmuskeln beziehen den Großteil ihres Energiestoffwechsels über Triglyzeride, außer bei (kurzdauernder) Höchstleistung, wo der Anteil der Glucose
mehrfach ansteigt und für bis zu 75% der ATP-Synthese genutzt wird -
unterstützt durch Lyse von Muskelglykogen, aber auch Nutzung von Blutzucker
(glucosesenkende Wirkung körperlicher Arbeit). Der Sympathikus
unterstützt diese Umstellung über ß2-Adrenozeptoren.
Die Energiegewinnung unter Sauerstoffverbrauch (aerobe Kapazität) geht bis zur anaeroben Schwelle,
bei der das kardiovaskulär-pulmonale System (Atmung, Durchblutung)
seine Leistungsgrenze erreicht - darüber hinaus kann ATP nur laktazid
(Abbau bis Brenztraubensäure → Lactat) gewonnen werden (Abfall des
Blut-pH: nicht-respiratorische Azidose).
Mit "Sauerstoffschuld" meint man diejenige
Menge O2,
die während der Muskelbelastung für oxidative Energiegewinnung genutzt
hätte werden können, aber wegen beschränkter Transportkapazität
(Durchblutung) nicht zur Verfügung stand. Sie wird typischerweise nach der Belastung
zur Wiederherstellung des Ruhezustandes verbraucht ("nachgezahlt").
Muskelfasern spezialisieren sich auf bestimmte Belastungformen. Man unterscheidet Myozyten vom
-- Typ I (slow-twich) -
gut kapillarisiert, schmal, myoglobinreich ("rote" Muskelfasern), mit
hoher aerober Kapazität - sie sind auf langanhaltende, mäßige Belastung
spezialisiert (Haltemuskulatur)
-- Typ II (fast-twitch) - wenig Mitochondrien und Myoglobin ("weiße"
Muskelfasern), rasch ermüdend, aber sehr schnell - ideal für flinke
Motorik und zur kurzen Entwicklung von Spitzenkraft.
|
Zustand der Muskelfaser  Energiestoffwechsel des Muskels
Energiestoffwechsel des Muskels  Muskeldurchblutung und Substratangebot
Muskeldurchblutung und Substratangebot  Aerob vs. anerob, Leistungsbereich
Aerob vs. anerob, Leistungsbereich  Länge, Kraft, Geschwindigkeit, Kontraktionsformen
Länge, Kraft, Geschwindigkeit, Kontraktionsformen  Muskeltraining
Muskeltraining  Fast- und Slow-twitch-Fasern
Fast- und Slow-twitch-Fasern
 Physiologie des Laufens
Physiologie des Laufens  Belastung und Muskelkater
Belastung und Muskelkater
 Aerobe Kapazität
Aerobe Kapazität  Sauerstoffschuld
Sauerstoffschuld

Core messages
Entspannung und Kontraktion
Die graphische Darstellung des
Verhältnisses zwischen Länge und Kraft einer Muskelfaser sagt viel über
deren Zustand aus ( Abbildung):
Abbildung):
 Abbildung: Ruhedehnungs- und isometrische Kontraktionsmaximums-Kurven
Abbildung: Ruhedehnungs- und isometrische Kontraktionsmaximums-Kurven
Nach einer Vorlage bei physio-pepia.com
Ein
Muskelpräparat wird zu verschiedenen Längen gedehnt.
Blaue Kurve: Passives Verhalten (Ruhedehnungskurve).
Grüne Kurve: Gemessene Kraft bei maximaler Reizung (elektrisch) unter isometrischen Bedingungen (Länge bleibt jeweils gleich).
Rote Kurve: Die Differenz der jeweils beiden Beträge ist durch die Kontraktion der Sarkomeren bedingt (aktiver Kraftanteil)

Die Ruhedehnungskurve
stellt das "passive" mechanische Verhalten des Muskels dar - je stärker
dieser gedehnt wird, desto mehr kommen Rückstellkräfte aus den
bindegewebigen Strukturen zum Vorschein (kollagene und elastische
Fasern u.a.).
Wird der Muskel gereizt, kontrahiert er und es
kommen "aktive" Kraftkomponenten dazu, die aus der Interaktion von
Aktin- und Myosinfilamenten in den Sarkomeren stammen. Dadurch ergeben
sich z.B. Kurven, welche definierte Kontraktionszustände beschreiben
(isotonische, isometrische, auxotonische Maxima usw).
Mit solchen Diagrammen lassen sich quantitative Aussagen über Zustand
und Verhalten von Muskelfasern (verschiedenen Typs) treffen. Der
Nachteil dieser Darstellungsform ist, dass solche Registrierungen kaum
in vivo, sondern hauptsächlich an isolierten Muskelpräparaten
vorgenommen werden können.
Voraussetzung
für Funktion und Leistungsfähigkeit der Muskulatur in vivo ist ihre adäquate
Versorgung mit Nährstoffen, Elektrolyten, Wachstumsfaktoren und Atemgas
(Durchblutung) sowie entsprechende Anregung durch das Nervensystem (motorische Vorderhornzellen). Die Aktivierung der Muskeln muss rasch erfolgen, dementsprechend werden sie durch schnell leitende Nervenfasern
versorgt, sowohl motorisch als auch sensorisch.
Arbeit und Leistung: Im physikalischen Sinne ist Arbeit als Kraft mal Weg (J = N.m), Leistung
als Arbeit pro Zeit (W = J/s) definiert. Kraft (force)
ist zur Beschleunigung einer Masse vonnöten; 1 Newton (N) ist z.B. die
Kraft, die man etwa braucht, um einen Apfel gegen den Effekt der
Schwerkraft (9,81 m.s-2) zu halten (1 N = 1 kg.m.s-2). Multipliziert man die Kraft mit dem Weg, entlang den die Masse bewegt wird, ergibt sich Arbeit (work) (1 J = 1 kg.m2.s-2); auch Energie (energy)
- z.B. Wärmeenergie - hat diese Dimension (z.B. kann die vollständige
Oxidation von einem Gramm Kohlenhydrat 17 kJ Arbeit leisten / Wärme
freisetzen: "Brennwert"). Leistung (power) schließlich ist die Menge an Arbeit (Energie), die für eine bestimmte Zeit vollbracht (freigesetzt) wird (1 W = 1 J.s-1).
Woher bezieht der Muskel seine Stoffwechselenergie? Das für den Antrieb
des kontraktilen Apparats notwendige ATP kann nur in minimaler Menge
gespeichert werden; eine erste Reserve bietet Kreatinphosphat (CP),
aber auch dieser Vorrat ist in Sekundenschnelle erschöpft ( Abbildung).
Abbildung).
 Über Kreatinphosphat s. dort
Über Kreatinphosphat s. dort

 Abbildung: Energiequellen bei Muskelarbeit
Modifiziert nach Edington DW, Edgerton VR. The biology of physical activity. Boston, Houghton Mifflin 1976
Abbildung: Energiequellen bei Muskelarbeit
Modifiziert nach Edington DW, Edgerton VR. The biology of physical activity. Boston, Houghton Mifflin 1976
Die unmittelbar verfügbaren Energiespeicher
für die Kontraktionsaktivität - ATP, Kreatinphosphat (CP) - sind zu Beginn
die einzige Energiequelle, innerhalb höchstens der ersten Minute der
Muskelaktivität aber erschöpft.
Anaerobe Glykolyse stellt den nächsten Energielieferanten dar, dieses
System stellt innerhalb einer Minute seinen Maximalbeitrag zur
Verfügung. Dieses System ist nur limitiert nutzbar, Lactat reichert
sich im Gewebe an (metabolische Azidose), die Effizienz der
Energiegewinnung ist limitiert.
Verzögert, aber fast unbegrenzt verfügbar ist oxidative
Energiegewinnung aus Kohlenhydraten und (spätestens wenn diese Speicher
auch zur Neige gehen) Fettsäuren, die aus dem enormen Energiedepot des
Fettgewebes gespeist werden
 Unmittelbarer Energielieferant für die Muskelkontraktion ist Adenosintriphosphat (ATP).
Wird der Muskel aktiviert, verbraucht sich das unmittelbar verfügbare
ATP (reicht für ca. 5 Kontraktionen) innerhalb weniger Sekunden. Die Art der anschließend zum
"Nachladen" des ATP-Pools verwendeten Energiequellen hängt von Dauer
und Profil der Muskelaktivität ab (
Unmittelbarer Energielieferant für die Muskelkontraktion ist Adenosintriphosphat (ATP).
Wird der Muskel aktiviert, verbraucht sich das unmittelbar verfügbare
ATP (reicht für ca. 5 Kontraktionen) innerhalb weniger Sekunden. Die Art der anschließend zum
"Nachladen" des ATP-Pools verwendeten Energiequellen hängt von Dauer
und Profil der Muskelaktivität ab ( Abbildung):
Abbildung):
 Kurzzeitig wird ATP aus einem in der Muskelzelle angelegten Speicher von Kreatinphosphat
(CP) nachgebildet - unter Wirkung der Kreatinkinase (Abbildungen). Dieser
Energievorrat reicht für 10-20 Sekunden
oder bis zu 50 Kontraktionen, dann ist er (bei fortgesetzter
Muskelaktivität) gänzlich erschöpft. In Situationen plötzlicher extremer Herausforderung (fight or flight) kann dieser Mechanismus von überlebenswichtiger Bedeutung sein.
Kurzzeitig wird ATP aus einem in der Muskelzelle angelegten Speicher von Kreatinphosphat
(CP) nachgebildet - unter Wirkung der Kreatinkinase (Abbildungen). Dieser
Energievorrat reicht für 10-20 Sekunden
oder bis zu 50 Kontraktionen, dann ist er (bei fortgesetzter
Muskelaktivität) gänzlich erschöpft. In Situationen plötzlicher extremer Herausforderung (fight or flight) kann dieser Mechanismus von überlebenswichtiger Bedeutung sein.
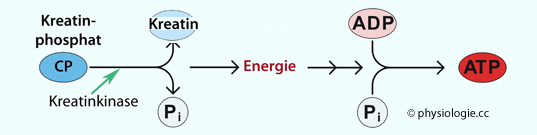 Muskelfasern enthalten im
Ruhezustand mehr Kreatinphosphat als ATP, bei einer Kontraktion nimmt
zunächst der CP-Pool (bei annähernd gleichbleibendem [ATP]) ab
(energetische Pufferfunktion).
Muskelfasern enthalten im
Ruhezustand mehr Kreatinphosphat als ATP, bei einer Kontraktion nimmt
zunächst der CP-Pool (bei annähernd gleichbleibendem [ATP]) ab
(energetische Pufferfunktion).
 Innerhalb von Sekunden springt die anaerobe Glykolyse
an. Sie kann noch vor Ablauf einer Minute mehr als die Hälfte des
Energiemusatzes des Muskels bestreiten, nachher nimmt ihr Beitrag
wieder ab und ist nach wenigen Minuten vollauf verschwunden.
Innerhalb von Sekunden springt die anaerobe Glykolyse
an. Sie kann noch vor Ablauf einer Minute mehr als die Hälfte des
Energiemusatzes des Muskels bestreiten, nachher nimmt ihr Beitrag
wieder ab und ist nach wenigen Minuten vollauf verschwunden.
 Aerober Substratabbau übernimmt dann die Energieproduktion
(
Aerober Substratabbau übernimmt dann die Energieproduktion
( Abbildung). Auch sie startet innerhalb weniger Sekunden, nach etwa
10 Minuten gipfelt der Beitrag des aeroben Kohlenhydratabbaus in der Muskulatur (diese nimmt Glucose auf, was den Blutzuckerspiegel senkt). Dieser Mechanismus wirkt über eine Stunde.
Abbildung). Auch sie startet innerhalb weniger Sekunden, nach etwa
10 Minuten gipfelt der Beitrag des aeroben Kohlenhydratabbaus in der Muskulatur (diese nimmt Glucose auf, was den Blutzuckerspiegel senkt). Dieser Mechanismus wirkt über eine Stunde.
 Etwa 10 Minuten nach Beginn der Arbeit beteiligt sich der aerobe Kohlenhydratabbau in der Leber, dieser nimmt etwa 2 Stunden lang an der Energiebereitstellung teil.
Etwa 10 Minuten nach Beginn der Arbeit beteiligt sich der aerobe Kohlenhydratabbau in der Leber, dieser nimmt etwa 2 Stunden lang an der Energiebereitstellung teil.
 Gut eine Viertelstunde nach Beginn der Aktivität beginnt der aerobe Fettsäureabbau,
sein Maximum ist nach 2 Stunden (oder mehr) erreicht, und für
Ausdauerbelastung bleibt dieser Mechanismus am Ende für die
ATP-Synthese alleine übrig.
Gut eine Viertelstunde nach Beginn der Aktivität beginnt der aerobe Fettsäureabbau,
sein Maximum ist nach 2 Stunden (oder mehr) erreicht, und für
Ausdauerbelastung bleibt dieser Mechanismus am Ende für die
ATP-Synthese alleine übrig.
Bei
intensiver Muskelbelastung stammt die Energie aus der
Hydrolyse von ATP (Sekunden), Kreatinphosphat, dann Glucose und
schließlich Fettsäuren
|
Der Anteil von Kohlenhydraten als Energiequelle im Muskel hängt so wie derjenige der Fette von der Belastung ab ( Abbildung):
Abbildung):
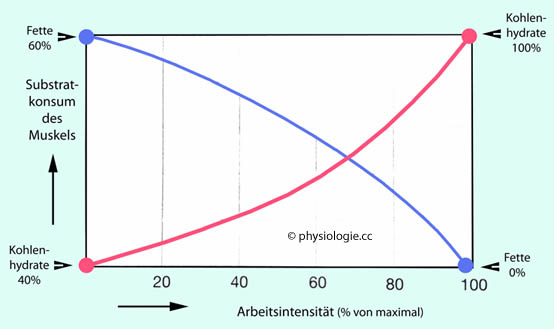
 Abbildung: Substratnutzung als Funktion der Muskelbelastung
Nach einer Vorlage bei Silverthorn, Human Physiology - an integrated approach, 4th ed. Pearson International 2007
Abbildung: Substratnutzung als Funktion der Muskelbelastung
Nach einer Vorlage bei Silverthorn, Human Physiology - an integrated approach, 4th ed. Pearson International 2007
Der ruhende Muskel utilisiert für seinen Energiestoffwechsel (ATP-Synthese) etwa zu 40% Kohlenhydrate und zu 60% Fette (links).
Fett hat einen wesentlich höheren Brennwert als Zucker, kann allerdings
nur oxidativ für den ATP-Nachschub genutzt werden - also bei
ausreichender Muskeldurchblutung. Auch bei mäßiger Inanspruchnahme von
Muskelkraft (z.B. Ausdauersport) dominiert die Nutzung von Fetten zur
Energieversorgung der Muskulatur, nimmt aber mit steigender Belastung
stetig ab (Mitte).
Nimmt die Arbeitsintensität weiter zu, gerät die Utilisation von Lipiden für die ATP-Synthese zunehmend unter Druck, die Sauerstoffzufuhr über den Blutkreislauf reicht nicht mehr für den gesamten oxidativen Anteil des Energiemetabolismus aus. Glucose
kann auch anoxidativ genutzt werden (Glykolyse), wenn auch mit geringer
ATP-Ausbeute. Bei Ausbelastung (rechts) zieht der Skelettmuskel
ausschließlich
Kohlenhydrate zur ATP-Synthese heran (rechts)
 Nur bei
niedriger Muskelbelastung reicht das Sauerstoffangebot über den
Kreislauf für oxidative Energiegewinnung (über Krebs-Zyklus und
oxidative Phosphorylierung). So können sowohl Lipide als auch
Kohlenhydrate zur ATP-Synthese herangezogen werden. Nimmt aber die
Muskelbelastung - und damit der ATP-Bedarf - an, sinkt die
Verfügbarkeit der Fettutilisation, und der Energiestoffwechsel greift
immer stärker auf anaerobe ATP-Gewinnung zurück (glykolytischer Metabolismus) - der zwar nur kurzfristig in Anspruch genommen werden kann (Lactacidose),
aber keinen Sauerstoff benötigt. Auf diese Weise kann die
Skelettmuskulatur kurzfristig auf Hochtouren funktionieren, auch wenn
die O2-Zufuhr nicht mehr dem Bedarf entsprechen
kann (die erwachsende "Sauerstoffschuld" wird nach der Spitzenbelastung
"zurückgezahlt").
Nur bei
niedriger Muskelbelastung reicht das Sauerstoffangebot über den
Kreislauf für oxidative Energiegewinnung (über Krebs-Zyklus und
oxidative Phosphorylierung). So können sowohl Lipide als auch
Kohlenhydrate zur ATP-Synthese herangezogen werden. Nimmt aber die
Muskelbelastung - und damit der ATP-Bedarf - an, sinkt die
Verfügbarkeit der Fettutilisation, und der Energiestoffwechsel greift
immer stärker auf anaerobe ATP-Gewinnung zurück (glykolytischer Metabolismus) - der zwar nur kurzfristig in Anspruch genommen werden kann (Lactacidose),
aber keinen Sauerstoff benötigt. Auf diese Weise kann die
Skelettmuskulatur kurzfristig auf Hochtouren funktionieren, auch wenn
die O2-Zufuhr nicht mehr dem Bedarf entsprechen
kann (die erwachsende "Sauerstoffschuld" wird nach der Spitzenbelastung
"zurückgezahlt").
Die Stoffwechselrate des Muskels kann - bezogen auf den Ruhezustand -
bei Aktivierung um das mehr als Hundertfache ansteigen. Das bedingt
nicht nur eine Steigerung des Atemgasaustauschs, sondern auch die
Mobilisierung innerer (Muskelglykogen, Neutralfette) und äußerer
Substrate (Leber: Glykogen, Fettgewebe: Neutralfette).
Muskelglykogen stellt eine Energiereserve für die Muskelzelle selbst dar
(Glykogen bis zu 3% der Zellmasse). Dies ist besonders für kurze,
intensive Belastungen hilfreich (auch bei ungenügendem
Sauerstoffangebot - anaerober Abbau bis Lactat). Die Aufnahme der Glucose aus dem Extrazellulärraum wird durch Insulin begünstigt (etwa 15-fach; ~4 mg/ml intrazelluläre Glucosekonzentration kann durch Insulinwirkung erreicht werden).
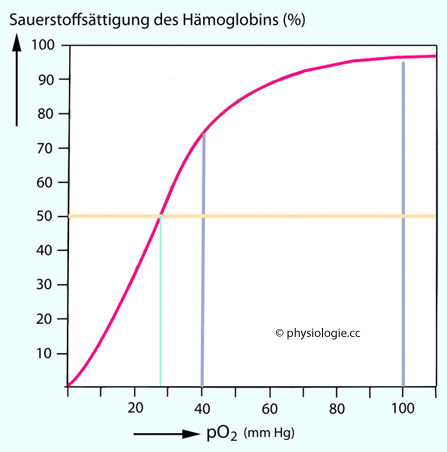
 Abbildung: Eine Hämoglobin-Bindungskurve
Abbildung: Eine Hämoglobin-Bindungskurve
Nach einer Vorlage bei Silverthorn, Human Physiology - an integrated approach, 4th ed. Pearson International 2007
Nach dieser (typischen) Bindungskurve ist das Hämoglobin bei einem pO2 von 40 mmHg zu ~75% gesättigt. Halbsättigung (gelbe horizontale Linie) besteht bei 27-28
mmHg (grüne vertikale Linie). Bei 25 mmHg (gerundeter Mittelwert für
mäßig aktive Skelettmuskelzellen) beträgt die Sättigung ~45%

 Mäßig aktive Skelettmuskelzellen haben einen pO2 von ungefährt 25 mmHg - das aus dem Muskel strömende venöse Blut hat dann diesen pO2. Bei diesem Sauerstoffpartialdruck hat das Hämoglobin mehr als die Hälfte seiner O2-Transportkapazität an die Zellen abgegeben, es ist nur mehr zu 45% mit Sauerstoff beladen (
Mäßig aktive Skelettmuskelzellen haben einen pO2 von ungefährt 25 mmHg - das aus dem Muskel strömende venöse Blut hat dann diesen pO2. Bei diesem Sauerstoffpartialdruck hat das Hämoglobin mehr als die Hälfte seiner O2-Transportkapazität an die Zellen abgegeben, es ist nur mehr zu 45% mit Sauerstoff beladen ( Abbildung). Bei starker Arbeitsbelastung nimmt die Hb-Sauerstoffsättigung weiter ab, bei 10% liegt der pO2 bei etwa 7 mmHg.
Abbildung). Bei starker Arbeitsbelastung nimmt die Hb-Sauerstoffsättigung weiter ab, bei 10% liegt der pO2 bei etwa 7 mmHg.
 Zur Beziehung Sauerstoffverbrauch - Belastungszunahme s. dort
Zur Beziehung Sauerstoffverbrauch - Belastungszunahme s. dort
 Abbildung):
Abbildung):
 Fettsäuren
und Ketonkörper
(fast unbeschränkte Verfügbarkeit über lange
Belastungsperioden). Fettsäuren liefern insgesamt etwa 80% des
Energieaufkommens der Skelettmuskulatur. Dabei darf der Durchsatz nicht
über 40% des maximal möglichen Sauerstoffverbrauchs liegen (was die
meiste Zeit zutrifft) - andernfalls wird zunehmend Glucose für die
Energiegewinnung herangezogen (für begrenzte Zeit). Die Aufnahme von Fetten (vor allem
aus VLDL) in die Muskelzelle erfolgt (wie im Fettgewebe) über Lipoproteinlipase, die von Muskelzellen - insbesondere nach Belastung - in hohem Maße exprimiert wird.
Fettsäuren
und Ketonkörper
(fast unbeschränkte Verfügbarkeit über lange
Belastungsperioden). Fettsäuren liefern insgesamt etwa 80% des
Energieaufkommens der Skelettmuskulatur. Dabei darf der Durchsatz nicht
über 40% des maximal möglichen Sauerstoffverbrauchs liegen (was die
meiste Zeit zutrifft) - andernfalls wird zunehmend Glucose für die
Energiegewinnung herangezogen (für begrenzte Zeit). Die Aufnahme von Fetten (vor allem
aus VLDL) in die Muskelzelle erfolgt (wie im Fettgewebe) über Lipoproteinlipase, die von Muskelzellen - insbesondere nach Belastung - in hohem Maße exprimiert wird.
Muskelzellen enthalten u.a. Fetttröpfchen (relativ klein:
Etwa 20µ Durchmesser), die als Energiereserve,
aber auch zur Entgiftung potentiell toxischer Fettsäuren dienen. Wie im Fettgewebe,
haben die Kügelchen eine Hülle aus Perlipin (das Triglyzeride vor Abbau
schützt), und weitere Proteine erfüllen enzymatische und
Transportfunktionen (wenn Perlipin phopsphoryliert wurde und der Abbau
aus Lipidtröpfchen erfolgen kann). Bei
geringer Muskelbelastung liefern die zelleigenen Fettreserven bis zu 85% der benötigten Energie, der
Rest der benötigten Fettsäuren stammt aus dem Blutkreislauf.
 Glucose (für hohen Energiedurchsatz) und Lactat (begrenzt durch das Sauerstoffangebot über den Kreislauf). Diese
werden verbraucht und nicht nachgebildet (keine Glukoneogenese im
Skelettmuskel). Im Vergleich zu anderen Geweben ist der Skelettmuskel
die wichtigste Stelle insulinabhängiger (GLUT4-vermittelter) Glucoseaufnahme (~80%); Muskelfasern exprimieren auch GLUT1, vermutlich für die basale Glucoseaufnahme. Auch NO
(aus Endothelzellen) fördert die Glucoseaufnahme der Muskelzelle. Bei
ausreichendem Glucoseangebot (hoher Insulinspiegel) bildet die
Muskelzelle die zur Synthese von Glykogen notwendigen Enzyme.
Muskelaktivität regt direkt die Glykogenolyse an.
Glucose (für hohen Energiedurchsatz) und Lactat (begrenzt durch das Sauerstoffangebot über den Kreislauf). Diese
werden verbraucht und nicht nachgebildet (keine Glukoneogenese im
Skelettmuskel). Im Vergleich zu anderen Geweben ist der Skelettmuskel
die wichtigste Stelle insulinabhängiger (GLUT4-vermittelter) Glucoseaufnahme (~80%); Muskelfasern exprimieren auch GLUT1, vermutlich für die basale Glucoseaufnahme. Auch NO
(aus Endothelzellen) fördert die Glucoseaufnahme der Muskelzelle. Bei
ausreichendem Glucoseangebot (hoher Insulinspiegel) bildet die
Muskelzelle die zur Synthese von Glykogen notwendigen Enzyme.
Muskelaktivität regt direkt die Glykogenolyse an.
 Aminosäuren
(vor allem verzweigtkettige: Leuzin, Isoleuzin, Valin, diese gelangen
nach Resorption im Darm direkt in die Muskeln - die Leber kümmert sich
wenig um sie - und stellen mehr als 30% aller Aminosäuren in
kontraktilen Filamenten). Aminosäuren können aus dem Abbau von Protein
- vor allem Aktin und Myosin - gewonnen werden (Muskelzellen sind reich
an Aminotransferasen, dabei fallen vor allem Alanin und Glutamin an -
via Leber können Aminosäuren aus dem Muskel zu Glucose verwandelt und
u.a. dem Gehirn zur Verfügung gestellt werden). Das passiert nicht nur im
generellen Hungerstoffwechsel, sondern auch lokal bei Inaktivität eines
Muskels (Immobilisierung).
Aminosäuren
(vor allem verzweigtkettige: Leuzin, Isoleuzin, Valin, diese gelangen
nach Resorption im Darm direkt in die Muskeln - die Leber kümmert sich
wenig um sie - und stellen mehr als 30% aller Aminosäuren in
kontraktilen Filamenten). Aminosäuren können aus dem Abbau von Protein
- vor allem Aktin und Myosin - gewonnen werden (Muskelzellen sind reich
an Aminotransferasen, dabei fallen vor allem Alanin und Glutamin an -
via Leber können Aminosäuren aus dem Muskel zu Glucose verwandelt und
u.a. dem Gehirn zur Verfügung gestellt werden). Das passiert nicht nur im
generellen Hungerstoffwechsel, sondern auch lokal bei Inaktivität eines
Muskels (Immobilisierung).
 Die Nutzung der Substrate für den Energiebedarf des Muskels ändern sich mit Grad und Dauer der Belastung.
Die Nutzung der Substrate für den Energiebedarf des Muskels ändern sich mit Grad und Dauer der Belastung.
 Bei niedriger Belastung (z.B. 25% VO2max) nutzt der Skelettmuskel vorwiegend (80-90%) Fettsäuren (die aus dem Fettgewebe
mobilisiert werden) für seinen Energieaufwand (hohe Energiedichte, aber
ausreichend Sauerstoff für oxidativen Abbau notwendig); etwa 10%
stammen aus dem Abbau von Neutralfettreserven der Myozyten selbst, weitere
Bei niedriger Belastung (z.B. 25% VO2max) nutzt der Skelettmuskel vorwiegend (80-90%) Fettsäuren (die aus dem Fettgewebe
mobilisiert werden) für seinen Energieaufwand (hohe Energiedichte, aber
ausreichend Sauerstoff für oxidativen Abbau notwendig); etwa 10%
stammen aus dem Abbau von Neutralfettreserven der Myozyten selbst, weitere ~10%
aus dem Abbau von Glucose aus dem Blut. Der Transport von Lipiden erfolgt über Lipoproteine im Blut.

Über den Lipidtransport via
Chylomikronen,
VLDL,
IDL und
LDL s.
dort
 Steigt die Belastung (z.B. auf 65% VO2max), nimmt der Absolutbetrag des Energieumsatzes entsprechend zu (z.B. bei Erhöhung von 25 auf 65% VO2max um einen Faktor 2,6). Die Prozentsätze
der Substratnutzung ändern sich deutlich: Kohlenhydrate werden stärker
genutzt, vor allem zu Beginn der Leistung. Jetzt kommen rund 25-40% aus
der Utilisation von Muskelglykogen (das bei 25% VO2max überhaupt nicht betroffen ist); der Anteil muskeleigener Neutralfette nimmt (während der ersten Stunde) auf bis zu 30% zu, Fettsäuren liefern anfangs nur noch 25-30%, später (wenn die Glykogenreserven zur Neige gehen) steigt der Anteil wieder auf ~50%
an; Glucose (die z.T. aus dem Abbau von Leberglykogen stammt, soferne
noch Vorräte vorhanden sind) wird nach wie vor aus dem Blut bezogen (5-15%,
mit der Belastungsdauer steigend; das entspricht einem Mehrfachen des
Glucoseumsatzes im Körper - von der Leber zur quergestreiften
Muskulatur - im Vergleich zu geringer Belastung).
Steigt die Belastung (z.B. auf 65% VO2max), nimmt der Absolutbetrag des Energieumsatzes entsprechend zu (z.B. bei Erhöhung von 25 auf 65% VO2max um einen Faktor 2,6). Die Prozentsätze
der Substratnutzung ändern sich deutlich: Kohlenhydrate werden stärker
genutzt, vor allem zu Beginn der Leistung. Jetzt kommen rund 25-40% aus
der Utilisation von Muskelglykogen (das bei 25% VO2max überhaupt nicht betroffen ist); der Anteil muskeleigener Neutralfette nimmt (während der ersten Stunde) auf bis zu 30% zu, Fettsäuren liefern anfangs nur noch 25-30%, später (wenn die Glykogenreserven zur Neige gehen) steigt der Anteil wieder auf ~50%
an; Glucose (die z.T. aus dem Abbau von Leberglykogen stammt, soferne
noch Vorräte vorhanden sind) wird nach wie vor aus dem Blut bezogen (5-15%,
mit der Belastungsdauer steigend; das entspricht einem Mehrfachen des
Glucoseumsatzes im Körper - von der Leber zur quergestreiften
Muskulatur - im Vergleich zu geringer Belastung).
 Bei extensiver Belastung schließlich (80-90% VO2max)
- etwa bei Marathonläufen - kann Glucose (aus Glykogenolyse) zum
führenden Energielieferanten des Muskels avancieren. Das ermöglicht
eine nur begrenzte Zeitspanne der Kraftentwicklung. Einige Tage nach
erschöpfender Belastung nimmt der Glykogengehalt des Muskels deutlich
zu (bis auf 3-4% der Muskelmasse). Wie genau all diese Umstellungen
gesteuert und koordiniert werden, ist noch Gegenstand der Forschung.
Bei extensiver Belastung schließlich (80-90% VO2max)
- etwa bei Marathonläufen - kann Glucose (aus Glykogenolyse) zum
führenden Energielieferanten des Muskels avancieren. Das ermöglicht
eine nur begrenzte Zeitspanne der Kraftentwicklung. Einige Tage nach
erschöpfender Belastung nimmt der Glykogengehalt des Muskels deutlich
zu (bis auf 3-4% der Muskelmasse). Wie genau all diese Umstellungen
gesteuert und koordiniert werden, ist noch Gegenstand der Forschung.

 Abbildung: Glucoseaustausch im Organismus
Abbildung: Glucoseaustausch im Organismus
Nach einer Vorlage in Koolman / Roehm, Color atlas of biochemistry. Thieme 2012
Eine
erwachsene Person speichert im Durchschnitt etwa 450 Gramm
Glykogen - 1/3 in der Leber, 2/3 in der Muskulatur.
Die Leber
nützt ihren Glykogenvorrat (~150 Gramm) zur postresorptiven
Stabilisierung des Blutzuckerspiegels (Fremdbedarf). Dieser Speicher
kann vollständig verbraucht werden (grüner Doppelpfeil links), er wird
durch Glukoneogenese wieder aufgefüllt.
Muskelglykogen
hingegen (insgesamt ~300 Gramm, bei trainierten Menschen auch mehr: bis zu ~3% der Muskelmasse) dient dem Eigenbedarf; der Speicher
nimmt dabei nomalerweise nur um ~100 Gramm ab (grüner Doppelpfeil
rechts). Die Leber verfügt über Glucose-6-Phosphatase, die Muskelzelle
nicht

Die Muskelmasse des Menschen besteht (im Ruhezustand) zu 1-2% aus Glykogen, abhängig vom Ernährungsmuster
- 0,5-1% bei fett- und eiweißbetonter, 2-4% bei stark
kohlenhydratreicher Kost. Beträgt z.B. das gesamte Muskelgewicht einer
erwachsenen Person 25-30 kg, ist bei ausgewogener Mischkost von einem
Muskelglykogenvorrat von ~400 g auszugehen.
 Zur kapillären Glucosezufuhr an den Muskel s. auch dort
Zur kapillären Glucosezufuhr an den Muskel s. auch dort
In der Physiologie bezeichnet
man als Arbeit alles, was den Energieumsatz im Muskel erhöht:
 Statische Arbeit
("Haltearbeit") bei konstanter Muskellänge (physikalisch-formal gesehen
ist das keine Arbeit, weil ja kein Weg zurückgelegt wird - jedenfalls
nicht nach aussen;
Statische Arbeit
("Haltearbeit") bei konstanter Muskellänge (physikalisch-formal gesehen
ist das keine Arbeit, weil ja kein Weg zurückgelegt wird - jedenfalls
nicht nach aussen;
 Dynamische Arbeit - diese kann positiv sein (der Muskel verkürzt sich) oder auch negativ ("Bremsarbeit" bei Dehnung, z.B. beim Bergabgehen).
Dynamische Arbeit - diese kann positiv sein (der Muskel verkürzt sich) oder auch negativ ("Bremsarbeit" bei Dehnung, z.B. beim Bergabgehen).
Entscheidend ist, dass bei Muskelaktivität auf jeden Fall "innere"
Arbeit geleistet wird, d.h. der Stoffwechsel der Muskelfasern
gesteigert wird. Der Großteil des aufgewendeten Energieumsatzes fließt
nicht in mechanische Leistung (diesen Anteil gibt der Wirkungsgrad an), sondern wird als Wärme frei (Muskel als Wärmemaschine).
 Im
Ruhezustand und bei stationärer Arbeit bezieht der Skelettmuskel ~75%
seiner Energie aus dem Abbau (oxidative Phosphorylierung) von Fettsäuren (nicht Glucose!). Diese vorwiegend
aus dem Fettgewebe stammende Energiequelle ist für sehr lange Zeiträume
verfügbar und wird normalerweise in den
Arbeitspausen wieder aufgefüllt.
Im
Ruhezustand und bei stationärer Arbeit bezieht der Skelettmuskel ~75%
seiner Energie aus dem Abbau (oxidative Phosphorylierung) von Fettsäuren (nicht Glucose!). Diese vorwiegend
aus dem Fettgewebe stammende Energiequelle ist für sehr lange Zeiträume
verfügbar und wird normalerweise in den
Arbeitspausen wieder aufgefüllt.
Bei kurzdauernden Höchstleistungen
hingegen steigt der Anteil der Glucose
an der Energieversorgung des
Muskels auf bis zu ~75% an. Aktivitätssteigerung des Sympathikus
bewirkt - über ß2-Rezeptoren - Glykogenolyse und Proteinsynthese, und
steigert die Aktivität der Na-K-Pumpe (was den Kaliumspiegel im Blutplasma senken
kann).
Die Glucoseproduktion in der Leber (Glykogenolyse, Glukoneogenese) wird vor allem durch Adrenalin und Noradrenalin angeregt, die gleichzeitig die Sekretion von Glucagon fördern und die von Insulin hemmen. All das unterstützt die hepatische Glucosefreisetzung.
 Zum aeroben / anaeroben Energiestoffwechsel des Muskels s. auch dort
Zum aeroben / anaeroben Energiestoffwechsel des Muskels s. auch dort
 Abbildung: Bilanz der Sauerstoffverteilung im Körper (gerundete Werte: gesunder junger Mann)
Nach einer Vorlage in Praktische Physiologie
Abbildung: Bilanz der Sauerstoffverteilung im Körper (gerundete Werte: gesunder junger Mann)
Nach einer Vorlage in Praktische Physiologie
Perfusion rot, Sauerstoffverbrauch blau. Aufteilung auf Muskulatur (inkl. Myokard) und Rest des Körpers (vgl.
dort).
Die Muskulatur verbraucht im Ruhezustand
(
links) nur 20% des Herzminutenvolumens (5 l/min) und ein Drittel des
gesamten Sauerstoffs (240 ml/min).
Diese Zahlen steigen bei
körperlicher Ausbelastung (
rechts) auf 85% (des Herzminutenvolumens von 20 l/min) und 95% (des Sauerstoffverbrauchs von 3210 ml/min)

Eine erwachsene Person kann etwa 450 Gramm Glykogen speichern (~150g in der Leber, ~300 g im Skelettmuskel).
 Leberglykogen
Leberglykogen dient zur Erhaltung des
Blutzuckerspiegels
in der
postresorptiven Phase, und dieser Vorrat ist starken
Schwankungen unterworfen (praktisch vollständige Entleerung möglich). Durch Glukoneogenese wird der
Speicher dann wieder komplettiert
 Muskelglykogen
Muskelglykogen
hingegen dient dem eigenen Bedarf und nicht der Blutzuckerregulation
(fehlende Glucose-6-Phosphatase, keine Glucoseabgabe aus der
Muskelzelle). Der Glykogengehalt im Muskel ist auch nicht so starken
Schwankungen unterworfen (±1/3, s. Abbildung oben).
 Blutzuckersenkende Wirkung
von Muskelaktivität: Die Glucoseaufnahme steigt auch ohne Insulin bei
erhöhtem Energieverbrauch der Muskelzelle und senkt dadurch den Glucosespiegel.
Blutzuckersenkende Wirkung
von Muskelaktivität: Die Glucoseaufnahme steigt auch ohne Insulin bei
erhöhtem Energieverbrauch der Muskelzelle und senkt dadurch den Glucosespiegel.
Aerob vs. anaerob, Leistungsbereich des Muskels
Plötzliche Kraftentwicklung
bedingt raschen Energieverbrauch, intrazelluläre Speicher werden
entsprechend schnell konsumiert (energiereiche Phosphate: ATP, CP)
und müssen nachgebildet werden. Dies erfolgt unter Sauerstoffverbrauch (aerob, Zitratzyklus) oder anaerob (Glykolyse bis Pyruvat → Lactat), was weniger Energie (Muskeltätigkeit für 20-30 Sekunden) bringt und den pH-Wert senkt (nicht-respiratorische Azidose).

Über die Steuerung der
Atmung bei körperlicher Belastung s.
dort
 Als aerobe Kapazität bezeichnet man die Leistungsfähigkeit des Muskels bis Erreichen der anaeroben Schwelle
(Aufrechterhaltung des Gleichgewichts zwischen Lactat-Neubildung und
-Abbau, d.h. Vermeidung einer leistungsbedingten Lactazidose).
Als aerobe Kapazität bezeichnet man die Leistungsfähigkeit des Muskels bis Erreichen der anaeroben Schwelle
(Aufrechterhaltung des Gleichgewichts zwischen Lactat-Neubildung und
-Abbau, d.h. Vermeidung einer leistungsbedingten Lactazidose).

 Abbildung: Diätplan und Ausdauer
Abbildung: Diätplan und Ausdauer
Nach einer Vorlage in Hinghofer-Szalkay H, Körperliche Belastung und Kohlenhydrate. Wien Med Wschr 1979; 129: 532-4
Fahrradergometrie
auf 75% der maximalen Leistung. Bei niedriger Kohlenhydratzufuhr mit
der Ernährung (fett- und eiweißreiche Kost, oben)
legt die Skelettmuskulatur einen Vorrat von 5-10 g Glykogen pro kg
Muskelgewebe an, der relativ rasch verbraucht ist; eine Energieausbeute
von 75% der maximal möglichen Leistung ist aus der Verbrennung von
Fettsäuren auf Dauer nicht möglich, die Ausdauerzeit beträgt ~1 Stunde.
Bei hoher Kohlenhydratzufuhr hingegen (unten)
kann die Muskulatur bis zu 40 g/kg Glykogen speichern, dementsprechend
länger kann der hohe Energiedurchsatz durch Kohlenhydratverbrennung
aufrechterhalten werden

Leistungsbereich und Leistungsreserve: Bei maximaler Aktivierung (synchroner vollständiger Tetanus aller motorischer Einheiten) kann der Muskel seinen maximalen Gesamtleistungsbereich ausschöpfen. Das ist allerdings nur unter Ausnahmebedingungen möglich - im Affekt, z.B. in lebensbedrohlichen Situationen, oder bei Einwirkung von Pharmaka (Doping) - und gefährdet die Integrität des Gewebes. Starke Willensanstrengung
mobilisiert sonst nur 35-65% der theoretisch möglichen Höchstleistung;
im Rahmen üblicher Leistungsbereitschaft wird höchstens ein Drittel der
Maximalkraft rekrutiert. Automatisierte Tätigkeiten nehmen gar nur 15% (oder weniger) des maximalen Leistungsbereichs in Anspruch.
Training steigert längerfristig (über
Tage bis Wochen) die Glykogenspeicherung im Skelettmuskel; so kann z.B. durch
entsprechende Kombination von Muskelbelastung und Diätform die
Glykogenspeicherung von <10 g/kg auf >30 g/kg und die
Ausdauerzeit z.B. im Radsport von einer Stunde auf drei Stunden erhöht
werden ( Abbildung).
Abbildung).
Ausdauertraining und Kreislauf: Zu den trainingsbedingten Anpassungen gehört auch eine Erhöhung des Plasmavolumens, wahrscheinlich bedingt durch gesteigerte Albuminsynthese durch die Leber (kolloidosmotischer Effekt)
- die Leber kann die Synthese (normalerweise etwa 20 g Albumin / 24 h)
auf entsprechende Reize hin mindestens verdreifachen. Die Produktion roter Blutkörperchen
- und damit von Hämoglobin, das Atemgase transportiert - steigt
ebenfalls an, allerdings nicht so stark - das Resultat ist ein Absinken
des Hämatokrit (sports anemia).
Die Bezeichnung "Anämie" ist dabei irreführend - die Transportkapazität
für Sauerstoff nimmt ja zu (und das Blut fließt leichter, s. Rheologie).
Die Kreislaufumstellung durch aerobes Training schließt weiters eine Steigerung des höchstmöglichen Herzzeitvolumens - und damit der Sauerstofftransportkapazität - ein, gekoppelt mit größerer Diffusionskapazität für Atemgase in den Lungen und einem erhöhten Maximum der alveolären Ventilation sowie einer Verbesserung der Abstimmung von Ventilation und Perfusion in den verschiedenen Lungenabschnitten.
In der Muskulatur kommt es trainingsbedingt zu erhöhtem maximalen
Blutfluss, Aussprossen neuer Mikrogefäße, Vergrößerung der
Austauschfläche Blut - Gewebe, Reduktion der Diffusionsstrecken,
Erhöhung der Mitochondrienzahl (bis zum Doppelten des Ausgangswertes).

 Abbildung: Metabolische Hyperämie
Nach Walløe L, Wesche J. Time course and magnitude of
blood flow changes in the human quadriceps muscles during and following
rhythmic exercise. J Physiol 1988; 405: 257-73
Abbildung: Metabolische Hyperämie
Nach Walløe L, Wesche J. Time course and magnitude of
blood flow changes in the human quadriceps muscles during and following
rhythmic exercise. J Physiol 1988; 405: 257-73
Registrierung (Ultraschall- Doppler)
der Strömungsgeschwindigkeit durch eine a. femoralis vor, während
("Belastung") und nach rhythmischen Kontraktionen des betreffenden m.
quadriceps femoris.
Zu Beginn der Belastung (hier 30% des Maximalwertes) nehmen die Spitzenwerte der
Strömungsgeschwindigkeit durch Anreicherung gefäßerweiternder
Substanzen (infolge ungenügender Sauerstoffzufuhr) erst allmählich zu,
die Vasodilatation erreicht erst nach 2-3 Minuten ihr Höchstmaß, eine
"Sauerstoffschlld" hat sich aufgebaut.
Nach Beendigung der Belastung müssen die vasodilatierenden Substanzen
erst aus dem Gewebe gebracht werden, während dieser Zeit ist die
Durchblutung noch erhöht (metabolische Hyperämie), das vermehrte
Sauerstoffangebot wird für die oxidative Restitution der
Energiespeicher genützt

 Als Sauerstoffschuld
(Oxygen debt / deficit,
Als Sauerstoffschuld
(Oxygen debt / deficit,  Abbildung) bezeichnet man die Tatsache, dass der Muskel zu
Beginn seiner Tätigkeit Energiereserven aufbraucht, die erst nach Ende
der Kontraktion oxidativ wieder ergänzt werden ("die Sauerstoffschuld
wird zurückgezahlt", indem vermehrt Sauerstoff aufgenommen wird: Excess postexercise O2 consumption EPOC). Bis die Energiereserven wieder aufgefüllt und die Verhältnisse des Ruhezustandes wieder hergestellt sind,
wird Energie aus mehreren Quellen direkt im Muskel bereitgestellt:
Vorhandenes ATP, Kreatinphosphat, an Myoglobin gebundener Sauerstoff,
anaerobe Glykolyse.
Abbildung) bezeichnet man die Tatsache, dass der Muskel zu
Beginn seiner Tätigkeit Energiereserven aufbraucht, die erst nach Ende
der Kontraktion oxidativ wieder ergänzt werden ("die Sauerstoffschuld
wird zurückgezahlt", indem vermehrt Sauerstoff aufgenommen wird: Excess postexercise O2 consumption EPOC). Bis die Energiereserven wieder aufgefüllt und die Verhältnisse des Ruhezustandes wieder hergestellt sind,
wird Energie aus mehreren Quellen direkt im Muskel bereitgestellt:
Vorhandenes ATP, Kreatinphosphat, an Myoglobin gebundener Sauerstoff,
anaerobe Glykolyse.
Die EPOC kann unterschiedlich lange Zeit in Anspruch nehmen. Eine
"rasche" Komponente kann nach einer Minute bereits abgeschlossen sein ( Abbildung),
wenn die vorausgehende Belastung gering war. Nach stärkerer
Belastung kann die Erholungsphase mehrere Minuten bis sogar Stunden
dauern ("langsame" Komponente), bedingt durch Lactazidose,
Gewebeschäden u.a. - Erholung und Reparaturvorgänge können viel Zeit in
Anspruch nehmen.
Abbildung),
wenn die vorausgehende Belastung gering war. Nach stärkerer
Belastung kann die Erholungsphase mehrere Minuten bis sogar Stunden
dauern ("langsame" Komponente), bedingt durch Lactazidose,
Gewebeschäden u.a. - Erholung und Reparaturvorgänge können viel Zeit in
Anspruch nehmen.
Belastbarkeit
ist die (mentale oder körperliche) Leistung, die ein Mensch ohne
Gefährdung seiner Gesundheit erbringen kann. Um eine bestimmte Belastung (gemessen z.B. in Watt) zu erbringen, nimmt er seine physiologischen Systeme in Anspruch; diese Beanspruchung
kann man z.B. an Blutdruck, Herzfrequenz oder Sauerstoffverbrauch
ablesen. Bei der Beziehung zwischen (physikalischer) Belastung und
(physiologischer) Beanspruchung spielen schließlich Leistungsvoraussetzungen eine Rolle, wie z.B. der Wirkungsgrad oder die Vordehnung der Muskeln.
Unter Leistungsfähigkeit
schließlich versteht man ein Persönlichkeitsmerkmal, das von
physiologischen Voraussetzungen (kardiovaskuläres, respiratorisches,
Nerven-, Muskelsystem u.a.) abhängt. Sie wird durch eine Vielzahl von
Faktoren beeinflusst, die nur zum Teil beeinflussbar sind (Training,
Ernährung, Begabung, Gesundheitszustand, Geschlecht, Alter).
Ist die körperliche Arbeit so intensiv, dass die aerobe Glykolyse überfordert ist und der Muskel zunehmend anaeroben Glucoseabbau
heranziehen muss, entsteht Lactat (Milchsäure), das in den Kreislauf
abgegeben wird. Steigt der Lactatspiegel im Blut auf >4 mM (Ruhewert
~1 mM), kann der Muskel seine Leistung nicht mehr steigern. Der Lactatspiegel kann bis zu 15 mM weiter ansteigen, bis die Erschöpfungsgrenze einen Abbruch der Muskelarbeit erzwingt.
Steigt der Lactatspiegel im Blut auf über 4 mM, ist eine Leistungssteigerung der Muskulatur nicht mehr möglich
|
Wie wird die Perfusion des Muskels gesteuert?
 Zur Steuerung der Muskeldurchblutung s. auch dort
Zur Steuerung der Muskeldurchblutung s. auch dort
Um ausreichend Sauerstoff und Substrate für den
Energiestoffwechsel (Fettsäuren, Glucose u.a.) an die Muskelfasern zu
transportieren, muss die Perfusion (die lokal bis auf das Hundertfache
des Ruhewertes zunehmen kann) entsprechend erhöht werden. Dazu tragen
lokale, nervöse und hormonelle Faktoren bei.
Das Herzzeitvolumen verteilt sich je nach Grad der Muskelaktivität sehr unterschiedlich auf die Organe und Gewebe ( Abbildung):
Abbildung):
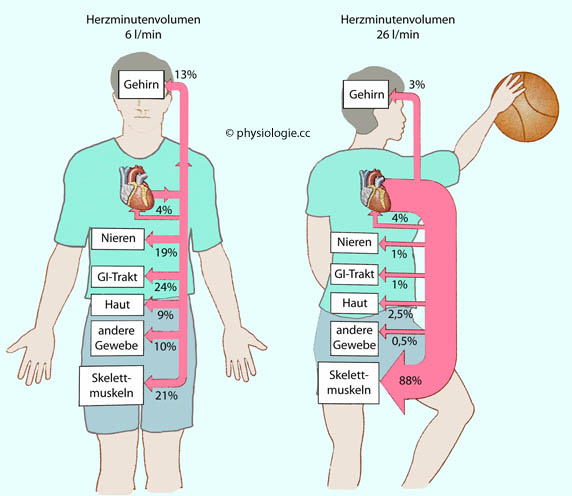
 Abbildung: Verteilung des Herzzeitvolumens in Ruhe und bei Muskelarbeit
Nach einer Vorlage bei Silverthorn, Human Physiology - an integrated approach, 4th ed. Pearson International 2007
Abbildung: Verteilung des Herzzeitvolumens in Ruhe und bei Muskelarbeit
Nach einer Vorlage bei Silverthorn, Human Physiology - an integrated approach, 4th ed. Pearson International 2007
Links:
Ein typisches Verteilungsmuster (das von zahlreichen weiteren Faktoren
beeinflusst werden kann) im Ruhezustand. Die Anteile am Herzzeitvolumen
(z.B. 6 l/min) sind in % gezeigt: Gehirn ~0,8 l/min, Coronargefäße ~0,25, Nieren ~1,1, Gastrointestinaltrakt ~1,4, Haut ~0,5, übrige Gewebe ~0,6, Skelettmuskulatur ~1,25 l/min.
Rechts: Die Verteilung bei ~vervierfachtem Herzzeitvolumen (von 6 auf 26 l/min): Gehirn ~0,8 l/min, Coronargefäße ~1, Nieren ~0,25, Gastrointestinaltrakt ~0,25, Haut ~0,65, übrige Gewebe ~0,5, Skelettmuskulatur ~22,8 l/min.

Aus den in der Abbildung gezeigten Beispiel geht hervor, dass - in absoluten Werten - bei körperlicher Belastung die Perfusion
von Gehirn, Haut (stark abhängig vom Wärmehaushalt!) und übrigen
Geweben in etwa gleich bleibt; diejenige von Skelettmuskulatur fast
20-fach, vom Myokard 4-fach ansteigt; und diejenige von Nieren und
Gastrointestinaltrakt stark abnimmt (in einer ergotropen Situation wird
hier durch den erhöhten Sympathikustonus Durchblutung eingespart -
Muskelgewebe deckt hingegen seinen Bedarf durch Autoregulation).
Die Autoregulation
verteilt die Durchblutung bedarfsgerecht auf die
Muskeln so, dass die aktiven (durch Gefäßerweiterung)
besonders
gut perfundiert werden; der Sympathikus
hat im Prinzip vasokonstriktorische Wirkung (auch an nichtaktiver
Muskulatur: "Kollaterale Vasokonstriktion"); die Blutspiegel an
Wachstumshormon und Cortisol nehmen während (akuter Stresseffekt: Bereitstellung von Glucose), der Insulinspiegel nimmt nach körperlicher Belastung zu (Einlagerung mobilisierter Reserven).
 Ruhedurchblutung: Inaktive Muskeln bleiben gering durchblutet (ausgeprägter Basaltonus, keine Vasodilatantien), sodass ein
größerer Prozentsatz des Herzminutenvolumens in die belasteten
Muskelpartien "umgeleitet" wird, während die Gefäße in den weniger
beteiligten Muskeln eng und relativ schwach durchblutet bleiben ("kollaterale Vasokonstriktion").
Ruhedurchblutung: Inaktive Muskeln bleiben gering durchblutet (ausgeprägter Basaltonus, keine Vasodilatantien), sodass ein
größerer Prozentsatz des Herzminutenvolumens in die belasteten
Muskelpartien "umgeleitet" wird, während die Gefäße in den weniger
beteiligten Muskeln eng und relativ schwach durchblutet bleiben ("kollaterale Vasokonstriktion").
 Antizipatorische Mechanismen, central command: Mit beginnender - und während - Muskelaktivität wird (parallel zur Aktivierung der motorischen Hirnrinde) das Kreislaufzentrum
so aktiviert, dass das Herzzeitvolumen zunimmt und der Sympathikustonus
ansteigt (was Vasokonstriktion in nicht aktiven Muskeln und anderen
Organen, wie Nieren und Splanchnikusgebiet, bedingt).
Antizipatorische Mechanismen, central command: Mit beginnender - und während - Muskelaktivität wird (parallel zur Aktivierung der motorischen Hirnrinde) das Kreislaufzentrum
so aktiviert, dass das Herzzeitvolumen zunimmt und der Sympathikustonus
ansteigt (was Vasokonstriktion in nicht aktiven Muskeln und anderen
Organen, wie Nieren und Splanchnikusgebiet, bedingt).
Oberste Instanz dieser zentralen Steuerung ist vor allem der mediale Präfrontalkortex,
zu dessen Aufgaben in dieser Situation die Bewegungsplanung gehört,
sowie Teile des limbischen Sytems (welches intensiv in das Frontalhirn
projiziert) wie die Insel und vordere Anteile des gyrus cinguli.
Diese kortikalen Zentren steuern kreislaufrelevante Aktivitäten des
lateralen Hypothalamus und des Kreislaufzentrums im verlängerten Mark
(vgl. dort).
 Muskelkontraktionen:
Nicht nur wirkt sich die Kreislaufregulation - zusätzlich zur
Autoregulation - auf die Perfusion der Skelettmuskulatur aus; umgekehrt
haben Muskelkontraktionen kardiovaskuläre Effekte, indem sie das Herz
durch rhythmisches Auspressen der venösen Gefäßgeflechte im Muskel
unterstützen (zusätzliche Pumpwirkung - funktioniert nur bei intakten
Venenklappen). Dabei nimmt der venöse Blutdruck in den Beinvenen
deutlich ab (folgende Abbildungen).
Muskelkontraktionen:
Nicht nur wirkt sich die Kreislaufregulation - zusätzlich zur
Autoregulation - auf die Perfusion der Skelettmuskulatur aus; umgekehrt
haben Muskelkontraktionen kardiovaskuläre Effekte, indem sie das Herz
durch rhythmisches Auspressen der venösen Gefäßgeflechte im Muskel
unterstützen (zusätzliche Pumpwirkung - funktioniert nur bei intakten
Venenklappen). Dabei nimmt der venöse Blutdruck in den Beinvenen
deutlich ab (folgende Abbildungen).

 Abbildung: Blutdruck in den Beinen - Effekt von Körperlage und Muskelpumpe
Nach einer Vorlage in Herring / Paterson, Levick's Introduction to Cardiovascular Physiology, 6th ed. 2018
Abbildung: Blutdruck in den Beinen - Effekt von Körperlage und Muskelpumpe
Nach einer Vorlage in Herring / Paterson, Levick's Introduction to Cardiovascular Physiology, 6th ed. 2018
Links:
Der mittlere Druckunterschied zwischen Arterien und Venen beträgt in
diesem Beispiel 85 mmHg. Der arterielle Mitteldruck beträgt etwa 95,
der venöse 10 mmHg.
Mitte: Beim Aufstehen nimmt der Druck in beiden Systemen aus hydrostatischen Gründen zu, der arterio-venöse Unterschied beträgt weiterhin 85 mmHg.
Rechts: Aktivität der Muskulatur (Gehen) aktiviert die Muskelpumpe,
der venöse Druck (blaue Kurve) nimmt als Folge des Auspressens von Blut
aus den Venen wieder ab (Druckpulsationen entsprechend
Muskelkontraktionen), der mittlere arterio-venöse Druckunterschied
nimmt zu (hier auf 130 mmHg)
Arterielle Pulsationen nicht berücksichtigt (rote Kurve: Arterieller Mitteldruck)
 Verstärkte Durchblutung bei Muskelarbeit wird durch vasodilatatorisch wirkende Mediatoren
erreicht, die in das Interstitium freigesetzt werden. Zu diesen lokalen Faktoren gehören
Verstärkte Durchblutung bei Muskelarbeit wird durch vasodilatatorisch wirkende Mediatoren
erreicht, die in das Interstitium freigesetzt werden. Zu diesen lokalen Faktoren gehören
 Kaliumionen (interstitielles [K+]
steigt zu Beginn der Muskelarbeit von 4-5 bis auf 10 mM - der
Rücktransport in die Zellen durch deren Na/K-ATPase ist vorübergehend
überfordert)
Kaliumionen (interstitielles [K+]
steigt zu Beginn der Muskelarbeit von 4-5 bis auf 10 mM - der
Rücktransport in die Zellen durch deren Na/K-ATPase ist vorübergehend
überfordert)
 Stickstoffmonoxid
Stickstoffmonoxid
 Lactat / H+
Lactat / H+
 Stickstoffmonoxid (NO) insbesondere in größeren arteriellen Versorgungsgefäßen, in denen die starke Blutströmung Scherkräfte am Endothel zu NO-Abgabe führen
Stickstoffmonoxid (NO) insbesondere in größeren arteriellen Versorgungsgefäßen, in denen die starke Blutströmung Scherkräfte am Endothel zu NO-Abgabe führen
 Erhöhung der Osmolarität: Der Kaliumspiegel im Interstitium intensiv
aktiver Muskeln kann sich mehr als verdoppeln, der Lactatspiegel von
<1 mM bis auf 30 mM ansteigen, die osmotische Konzentration um bis
zu 40 mOsm zunehmen
Erhöhung der Osmolarität: Der Kaliumspiegel im Interstitium intensiv
aktiver Muskeln kann sich mehr als verdoppeln, der Lactatspiegel von
<1 mM bis auf 30 mM ansteigen, die osmotische Konzentration um bis
zu 40 mOsm zunehmen
 Veränderungen der Gaspartialdrucke (Anstieg pCO2, Abfall pO2).
Veränderungen der Gaspartialdrucke (Anstieg pCO2, Abfall pO2).
Dazu kommen zentrale
Elemente: Nervale und hormonelle Regulation trägt zur Vasodilatation in
der Skelettmuskulatur bei.
 Die Arteriolen in der Skelettmuskulatur verfügen sowohl über α1- als auch über ß2-Adrenozeptoren.
Erstere kontrahieren, letztere dilatieren die Gefäße; erstere haben
geringere Affinität zu Adrenalin als letztere. Daher überwiegt der
gefäßerweiternde Effekt - Adrenalin erhöht die Durchblutung
der Muskeln.
Die Arteriolen in der Skelettmuskulatur verfügen sowohl über α1- als auch über ß2-Adrenozeptoren.
Erstere kontrahieren, letztere dilatieren die Gefäße; erstere haben
geringere Affinität zu Adrenalin als letztere. Daher überwiegt der
gefäßerweiternde Effekt - Adrenalin erhöht die Durchblutung
der Muskeln.
Zu berücksichtigen ist die Komprimierung der Gefäße bei der Muskeltätigkeit ("Muskelpumpe"),
welche in Zusammenarbeit mit den Venenklappen des Rücktransport des
Blutes zum Herzen sichert (insbesondere in den Beinen, wo der Effekt
des hydrostatischen Drucks überwunden werden muss).
 Zu den kardiovaskulären Umstellungen bei Muskelbelastung zählen
weiters erhöhter venöser Rückstrom von Blut zum Herzen, Freisetzung von
Adrenalin aus dem Nebennierenmark sowie eine situationsadäquate
Regulation der Körpertemperatur.
Zu den kardiovaskulären Umstellungen bei Muskelbelastung zählen
weiters erhöhter venöser Rückstrom von Blut zum Herzen, Freisetzung von
Adrenalin aus dem Nebennierenmark sowie eine situationsadäquate
Regulation der Körpertemperatur.
Insbesondere
bei Arbeit in heißer Umgebung kommt es zu einem Konflikt zwischen den
metabolischen Bedürfnissen der arbeitenden Muskulatur und der
Notwendigkeit, den Köper (über die Haut) zu kühlen. Die Intaktheit des
zentralen Blutvolumens ist in solchen Situationen durch mehrere
Faktoren gefährdet:
 Flüssigkeit wandert aus der Blutbahn in den interstitiellen Raum (2a in der
Flüssigkeit wandert aus der Blutbahn in den interstitiellen Raum (2a in der  Abbildung)
Abbildung)
 Flüssigkeit geht durch Schwitzen verloren (2b)
Flüssigkeit geht durch Schwitzen verloren (2b)
 Dilatation der Hautgefäße bewirkt Umverteilung von Blut in die
Hautvenen, mit der Folge einer Reduktion des venösen Rückstroms zum
Herzen (
Dilatation der Hautgefäße bewirkt Umverteilung von Blut in die
Hautvenen, mit der Folge einer Reduktion des venösen Rückstroms zum
Herzen ( 2c)
2c)
Als Folge nimmt das zentrale Blutvolumen - dessen Größe
einerseits vom extrazellulären Flüssigkeitsvolumen, andererseits vom
Muster der vasomotorischen Einflüsse abhängt, 3 in der  Abbildung) - ab und muss
prioritär "verteidigt" werden. Dies erfolgt via Niederdruckrezeptoren,
Kreislaufzentrum, sympathischen Efferenzen und Vasokonstriktion von
Gefäßen im Splanchnicusbereich, in der Haut und in der Muskulatur (4).
Abbildung) - ab und muss
prioritär "verteidigt" werden. Dies erfolgt via Niederdruckrezeptoren,
Kreislaufzentrum, sympathischen Efferenzen und Vasokonstriktion von
Gefäßen im Splanchnicusbereich, in der Haut und in der Muskulatur (4).
 Nach der Muskeltätigkeit kommt es typischerweise zu reaktiver Hyperämie,
in deren Verlauf die während der Muskelaktivität durch ungenügende
Perfusion entstandenen Versorgungsdefizite wieder ausgeglichen werden
(insbesondere bei statischer, d.h. Haltearbeit, welche die Durchblutung
stark einschränkt - im Gegensatz zu dynamischer Muskelbelastung).
Nach der Muskeltätigkeit kommt es typischerweise zu reaktiver Hyperämie,
in deren Verlauf die während der Muskelaktivität durch ungenügende
Perfusion entstandenen Versorgungsdefizite wieder ausgeglichen werden
(insbesondere bei statischer, d.h. Haltearbeit, welche die Durchblutung
stark einschränkt - im Gegensatz zu dynamischer Muskelbelastung).
In der folgenden Tabelle werden typische Ruhe- und Belastungswerte
(gesunde jugendliche Probanden) zusammengefasst (Spitzentrainierte
können höhere Werte aufweisen):
|
Ruhe
|
körperliche Ausbelastung
|
Herzzeitvolumen, liegend (l/min)
|
7
|
15-30
|
Herzfrequenz (bpm)
|
70
|
bis 200
|
Schlagvolumen (ml)
|
60-70
|
80-150
|
systolischer Blutdruck
|
120
|
180
|
diastolischer Blutdruck
|
80
|
80
|
Sauerstoffaufnahme
(l/min)
|
0,3
|
3-4
|
Atemzugvolumen (ml)
|
350
|
bis 2000
|
Atemfrequenz (Anzahl Atemzüge / min)
|
12-16
|
45-60
|
Sauerstoffausschöpfung (ml O2 / l Blut)
|
40-60
|
120-180 (Kapazität ~200)
|
Atemminutenvolumen
(l/min)
|
4-5
|
90-120
|

Muskelarbeit und Muskelschwellung:
Muskelaktivität erhöht sowohl intrazellulär (Lactat, Abbau von Kreatinphosphat) als auch extrazellulär (Lactat, Kaliumionen) die
Osmolalität um bis zu 10% (
~30 mOsm). Das führt zu einem osmotisch bedingten Wassereinstrom aus dem Blut (das Endothel der Muskelkapillaren ist reich an Aquaporinen). Auf diese Weise kann das Muskelvolumen vorübergehend um bis zu ~20% ansteigen, teils intra-, teils extrazellulär.
Weiters führt (autoregulative) Vasodilatation im arbeitenden Muskel zu Druckanstieg in den Kapillaren und verstärkter Auswärtsfiltration. Schließlich nimmt auch die Zahl offener Kapillaren zu (capillary recruitment), und dadurch steigt die Filtrationskapazität.
Die Nutzung energiereicher Substrate unterliegt auch hormonellen
Einflüssen. Körperliche Belastung steigert den Blutspiegel einer Reihe
von "Stresshormonen", wie Adrenalin, Wachstumshormon, Cortisol, auch
Glukagon. Sie alle steigern den Blutzuckerspiegel und erleichtern so die Energieversorgung der Skelettmuskulatur. Die
Insulinfreisetzung aus dem Pankreas wird durch erhöhten
Sympathikustonus unterdrückt, die Freisetzung von Fettsäuren aus
Adipozyten hingegen gefördert (Fettsäuren stellen den führenden
Energielieferanten für die Muskulatur dar). Nach Beendigung der
Belastung steigt der Insulinspiegel im Blut, was das Auffüllen von
Energiereserven im Muskel (GLUT4) unterstützt.
Länge, Kraft, Geschwindigkeit und Form der Kontraktion

Dehnt man einen Muskel, treten passive Gegenkräfte auf (sowohl aus den Muskelfasern als auch aus bindegewebigen Strukturen).
Die entsprechende Längen-Kraft-Beziehung wird durch die Ruhedehnungskurve
beschrieben ( Abbildung oben: blaue Kurve). Kommt es zusätzlich zur
Aktivierung des kontraktilen Apparats, entsteht
Kontraktionskraft (
Abbildung oben: blaue Kurve). Kommt es zusätzlich zur
Aktivierung des kontraktilen Apparats, entsteht
Kontraktionskraft ( rote Kurve für isometrische Maximalkontraktionen).
rote Kurve für isometrische Maximalkontraktionen).
In Summe ist die resultierende Kraft
(grün) bei geringer Faserlänge weitgehend eine aktive Komponente, bei
stark (vor)gedehnter Faser nimmt der "passive" Teil zu (und der aktive
ab, da die Überlappung von Aktin- und Myosinfilamenten und damit die
Zahl der aktiven Querbrücken abnimmt). Die aktive Kraftausbeute ist am
höchsten, wenn die Faser etwa ihre normale Ruhelänge hat (Sarkomerlänge etwas mehr als 2 µm); unter ~70%
und über ~150% der Ruhelänge kommt es kaum noch zu Kraftentwicklung (ungünstige Positionierung der Querbrücken im Sarkomer).
Wirkungsgrad: Die Effizienz
der Muskelarbeit lässt sich über ihren Wirkungsgrad angeben. Der Wirkungsgrad ist folgendermaßen definiert:
| Wirkungsgrad = mechanische Arbeit / gesamter Stoffwechselaufwand |
Dies ist eine dimensionslose Zahl, die ein Energieverhältnis
bezeichnet, nämlich die von der betreffenden Muskulatur für
Arbeitsleistung verbrauchte bezogen auf die insgesamt umgesetzte
Stoffwechselenergie (z.B. angegeben in kJ). Der Wirkungsgrad
von Muskeln beträgt maximal ~26% (bei statischer Haltearbeit -
ismetrische Kontraktion - beträgt er 0, weil dabei keine mechanische
Arbeit geleistet wird).


Abbildung: Kraft-Geschwindigkeits-Beziehung (Skelettmuskel)
Nach
Sejersted OM, Sjøgaard G. Dynamics and Consequences of Potassium Shifts
in Skeletal Muscle and Heart During Exercise. Physiol Rev 2000; 80:
1411-81
Maximale
Kraft bei geringster Kontraktionsgeschwindigkeit, maximale
Kontraktionsgeschwindigkeit (Vmax) bei geringster Kraft (dünne Kurven).
Höchste Leistung bei mittlerer Kraft und Kontraktionsgeschwindigkeit
(dicke Kurven).
Durchgezogene Kurven und rote Pfeilspitzen: Erholter
Muskel, strichlierte Kurven und blaue Pfeilspitzen: erschöpfter Muskel,
dazwischen (Pfeile): Ermüdung

 Kontraktionsformen: Meist geht eine
Muskelkontraktion sowohl mit Verkürzung als auch Kraftentfaltung
einher; diese Komponenten lassen sich jedoch trennen, entweder zeitlich
(z.B. zuerst Kraftanstieg, dann Verkürzung -
"Unterstützungskontraktion", oder plyometrische
Kontraktionsformen: Meist geht eine
Muskelkontraktion sowohl mit Verkürzung als auch Kraftentfaltung
einher; diese Komponenten lassen sich jedoch trennen, entweder zeitlich
(z.B. zuerst Kraftanstieg, dann Verkürzung -
"Unterstützungskontraktion", oder plyometrische
 Kontraktionsformen - z.B. bei Hochspringen, Sprint), oder entsprechend Arretierung auf Verkürzung bei
konstanter Kraftentfaltung ("isotonisch"
Kontraktionsformen - z.B. bei Hochspringen, Sprint), oder entsprechend Arretierung auf Verkürzung bei
konstanter Kraftentfaltung ("isotonisch"  ) oder Kraftentwicklung bei
konstanter Länge ("isometrisch"
) oder Kraftentwicklung bei
konstanter Länge ("isometrisch"  ).
).
Der Muskel kann sich während seiner
Kraftentfaltung verkürzen (konzentrisch), aber auch gedehnt werden (exzentrische Kontraktion). So ergeben sich kennzeichnende Relationen zwischen Kraft, Geschwindigkeit und Leistung des Muskels.
 Die Kontraktionsgeschwindigkeit nimmt mit zunehmender Kraft, die der Muskel aufbringt, ab, und vice versa.
Die Kontraktionsgeschwindigkeit nimmt mit zunehmender Kraft, die der Muskel aufbringt, ab, und vice versa.
Die höchste Leistung erbringt ein Muskel bei ~1/3 seiner Maximalkraft und ~1/3 seiner maximalen Verkürzungsgeschwindigkeit
|
Einzelzuckungen erfolgen durch singuläre
Entladungen der motorischen Vorderhornzellen (wie bei der Testung von Muskelspindelreflexen,
z.B. dem Patellarsehnenreflex). Tetanische
Kontraktionen sind die
physiologische Kontraktionsform; (physiologischer) Tetanus
bedeutet die Verschmelzung des Effekts einzelner Aktionspotentiale,
deren rasche Abfolge zu einer weitgehenden Aktivierung des
intrazellulär gespeicherten Calciums und dadurch maximaler
Kontraktionskraft ("Maximum") führt.
 Ein "Maximum" (auxotonisch, isometrisch, isotonisch) ist dadurch gekennzeichnet, dass alle Muskelfasern an der Kontraktion teilnehmen.
Ein "Maximum" (auxotonisch, isometrisch, isotonisch) ist dadurch gekennzeichnet, dass alle Muskelfasern an der Kontraktion teilnehmen.
Schließlich steigt die Kraftausbeute in einem Muskel mit der Zahl der aktivierten motorischen Einheiten;
diese hängt vom Entladungsverhalten der entsprechenden motorischen
Vorderhornzellen ab (d.h. wie viele der im Muskel vorhandenen motorischen
Einheiten vom ZNS "eingeschaltet" werden).
Größe der motorischen Einheit: Kleine motorische
Vorderhornzellen versorgen kleinere motorische Einheiten und werden
früher überschwellig erregt (EPSP-Summation)
als große; kleine motorische Einheiten sind also öfter aktiv als große,
die nur bei hohen mechanischen Anforderungen aktiviert werden (recruitment).
 Regelmäßige Belastung und Kontraktionsauslösung ist der
physiologische Anreiz zu anabolem Stoffwechsel (Erhaltung des Bestandes
an Energiegewinnungsapparat, kontraktilen Proteinen etc.). Atrophie ist der Abbau von Muskelmasse aufgrund ungenügender Belastung und/oder Durchblutung. Hypertrophie ist eine erhöhte Masse und Kraft bestehender Muskelfasern, Hyperplasie eine Neubildung von Muskelfasern.
Regelmäßige Belastung und Kontraktionsauslösung ist der
physiologische Anreiz zu anabolem Stoffwechsel (Erhaltung des Bestandes
an Energiegewinnungsapparat, kontraktilen Proteinen etc.). Atrophie ist der Abbau von Muskelmasse aufgrund ungenügender Belastung und/oder Durchblutung. Hypertrophie ist eine erhöhte Masse und Kraft bestehender Muskelfasern, Hyperplasie eine Neubildung von Muskelfasern.
Die
Muskulatur ist - je nach hauptsächlich zu verrichtendem Arbeitsprofil
(Gelenk, auf das einzuwirken ist) - spezialisiert auf z.B. rasche
Kraftentwicklung oder ausdauernde Haltearbeit.

Abbildung: Slow- vs. Fast-twitch-Fasern
Nach einer Vorlage bei McGraw-Hill, in: classes.midlandstech.edu
"Rote" (myoglobinreiche) Typ-I-Fasern
sind ausdauernd, aber langsam (slow twitch), sie decken ihren Energiebedarf
unmittelbar aerob und sind daher besser kapillarisiert.
"Weiße" Typ-II-Fasern reagieren schnell (fast twitch), gehen dabei eine "Sauerstoffschuld" ein und ermüden rasch; der Kapillarisierungsgrad ist geringer.
Frauen verfügen über mehr Typ-I-Fasern als Männer (Ausdauer),
Männer hingegen über mehr Typ-II-Fasern (Spitzenkraft)

Tatsächlich sind
Muskelfasern unterschiedlich mit Mechanismen zur Kraftentfaltung /
Verkürzung und Energiegewinnung ausgestattet (abhängig vom Ausmaß der ATPase-Aktivität der Myosinköpfe) und lassen sich
folgendermaßen klassifizieren:
 ”Rote“ Muskelfasern
(langsam kontrahierende, Typ I, 'slow-twitch' -
”Rote“ Muskelfasern
(langsam kontrahierende, Typ I, 'slow-twitch' -  Abbildung) sind eher dünn, dicht kapillarisiert, verfügen über
viel
Myoglobin (Sauerstoffspeicher - größere O2-Reserve als Typ II-Fasern) und Mitochondrien, haben hohe aerobe
Kapazität,
vollbringen vorwiegend Haltearbeit
(z.B. Rückenmuskulatur) und ermüden sehr langsam bis gar nicht. Ihre
Kraftausbeute pro Zuckung ist aber gering (etwa ein Zehntel der
Kraftentwicklung von Fasern des Typs IIx).
Skelettmuskeln
sind unterschiedlich mit Typ-I-Fasern
ausgestattet, z.B. zu ~35% im Trizeps (rasch aktiviert, rasch
ermüdend), ~90% im Soleus (ausdauernd, Haltearbeit). Typ-I-Fasern sind
von Inaktivität (z.B. längere Bettlägerigkeit) besonders betroffen; so
nimmt der M. soleus in solchen Situationen stark an Masse und Kraft ab.
Abbildung) sind eher dünn, dicht kapillarisiert, verfügen über
viel
Myoglobin (Sauerstoffspeicher - größere O2-Reserve als Typ II-Fasern) und Mitochondrien, haben hohe aerobe
Kapazität,
vollbringen vorwiegend Haltearbeit
(z.B. Rückenmuskulatur) und ermüden sehr langsam bis gar nicht. Ihre
Kraftausbeute pro Zuckung ist aber gering (etwa ein Zehntel der
Kraftentwicklung von Fasern des Typs IIx).
Skelettmuskeln
sind unterschiedlich mit Typ-I-Fasern
ausgestattet, z.B. zu ~35% im Trizeps (rasch aktiviert, rasch
ermüdend), ~90% im Soleus (ausdauernd, Haltearbeit). Typ-I-Fasern sind
von Inaktivität (z.B. längere Bettlägerigkeit) besonders betroffen; so
nimmt der M. soleus in solchen Situationen stark an Masse und Kraft ab.
Es besteht auch eine deutliche Geschlechtsabhängigkeit (
Sexualdimorphismus)
bei der Verteilung der Muskelfasertypen: Frauen verfügen über mehr
Typ-I-Fasern als Männer, was ihr Bewegungssystem ausdauernder macht -
Männer können hingegen höhere Spitzenbelastungen tolerieren.
 ”Weiße“
Muskelfasern
(rasch kontrahierende, Typ II, 'fast-twitch') haben hingegen weniger Myoglobin, aber höhere ATPase-Aktivität als rote Fasern und dienen
schnellen,
”phasischen“ Kontraktionen. Sie entwickeln rasch Spitzenkräfte und sind
auf kurze Arbeitszyklen spezialisiert. Sie verfügen über relativ wenig
Mitochondrien, stützen sich überwiegend auf glykolytische
Energiegewinnung
(sie enthalten viel Glykogen) und sind rasch ermüdbar (z.B.
Bizeps, Trizeps). Ihr Kapillarisierungsgrad ist geringer als bei
Typ-I-Fasern, d.h. jede Kapillare versorgt ein größeres
Muskelfasergebiet als das Kapillaren in slow-twitch-Fasern tun - wegen
des relativ geringeren Sauerstoffbedarfs können sie es sich leisten.
”Weiße“
Muskelfasern
(rasch kontrahierende, Typ II, 'fast-twitch') haben hingegen weniger Myoglobin, aber höhere ATPase-Aktivität als rote Fasern und dienen
schnellen,
”phasischen“ Kontraktionen. Sie entwickeln rasch Spitzenkräfte und sind
auf kurze Arbeitszyklen spezialisiert. Sie verfügen über relativ wenig
Mitochondrien, stützen sich überwiegend auf glykolytische
Energiegewinnung
(sie enthalten viel Glykogen) und sind rasch ermüdbar (z.B.
Bizeps, Trizeps). Ihr Kapillarisierungsgrad ist geringer als bei
Typ-I-Fasern, d.h. jede Kapillare versorgt ein größeres
Muskelfasergebiet als das Kapillaren in slow-twitch-Fasern tun - wegen
des relativ geringeren Sauerstoffbedarfs können sie es sich leisten.
In der Gruppe der Typ II-Fasern unterscheidet man weiters
 Typ IIa (fast, fatigue-resistant - relativ ausdauernd, ermüden langsam, mäßige Kraftausbeute pro Kontraktion) und
Typ IIa (fast, fatigue-resistant - relativ ausdauernd, ermüden langsam, mäßige Kraftausbeute pro Kontraktion) und
 Typ IIx (fast, fatiguable - extrem glykolyseabhängig, ermüden rapide, hohe Kraftausbeute pro Kontraktion).
Typ IIx (fast, fatiguable - extrem glykolyseabhängig, ermüden rapide, hohe Kraftausbeute pro Kontraktion).

 Alter und Muskelfitness: Typ-II-Fasern
nehmen an Kraft und Volumen vor allem mit zunehmendem Alter
ab, wenn die Muskeln nicht fit gehalten werden. Regelmäßiges
Krafttraining verringert diesen altersabhängigen Verlust an
fast-twitch-Muskelfasern und hat darüber hinaus weitere
gesundheitsfördernde Effekte (Kreislauf: Blutdruck; Metabolismus:
Diabetesprävention; Knochen: Osteoporoseprophylaxe; Gelenke: Nährstoffversorgung, Stabilisierung; Endorphinsekretion: Stressreduktion).
Alter und Muskelfitness: Typ-II-Fasern
nehmen an Kraft und Volumen vor allem mit zunehmendem Alter
ab, wenn die Muskeln nicht fit gehalten werden. Regelmäßiges
Krafttraining verringert diesen altersabhängigen Verlust an
fast-twitch-Muskelfasern und hat darüber hinaus weitere
gesundheitsfördernde Effekte (Kreislauf: Blutdruck; Metabolismus:
Diabetesprävention; Knochen: Osteoporoseprophylaxe; Gelenke: Nährstoffversorgung, Stabilisierung; Endorphinsekretion: Stressreduktion).
Die Muskelfasertypen I und II unterscheiden sich auch in ihrer biochemischen Ausstattung (Tabelle):
Skelettmuskelfasertypen im Vergleich
Modifiziert nach MaxIntosh BR, Gardiner PF, McComas AJ: Skeletal Muscle: Form and Function. Human Kinetics 2006
|
Eigenschaft
|
Typ I
|
Typ IIa
|
Typ IIx
|
Geschwindigkeit
|
langsam
|
rasch
|
rasch
|
Kraft
|
gering
|
mittel
|
hoch
|
Ermüdbarkeit
|
gering
|
gering
|
hoch
|
Glykogengehalt
|
niedrig
|
hoch
|
hoch
|
Kapillardichte
|
hoch
|
mittel
|
gering
|
Myoglobinkonzentration
|
hoch
|
hoch
|
niedrig
|
Rotfärbung
|
dunkel
|
dunkel
|
hell
|
Mitochondriendichte
|
hoch
|
hoch
|
gering
|
Motorische Einheit
|
langsam-oxidativ (SO)
|
rasch-oxidativ / glykolytisch (FOG)
|
rasch-glykolytisch (FG)
|
Kapazität oxidativer Enzyme
|
hoch
|
mittel bis hoch
|
niedrig
|
Phosphorylase-Aktivität*
|
niedrig
|
hoch
|
hoch
|
Lactatdehydrogenase-
Aktivität**
|
niedrig
|
hoch
|
hoch
|
Phospholamban***
|
vorhanden
(auch SERCA)
|
|
(nur Serca)
|
* Phosphorylasen produzieren u.a. Glucose-1-Phosphat aus Glykogen
** Lactatdehydrogenase (LDH) erleichtert die Konversion zwischen Lactat und Pyruvat
*** Phosphoryliertes Phospholamban 
fördert die Ca
++-Aufnahme ins sarkoplasmatische Retikulum
Dementsprechend können Typ-II-Fasern hohe tetanische Kraft
entfalten - allerdings ermüden sie während des Tetanus auch rasch -,
und ihr Energieverbrauch ist (im Vergleich zur roten Muskulatur) hoch.
 Die Typisierung der verschiedenen Muskelfasern ist idealtypisch zu verstehen, tatsächlich gibt es ein Kontinuum
von Typ I- bis Typ IIx-Fasern. Außerdem kann sich diese Verteilung auch
ändern, je nachdem, wie das Belastungsprofil des Muskels über eine
längere Zeit aussieht (Trainingsabhängigkeit).
Die Typisierung der verschiedenen Muskelfasern ist idealtypisch zu verstehen, tatsächlich gibt es ein Kontinuum
von Typ I- bis Typ IIx-Fasern. Außerdem kann sich diese Verteilung auch
ändern, je nachdem, wie das Belastungsprofil des Muskels über eine
längere Zeit aussieht (Trainingsabhängigkeit).

Krafttraining hingegen (anaerobisches, strength training)
wirkt auf Typ IIx-Fasern trophisch (rasche Kraftentfaltung mit erhöhtem
Besatz mit kontraktilen Proteinen). Der Durchmesser der Muskelfasern
nimmt zu ("body building"), ihre Durchhaltedauer ist aber gering ( Abbildung).
Abbildung).
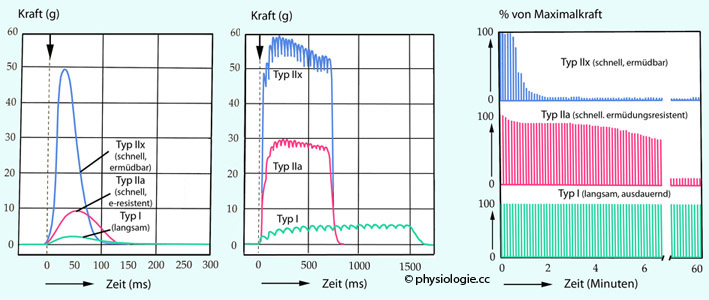
 Abbildung: Kraftentfaltung und Ermüdbarkeit verschiedener Muskelfasertypen
Nach einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Abbildung: Kraftentfaltung und Ermüdbarkeit verschiedener Muskelfasertypen
Nach einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Links:
Kraftentwicklung nach elektrischer Reizung, die ein einzelnes
Aktionspotential auslöst (Einzelzuckungen). Die höchste
Kraftentwicklung zeigen Typ IIx-Muskelfasern, die geringste Typ
I-Muskelfasern.
Mitte: Kraftentwicklung nach repetitiver elektrischer Reizung, die eine Aktionspotentialsalve auslöst (unvollständiger
Tetanus). Zeichen der Ermüdung zeigen sich vor allem bei Typ
IIx-Fasern, weniger bei Typ IIa-Fasern, bei Typ I-Fasern gar nicht.
Rechts: Kraftentwicklung
bei fortgesetzter kontinuierlicher Reizung (Registrierdauer 60
Minuten). Typ I-Fasern entwickeln relativ geringe Kraft,
ermüden aber nicht (die Kraftentwicklung bleibt konstant bei dem
Betrag, der zu Beginn der Reizung registriert wurde); Typ II-Fasern
entwickeln höhere Kräfte, aber nur
für kurze Zeit (insbesondere der Typ IIx).

Ermüdung der Muskeln kann im Organ selbst (peripher) oder durch nachlassenden Antrieb aus dem ZNS (zentral) begründet sein. Periphere
Ermüdung involviert nachlassende Erregbarkeit sowie sinkende
Freisetzung von Calciumionen im Muskel. Bei hoher Erregungsfrequenz (high-frequency fatigue)
liegt die Ermüdung an einer Überforderung der Na/K-ATPasen der
Zellmembran, Inaktivierung spannungsgesteuerter Natriumkanäle und damit
abnehmende Generierung und Leitung von Aktionspotentialen. Diese Art
der Ermüdung betrifft vor allem Typ II- motorische Einheiten. Bei Typ
I- motorischen Einheiten stellt sich bei Dauerbelastung low-frequency fatigue ein: Die Ca++-Freisetzung
aus dem sarkoplasmatischen Retikulum nimmt ab, bedingt durch
Erschöpfung der SERCA und damit mangelndem Wiederauffüllen der Speicher
in der Kontraktionspause.
Zu den peripheren Mechanismen der Ermüdung kommen auch zentrale (central fatigue),
bedingt durch veränderte Meldungen sensorischer Afferenzen,
nachlassende efferente Impulse zu motorischen Vorderhornzellen, die
außerdem mit der Zeit an Erregbarkeit einbüßen. Trainierte Sportler
können den Einfluss solcher Faktoren minimieren, auch anspornende
externe Reize (Zurufe etc) wirken stimulierend.
Zusammengefasst: Bei geringer Arbeitsleistung werden vor allem Typ-I-Fasern - mit niedriger Stimulationsfrequenz - beansprucht (unabhängig von der Belastungsdauer); bei starker Belastung (kurzdauernde Höchstleitung) werden zusätzlich Typ-II-Fasern - mit hoher Stimulationsfrequenz - rekrutiert.
 Die
Ausstattung des Muskels mit Typ-I vs. Typ-II-Fasern kann sich je nach
Anforderungen ändern, z.B. gibt es bei längerer Bettruhe in Muskeln,
die normalerweise Haltearbeit leisten, eine Musterverschiebung von Typ
I zu Typ II ("Dekonditionierungseffekt" Richtung fast-twitch-Fasern). Als Trainingseffekt - mit anhaltender Belastung - tritt umgekehrt eine Verschiebung in Richtung Typ I auf, womit Ausdauerleistungen möglich werden.
Die
Ausstattung des Muskels mit Typ-I vs. Typ-II-Fasern kann sich je nach
Anforderungen ändern, z.B. gibt es bei längerer Bettruhe in Muskeln,
die normalerweise Haltearbeit leisten, eine Musterverschiebung von Typ
I zu Typ II ("Dekonditionierungseffekt" Richtung fast-twitch-Fasern). Als Trainingseffekt - mit anhaltender Belastung - tritt umgekehrt eine Verschiebung in Richtung Typ I auf, womit Ausdauerleistungen möglich werden.
Wie man Muskeln und Kreislauf trainieren kann
Muskeltraining (body building)
erhöht die Kraft und dann auch den Durchmesser der Muskelfasern (nicht ihre Zahl). Das Training kann auf größtmögliche Kraft oder Ausdauer optimiert werden. Krafttraining zielt auf Hypertrophie und bessere neuromuskuläre Koordination ab, es kann isometrisch oder dynamisch erfolgen. Ausdauertraining wiederum kann auf anaerobe oder aerobe Ausdauer abstellen.
Die Kapillarisierung der Muskeln - dies steigert den maximal erzielbaren Austausch von Atemgasen - und die maximal mögliche Muskelperfusion steigen an, die Zahl der Mitochondrien steigt, wodurch die aerobe Kapazität zunimmt. Auch die Größe der Mitochondrien nimmt zu, ebenfalls die Myoglobinkonzentration. Die Muskelzellen exprimieren mehr GLUT4,
werden sensitiver gegenüber Insulin, steigern die Aktivität der
Lipoproteinlipase, von oxidativen Enzymen (Zitratzyklus, ß-Oxidation)
sowie der Glykogensynthase.
Die systemischen Hauptfaktoren der Anpassung an erhöhte Muskelbelastung sind die folgenden:
 Die Atemmechanik wird effizienter (optimierte Bewegungskoordination), das maximale Atemminutenvolumen verdoppelt sich von ~100 l/min auf ~200 l/min (das Ruhe-Atemminutenvolumen bleibt mit 6-8 l/min unverändert).
Die Atemmechanik wird effizienter (optimierte Bewegungskoordination), das maximale Atemminutenvolumen verdoppelt sich von ~100 l/min auf ~200 l/min (das Ruhe-Atemminutenvolumen bleibt mit 6-8 l/min unverändert).
 Der maximale Sauerstoffverbrauch kann bis auf 80 ml/min/kg KG etwa verdoppelt werden (der Ruhewert bleibt unverändert bei 3,5 ml O2/min/kg KG).
Der maximale Sauerstoffverbrauch kann bis auf 80 ml/min/kg KG etwa verdoppelt werden (der Ruhewert bleibt unverändert bei 3,5 ml O2/min/kg KG).
 Das Schlagvolumen
des Herzens kann bis auf das Doppelte zunehmen (Ruhe: Untrainiert 70
ml, hochtrainiert bis 140 ml; Belastung: Untrainiert 100 ml,
hochtrainiert bis 190 ml), dies ermöglicht die bei Spitzenbelastung nötige Erhöhung des maximalen Herzminutenvolumens von ~15 auf bis zu ~30 l/min (
Das Schlagvolumen
des Herzens kann bis auf das Doppelte zunehmen (Ruhe: Untrainiert 70
ml, hochtrainiert bis 140 ml; Belastung: Untrainiert 100 ml,
hochtrainiert bis 190 ml), dies ermöglicht die bei Spitzenbelastung nötige Erhöhung des maximalen Herzminutenvolumens von ~15 auf bis zu ~30 l/min ( s. auch dort). Auch das enddiastolische Volumen nimmt linksventrikulär zu, und das Gesamtvolumen des Herzens kann sich von ~700 auf ~1400 ml erhöhen. Das Ruhe-Herzzeitvolumen bleibt unverändert.
s. auch dort). Auch das enddiastolische Volumen nimmt linksventrikulär zu, und das Gesamtvolumen des Herzens kann sich von ~700 auf ~1400 ml erhöhen. Das Ruhe-Herzzeitvolumen bleibt unverändert.
Das Ruhe-Schlagvolumen des Herzens sowie das Blutvolumen im Kreislauf steigen infolge körperlichen Trainings, die Ruhe-Herzfrequenz nimmt ab
|
 Der Ruhepuls
des trainierten Menschen nimmt durch erhöhten Vagustonus ab (bis unter
40 bpm). Kombiniert mit dem größeren Schlagvolumen ergibt das eine
höhere Kapazität für die Steigerung der Auswurfleistung des Herzens bei
körperlicher Belastung. Die maximale Herzfrequenz ändert sich durch Training hingegen nicht (~200 bpm).
Der Ruhepuls
des trainierten Menschen nimmt durch erhöhten Vagustonus ab (bis unter
40 bpm). Kombiniert mit dem größeren Schlagvolumen ergibt das eine
höhere Kapazität für die Steigerung der Auswurfleistung des Herzens bei
körperlicher Belastung. Die maximale Herzfrequenz ändert sich durch Training hingegen nicht (~200 bpm).
 Das Blutvolumen nimmt zu (Hypervolämie), dadurch nimmt die maximale Perfusionskapazität des
Kreislaufs zu und es können höhere Volumenverluste durch Schwitzen
verkraftet werden.
Das Blutvolumen nimmt zu (Hypervolämie), dadurch nimmt die maximale Perfusionskapazität des
Kreislaufs zu und es können höhere Volumenverluste durch Schwitzen
verkraftet werden.
 Die Pufferkapazität des Blutes nimmt zu, dadurch werden Lactatspitzen bei Hochleistung besser abgefangen.
Die Pufferkapazität des Blutes nimmt zu, dadurch werden Lactatspitzen bei Hochleistung besser abgefangen.
 Die Körperzusammensetzung ändert sich: Die Muskelmasse steigt (lean body mass), Körperfett nimmt ab.
Die Körperzusammensetzung ändert sich: Die Muskelmasse steigt (lean body mass), Körperfett nimmt ab.
Typische Werte physiologischer Zustandsvariablen in Ruhe und bei maximaler Belastung
Untrainierte vs. trainierte Personen

Modifiziert nach Gekle et al, Taschenbuch Physiologie, Thieme 2010 |
|
Untrainiert
|
Trainiert
|
In Ruhe
|
Maximal
|
In Ruhe
|
Maximal
|
Herzgewicht (g)
|
300
|
500
|
Herzfrequenz (bpm)
|
80
|
180
|
40
|
180-200
|
Schlagvolumen (ml)
|
70
|
100
|
140
|
190
|
Herzzeitvolumen (l/min)
|
5,6
|
15-20
|
5,6
|
25-30
|
Atemzeitvolumen (l/min)
|
~8
|
~100
|
~8
|
~200
|
Sauerstoffaufnahme (l/min)
|
0,3
|
2,8
|
0,3
|
5,2
|
Blutvolumen (l)
|
5,6
|
5,9
|
Systol. Blutdruck (mmHg)
|
~120
|
~200
|
~120
|
~200
|
Diastol. Blutdruck (mmHg)
|
~80
|
~80
|
~80
|
~80
|
Laufen, Blutzucker, Alterung, Immobilisierung
 Optimierung: Der Energieverbrauch nimmt beim Gehen mit
zunehmendem Fortbewegungstempo - vor allem bei höherer Geschwindigkeit
nichtlinear - zu; der Mensch bewegt sich bei über ~8 km/h im Laufen
energieeffizienter fort, d.h. der Sauerstoffverbrauch ist im Laufen
geringer als beim Gehen mit gleichem Tempo (
Optimierung: Der Energieverbrauch nimmt beim Gehen mit
zunehmendem Fortbewegungstempo - vor allem bei höherer Geschwindigkeit
nichtlinear - zu; der Mensch bewegt sich bei über ~8 km/h im Laufen
energieeffizienter fort, d.h. der Sauerstoffverbrauch ist im Laufen
geringer als beim Gehen mit gleichem Tempo ( Abbildung).
Abbildung).
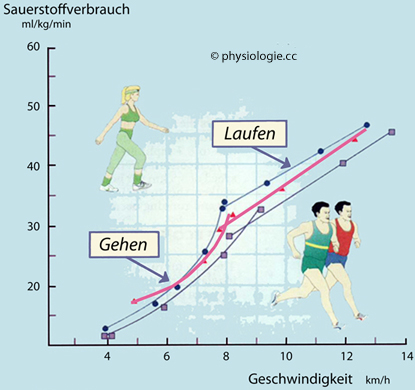
 Abbildung: Energieverbrauch (Sauerstoffaufnahme) als Funktion der Art und Geschwindigkeit der Fortbewegung
Nach Falls HB, Humphrey LD: Energy cost of running and walking in young women. Med Sci Sports 1976; 8: 9-13
Abbildung: Energieverbrauch (Sauerstoffaufnahme) als Funktion der Art und Geschwindigkeit der Fortbewegung
Nach Falls HB, Humphrey LD: Energy cost of running and walking in young women. Med Sci Sports 1976; 8: 9-13
Messergebnisse aus verschiedenen Untersuchungen (Symbole / Farben) kompiliert. Insgesamt zeigt sich: Beim
Gehen (4-8 km/h) steigt der Sauerstoffverbrauch nichtlinear mit zunehmender
Geschwindigkeit. Bei ~8 km/h erfolgt der Wechsel von Gehen zu Laufen. Im Laufen nimmt der O2-Verbrauch nur noch linear mit der Geschwindigkeit zu

Auch gibt
es eine optimale Schrittlänge und -Frequenz, bei der am wenigsten
Energie benötigt wird.
Körperliche Belastung steigert den Glucoseverbrauch in den Muskelzellen und erleichtert die Glucoseaufnahme; dies senkt den Blutzuckerspiegel.
Gleichzeitig senkt der erhöhte Sympathikustonus die Insulinfreisetzung aus den ß-Zellen des Pankreas, insbesondere bei trainierten Personen - hier kann der Insulinspiegel bei Belastungen um ~150 Watt über mehrere Minuten auf die Hälfte des Ruhewertes absínken.

 Wesentlich dramatischer ist die Auswirkung einer Immobilisierung, z.B.
nach einem schweren Unfall oder bei Intensivpatienten ("Astronautensyndrom"), wo es durch plötzliches
Erliegen des Muskeltrainings durch Gehen und allgemeine Aktivitäten des
täglichen Lebens zu einer Einbuße der Muskelleistung und
-Belastbarkeit führt, die in wenigen Tagen ein Ausmaß erreicht, das sonst nur über den Zeitraum der gesamten
Lebensspanne zu beobachten ist.
Wesentlich dramatischer ist die Auswirkung einer Immobilisierung, z.B.
nach einem schweren Unfall oder bei Intensivpatienten ("Astronautensyndrom"), wo es durch plötzliches
Erliegen des Muskeltrainings durch Gehen und allgemeine Aktivitäten des
täglichen Lebens zu einer Einbuße der Muskelleistung und
-Belastbarkeit führt, die in wenigen Tagen ein Ausmaß erreicht, das sonst nur über den Zeitraum der gesamten
Lebensspanne zu beobachten ist.
 Frühzeitige Mobilisierung und konsequentes Aufbautraining stellen nach
einer längerer Periode muskulärer Inaktivität die körperliche
Leistungsfähigkeit wieder her.
Frühzeitige Mobilisierung und konsequentes Aufbautraining stellen nach
einer längerer Periode muskulärer Inaktivität die körperliche
Leistungsfähigkeit wieder her.
Was ist ein "Muskelkater"?
Muskelkater und Heilungsprozesse:
Starke Belastung der Muskulatur - insbesondere nach Bremsbelastungen - führt zu Verletzungen (Mikroläsionen in
Myofibrillen und Sarkolemm) und Flüssigkeitseinlagerung im Muskelgewebe (Schwellung der Myozyten).
Zusätzlich treten zelluläre Proteine in den Extrazellulärraum über, was
Entzündung auslöst (Auftreten von Bradykinin, Histamin,
Prostaglandinen). Auch die extrazelluläre Kaliumkonzentration nimmt zu. Die  Abbildung zeigt die zeitliche Abfolge der Reparaturvorgänge.
Abbildung zeigt die zeitliche Abfolge der Reparaturvorgänge.

 Abbildung: Reparatur nach intensiver Muskelbelastung
Abbildung: Reparatur nach intensiver Muskelbelastung
Nach Peake JM, Neubauer O, Della Gatta PA, Nosaka K, Muscle damage and inflammation during recovery from exercise. J Appl Physiol 2017; 122: 559-70
In den ersten Stunden nach der Muskelbelastung ist das Entzündungsgeschehen überwiegend von neutrophilen Granulozyten bestimmt. Sie schaffen zellulären "Abfall" beiseite und bilden frühe Zytokine. Mastzellen gelangen in das Muskelgewebe und bilden Histamin und Chemokine.
4 bis 24 Stunden nach Auftreten der Mikrotraumen treten Makrophagen auf, sie räumen beschädigtes Gewebe ab, sezernieren entzündungsfördernde Zytokine und regen die Proliferation von Myoblasten an.
Nach etwa 24 Stunden werden sie durch entzündungshemmende Makrophagen, CD8-
und T-regulierende Lymphozyten ersetzt. Diese bilden
antiinflammatorische Zytokine, rekrutieren Makrophagen, regen die
Proliferation von Myoblasten und die Expansion des Satelliten-Zellpools
an. Auch werden weitere Stromazellen (Fibroblasten- und
Fettzell-Vorläufer, Perizyten) sowie die Differenzierung von Myoblasten
angeregt. Myogenin ist ein regenerationsförderndes Protein.
Schließlich haben nach etwa 7 Tagen die Muskelfasern (neue und regenerierte) die normale Ultrastruktur wiederhergestellt.
 Zytokine s. dort
Zytokine s. dort  Wachstumsfaktoren s. dort
Wachstumsfaktoren s. dort
 Dies alles reizt Schmerzfasern und erzeugt Muskelkater (Delayed onset muscle soreness DOMS):
Dieser hat nichts mit Milchsäure (Übersäuerung) zu tun, wie oft
behauptet wird, da sich der Lactatgehalt im Muskel nach der Belastung
sehr rasch wieder normalisiert (Lactat-Halbwertszeit ~20 Minuten).
Muskelkater tritt 1-3 Tage nach der Überlastung auf und geht auf
Mikrotraumata im Muskelgewebe zurück.
Dabei spielen zahlreiche Zellen eine Rolle, die zeitllich gestaffelt in
Aktion treten (
Dies alles reizt Schmerzfasern und erzeugt Muskelkater (Delayed onset muscle soreness DOMS):
Dieser hat nichts mit Milchsäure (Übersäuerung) zu tun, wie oft
behauptet wird, da sich der Lactatgehalt im Muskel nach der Belastung
sehr rasch wieder normalisiert (Lactat-Halbwertszeit ~20 Minuten).
Muskelkater tritt 1-3 Tage nach der Überlastung auf und geht auf
Mikrotraumata im Muskelgewebe zurück.
Dabei spielen zahlreiche Zellen eine Rolle, die zeitllich gestaffelt in
Aktion treten ( Abbildung): Die Gewebetraumen stimulieren z.B.
Satellitenzellen (Muskelstammzellen), Neutrophile, Makrophagen,
T-Lymphozyten und Mastzellen (Entzündung), Gefäßwandzellen
(Endothelzellen, Perizyten) und Stromazellen wie Fibroblasten. Diese
Zellen interagieren untereinander sowie mit der extrazellulären Matrix
des Skelettmuskels.
Abbildung): Die Gewebetraumen stimulieren z.B.
Satellitenzellen (Muskelstammzellen), Neutrophile, Makrophagen,
T-Lymphozyten und Mastzellen (Entzündung), Gefäßwandzellen
(Endothelzellen, Perizyten) und Stromazellen wie Fibroblasten. Diese
Zellen interagieren untereinander sowie mit der extrazellulären Matrix
des Skelettmuskels.
 Mäßige Muskelaktivität ist die
beste Unterstützung für die Heilungsvorgänge, da so die
Durchblutung angeregt wird, ohne weitere Verletzungen zu verursachen.
Mäßige Muskelaktivität ist die
beste Unterstützung für die Heilungsvorgänge, da so die
Durchblutung angeregt wird, ohne weitere Verletzungen zu verursachen.

  Die Ruhedehnungskurve eines Muskels zeigt sein passives
Kraft-Längen- Verhalten. Kontrahiert sich der Muskel, entfernt sich der
Zustandspunkt im Kraft-Längen- Diagramm von der Ruhedehnungskurve - in
Abhängigkeit von Zustand (z.B. Durchblutung), Kontraktionsform (z.B.
auxotonisch) und Reizbedingungen (z.B. Maximum)
Die Ruhedehnungskurve eines Muskels zeigt sein passives
Kraft-Längen- Verhalten. Kontrahiert sich der Muskel, entfernt sich der
Zustandspunkt im Kraft-Längen- Diagramm von der Ruhedehnungskurve - in
Abhängigkeit von Zustand (z.B. Durchblutung), Kontraktionsform (z.B.
auxotonisch) und Reizbedingungen (z.B. Maximum)
 Der Skelettmuskel deckt seine Energie hauptsächlich aus der oxidativen
Phosphorylierung von Fettsäuren; kurzdauernde Höchstleistungen steigern
den Glucoseanteil bei der Energiegewinnung (jeweils bis ~75%)
Der Skelettmuskel deckt seine Energie hauptsächlich aus der oxidativen
Phosphorylierung von Fettsäuren; kurzdauernde Höchstleistungen steigern
den Glucoseanteil bei der Energiegewinnung (jeweils bis ~75%)
 Der Vorrat an ATP und Kreatinphosphat reicht für 10-20 Sekunden
Muskeltätigkeit. Anaerobe Glykolyse bestreitet für einige Minuten den
Großteil des Energiemusatzes, für längere Zeit bedarf es der aeroben
Glykolyse. Zuerst wird auf Glykogenvorräte im Muskel zurückgegriffen;
der aerobe Glykogenabbau in der Leber nimmt höchstens für einige
Stunden an der Energiebereitstellung teil. Der aerobe Fettsäureabbau
erreicht sein Maximum nach ≥2 Stunden und ist bei Ausdauerbelastung der
entscheidende Energielieferant
Der Vorrat an ATP und Kreatinphosphat reicht für 10-20 Sekunden
Muskeltätigkeit. Anaerobe Glykolyse bestreitet für einige Minuten den
Großteil des Energiemusatzes, für längere Zeit bedarf es der aeroben
Glykolyse. Zuerst wird auf Glykogenvorräte im Muskel zurückgegriffen;
der aerobe Glykogenabbau in der Leber nimmt höchstens für einige
Stunden an der Energiebereitstellung teil. Der aerobe Fettsäureabbau
erreicht sein Maximum nach ≥2 Stunden und ist bei Ausdauerbelastung der
entscheidende Energielieferant
 Aerobe Kapazität ist die Leistungsfähigkeit des Muskels bis zum
Erreichen der anaeroben Schwelle (hier beginnt leistungsbedingte
Laktazidose). Automatisierte Tätigkeiten mobilisieren höchstens 15%,
übliche Leistungsbereitschaft ~35%, maximale Willensanstrengung bis zu
65% der theoretisch möglichen Höchstleistung der Muskeln
Aerobe Kapazität ist die Leistungsfähigkeit des Muskels bis zum
Erreichen der anaeroben Schwelle (hier beginnt leistungsbedingte
Laktazidose). Automatisierte Tätigkeiten mobilisieren höchstens 15%,
übliche Leistungsbereitschaft ~35%, maximale Willensanstrengung bis zu
65% der theoretisch möglichen Höchstleistung der Muskeln
 Auroregulation passt die Durchblutung der Skelettmuskulatur an den
Bedarf an. Das Herzminutenvolumen kommt vor allem aktiven Muskelpartien
zugute, Autoregulation weitet ihre Arteriolen - weniger belastete
werden nur schwach durchblutet (kollaterale Vasokonstriktion).
Vasodilatatorisch wirken Kaliumionen, Stickstoffmonoxid, Lactat,
Wasserstoffionen, Erhöhung der Osmolalität, Anstieg des pCO2, Abfall des pO2.
War die Durchblutung während der Belastungsphase unzureichend (Anreicherung von Vasodilatantien), kommt es
anschließend zu reaktiver Hyperämie
Auroregulation passt die Durchblutung der Skelettmuskulatur an den
Bedarf an. Das Herzminutenvolumen kommt vor allem aktiven Muskelpartien
zugute, Autoregulation weitet ihre Arteriolen - weniger belastete
werden nur schwach durchblutet (kollaterale Vasokonstriktion).
Vasodilatatorisch wirken Kaliumionen, Stickstoffmonoxid, Lactat,
Wasserstoffionen, Erhöhung der Osmolalität, Anstieg des pCO2, Abfall des pO2.
War die Durchblutung während der Belastungsphase unzureichend (Anreicherung von Vasodilatantien), kommt es
anschließend zu reaktiver Hyperämie
 Der Wirkungsgrad ist eine dimensionslose Zahl und bezeichnet das
Verhältnis der bei der Kontraktion mechanisch erbrachten zur
insgesamt im Muskel umgesetzten Energie. Der Wirkungsgrad von Muskeln
beträgt maximal 1/4
Der Wirkungsgrad ist eine dimensionslose Zahl und bezeichnet das
Verhältnis der bei der Kontraktion mechanisch erbrachten zur
insgesamt im Muskel umgesetzten Energie. Der Wirkungsgrad von Muskeln
beträgt maximal 1/4
 Man unterscheidet folgende Kontraktionsformen: Isometrisch
(konstante Länge), isotonosch (konstante Spannung), auxotonisch (beides
verändert sich), konzentrisch (Verkürzung) oder exzentrisch (Dehnung
während der Kraftentfaltung), Einzelzuckung (einzelnes
Aktionspotenzial), Tetanus (Summation, physiologisch),
Maximum (alle Fasern aktiviert). Die höchste Leistung erbringt der
Muskel bei ~1/3 seiner Maximalkraft und ~1/3 seiner maximalen
Verkürzungsgeschwindigkeit
Man unterscheidet folgende Kontraktionsformen: Isometrisch
(konstante Länge), isotonosch (konstante Spannung), auxotonisch (beides
verändert sich), konzentrisch (Verkürzung) oder exzentrisch (Dehnung
während der Kraftentfaltung), Einzelzuckung (einzelnes
Aktionspotenzial), Tetanus (Summation, physiologisch),
Maximum (alle Fasern aktiviert). Die höchste Leistung erbringt der
Muskel bei ~1/3 seiner Maximalkraft und ~1/3 seiner maximalen
Verkürzungsgeschwindigkeit
 Typ I- (slow-twitch, ”rote“) Muskelfasern kontrahieren langsam, sind
eher dünn, dicht kapillarisiert, mitochondrienreich, haben hohe aerobe
Kapazität, vollbringen vorwiegend Haltearbeit und ermüden kaum. Typ II-
(fast-twitch, ”weiße“) Muskelfasern haben weniger Kapillaren,
kontrahieren rasch, liefern kurze Arbeitszyklen, haben viel Glykogen,
aber wenig Kapillaren und Mitochondrien; sie stützen
sich überwiegend auf glykolytische Energiegewinnung
Typ I- (slow-twitch, ”rote“) Muskelfasern kontrahieren langsam, sind
eher dünn, dicht kapillarisiert, mitochondrienreich, haben hohe aerobe
Kapazität, vollbringen vorwiegend Haltearbeit und ermüden kaum. Typ II-
(fast-twitch, ”weiße“) Muskelfasern haben weniger Kapillaren,
kontrahieren rasch, liefern kurze Arbeitszyklen, haben viel Glykogen,
aber wenig Kapillaren und Mitochondrien; sie stützen
sich überwiegend auf glykolytische Energiegewinnung
 Körperliches Training steigert das Schlagvolumen des Herzens (bis
+100%) sowie Volumen und Pufferkapazität des Blutes; die
Ruhe-Herzfrequenz nimmt ab (erhöhter Vagustonus). Maximales Atemzeitvolumen
und maximaler Sauerstoffverbrauch steigen bis um 100%
Körperliches Training steigert das Schlagvolumen des Herzens (bis
+100%) sowie Volumen und Pufferkapazität des Blutes; die
Ruhe-Herzfrequenz nimmt ab (erhöhter Vagustonus). Maximales Atemzeitvolumen
und maximaler Sauerstoffverbrauch steigen bis um 100%
 Körperliche Belastung steigert den Glucoseverbrauch in den Muskeln; das
senkt den Blutzuckerspiegel
Körperliche Belastung steigert den Glucoseverbrauch in den Muskeln; das
senkt den Blutzuckerspiegel
|

 Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.
Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.





 Energiestoffwechsel des Muskels
Energiestoffwechsel des Muskels  Muskeldurchblutung und Substratangebot
Muskeldurchblutung und Substratangebot  Aerob vs. anerob, Leistungsbereich
Aerob vs. anerob, Leistungsbereich  Länge, Kraft, Geschwindigkeit, Kontraktionsformen
Länge, Kraft, Geschwindigkeit, Kontraktionsformen  Muskeltraining
Muskeltraining  Fast- und Slow-twitch-Fasern
Fast- und Slow-twitch-Fasern
 Physiologie des Laufens
Physiologie des Laufens  Belastung und Muskelkater
Belastung und Muskelkater Aerobe Kapazität
Aerobe Kapazität  Sauerstoffschuld
Sauerstoffschuld
 Über die Steuerung der Muskulatur auf der Ebene des Rückenmarks, Hirnstamms, Kleinhirns, der Basalganglien, des Thalamus und des Großhirns, sowie die Steuerung der Augenbewegungen sowie über Spiegelneurone s. dort.
Über die Steuerung der Muskulatur auf der Ebene des Rückenmarks, Hirnstamms, Kleinhirns, der Basalganglien, des Thalamus und des Großhirns, sowie die Steuerung der Augenbewegungen sowie über Spiegelneurone s. dort. Abbildung):
Abbildung):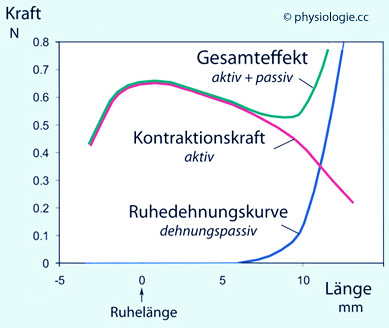
 Abbildung: Ruhedehnungs- und isometrische Kontraktionsmaximums-Kurven
Abbildung: Ruhedehnungs- und isometrische Kontraktionsmaximums-Kurven
 Abbildung).
Abbildung).
 Abbildung: Energiequellen bei Muskelarbeit
Abbildung: Energiequellen bei Muskelarbeit
 Abbildung):
Abbildung): Kurzzeitig wird ATP aus einem in der Muskelzelle angelegten Speicher von Kreatinphosphat
(CP) nachgebildet - unter Wirkung der Kreatinkinase (Abbildungen). Dieser
Energievorrat reicht für 10-20 Sekunden
oder bis zu 50 Kontraktionen, dann ist er (bei fortgesetzter
Muskelaktivität) gänzlich erschöpft. In Situationen plötzlicher extremer Herausforderung (fight or flight) kann dieser Mechanismus von überlebenswichtiger Bedeutung sein.
Kurzzeitig wird ATP aus einem in der Muskelzelle angelegten Speicher von Kreatinphosphat
(CP) nachgebildet - unter Wirkung der Kreatinkinase (Abbildungen). Dieser
Energievorrat reicht für 10-20 Sekunden
oder bis zu 50 Kontraktionen, dann ist er (bei fortgesetzter
Muskelaktivität) gänzlich erschöpft. In Situationen plötzlicher extremer Herausforderung (fight or flight) kann dieser Mechanismus von überlebenswichtiger Bedeutung sein.
 Innerhalb von Sekunden springt die anaerobe Glykolyse
an. Sie kann noch vor Ablauf einer Minute mehr als die Hälfte des
Energiemusatzes des Muskels bestreiten, nachher nimmt ihr Beitrag
wieder ab und ist nach wenigen Minuten vollauf verschwunden.
Innerhalb von Sekunden springt die anaerobe Glykolyse
an. Sie kann noch vor Ablauf einer Minute mehr als die Hälfte des
Energiemusatzes des Muskels bestreiten, nachher nimmt ihr Beitrag
wieder ab und ist nach wenigen Minuten vollauf verschwunden. Aerober Substratabbau übernimmt dann die Energieproduktion
(
Aerober Substratabbau übernimmt dann die Energieproduktion
( Abbildung). Auch sie startet innerhalb weniger Sekunden, nach etwa
10 Minuten gipfelt der Beitrag des aeroben Kohlenhydratabbaus in der Muskulatur (diese nimmt Glucose auf, was den Blutzuckerspiegel senkt). Dieser Mechanismus wirkt über eine Stunde.
Abbildung). Auch sie startet innerhalb weniger Sekunden, nach etwa
10 Minuten gipfelt der Beitrag des aeroben Kohlenhydratabbaus in der Muskulatur (diese nimmt Glucose auf, was den Blutzuckerspiegel senkt). Dieser Mechanismus wirkt über eine Stunde. Etwa 10 Minuten nach Beginn der Arbeit beteiligt sich der aerobe Kohlenhydratabbau in der Leber, dieser nimmt etwa 2 Stunden lang an der Energiebereitstellung teil.
Etwa 10 Minuten nach Beginn der Arbeit beteiligt sich der aerobe Kohlenhydratabbau in der Leber, dieser nimmt etwa 2 Stunden lang an der Energiebereitstellung teil. Gut eine Viertelstunde nach Beginn der Aktivität beginnt der aerobe Fettsäureabbau,
sein Maximum ist nach 2 Stunden (oder mehr) erreicht, und für
Ausdauerbelastung bleibt dieser Mechanismus am Ende für die
ATP-Synthese alleine übrig.
Gut eine Viertelstunde nach Beginn der Aktivität beginnt der aerobe Fettsäureabbau,
sein Maximum ist nach 2 Stunden (oder mehr) erreicht, und für
Ausdauerbelastung bleibt dieser Mechanismus am Ende für die
ATP-Synthese alleine übrig. Abbildung):
Abbildung):
 Abbildung: Substratnutzung als Funktion der Muskelbelastung
Abbildung: Substratnutzung als Funktion der Muskelbelastung

 Abbildung: Eine Hämoglobin-Bindungskurve
Abbildung: Eine Hämoglobin-Bindungskurve 
 Mäßig aktive Skelettmuskelzellen haben einen pO2 von ungefährt 25 mmHg - das aus dem Muskel strömende venöse Blut hat dann diesen pO2. Bei diesem Sauerstoffpartialdruck hat das Hämoglobin mehr als die Hälfte seiner O2-Transportkapazität an die Zellen abgegeben, es ist nur mehr zu 45% mit Sauerstoff beladen (
Mäßig aktive Skelettmuskelzellen haben einen pO2 von ungefährt 25 mmHg - das aus dem Muskel strömende venöse Blut hat dann diesen pO2. Bei diesem Sauerstoffpartialdruck hat das Hämoglobin mehr als die Hälfte seiner O2-Transportkapazität an die Zellen abgegeben, es ist nur mehr zu 45% mit Sauerstoff beladen ( Abbildung). Bei starker Arbeitsbelastung nimmt die Hb-Sauerstoffsättigung weiter ab, bei 10% liegt der pO2 bei etwa 7 mmHg.
Abbildung). Bei starker Arbeitsbelastung nimmt die Hb-Sauerstoffsättigung weiter ab, bei 10% liegt der pO2 bei etwa 7 mmHg. Zur Beziehung Sauerstoffverbrauch - Belastungszunahme s. dort
Zur Beziehung Sauerstoffverbrauch - Belastungszunahme s. dort Abbildung):
Abbildung): 
 Abbildung: Muskelstoffwechsel
Abbildung: Muskelstoffwechsel
 Die Nutzung der Substrate für den Energiebedarf des Muskels ändern sich mit Grad und Dauer der Belastung.
Die Nutzung der Substrate für den Energiebedarf des Muskels ändern sich mit Grad und Dauer der Belastung.  Bei niedriger Belastung (z.B. 25% VO2max) nutzt der Skelettmuskel vorwiegend (80-90%) Fettsäuren (die aus dem Fettgewebe
mobilisiert werden) für seinen Energieaufwand (hohe Energiedichte, aber
ausreichend Sauerstoff für oxidativen Abbau notwendig); etwa 10%
stammen aus dem Abbau von Neutralfettreserven der Myozyten selbst, weitere ~10% aus dem Abbau von Glucose aus dem Blut. Der Transport von Lipiden erfolgt über Lipoproteine im Blut.
Bei niedriger Belastung (z.B. 25% VO2max) nutzt der Skelettmuskel vorwiegend (80-90%) Fettsäuren (die aus dem Fettgewebe
mobilisiert werden) für seinen Energieaufwand (hohe Energiedichte, aber
ausreichend Sauerstoff für oxidativen Abbau notwendig); etwa 10%
stammen aus dem Abbau von Neutralfettreserven der Myozyten selbst, weitere ~10% aus dem Abbau von Glucose aus dem Blut. Der Transport von Lipiden erfolgt über Lipoproteine im Blut. Steigt die Belastung (z.B. auf 65% VO2max), nimmt der Absolutbetrag des Energieumsatzes entsprechend zu (z.B. bei Erhöhung von 25 auf 65% VO2max um einen Faktor 2,6). Die Prozentsätze
der Substratnutzung ändern sich deutlich: Kohlenhydrate werden stärker
genutzt, vor allem zu Beginn der Leistung. Jetzt kommen rund 25-40% aus
der Utilisation von Muskelglykogen (das bei 25% VO2max überhaupt nicht betroffen ist); der Anteil muskeleigener Neutralfette nimmt (während der ersten Stunde) auf bis zu 30% zu, Fettsäuren liefern anfangs nur noch 25-30%, später (wenn die Glykogenreserven zur Neige gehen) steigt der Anteil wieder auf ~50%
an; Glucose (die z.T. aus dem Abbau von Leberglykogen stammt, soferne
noch Vorräte vorhanden sind) wird nach wie vor aus dem Blut bezogen (5-15%,
mit der Belastungsdauer steigend; das entspricht einem Mehrfachen des
Glucoseumsatzes im Körper - von der Leber zur quergestreiften
Muskulatur - im Vergleich zu geringer Belastung).
Steigt die Belastung (z.B. auf 65% VO2max), nimmt der Absolutbetrag des Energieumsatzes entsprechend zu (z.B. bei Erhöhung von 25 auf 65% VO2max um einen Faktor 2,6). Die Prozentsätze
der Substratnutzung ändern sich deutlich: Kohlenhydrate werden stärker
genutzt, vor allem zu Beginn der Leistung. Jetzt kommen rund 25-40% aus
der Utilisation von Muskelglykogen (das bei 25% VO2max überhaupt nicht betroffen ist); der Anteil muskeleigener Neutralfette nimmt (während der ersten Stunde) auf bis zu 30% zu, Fettsäuren liefern anfangs nur noch 25-30%, später (wenn die Glykogenreserven zur Neige gehen) steigt der Anteil wieder auf ~50%
an; Glucose (die z.T. aus dem Abbau von Leberglykogen stammt, soferne
noch Vorräte vorhanden sind) wird nach wie vor aus dem Blut bezogen (5-15%,
mit der Belastungsdauer steigend; das entspricht einem Mehrfachen des
Glucoseumsatzes im Körper - von der Leber zur quergestreiften
Muskulatur - im Vergleich zu geringer Belastung).  Bei extensiver Belastung schließlich (80-90% VO2max)
- etwa bei Marathonläufen - kann Glucose (aus Glykogenolyse) zum
führenden Energielieferanten des Muskels avancieren. Das ermöglicht
eine nur begrenzte Zeitspanne der Kraftentwicklung. Einige Tage nach
erschöpfender Belastung nimmt der Glykogengehalt des Muskels deutlich
zu (bis auf 3-4% der Muskelmasse). Wie genau all diese Umstellungen
gesteuert und koordiniert werden, ist noch Gegenstand der Forschung.
Bei extensiver Belastung schließlich (80-90% VO2max)
- etwa bei Marathonläufen - kann Glucose (aus Glykogenolyse) zum
führenden Energielieferanten des Muskels avancieren. Das ermöglicht
eine nur begrenzte Zeitspanne der Kraftentwicklung. Einige Tage nach
erschöpfender Belastung nimmt der Glykogengehalt des Muskels deutlich
zu (bis auf 3-4% der Muskelmasse). Wie genau all diese Umstellungen
gesteuert und koordiniert werden, ist noch Gegenstand der Forschung.
 Abbildung: Glucoseaustausch im Organismus
Abbildung: Glucoseaustausch im Organismus
 Zur kapillären Glucosezufuhr an den Muskel s. auch dort
Zur kapillären Glucosezufuhr an den Muskel s. auch dort Statische Arbeit
("Haltearbeit") bei konstanter Muskellänge (physikalisch-formal gesehen
ist das keine Arbeit, weil ja kein Weg zurückgelegt wird - jedenfalls
nicht nach aussen;
Statische Arbeit
("Haltearbeit") bei konstanter Muskellänge (physikalisch-formal gesehen
ist das keine Arbeit, weil ja kein Weg zurückgelegt wird - jedenfalls
nicht nach aussen; Dynamische Arbeit - diese kann positiv sein (der Muskel verkürzt sich) oder auch negativ ("Bremsarbeit" bei Dehnung, z.B. beim Bergabgehen).
Dynamische Arbeit - diese kann positiv sein (der Muskel verkürzt sich) oder auch negativ ("Bremsarbeit" bei Dehnung, z.B. beim Bergabgehen). Im
Ruhezustand und bei stationärer Arbeit bezieht der Skelettmuskel ~75%
seiner Energie aus dem Abbau (oxidative Phosphorylierung) von Fettsäuren (nicht Glucose!). Diese vorwiegend
aus dem Fettgewebe stammende Energiequelle ist für sehr lange Zeiträume
verfügbar und wird normalerweise in den
Arbeitspausen wieder aufgefüllt.
Im
Ruhezustand und bei stationärer Arbeit bezieht der Skelettmuskel ~75%
seiner Energie aus dem Abbau (oxidative Phosphorylierung) von Fettsäuren (nicht Glucose!). Diese vorwiegend
aus dem Fettgewebe stammende Energiequelle ist für sehr lange Zeiträume
verfügbar und wird normalerweise in den
Arbeitspausen wieder aufgefüllt.  Zum aeroben / anaeroben Energiestoffwechsel des Muskels s. auch dort
Zum aeroben / anaeroben Energiestoffwechsel des Muskels s. auch dort
 Abbildung: Bilanz der Sauerstoffverteilung im Körper (gerundete Werte: gesunder junger Mann)
Abbildung: Bilanz der Sauerstoffverteilung im Körper (gerundete Werte: gesunder junger Mann)
 Leberglykogen dient zur Erhaltung des Blutzuckerspiegels
in der postresorptiven Phase, und dieser Vorrat ist starken
Schwankungen unterworfen (praktisch vollständige Entleerung möglich). Durch Glukoneogenese wird der
Speicher dann wieder komplettiert
Leberglykogen dient zur Erhaltung des Blutzuckerspiegels
in der postresorptiven Phase, und dieser Vorrat ist starken
Schwankungen unterworfen (praktisch vollständige Entleerung möglich). Durch Glukoneogenese wird der
Speicher dann wieder komplettiert Muskelglykogen
hingegen dient dem eigenen Bedarf und nicht der Blutzuckerregulation
(fehlende Glucose-6-Phosphatase, keine Glucoseabgabe aus der
Muskelzelle). Der Glykogengehalt im Muskel ist auch nicht so starken
Schwankungen unterworfen (±1/3, s. Abbildung oben).
Muskelglykogen
hingegen dient dem eigenen Bedarf und nicht der Blutzuckerregulation
(fehlende Glucose-6-Phosphatase, keine Glucoseabgabe aus der
Muskelzelle). Der Glykogengehalt im Muskel ist auch nicht so starken
Schwankungen unterworfen (±1/3, s. Abbildung oben).  Blutzuckersenkende Wirkung
von Muskelaktivität: Die Glucoseaufnahme steigt auch ohne Insulin bei
erhöhtem Energieverbrauch der Muskelzelle und senkt dadurch den Glucosespiegel.
Blutzuckersenkende Wirkung
von Muskelaktivität: Die Glucoseaufnahme steigt auch ohne Insulin bei
erhöhtem Energieverbrauch der Muskelzelle und senkt dadurch den Glucosespiegel. Als aerobe Kapazität bezeichnet man die Leistungsfähigkeit des Muskels bis Erreichen der anaeroben Schwelle
(Aufrechterhaltung des Gleichgewichts zwischen Lactat-Neubildung und
-Abbau, d.h. Vermeidung einer leistungsbedingten Lactazidose).
Als aerobe Kapazität bezeichnet man die Leistungsfähigkeit des Muskels bis Erreichen der anaeroben Schwelle
(Aufrechterhaltung des Gleichgewichts zwischen Lactat-Neubildung und
-Abbau, d.h. Vermeidung einer leistungsbedingten Lactazidose).
 Abbildung: Diätplan und Ausdauer
Abbildung: Diätplan und Ausdauer
 Abbildung).
Abbildung). Abbildung: Metabolische Hyperämie
Abbildung: Metabolische Hyperämie
 Als Sauerstoffschuld
(Oxygen debt / deficit,
Als Sauerstoffschuld
(Oxygen debt / deficit,  Abbildung) bezeichnet man die Tatsache, dass der Muskel zu
Beginn seiner Tätigkeit Energiereserven aufbraucht, die erst nach Ende
der Kontraktion oxidativ wieder ergänzt werden ("die Sauerstoffschuld
wird zurückgezahlt", indem vermehrt Sauerstoff aufgenommen wird: Excess postexercise O2 consumption EPOC). Bis die Energiereserven wieder aufgefüllt und die Verhältnisse des Ruhezustandes wieder hergestellt sind,
wird Energie aus mehreren Quellen direkt im Muskel bereitgestellt:
Vorhandenes ATP, Kreatinphosphat, an Myoglobin gebundener Sauerstoff,
anaerobe Glykolyse.
Abbildung) bezeichnet man die Tatsache, dass der Muskel zu
Beginn seiner Tätigkeit Energiereserven aufbraucht, die erst nach Ende
der Kontraktion oxidativ wieder ergänzt werden ("die Sauerstoffschuld
wird zurückgezahlt", indem vermehrt Sauerstoff aufgenommen wird: Excess postexercise O2 consumption EPOC). Bis die Energiereserven wieder aufgefüllt und die Verhältnisse des Ruhezustandes wieder hergestellt sind,
wird Energie aus mehreren Quellen direkt im Muskel bereitgestellt:
Vorhandenes ATP, Kreatinphosphat, an Myoglobin gebundener Sauerstoff,
anaerobe Glykolyse.  Abbildung),
wenn die vorausgehende Belastung gering war. Nach stärkerer
Belastung kann die Erholungsphase mehrere Minuten bis sogar Stunden
dauern ("langsame" Komponente), bedingt durch Lactazidose,
Gewebeschäden u.a. - Erholung und Reparaturvorgänge können viel Zeit in
Anspruch nehmen.
Abbildung),
wenn die vorausgehende Belastung gering war. Nach stärkerer
Belastung kann die Erholungsphase mehrere Minuten bis sogar Stunden
dauern ("langsame" Komponente), bedingt durch Lactazidose,
Gewebeschäden u.a. - Erholung und Reparaturvorgänge können viel Zeit in
Anspruch nehmen. Abbildung):
Abbildung):
 Abbildung: Verteilung des Herzzeitvolumens in Ruhe und bei Muskelarbeit
Abbildung: Verteilung des Herzzeitvolumens in Ruhe und bei Muskelarbeit
 Ruhedurchblutung: Inaktive Muskeln bleiben gering durchblutet (ausgeprägter Basaltonus, keine Vasodilatantien), sodass ein
größerer Prozentsatz des Herzminutenvolumens in die belasteten
Muskelpartien "umgeleitet" wird, während die Gefäße in den weniger
beteiligten Muskeln eng und relativ schwach durchblutet bleiben ("kollaterale Vasokonstriktion").
Ruhedurchblutung: Inaktive Muskeln bleiben gering durchblutet (ausgeprägter Basaltonus, keine Vasodilatantien), sodass ein
größerer Prozentsatz des Herzminutenvolumens in die belasteten
Muskelpartien "umgeleitet" wird, während die Gefäße in den weniger
beteiligten Muskeln eng und relativ schwach durchblutet bleiben ("kollaterale Vasokonstriktion"). Antizipatorische Mechanismen, central command: Mit beginnender - und während - Muskelaktivität wird (parallel zur Aktivierung der motorischen Hirnrinde) das Kreislaufzentrum
so aktiviert, dass das Herzzeitvolumen zunimmt und der Sympathikustonus
ansteigt (was Vasokonstriktion in nicht aktiven Muskeln und anderen
Organen, wie Nieren und Splanchnikusgebiet, bedingt).
Antizipatorische Mechanismen, central command: Mit beginnender - und während - Muskelaktivität wird (parallel zur Aktivierung der motorischen Hirnrinde) das Kreislaufzentrum
so aktiviert, dass das Herzzeitvolumen zunimmt und der Sympathikustonus
ansteigt (was Vasokonstriktion in nicht aktiven Muskeln und anderen
Organen, wie Nieren und Splanchnikusgebiet, bedingt).  Muskelkontraktionen:
Nicht nur wirkt sich die Kreislaufregulation - zusätzlich zur
Autoregulation - auf die Perfusion der Skelettmuskulatur aus; umgekehrt
haben Muskelkontraktionen kardiovaskuläre Effekte, indem sie das Herz
durch rhythmisches Auspressen der venösen Gefäßgeflechte im Muskel
unterstützen (zusätzliche Pumpwirkung - funktioniert nur bei intakten
Venenklappen). Dabei nimmt der venöse Blutdruck in den Beinvenen
deutlich ab (folgende Abbildungen).
Muskelkontraktionen:
Nicht nur wirkt sich die Kreislaufregulation - zusätzlich zur
Autoregulation - auf die Perfusion der Skelettmuskulatur aus; umgekehrt
haben Muskelkontraktionen kardiovaskuläre Effekte, indem sie das Herz
durch rhythmisches Auspressen der venösen Gefäßgeflechte im Muskel
unterstützen (zusätzliche Pumpwirkung - funktioniert nur bei intakten
Venenklappen). Dabei nimmt der venöse Blutdruck in den Beinvenen
deutlich ab (folgende Abbildungen).
 Abbildung: Blutdruck in den Beinen - Effekt von Körperlage und Muskelpumpe
Abbildung: Blutdruck in den Beinen - Effekt von Körperlage und Muskelpumpe Verstärkte Durchblutung bei Muskelarbeit wird durch vasodilatatorisch wirkende Mediatoren
erreicht, die in das Interstitium freigesetzt werden. Zu diesen lokalen Faktoren gehören
Verstärkte Durchblutung bei Muskelarbeit wird durch vasodilatatorisch wirkende Mediatoren
erreicht, die in das Interstitium freigesetzt werden. Zu diesen lokalen Faktoren gehören  Kaliumionen (interstitielles [K+]
steigt zu Beginn der Muskelarbeit von 4-5 bis auf 10 mM - der
Rücktransport in die Zellen durch deren Na/K-ATPase ist vorübergehend
überfordert)
Kaliumionen (interstitielles [K+]
steigt zu Beginn der Muskelarbeit von 4-5 bis auf 10 mM - der
Rücktransport in die Zellen durch deren Na/K-ATPase ist vorübergehend
überfordert) Stickstoffmonoxid
Stickstoffmonoxid Lactat / H+
Lactat / H+ Stickstoffmonoxid (NO) insbesondere in größeren arteriellen Versorgungsgefäßen, in denen die starke Blutströmung Scherkräfte am Endothel zu NO-Abgabe führen
Stickstoffmonoxid (NO) insbesondere in größeren arteriellen Versorgungsgefäßen, in denen die starke Blutströmung Scherkräfte am Endothel zu NO-Abgabe führen
 Erhöhung der Osmolarität: Der Kaliumspiegel im Interstitium intensiv
aktiver Muskeln kann sich mehr als verdoppeln, der Lactatspiegel von
<1 mM bis auf 30 mM ansteigen, die osmotische Konzentration um bis
zu 40 mOsm zunehmen
Erhöhung der Osmolarität: Der Kaliumspiegel im Interstitium intensiv
aktiver Muskeln kann sich mehr als verdoppeln, der Lactatspiegel von
<1 mM bis auf 30 mM ansteigen, die osmotische Konzentration um bis
zu 40 mOsm zunehmen Veränderungen der Gaspartialdrucke (Anstieg pCO2, Abfall pO2).
Veränderungen der Gaspartialdrucke (Anstieg pCO2, Abfall pO2).  Die Arteriolen in der Skelettmuskulatur verfügen sowohl über α1- als auch über ß2-Adrenozeptoren.
Erstere kontrahieren, letztere dilatieren die Gefäße; erstere haben
geringere Affinität zu Adrenalin als letztere. Daher überwiegt der
gefäßerweiternde Effekt - Adrenalin erhöht die Durchblutung
der Muskeln.
Die Arteriolen in der Skelettmuskulatur verfügen sowohl über α1- als auch über ß2-Adrenozeptoren.
Erstere kontrahieren, letztere dilatieren die Gefäße; erstere haben
geringere Affinität zu Adrenalin als letztere. Daher überwiegt der
gefäßerweiternde Effekt - Adrenalin erhöht die Durchblutung
der Muskeln. Zu den kardiovaskulären Umstellungen bei Muskelbelastung zählen
weiters erhöhter venöser Rückstrom von Blut zum Herzen, Freisetzung von
Adrenalin aus dem Nebennierenmark sowie eine situationsadäquate
Regulation der Körpertemperatur.
Zu den kardiovaskulären Umstellungen bei Muskelbelastung zählen
weiters erhöhter venöser Rückstrom von Blut zum Herzen, Freisetzung von
Adrenalin aus dem Nebennierenmark sowie eine situationsadäquate
Regulation der Körpertemperatur.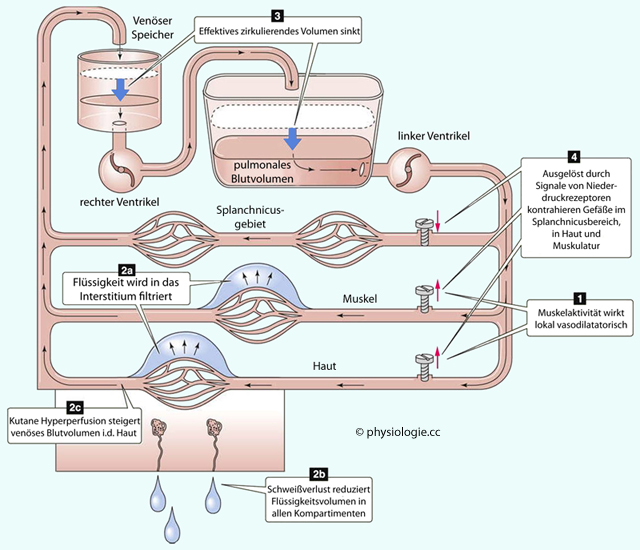
 Abbildung: Wie sich körperliche Belastung auf das zentrale Blutvolumen auswirkt
Abbildung: Wie sich körperliche Belastung auf das zentrale Blutvolumen auswirkt
 Flüssigkeit wandert aus der Blutbahn in den interstitiellen Raum (2a in der
Flüssigkeit wandert aus der Blutbahn in den interstitiellen Raum (2a in der  Abbildung)
Abbildung) Flüssigkeit geht durch Schwitzen verloren (2b)
Flüssigkeit geht durch Schwitzen verloren (2b) Dilatation der Hautgefäße bewirkt Umverteilung von Blut in die
Hautvenen, mit der Folge einer Reduktion des venösen Rückstroms zum
Herzen (
Dilatation der Hautgefäße bewirkt Umverteilung von Blut in die
Hautvenen, mit der Folge einer Reduktion des venösen Rückstroms zum
Herzen ( 2c)
2c) Abbildung) - ab und muss
prioritär "verteidigt" werden. Dies erfolgt via Niederdruckrezeptoren,
Kreislaufzentrum, sympathischen Efferenzen und Vasokonstriktion von
Gefäßen im Splanchnicusbereich, in der Haut und in der Muskulatur (4).
Abbildung) - ab und muss
prioritär "verteidigt" werden. Dies erfolgt via Niederdruckrezeptoren,
Kreislaufzentrum, sympathischen Efferenzen und Vasokonstriktion von
Gefäßen im Splanchnicusbereich, in der Haut und in der Muskulatur (4). Nach der Muskeltätigkeit kommt es typischerweise zu reaktiver Hyperämie,
in deren Verlauf die während der Muskelaktivität durch ungenügende
Perfusion entstandenen Versorgungsdefizite wieder ausgeglichen werden
(insbesondere bei statischer, d.h. Haltearbeit, welche die Durchblutung
stark einschränkt - im Gegensatz zu dynamischer Muskelbelastung).
Nach der Muskeltätigkeit kommt es typischerweise zu reaktiver Hyperämie,
in deren Verlauf die während der Muskelaktivität durch ungenügende
Perfusion entstandenen Versorgungsdefizite wieder ausgeglichen werden
(insbesondere bei statischer, d.h. Haltearbeit, welche die Durchblutung
stark einschränkt - im Gegensatz zu dynamischer Muskelbelastung).
 Abbildung oben: blaue Kurve). Kommt es zusätzlich zur
Aktivierung des kontraktilen Apparats, entsteht
Kontraktionskraft (
Abbildung oben: blaue Kurve). Kommt es zusätzlich zur
Aktivierung des kontraktilen Apparats, entsteht
Kontraktionskraft ( rote Kurve für isometrische Maximalkontraktionen).
rote Kurve für isometrische Maximalkontraktionen). 
 Abbildung: Kraft-Geschwindigkeits-Beziehung (Skelettmuskel)
Abbildung: Kraft-Geschwindigkeits-Beziehung (Skelettmuskel)
 Kontraktionsformen: Meist geht eine
Muskelkontraktion sowohl mit Verkürzung als auch Kraftentfaltung
einher; diese Komponenten lassen sich jedoch trennen, entweder zeitlich
(z.B. zuerst Kraftanstieg, dann Verkürzung -
"Unterstützungskontraktion", oder plyometrische
Kontraktionsformen: Meist geht eine
Muskelkontraktion sowohl mit Verkürzung als auch Kraftentfaltung
einher; diese Komponenten lassen sich jedoch trennen, entweder zeitlich
(z.B. zuerst Kraftanstieg, dann Verkürzung -
"Unterstützungskontraktion", oder plyometrische
 Kontraktionsformen - z.B. bei Hochspringen, Sprint), oder entsprechend Arretierung auf Verkürzung bei
konstanter Kraftentfaltung ("isotonisch"
Kontraktionsformen - z.B. bei Hochspringen, Sprint), oder entsprechend Arretierung auf Verkürzung bei
konstanter Kraftentfaltung ("isotonisch"  ) oder Kraftentwicklung bei
konstanter Länge ("isometrisch"
) oder Kraftentwicklung bei
konstanter Länge ("isometrisch"  ).
).  Die Kontraktionsgeschwindigkeit nimmt mit zunehmender Kraft, die der Muskel aufbringt, ab, und vice versa.
Die Kontraktionsgeschwindigkeit nimmt mit zunehmender Kraft, die der Muskel aufbringt, ab, und vice versa.  Ein "Maximum" (auxotonisch, isometrisch, isotonisch) ist dadurch gekennzeichnet, dass alle Muskelfasern an der Kontraktion teilnehmen.
Ein "Maximum" (auxotonisch, isometrisch, isotonisch) ist dadurch gekennzeichnet, dass alle Muskelfasern an der Kontraktion teilnehmen.  Regelmäßige Belastung und Kontraktionsauslösung ist der
physiologische Anreiz zu anabolem Stoffwechsel (Erhaltung des Bestandes
an Energiegewinnungsapparat, kontraktilen Proteinen etc.). Atrophie ist der Abbau von Muskelmasse aufgrund ungenügender Belastung und/oder Durchblutung. Hypertrophie ist eine erhöhte Masse und Kraft bestehender Muskelfasern, Hyperplasie eine Neubildung von Muskelfasern.
Regelmäßige Belastung und Kontraktionsauslösung ist der
physiologische Anreiz zu anabolem Stoffwechsel (Erhaltung des Bestandes
an Energiegewinnungsapparat, kontraktilen Proteinen etc.). Atrophie ist der Abbau von Muskelmasse aufgrund ungenügender Belastung und/oder Durchblutung. Hypertrophie ist eine erhöhte Masse und Kraft bestehender Muskelfasern, Hyperplasie eine Neubildung von Muskelfasern.
 Abbildung: Slow- vs. Fast-twitch-Fasern
Abbildung: Slow- vs. Fast-twitch-Fasern
 ”Rote“ Muskelfasern
(langsam kontrahierende, Typ I, 'slow-twitch' -
”Rote“ Muskelfasern
(langsam kontrahierende, Typ I, 'slow-twitch' -  Abbildung) sind eher dünn, dicht kapillarisiert, verfügen über
viel
Myoglobin (Sauerstoffspeicher - größere O2-Reserve als Typ II-Fasern) und Mitochondrien, haben hohe aerobe
Kapazität,
vollbringen vorwiegend Haltearbeit
(z.B. Rückenmuskulatur) und ermüden sehr langsam bis gar nicht. Ihre
Kraftausbeute pro Zuckung ist aber gering (etwa ein Zehntel der
Kraftentwicklung von Fasern des Typs IIx).
Abbildung) sind eher dünn, dicht kapillarisiert, verfügen über
viel
Myoglobin (Sauerstoffspeicher - größere O2-Reserve als Typ II-Fasern) und Mitochondrien, haben hohe aerobe
Kapazität,
vollbringen vorwiegend Haltearbeit
(z.B. Rückenmuskulatur) und ermüden sehr langsam bis gar nicht. Ihre
Kraftausbeute pro Zuckung ist aber gering (etwa ein Zehntel der
Kraftentwicklung von Fasern des Typs IIx). ”Weiße“
Muskelfasern
(rasch kontrahierende, Typ II, 'fast-twitch') haben hingegen weniger Myoglobin, aber höhere ATPase-Aktivität als rote Fasern und dienen
schnellen,
”phasischen“ Kontraktionen. Sie entwickeln rasch Spitzenkräfte und sind
auf kurze Arbeitszyklen spezialisiert. Sie verfügen über relativ wenig
Mitochondrien, stützen sich überwiegend auf glykolytische
Energiegewinnung
(sie enthalten viel Glykogen) und sind rasch ermüdbar (z.B.
Bizeps, Trizeps). Ihr Kapillarisierungsgrad ist geringer als bei
Typ-I-Fasern, d.h. jede Kapillare versorgt ein größeres
Muskelfasergebiet als das Kapillaren in slow-twitch-Fasern tun - wegen
des relativ geringeren Sauerstoffbedarfs können sie es sich leisten.
”Weiße“
Muskelfasern
(rasch kontrahierende, Typ II, 'fast-twitch') haben hingegen weniger Myoglobin, aber höhere ATPase-Aktivität als rote Fasern und dienen
schnellen,
”phasischen“ Kontraktionen. Sie entwickeln rasch Spitzenkräfte und sind
auf kurze Arbeitszyklen spezialisiert. Sie verfügen über relativ wenig
Mitochondrien, stützen sich überwiegend auf glykolytische
Energiegewinnung
(sie enthalten viel Glykogen) und sind rasch ermüdbar (z.B.
Bizeps, Trizeps). Ihr Kapillarisierungsgrad ist geringer als bei
Typ-I-Fasern, d.h. jede Kapillare versorgt ein größeres
Muskelfasergebiet als das Kapillaren in slow-twitch-Fasern tun - wegen
des relativ geringeren Sauerstoffbedarfs können sie es sich leisten. Typ IIa (fast, fatigue-resistant - relativ ausdauernd, ermüden langsam, mäßige Kraftausbeute pro Kontraktion) und
Typ IIa (fast, fatigue-resistant - relativ ausdauernd, ermüden langsam, mäßige Kraftausbeute pro Kontraktion) und Typ IIx (fast, fatiguable - extrem glykolyseabhängig, ermüden rapide, hohe Kraftausbeute pro Kontraktion).
Typ IIx (fast, fatiguable - extrem glykolyseabhängig, ermüden rapide, hohe Kraftausbeute pro Kontraktion).
 Alter und Muskelfitness: Typ-II-Fasern
nehmen an Kraft und Volumen vor allem mit zunehmendem Alter
ab, wenn die Muskeln nicht fit gehalten werden. Regelmäßiges
Krafttraining verringert diesen altersabhängigen Verlust an
fast-twitch-Muskelfasern und hat darüber hinaus weitere
gesundheitsfördernde Effekte (Kreislauf: Blutdruck; Metabolismus:
Diabetesprävention; Knochen: Osteoporoseprophylaxe; Gelenke: Nährstoffversorgung, Stabilisierung; Endorphinsekretion: Stressreduktion).
Alter und Muskelfitness: Typ-II-Fasern
nehmen an Kraft und Volumen vor allem mit zunehmendem Alter
ab, wenn die Muskeln nicht fit gehalten werden. Regelmäßiges
Krafttraining verringert diesen altersabhängigen Verlust an
fast-twitch-Muskelfasern und hat darüber hinaus weitere
gesundheitsfördernde Effekte (Kreislauf: Blutdruck; Metabolismus:
Diabetesprävention; Knochen: Osteoporoseprophylaxe; Gelenke: Nährstoffversorgung, Stabilisierung; Endorphinsekretion: Stressreduktion). fördert die Ca++-Aufnahme ins sarkoplasmatische Retikulum
fördert die Ca++-Aufnahme ins sarkoplasmatische Retikulum Die Typisierung der verschiedenen Muskelfasern ist idealtypisch zu verstehen, tatsächlich gibt es ein Kontinuum
von Typ I- bis Typ IIx-Fasern. Außerdem kann sich diese Verteilung auch
ändern, je nachdem, wie das Belastungsprofil des Muskels über eine
längere Zeit aussieht (Trainingsabhängigkeit).
Die Typisierung der verschiedenen Muskelfasern ist idealtypisch zu verstehen, tatsächlich gibt es ein Kontinuum
von Typ I- bis Typ IIx-Fasern. Außerdem kann sich diese Verteilung auch
ändern, je nachdem, wie das Belastungsprofil des Muskels über eine
längere Zeit aussieht (Trainingsabhängigkeit). Abbildung).
Abbildung).
 Abbildung: Kraftentfaltung und Ermüdbarkeit verschiedener Muskelfasertypen
Abbildung: Kraftentfaltung und Ermüdbarkeit verschiedener Muskelfasertypen
 Die
Ausstattung des Muskels mit Typ-I vs. Typ-II-Fasern kann sich je nach
Anforderungen ändern, z.B. gibt es bei längerer Bettruhe in Muskeln,
die normalerweise Haltearbeit leisten, eine Musterverschiebung von Typ
I zu Typ II ("Dekonditionierungseffekt" Richtung fast-twitch-Fasern). Als Trainingseffekt - mit anhaltender Belastung - tritt umgekehrt eine Verschiebung in Richtung Typ I auf, womit Ausdauerleistungen möglich werden.
Die
Ausstattung des Muskels mit Typ-I vs. Typ-II-Fasern kann sich je nach
Anforderungen ändern, z.B. gibt es bei längerer Bettruhe in Muskeln,
die normalerweise Haltearbeit leisten, eine Musterverschiebung von Typ
I zu Typ II ("Dekonditionierungseffekt" Richtung fast-twitch-Fasern). Als Trainingseffekt - mit anhaltender Belastung - tritt umgekehrt eine Verschiebung in Richtung Typ I auf, womit Ausdauerleistungen möglich werden. Die Atemmechanik wird effizienter (optimierte Bewegungskoordination), das maximale Atemminutenvolumen verdoppelt sich von ~100 l/min auf ~200 l/min (das Ruhe-Atemminutenvolumen bleibt mit 6-8 l/min unverändert).
Die Atemmechanik wird effizienter (optimierte Bewegungskoordination), das maximale Atemminutenvolumen verdoppelt sich von ~100 l/min auf ~200 l/min (das Ruhe-Atemminutenvolumen bleibt mit 6-8 l/min unverändert). Der maximale Sauerstoffverbrauch kann bis auf 80 ml/min/kg KG etwa verdoppelt werden (der Ruhewert bleibt unverändert bei 3,5 ml O2/min/kg KG).
Der maximale Sauerstoffverbrauch kann bis auf 80 ml/min/kg KG etwa verdoppelt werden (der Ruhewert bleibt unverändert bei 3,5 ml O2/min/kg KG).  Das Schlagvolumen
des Herzens kann bis auf das Doppelte zunehmen (Ruhe: Untrainiert 70
ml, hochtrainiert bis 140 ml; Belastung: Untrainiert 100 ml,
hochtrainiert bis 190 ml), dies ermöglicht die bei Spitzenbelastung nötige Erhöhung des maximalen Herzminutenvolumens von ~15 auf bis zu ~30 l/min (
Das Schlagvolumen
des Herzens kann bis auf das Doppelte zunehmen (Ruhe: Untrainiert 70
ml, hochtrainiert bis 140 ml; Belastung: Untrainiert 100 ml,
hochtrainiert bis 190 ml), dies ermöglicht die bei Spitzenbelastung nötige Erhöhung des maximalen Herzminutenvolumens von ~15 auf bis zu ~30 l/min ( s. auch dort). Auch das enddiastolische Volumen nimmt linksventrikulär zu, und das Gesamtvolumen des Herzens kann sich von ~700 auf ~1400 ml erhöhen. Das Ruhe-Herzzeitvolumen bleibt unverändert.
s. auch dort). Auch das enddiastolische Volumen nimmt linksventrikulär zu, und das Gesamtvolumen des Herzens kann sich von ~700 auf ~1400 ml erhöhen. Das Ruhe-Herzzeitvolumen bleibt unverändert. Der Ruhepuls
des trainierten Menschen nimmt durch erhöhten Vagustonus ab (bis unter
40 bpm). Kombiniert mit dem größeren Schlagvolumen ergibt das eine
höhere Kapazität für die Steigerung der Auswurfleistung des Herzens bei
körperlicher Belastung. Die maximale Herzfrequenz ändert sich durch Training hingegen nicht (~200 bpm).
Der Ruhepuls
des trainierten Menschen nimmt durch erhöhten Vagustonus ab (bis unter
40 bpm). Kombiniert mit dem größeren Schlagvolumen ergibt das eine
höhere Kapazität für die Steigerung der Auswurfleistung des Herzens bei
körperlicher Belastung. Die maximale Herzfrequenz ändert sich durch Training hingegen nicht (~200 bpm). Das Blutvolumen nimmt zu (Hypervolämie), dadurch nimmt die maximale Perfusionskapazität des
Kreislaufs zu und es können höhere Volumenverluste durch Schwitzen
verkraftet werden.
Das Blutvolumen nimmt zu (Hypervolämie), dadurch nimmt die maximale Perfusionskapazität des
Kreislaufs zu und es können höhere Volumenverluste durch Schwitzen
verkraftet werden. Die Pufferkapazität des Blutes nimmt zu, dadurch werden Lactatspitzen bei Hochleistung besser abgefangen.
Die Pufferkapazität des Blutes nimmt zu, dadurch werden Lactatspitzen bei Hochleistung besser abgefangen.  Die Körperzusammensetzung ändert sich: Die Muskelmasse steigt (lean body mass), Körperfett nimmt ab.
Die Körperzusammensetzung ändert sich: Die Muskelmasse steigt (lean body mass), Körperfett nimmt ab.
 Optimierung: Der Energieverbrauch nimmt beim Gehen mit
zunehmendem Fortbewegungstempo - vor allem bei höherer Geschwindigkeit
nichtlinear - zu; der Mensch bewegt sich bei über ~8 km/h im Laufen
energieeffizienter fort, d.h. der Sauerstoffverbrauch ist im Laufen
geringer als beim Gehen mit gleichem Tempo (
Optimierung: Der Energieverbrauch nimmt beim Gehen mit
zunehmendem Fortbewegungstempo - vor allem bei höherer Geschwindigkeit
nichtlinear - zu; der Mensch bewegt sich bei über ~8 km/h im Laufen
energieeffizienter fort, d.h. der Sauerstoffverbrauch ist im Laufen
geringer als beim Gehen mit gleichem Tempo ( Abbildung).
Abbildung). 
 Abbildung: Energieverbrauch (Sauerstoffaufnahme) als Funktion der Art und Geschwindigkeit der Fortbewegung
Abbildung: Energieverbrauch (Sauerstoffaufnahme) als Funktion der Art und Geschwindigkeit der Fortbewegung
 Wesentlich dramatischer ist die Auswirkung einer Immobilisierung, z.B.
nach einem schweren Unfall oder bei Intensivpatienten ("Astronautensyndrom"), wo es durch plötzliches
Erliegen des Muskeltrainings durch Gehen und allgemeine Aktivitäten des
täglichen Lebens zu einer Einbuße der Muskelleistung und
-Belastbarkeit führt, die in wenigen Tagen ein Ausmaß erreicht, das sonst nur über den Zeitraum der gesamten
Lebensspanne zu beobachten ist.
Wesentlich dramatischer ist die Auswirkung einer Immobilisierung, z.B.
nach einem schweren Unfall oder bei Intensivpatienten ("Astronautensyndrom"), wo es durch plötzliches
Erliegen des Muskeltrainings durch Gehen und allgemeine Aktivitäten des
täglichen Lebens zu einer Einbuße der Muskelleistung und
-Belastbarkeit führt, die in wenigen Tagen ein Ausmaß erreicht, das sonst nur über den Zeitraum der gesamten
Lebensspanne zu beobachten ist.  Frühzeitige Mobilisierung und konsequentes Aufbautraining stellen nach
einer längerer Periode muskulärer Inaktivität die körperliche
Leistungsfähigkeit wieder her.
Frühzeitige Mobilisierung und konsequentes Aufbautraining stellen nach
einer längerer Periode muskulärer Inaktivität die körperliche
Leistungsfähigkeit wieder her. Abbildung zeigt die zeitliche Abfolge der Reparaturvorgänge.
Abbildung zeigt die zeitliche Abfolge der Reparaturvorgänge.
 Abbildung: Reparatur nach intensiver Muskelbelastung
Abbildung: Reparatur nach intensiver Muskelbelastung
 Abbildung): Die Gewebetraumen stimulieren z.B.
Satellitenzellen (Muskelstammzellen), Neutrophile, Makrophagen,
T-Lymphozyten und Mastzellen (Entzündung), Gefäßwandzellen
(Endothelzellen, Perizyten) und Stromazellen wie Fibroblasten. Diese
Zellen interagieren untereinander sowie mit der extrazellulären Matrix
des Skelettmuskels.
Abbildung): Die Gewebetraumen stimulieren z.B.
Satellitenzellen (Muskelstammzellen), Neutrophile, Makrophagen,
T-Lymphozyten und Mastzellen (Entzündung), Gefäßwandzellen
(Endothelzellen, Perizyten) und Stromazellen wie Fibroblasten. Diese
Zellen interagieren untereinander sowie mit der extrazellulären Matrix
des Skelettmuskels. Mäßige Muskelaktivität ist die
beste Unterstützung für die Heilungsvorgänge, da so die
Durchblutung angeregt wird, ohne weitere Verletzungen zu verursachen.
Mäßige Muskelaktivität ist die
beste Unterstützung für die Heilungsvorgänge, da so die
Durchblutung angeregt wird, ohne weitere Verletzungen zu verursachen. 
 Die Ruhedehnungskurve eines Muskels zeigt sein passives
Kraft-Längen- Verhalten. Kontrahiert sich der Muskel, entfernt sich der
Zustandspunkt im Kraft-Längen- Diagramm von der Ruhedehnungskurve - in
Abhängigkeit von Zustand (z.B. Durchblutung), Kontraktionsform (z.B.
auxotonisch) und Reizbedingungen (z.B. Maximum)
Die Ruhedehnungskurve eines Muskels zeigt sein passives
Kraft-Längen- Verhalten. Kontrahiert sich der Muskel, entfernt sich der
Zustandspunkt im Kraft-Längen- Diagramm von der Ruhedehnungskurve - in
Abhängigkeit von Zustand (z.B. Durchblutung), Kontraktionsform (z.B.
auxotonisch) und Reizbedingungen (z.B. Maximum)  Der Skelettmuskel deckt seine Energie hauptsächlich aus der oxidativen
Phosphorylierung von Fettsäuren; kurzdauernde Höchstleistungen steigern
den Glucoseanteil bei der Energiegewinnung (jeweils bis ~75%)
Der Skelettmuskel deckt seine Energie hauptsächlich aus der oxidativen
Phosphorylierung von Fettsäuren; kurzdauernde Höchstleistungen steigern
den Glucoseanteil bei der Energiegewinnung (jeweils bis ~75%) Der Vorrat an ATP und Kreatinphosphat reicht für 10-20 Sekunden
Muskeltätigkeit. Anaerobe Glykolyse bestreitet für einige Minuten den
Großteil des Energiemusatzes, für längere Zeit bedarf es der aeroben
Glykolyse. Zuerst wird auf Glykogenvorräte im Muskel zurückgegriffen;
der aerobe Glykogenabbau in der Leber nimmt höchstens für einige
Stunden an der Energiebereitstellung teil. Der aerobe Fettsäureabbau
erreicht sein Maximum nach ≥2 Stunden und ist bei Ausdauerbelastung der
entscheidende Energielieferant
Der Vorrat an ATP und Kreatinphosphat reicht für 10-20 Sekunden
Muskeltätigkeit. Anaerobe Glykolyse bestreitet für einige Minuten den
Großteil des Energiemusatzes, für längere Zeit bedarf es der aeroben
Glykolyse. Zuerst wird auf Glykogenvorräte im Muskel zurückgegriffen;
der aerobe Glykogenabbau in der Leber nimmt höchstens für einige
Stunden an der Energiebereitstellung teil. Der aerobe Fettsäureabbau
erreicht sein Maximum nach ≥2 Stunden und ist bei Ausdauerbelastung der
entscheidende Energielieferant  Aerobe Kapazität ist die Leistungsfähigkeit des Muskels bis zum
Erreichen der anaeroben Schwelle (hier beginnt leistungsbedingte
Laktazidose). Automatisierte Tätigkeiten mobilisieren höchstens 15%,
übliche Leistungsbereitschaft ~35%, maximale Willensanstrengung bis zu
65% der theoretisch möglichen Höchstleistung der Muskeln
Aerobe Kapazität ist die Leistungsfähigkeit des Muskels bis zum
Erreichen der anaeroben Schwelle (hier beginnt leistungsbedingte
Laktazidose). Automatisierte Tätigkeiten mobilisieren höchstens 15%,
übliche Leistungsbereitschaft ~35%, maximale Willensanstrengung bis zu
65% der theoretisch möglichen Höchstleistung der Muskeln Auroregulation passt die Durchblutung der Skelettmuskulatur an den
Bedarf an. Das Herzminutenvolumen kommt vor allem aktiven Muskelpartien
zugute, Autoregulation weitet ihre Arteriolen - weniger belastete
werden nur schwach durchblutet (kollaterale Vasokonstriktion).
Vasodilatatorisch wirken Kaliumionen, Stickstoffmonoxid, Lactat,
Wasserstoffionen, Erhöhung der Osmolalität, Anstieg des pCO2, Abfall des pO2.
War die Durchblutung während der Belastungsphase unzureichend (Anreicherung von Vasodilatantien), kommt es
anschließend zu reaktiver Hyperämie
Auroregulation passt die Durchblutung der Skelettmuskulatur an den
Bedarf an. Das Herzminutenvolumen kommt vor allem aktiven Muskelpartien
zugute, Autoregulation weitet ihre Arteriolen - weniger belastete
werden nur schwach durchblutet (kollaterale Vasokonstriktion).
Vasodilatatorisch wirken Kaliumionen, Stickstoffmonoxid, Lactat,
Wasserstoffionen, Erhöhung der Osmolalität, Anstieg des pCO2, Abfall des pO2.
War die Durchblutung während der Belastungsphase unzureichend (Anreicherung von Vasodilatantien), kommt es
anschließend zu reaktiver Hyperämie  Der Wirkungsgrad ist eine dimensionslose Zahl und bezeichnet das
Verhältnis der bei der Kontraktion mechanisch erbrachten zur
insgesamt im Muskel umgesetzten Energie. Der Wirkungsgrad von Muskeln
beträgt maximal 1/4
Der Wirkungsgrad ist eine dimensionslose Zahl und bezeichnet das
Verhältnis der bei der Kontraktion mechanisch erbrachten zur
insgesamt im Muskel umgesetzten Energie. Der Wirkungsgrad von Muskeln
beträgt maximal 1/4 Man unterscheidet folgende Kontraktionsformen: Isometrisch
(konstante Länge), isotonosch (konstante Spannung), auxotonisch (beides
verändert sich), konzentrisch (Verkürzung) oder exzentrisch (Dehnung
während der Kraftentfaltung), Einzelzuckung (einzelnes
Aktionspotenzial), Tetanus (Summation, physiologisch),
Maximum (alle Fasern aktiviert). Die höchste Leistung erbringt der
Muskel bei ~1/3 seiner Maximalkraft und ~1/3 seiner maximalen
Verkürzungsgeschwindigkeit
Man unterscheidet folgende Kontraktionsformen: Isometrisch
(konstante Länge), isotonosch (konstante Spannung), auxotonisch (beides
verändert sich), konzentrisch (Verkürzung) oder exzentrisch (Dehnung
während der Kraftentfaltung), Einzelzuckung (einzelnes
Aktionspotenzial), Tetanus (Summation, physiologisch),
Maximum (alle Fasern aktiviert). Die höchste Leistung erbringt der
Muskel bei ~1/3 seiner Maximalkraft und ~1/3 seiner maximalen
Verkürzungsgeschwindigkeit Typ I- (slow-twitch, ”rote“) Muskelfasern kontrahieren langsam, sind
eher dünn, dicht kapillarisiert, mitochondrienreich, haben hohe aerobe
Kapazität, vollbringen vorwiegend Haltearbeit und ermüden kaum. Typ II-
(fast-twitch, ”weiße“) Muskelfasern haben weniger Kapillaren,
kontrahieren rasch, liefern kurze Arbeitszyklen, haben viel Glykogen,
aber wenig Kapillaren und Mitochondrien; sie stützen
sich überwiegend auf glykolytische Energiegewinnung
Typ I- (slow-twitch, ”rote“) Muskelfasern kontrahieren langsam, sind
eher dünn, dicht kapillarisiert, mitochondrienreich, haben hohe aerobe
Kapazität, vollbringen vorwiegend Haltearbeit und ermüden kaum. Typ II-
(fast-twitch, ”weiße“) Muskelfasern haben weniger Kapillaren,
kontrahieren rasch, liefern kurze Arbeitszyklen, haben viel Glykogen,
aber wenig Kapillaren und Mitochondrien; sie stützen
sich überwiegend auf glykolytische Energiegewinnung Körperliches Training steigert das Schlagvolumen des Herzens (bis
+100%) sowie Volumen und Pufferkapazität des Blutes; die
Ruhe-Herzfrequenz nimmt ab (erhöhter Vagustonus). Maximales Atemzeitvolumen
und maximaler Sauerstoffverbrauch steigen bis um 100%
Körperliches Training steigert das Schlagvolumen des Herzens (bis
+100%) sowie Volumen und Pufferkapazität des Blutes; die
Ruhe-Herzfrequenz nimmt ab (erhöhter Vagustonus). Maximales Atemzeitvolumen
und maximaler Sauerstoffverbrauch steigen bis um 100% Körperliche Belastung steigert den Glucoseverbrauch in den Muskeln; das
senkt den Blutzuckerspiegel
Körperliche Belastung steigert den Glucoseverbrauch in den Muskeln; das
senkt den Blutzuckerspiegel