




 Blutströmung und Blutviskosität
Blutströmung und Blutviskosität
 Fahraeus-Lindqvist-Effekt: Robin Fåhræus, Johan Torsten Lindqvist (1906-2007)
Fahraeus-Lindqvist-Effekt: Robin Fåhræus, Johan Torsten Lindqvist (1906-2007)| Die
Fließfähigkeit des Blutes ist ein kritischer Faktor für die Blutversorgung der Gewebe. Einerseits steigt
mit dem Hämatokrit die O2-Transportkapazität des Blutes, andererseits sinkt seine Fließfähigkeit - die Viskosität nimmt zu, insbesondere bei Hämatokritwerten über 0,5 (50%). Rote Blutkörperchen sind sehr flexibel. So bleibt das Blut trotz hohen Volumenanteils an Erythrozyten flüssig: Ihre Membran kann um den Zellinhalt "rollen", die Blutkörperchen können ihre Form dem Strömungsprofil anpassen. Blutkörperchen ordnen sich in der Mikrozirkulation vor allem im Zentrum des Blutstroms an, das erleichtert die Passage und verringert den Strömungswiderstand. Daher ist die effektive Viskosität bei Gefäßen von etwa 10 µm Durchmesser am geringsten (Fahraeus-Lindqvist-Effekt). Die an der Gefäßwand auftretenden Scherkräfte des vorüberströmenden Blutes werden von den Endothelzellen aufgenommen und auf ihr Zytoskelett übertragen; das löst die Freisetzung von Stoffen aus, die ihrerseits den Gefäßzustand (Gefäßweite) beeinflussen. So nimmt die Bildung von NO (Stickstoffmonoxid) mit steigender Schubspannung am Endothel zu, sodass sich das Gefäß erweitert. |
 Blutviskosität
Blutviskosität  Hämatokrit, Sauerstofftransport, Tunnel- und Fahraeus-Lindqvist-Effekt
Hämatokrit, Sauerstofftransport, Tunnel- und Fahraeus-Lindqvist-Effekt  Laminare und turbulente Strömung
Laminare und turbulente Strömung (Hämo-) Rheologie
(Hämo-) Rheologie
 Core messages
Core messages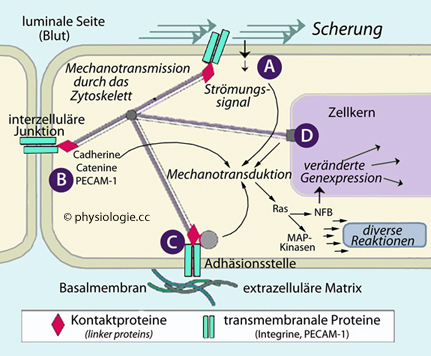
 Abbildung: Scherkräfte und Mechanotransduktion in Endothelzellen
Abbildung: Scherkräfte und Mechanotransduktion in Endothelzellen s. auch dort
s. auch dort Catenine sind intrazelluläre Schaltstellen zwischen Cadherinen und Aktinfilamenten des Zytoskeletts
Catenine sind intrazelluläre Schaltstellen zwischen Cadherinen und Aktinfilamenten des Zytoskeletts  Integrine sind Membranproteine, die extrazelluläre Kontakte herstellen
Integrine sind Membranproteine, die extrazelluläre Kontakte herstellen  MAP-Kinasen sind mitogenaktivierte Proteinkinasen
MAP-Kinasen sind mitogenaktivierte Proteinkinasen  NFB (nuclear factor light-chain-enhancer of activated B cells) ist ein Transkriptionsfaktor
NFB (nuclear factor light-chain-enhancer of activated B cells) ist ein Transkriptionsfaktor  PECAM-1 (Platelet endothelial cell adhesion molecule) ist ein Adhäsionsmolekül
PECAM-1 (Platelet endothelial cell adhesion molecule) ist ein Adhäsionsmolekül  Ras (nach rat sarcoma) ist eine GTPase
Ras (nach rat sarcoma) ist eine GTPase
 Rheologie beschäftigt sich mit dem Fließ- und Verformungsverhalten von Materie, z.B. der Strömungsmechanik; Hämorheologie
Rheologie beschäftigt sich mit dem Fließ- und Verformungsverhalten von Materie, z.B. der Strömungsmechanik; Hämorheologie  mit der Strömung von Blut und seinen Komponenten.
mit der Strömung von Blut und seinen Komponenten. Konzentration der Blutkörperchen (Hämatokrit
Konzentration der Blutkörperchen (Hämatokrit  )
) Verformbarkeit (Flexibilität) der
Blutkörperchen
Verformbarkeit (Flexibilität) der
Blutkörperchen Art der Strömung (laminar? turbulent?)
Art der Strömung (laminar? turbulent?) Fließeigenschaften
des
Blutplasmas
Fließeigenschaften
des
Blutplasmas Temperatur des Blutes
Temperatur des Blutes Mit
zunehmender mechanischer Beanspruchung (Scherung in
der Strömung) nehmen innere Widerstände ab und die Fließfähigkeit des
Blutes zu (bei langsamer fließendem, insbesondere bei stehendem
Blut nimmt die Fließfähigkeit ab), ein Verhalten, das man als thixotrop
bezeichnet. (Blut soll im Kreislauf nicht aufhören zu fließen.)
Mit
zunehmender mechanischer Beanspruchung (Scherung in
der Strömung) nehmen innere Widerstände ab und die Fließfähigkeit des
Blutes zu (bei langsamer fließendem, insbesondere bei stehendem
Blut nimmt die Fließfähigkeit ab), ein Verhalten, das man als thixotrop
bezeichnet. (Blut soll im Kreislauf nicht aufhören zu fließen.) was etwa Fließzähigkeit heißt.
was etwa Fließzähigkeit heißt.
 Schubspannung an den Endothelzellen regt die Aktivität endothelialer NO-Synthase an
Schubspannung an den Endothelzellen regt die Aktivität endothelialer NO-Synthase an NO diffundiert in benachbarte glatte Gefäßmuskelzellen
NO diffundiert in benachbarte glatte Gefäßmuskelzellen  und stimuliert dort die Bildung von cGMP (aus GTP)
und stimuliert dort die Bildung von cGMP (aus GTP) das regt die cGMP-abhängige Proteinkinase (PKG) an
das regt die cGMP-abhängige Proteinkinase (PKG) an die PKG öffnet calciumabhängige Kaliumkanäle, Kaliumionen strömen aus der Zelle
die PKG öffnet calciumabhängige Kaliumkanäle, Kaliumionen strömen aus der Zelle die glatten Muskelzellen der Gefäßwand hyperpolarisieren, relaxieren, der Blutdruck dehnt das Gefäß weiter auf (Vasodilatation), der Gefäßquerschnitt nimmt zu, die Strömungsgeschwindigkeit sinkt
die glatten Muskelzellen der Gefäßwand hyperpolarisieren, relaxieren, der Blutdruck dehnt das Gefäß weiter auf (Vasodilatation), der Gefäßquerschnitt nimmt zu, die Strömungsgeschwindigkeit sinkt die Schubspannung am Endothel nimmt ab (negative Rückkopplung).
die Schubspannung am Endothel nimmt ab (negative Rückkopplung). Vermehrte
Schubspannung am Endothel führt zu Vasodilatation, was die
Schubspannung wieder absenkt (und vice versa) - die Gefäßwand
autoreguliert den Gefäßdurchmesser.
Vermehrte
Schubspannung am Endothel führt zu Vasodilatation, was die
Schubspannung wieder absenkt (und vice versa) - die Gefäßwand
autoreguliert den Gefäßdurchmesser.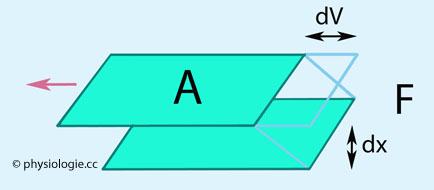
 Abbildung: Viskosität ist definiert als Schubspannung (F/A) pro Scherrate (dV/dx)
Abbildung: Viskosität ist definiert als Schubspannung (F/A) pro Scherrate (dV/dx)

 Schubspannung
ist die Kraft F, die auf eine Flüssigkeitsschicht der Fläche A
ausgeübt wird, um sie über eine bestimmte Strecke dV zu bewegen, um innere Widerstände in der
Flüssigkeit zu überwinden. Die Dimension ist Kraft pro Fläche (Einheit im SI-System ist das Pascal: Pa = N/m2). In Gefäßen nimmt die Schubspannung bei laminarer Strömung von der Wand zum axialen Mittelstrom hin ab.
Schubspannung
ist die Kraft F, die auf eine Flüssigkeitsschicht der Fläche A
ausgeübt wird, um sie über eine bestimmte Strecke dV zu bewegen, um innere Widerstände in der
Flüssigkeit zu überwinden. Die Dimension ist Kraft pro Fläche (Einheit im SI-System ist das Pascal: Pa = N/m2). In Gefäßen nimmt die Schubspannung bei laminarer Strömung von der Wand zum axialen Mittelstrom hin ab. Als Scherrate bezeichnet
man die Relativbewegung dV einer gedachten Flüssigkeitsschicht pro
Schichtdicke dx (Geschwindigkeit pro Abstand, Dimension Zeit-1).
Als Scherrate bezeichnet
man die Relativbewegung dV einer gedachten Flüssigkeitsschicht pro
Schichtdicke dx (Geschwindigkeit pro Abstand, Dimension Zeit-1). (1 P = 0,1 Pa.s). Das Centi-Poise (cP) wird in der Physiologie verwendet, um die Viskosität
von Körperflüssigkeiten anzugeben (1 cP = 1 mPa.s. Wasser hat 1 cP, Plasma ~2 cP, Blut ~4 cP, abhängig vor allem vom Hämatokrit,
(1 P = 0,1 Pa.s). Das Centi-Poise (cP) wird in der Physiologie verwendet, um die Viskosität
von Körperflüssigkeiten anzugeben (1 cP = 1 mPa.s. Wasser hat 1 cP, Plasma ~2 cP, Blut ~4 cP, abhängig vor allem vom Hämatokrit,  Abbildung).
Abbildung). Flüssigkeiten können ganz verschiedene Formen variabler Viskosität
aufweisen; die Fließeigenschaften des Blutes hängen von Scherrate und
physikalisch-physiologischen Eigenschaften der Gefäße und
Blutkörperchen ab.
Flüssigkeiten können ganz verschiedene Formen variabler Viskosität
aufweisen; die Fließeigenschaften des Blutes hängen von Scherrate und
physikalisch-physiologischen Eigenschaften der Gefäße und
Blutkörperchen ab. Viskosimetrie: Mit üblichen Messgeräten
ermittelte Werte für die Blutviskosität erlauben nur eine eingeschränkte Aussage über das
tatsächliche Strömungsverhalten in der Mikrozirkulation.
(Halb)mikroskopische Methoden geben mehr Aufschluss über physiologisch
und medizinisch relevante Fließeigenschaften (s. weiter unten).
Viskosimetrie: Mit üblichen Messgeräten
ermittelte Werte für die Blutviskosität erlauben nur eine eingeschränkte Aussage über das
tatsächliche Strömungsverhalten in der Mikrozirkulation.
(Halb)mikroskopische Methoden geben mehr Aufschluss über physiologisch
und medizinisch relevante Fließeigenschaften (s. weiter unten).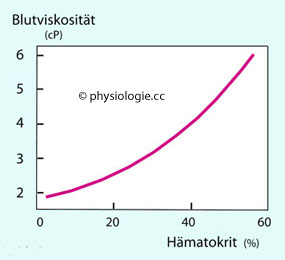
 Abbildung: Die Viskosität von Blutproben nimmt mit dem Hämatokrit nichtlinear zu
Abbildung: Die Viskosität von Blutproben nimmt mit dem Hämatokrit nichtlinear zu
 Hämatokrit
Hämatokrit Größe und Verformbarkeit der Blutkörperchen (innere Viskosität)
Größe und Verformbarkeit der Blutkörperchen (innere Viskosität) Geometrie und
adhäsive Eigenschaften der Gefäßwand
Geometrie und
adhäsive Eigenschaften der Gefäßwand  Allfällige Aktivierung der Blutstillung (Thrombozytenaktivierung, Gerinnselbildung)
Allfällige Aktivierung der Blutstillung (Thrombozytenaktivierung, Gerinnselbildung) Bluttemperatur:
Kühlt man Blut von Körpertemperatur auf 0°C ab, steigt seine Viskosität
um einen Faktor 2,5 an. Die allfällige Anwesenheit von Kryoglobulinen
(kälteempfindlichen Antikörpern) kann diesen Effekt verstärken.
Bluttemperatur:
Kühlt man Blut von Körpertemperatur auf 0°C ab, steigt seine Viskosität
um einen Faktor 2,5 an. Die allfällige Anwesenheit von Kryoglobulinen
(kälteempfindlichen Antikörpern) kann diesen Effekt verstärken. Abbildung). Das bedeutet,
dass hohe Hämatokritwerte die
Mikrozirkulation zusehends erschweren: Trotz hoher Hämoglobinmenge kann
immer weniger Sauerstoff an das Gewebe gelangen.
Abbildung). Das bedeutet,
dass hohe Hämatokritwerte die
Mikrozirkulation zusehends erschweren: Trotz hoher Hämoglobinmenge kann
immer weniger Sauerstoff an das Gewebe gelangen. Niedriger Hämatokrit (Werte ab ~15% sind mit physiologischen
Körperfunktionen weitgehend vereinbar, die körperliche Belastbarkeit
ist eingeschränkt) hat den Nachteil geringer Hämoglobinmenge, lässt
Blut aber besonders leicht fließen und beschleunigt dadurch den
Atemgastransport
Niedriger Hämatokrit (Werte ab ~15% sind mit physiologischen
Körperfunktionen weitgehend vereinbar, die körperliche Belastbarkeit
ist eingeschränkt) hat den Nachteil geringer Hämoglobinmenge, lässt
Blut aber besonders leicht fließen und beschleunigt dadurch den
Atemgastransport
 Hoher Hämatokrit (Werte >55%) bedeutet zwar viel Hämoglobin, das Blut gelangt
aber bei abnehmender Fließfähigkeit nur schwer durch die Mikrozirkulation (Beispiel Verkehrsüberlastung: Viele Transporter, dennoch geringe Transportquote)
Hoher Hämatokrit (Werte >55%) bedeutet zwar viel Hämoglobin, das Blut gelangt
aber bei abnehmender Fließfähigkeit nur schwer durch die Mikrozirkulation (Beispiel Verkehrsüberlastung: Viele Transporter, dennoch geringe Transportquote)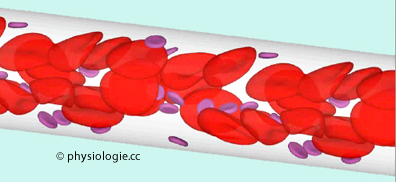
 Abbildung: Erythrozyten und Thrombozyten strömen durch ein kleines Gefäß (~15 µm Durchmesser)
Abbildung: Erythrozyten und Thrombozyten strömen durch ein kleines Gefäß (~15 µm Durchmesser) vgl. dort
vgl. dort
 Direkt am Endothel entlang strömt eine Plasmaschichte (geringe Viskosität)
Direkt am Endothel entlang strömt eine Plasmaschichte (geringe Viskosität) Die Blutkörperchen verformen sich entsprechend dem Strömungsprofil
(größte Geschwindigkeit in der Mitte des Gefäßes - durch kleine
Kapillaren schlüpfen Erythrozyten "pfeilspitzenförmig"). Der Fahraeus-Lindqvist-Effekt sagt aus, dass Blut besonders leicht durch das Kapillargebiet strömt, also eine niedrige effektive Viskosität aufweist
Die Blutkörperchen verformen sich entsprechend dem Strömungsprofil
(größte Geschwindigkeit in der Mitte des Gefäßes - durch kleine
Kapillaren schlüpfen Erythrozyten "pfeilspitzenförmig"). Der Fahraeus-Lindqvist-Effekt sagt aus, dass Blut besonders leicht durch das Kapillargebiet strömt, also eine niedrige effektive Viskosität aufweist| Die
effektive ("scheinbare") Blutviskosität nimmt in der Mikrozirkulation
ab und nähert sich der von Plasma an (geringster Betrag bei 7-10 µm
Gefäßdurchmesser) |
 Der 'Tunneleffekt'
schließlich sagt aus, dass die Blutkörperchen im
Axialstrom besonders rasch durch Kapillaren strömen, während Plasma
langsamer weiterkommt. So ist der
Hämatokrit in der Mikrozirkulation niedrig, meist weniger als die
Hälfte des Wertes in einer Blutprobe, die aus einem größeren Gefäß
stammt (daher beträgt der Ganzkörper-Hämatokrit nur ~87% des aus einer Blutprobe ermittelten Wertes)
Der 'Tunneleffekt'
schließlich sagt aus, dass die Blutkörperchen im
Axialstrom besonders rasch durch Kapillaren strömen, während Plasma
langsamer weiterkommt. So ist der
Hämatokrit in der Mikrozirkulation niedrig, meist weniger als die
Hälfte des Wertes in einer Blutprobe, die aus einem größeren Gefäß
stammt (daher beträgt der Ganzkörper-Hämatokrit nur ~87% des aus einer Blutprobe ermittelten Wertes) Beispiel: Gemessener Hämatokrit 0,4 (40%) → Ganzkörperhämatokrit ~0,35 (35%)
Beispiel: Gemessener Hämatokrit 0,4 (40%) → Ganzkörperhämatokrit ~0,35 (35%)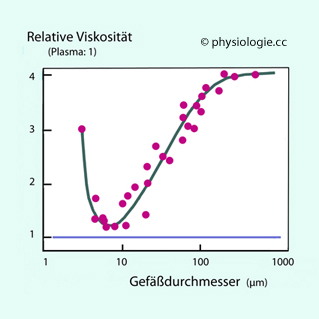
 Abbildung: Effektive Viskosität als Funktion des Gefäßdurchmessers
Abbildung: Effektive Viskosität als Funktion des Gefäßdurchmessers
 Abbildung). Dies ist vor allem durch den Fahraeus-Lindquist-Effekt
Abbildung). Dies ist vor allem durch den Fahraeus-Lindquist-Effekt  bedingt.
bedingt. Abbildung: linkes Kurvenende), bis die
Blutzellen die Kapillare nicht mehr
passieren können und es zu Stase (Stop der Bewegung des Blutes durch das Gefäß) kommt.
Abbildung: linkes Kurvenende), bis die
Blutzellen die Kapillare nicht mehr
passieren können und es zu Stase (Stop der Bewegung des Blutes durch das Gefäß) kommt. 
 Abbildung: Viskosimetrie: Formen des Messteils
Abbildung: Viskosimetrie: Formen des Messteils
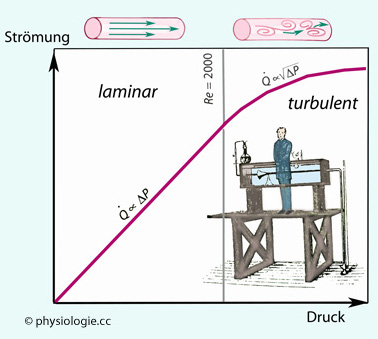
 Abbildung: Druck-Strömungs-Verhalten einer Newtonischen Flüssigkeit in einem starren Rohr
Abbildung: Druck-Strömungs-Verhalten einer Newtonischen Flüssigkeit in einem starren Rohr
 quantifiziert werden, die bei Rohrströmungen (Blutgefäße, Bronchien...) folgendermaßen errechnet wird:
quantifiziert werden, die bei Rohrströmungen (Blutgefäße, Bronchien...) folgendermaßen errechnet wird:| Re = (d.ν.ρ) / η |
| Turbulente Strömung entsteht umso wahrscheinlicher, je höher die Strömungsgeschwindigkeit ist |
 Ab Re-Werten
von ~400 treten lokalisierte Wirbel auf, vor allem an
Gefäßaufzweigungen - was z.B. in herznahen Abschnitten der Aorta und
Pulmonalarterie während der Austreibungszeit physiologisch ist. In der Aortenwurzel
erreicht der Re-Wert einen Betrag von ~4600 (Durchmesser d=2,5 cm,
Spitzengeschwindigkeit ν=70 cm/s, Blutdichte ρ=1,05 g/ml,
Blutviskosität η=4 mPa.s bzw. 0,04 gcm-1s-1), insbesondere bei Anämie, bei Schwangeren (sinkender Hämatokrit → geringe Blutviskosität) oder körperlicher Belastung (Spitzengeschwindigkeit steigt) können Strömungsgeräusche als Zeichen von Turbulenzen auftreten.
Ab Re-Werten
von ~400 treten lokalisierte Wirbel auf, vor allem an
Gefäßaufzweigungen - was z.B. in herznahen Abschnitten der Aorta und
Pulmonalarterie während der Austreibungszeit physiologisch ist. In der Aortenwurzel
erreicht der Re-Wert einen Betrag von ~4600 (Durchmesser d=2,5 cm,
Spitzengeschwindigkeit ν=70 cm/s, Blutdichte ρ=1,05 g/ml,
Blutviskosität η=4 mPa.s bzw. 0,04 gcm-1s-1), insbesondere bei Anämie, bei Schwangeren (sinkender Hämatokrit → geringe Blutviskosität) oder körperlicher Belastung (Spitzengeschwindigkeit steigt) können Strömungsgeräusche als Zeichen von Turbulenzen auftreten.  Bei Widerstandsgefäßen,
die einen sehr kleinen Durchmesser haben und wo das Blut langsam
strömt, erreicht [Re] lediglich einen Betrag von ~0,5 - die Strömung
bleibt laminar.
Bei Widerstandsgefäßen,
die einen sehr kleinen Durchmesser haben und wo das Blut langsam
strömt, erreicht [Re] lediglich einen Betrag von ~0,5 - die Strömung
bleibt laminar.  In der Mikrozirkulation
treten Turbulenzen erst recht nicht auf (sehr geringe Durchmesser und
Strömungsgeschwindigkeiten) - unbeschadet des zusätzlich ins Spiel
kommenden Fahraeus-Lindquist-Effekts:
Bei Gefäßdurchmessern um 10µm ist die Viskosität herabgesetzt ([Re]
steigt), bei noch geringerem Durchmesser steigt sie an ([Re] sinkt).
In der Mikrozirkulation
treten Turbulenzen erst recht nicht auf (sehr geringe Durchmesser und
Strömungsgeschwindigkeiten) - unbeschadet des zusätzlich ins Spiel
kommenden Fahraeus-Lindquist-Effekts:
Bei Gefäßdurchmessern um 10µm ist die Viskosität herabgesetzt ([Re]
steigt), bei noch geringerem Durchmesser steigt sie an ([Re] sinkt).  Als Faustregel kann gelten: Blutströmung erfolgt bei Re-Werten <2000 laminar, bei Werten >3000 meist turbulent.
Als Faustregel kann gelten: Blutströmung erfolgt bei Re-Werten <2000 laminar, bei Werten >3000 meist turbulent.
 Die
Fließeigenschaften des Blutes (messbar mittels Blutviskosimetrie) hängen ab von Hämatokrit (nichtlinear),
Flexibilität der Blutkörperchen, Art der Strömung, Geometrie und adhäsiven Eigenschaften der Gefäßwand und Viskosität des
Blutplasmas. Der Blutfluss wird durch Reibung zwischen den strömenden Schichten und an der Gefäßwand behindert (Viskosität - Dimension Kraft mal Zeit pro Fläche, Einheit cP = mPa.s - Maß für innere Reibung). Direkt am Endothel strömt eine Plasmaschicht; die Viskosität von Blutplasma beträgt ≤2 cP (Plasmaproteine ~70 g/l), diejenige von Blut (komplexe, nicht-newtonische Flüssigkeit) ~4 cP, sinkend (fließfähiger) mit zunehmender Scherung, höher (weniger fließfähig) bei langsamer Strömung (Blutviskosität kann bis
~20 cP steigen: Thixotropie; interzelluläre Haftungspunkte können durch zurückkehrende Strömung wieder gelöst werden). Scherkräfte ändern die Permeabilität deformationsempfindlicher endothelialer Kationenkanäle und
induzieren Vasodilatation durch proportional zunehmende NO-Synthese Die
Fließeigenschaften des Blutes (messbar mittels Blutviskosimetrie) hängen ab von Hämatokrit (nichtlinear),
Flexibilität der Blutkörperchen, Art der Strömung, Geometrie und adhäsiven Eigenschaften der Gefäßwand und Viskosität des
Blutplasmas. Der Blutfluss wird durch Reibung zwischen den strömenden Schichten und an der Gefäßwand behindert (Viskosität - Dimension Kraft mal Zeit pro Fläche, Einheit cP = mPa.s - Maß für innere Reibung). Direkt am Endothel strömt eine Plasmaschicht; die Viskosität von Blutplasma beträgt ≤2 cP (Plasmaproteine ~70 g/l), diejenige von Blut (komplexe, nicht-newtonische Flüssigkeit) ~4 cP, sinkend (fließfähiger) mit zunehmender Scherung, höher (weniger fließfähig) bei langsamer Strömung (Blutviskosität kann bis
~20 cP steigen: Thixotropie; interzelluläre Haftungspunkte können durch zurückkehrende Strömung wieder gelöst werden). Scherkräfte ändern die Permeabilität deformationsempfindlicher endothelialer Kationenkanäle und
induzieren Vasodilatation durch proportional zunehmende NO-Synthese  Die
Sauerstoff-Transportkapazität strömenden Blutes ist bei physiologischen
Hämatokritwerten am höchsten (niedriger Hämatokrit = wenig Hämoglobin,
hoher Hämatokrit = abnehmende Fließfähigkeit;
Sauerstoffmangel kann über Anregung der Erythropoese Hämatokritwerte
bis zu ~70% verursachen, entsprechend ~8 Mio Erys / µl). Blutkörperchen
verformen sich entsprechend dem Strömungsprofil (größte Geschwindigkeit
in der Gefäßmitte, Erythrozyten pfeilspitzenförmig): Blut strömt durch das Kapillargebiet besonders leicht (Minimalwert bei ~6 µm Kapillardurchmesser: Fahraeus-Lindqvist- Effekt) und Blutkörperchen im Axialstrom besonders rasch (Tunneleffekt),
was den Hämatokrit in der Mikrozirkulation senkt (Ganzkörper-Hämatokrit
~87% des aus einer Blutprobe ermittelten Wertes) Die
Sauerstoff-Transportkapazität strömenden Blutes ist bei physiologischen
Hämatokritwerten am höchsten (niedriger Hämatokrit = wenig Hämoglobin,
hoher Hämatokrit = abnehmende Fließfähigkeit;
Sauerstoffmangel kann über Anregung der Erythropoese Hämatokritwerte
bis zu ~70% verursachen, entsprechend ~8 Mio Erys / µl). Blutkörperchen
verformen sich entsprechend dem Strömungsprofil (größte Geschwindigkeit
in der Gefäßmitte, Erythrozyten pfeilspitzenförmig): Blut strömt durch das Kapillargebiet besonders leicht (Minimalwert bei ~6 µm Kapillardurchmesser: Fahraeus-Lindqvist- Effekt) und Blutkörperchen im Axialstrom besonders rasch (Tunneleffekt),
was den Hämatokrit in der Mikrozirkulation senkt (Ganzkörper-Hämatokrit
~87% des aus einer Blutprobe ermittelten Wertes) Die Strömung in Blutgefäßen erfolgt üblicherweise laminar: Die äußerste
Schicht gleitet (langsam) am Endothel vorbei, mit Annäherung an die
Gefäßmitte steigt die Geschwindigkeit. Blutkörperchen passen ihre Form
diesem Geschwindigkeitsprofil an, erschweren die Strömung aber dennoch,
insbesondere in kleinen Gefäßen. Ändern sich bestimmte Parameter der
Strömung, steigt die Wahrscheinlichkeit von Wirbelbildungen (turbulente
Strömung in größeren Gefäßen: Blut strömt teils quer zur Gefäßachse).
Gefäßweite (Innendurchmesser d), mittlere Strömungsgeschwindigkeit (ν)
und Dichte (ρ) begünstigen das Auftreten von Turbulenzen, zunehmende
Viskosität (η) macht Turbulenzen weniger wahrscheinlich (Anämie →
sinkender Hämatokrit → geringe Blutviskosität → Turbulenzen
wahrscheinlicher, akustisch wahrnehmbar). Die Reynolds-Zahl (Re) wird
errechnet als Re = (d x ν x ρ) / η. Wird ein kritischer Wert
überschritten, ist es wahrscheinlich, dass Turbulenzen auftreten. Ab
Werten von ~400 treten im Kreislauf lokalisierte Wirbel auf, vor allem an
Aufzweigungen großer Gefäße. An kleinen Gefäßen treten keine
Turbulenzen auf, der Re-Wert ist zu niedrig Die Strömung in Blutgefäßen erfolgt üblicherweise laminar: Die äußerste
Schicht gleitet (langsam) am Endothel vorbei, mit Annäherung an die
Gefäßmitte steigt die Geschwindigkeit. Blutkörperchen passen ihre Form
diesem Geschwindigkeitsprofil an, erschweren die Strömung aber dennoch,
insbesondere in kleinen Gefäßen. Ändern sich bestimmte Parameter der
Strömung, steigt die Wahrscheinlichkeit von Wirbelbildungen (turbulente
Strömung in größeren Gefäßen: Blut strömt teils quer zur Gefäßachse).
Gefäßweite (Innendurchmesser d), mittlere Strömungsgeschwindigkeit (ν)
und Dichte (ρ) begünstigen das Auftreten von Turbulenzen, zunehmende
Viskosität (η) macht Turbulenzen weniger wahrscheinlich (Anämie →
sinkender Hämatokrit → geringe Blutviskosität → Turbulenzen
wahrscheinlicher, akustisch wahrnehmbar). Die Reynolds-Zahl (Re) wird
errechnet als Re = (d x ν x ρ) / η. Wird ein kritischer Wert
überschritten, ist es wahrscheinlich, dass Turbulenzen auftreten. Ab
Werten von ~400 treten im Kreislauf lokalisierte Wirbel auf, vor allem an
Aufzweigungen großer Gefäße. An kleinen Gefäßen treten keine
Turbulenzen auf, der Re-Wert ist zu niedrig |
