

Eine Reise durch die Physiologie - Wie der Körper des Menschen funktioniert

Transport
im kardiovaskulären System (Kreislauf, Blut, Lymphe)

 Venensystem
Venensystem
© H. Hinghofer-Szalkay
 DeJager-Krogh-Effekt: S. DeJager, August Krogh
DeJager-Krogh-Effekt: S. DeJager, August Krogh
Frank-Starling-Mechanismus: Otto
Frank, Ernest Starling
Guyton's cross plot: Arthur Guyton
Kollaps: collabor = zusammenfallen, -brechen, -stürzen (labo = wanken, schwanken)
Orthostase: ὀρθός = (auf)recht, richtig; stare = (aufrecht) stehen
Synkope: σύν = zusammen, κὁπτω = schlagen
Thrombus: θρόμβος = Klumpen, Pfropf
Das
Blutvolumen befindet sich zu etwa 55% in den Venen, 25% im "kleinen"
Kreislauf (Lunge und Herzräume), 15% im Arteriensystem, und 5% in
der Mikrozirkulation. Abgesehen von hydrostatischen Druckschichtungen (Blutdruck oben niedriger als unten) nehmen die Druckwerte von der Herzkammer (während der Systole) bis zum Vorhof hin kontinuierlich ab - entsprechend der Richtung des Blutstroms.
Das rechte
Herz schöpft aus dem Niederdrucksystem (große Venen) und pumpt in den
Lungenkreislauf. Der Indikator für seine Vorlast ist der zentrale Venendruck (central venous pressure CVP), für seine Nachlast der Pulmonalarteriendruck. Beim linken Ventrikel zeigt der pulmonalkapilläre Druck (PCWP: pulmonary capillary wedge pressure) die Vorlast an, der Aortendruck die Nachlast.
Im kardiovaskulären Zustandspunkt des betreffenden Druck-Strömungs-Diagramms überkreuzen sich die Kurve des venösen Rückstroms und die Starling-Kurve, d.h. hier gilt ein Druck- und ein Strömungswert, der sowohl der Hydrodynamik des Gefäßsystems als auch der Frank-Starling-Charakteristik des Herzens entspricht.
Venen werden von der arteriellen Seite aus befüllt; retrograde Strömung wird vielerorts durch Venenklappen
verhindert. Je mehr Blut in Venen zwischengespeichert wird, desto
stärker
sinkt der venöse Rückstrom zum Herzen (und damit vorübergehend das
Herzminutenvolumen); entleeren sie sich (durch Kompression von außen
oder elastische Retraktion bei verringerter arterieller Befüllung),
nimmt der Rückstrom zu, und das
Herzminutenvolumen steigt.
Die Venen in Haut und Subkutis sind sehr dehnbar (hohe Compliance),
ebenso die Venen des Splanchnikusgebietes (Baucheingeweide). Der
Füllungsgrad kutaner Venengeflechte steht unter dem Einfluss der Thermoregulation (Wärmeabgabe), Kreislaufreflexe
beteiligen sich an der Steuerung der Gefäße im Bauchraum. Die
Venengeflechte in der Skelettmuskulatur könnten ebenfalls viel Blut
aufnehmen, das tun sie aber in der Regel nicht, da sie von der
aktiven Muskulatur (die stärker durchblutet ist) "massiert" und damit
laufend entleert werden ("Muskelpumpe").
|
Der "Arbeitspunkt" des Kreislaufs  Verteilung des Blutvolumens
Verteilung des Blutvolumens  Dynamische Speicherung
Dynamische Speicherung  DeJager-Krogh- Mechanismus
DeJager-Krogh- Mechanismus  Steuerung venöser Speicherung
Steuerung venöser Speicherung  Vorlast für rechtes und linkes Herz: Zentraler Venendruck, PCWP
Vorlast für rechtes und linkes Herz: Zentraler Venendruck, PCWP  Orthostase
Orthostase  Wasserimmersion
Wasserimmersion  Muskelpumpe
Muskelpumpe  Atempumpe, Venenpuls
Atempumpe, Venenpuls  Hydrostatik, Orthostase
Hydrostatik, Orthostase
 Systemischer Blutdruck
Systemischer Blutdruck
 Praktische Aspekte
Praktische Aspekte  Core messages
Core messages
Im
Venensystem befindet sich der Großteil (60-70%) des Blutvolumens. Die
Verteilung des Blutes innerhalb des Systems hängt ab vom Kontraktionsgrad der Gefäße (peripherer venöser Tonus) sowie weiteren Faktoren (Körperlage, Muskelpumpe, Atmung, Herzaktivität).
Daraus ergibt sich ein diastolischer Füllungsdruck des rechten Herzens
(im Bereich der Mündung der Hohlvenen in den rechten Vorhof), der
mittels venösem Katheter gemessen werden kann und als Zentralvenendruck (CVP, central venous pressure)
bezeichnet wird. Sein Betrag hängt von den genannten Größen ab und ist
ein wichtiger Indikator für den Zustand des kardiovaskulären Systems.
Die Strömungs-Druck-Kurven von Herz und Kreislauf treffen sich im "Arbeitspunkt" des kardiovaskulären Systems
Sowohl
die Funktionsweise des Herzens als auch die der Blutgefäße folgen ihrer
spezifischen Dynamik. Da diese beiden Systeme hydromechanisch
miteinander verknüpft sind (beide sind Teil des Blutkreislaufs),
stimmen ihre Druck-Volumen-Charakteristika in bestimmten
"Arbeitspunkten" überein (d.h. ihre Druck-Volumen-Kurven überschneiden
sich zu jedem Zeitpunkt bei einem jeweils bestimmten Druck- und
Volumenbetrag). Eine solche Abstimmung gibt es sowohl für den
arteriellen (rechtes Herz und Pulmonalarterie, linkes Herz und Aorta)
als auch für den venösen Schenkel der Teilkreisläufe (rechtes Herz und
Hohlvenensystem, linkes Herz und Pulmonalvenen).
 Über Vor- und Nachlast des rechten und linken Herzens s. dort
Über Vor- und Nachlast des rechten und linken Herzens s. dort


Abbildung: Verteilung des Blutvolumens
Nach
einer Vorlage in Gauer OH, Kreislauf des Blutes. Gauer / Kramer / Jung,
Physiologie des Menschen, Band 3: Herz und Kreislauf, U&S 1972
Im
Hochdrucksystem bedindet sich weniger als ein Fünftel des gesamten
Blutvolumens. Das zentrale Blutvolumen ist die Füllungsreserve für das
linke Herz. Aus dem Kreislauf austretende Proteine gelangen in das
Interstitium und über den Lymphkreislauf in die Blutbahn zurück

Die Druckverhältnisse im kardiovaskulären System hängen von
mehreren Faktoren ab: Der Lage in Bezug zum geltenden
Beschleunigungsvektor (üblicherweise: Schwerkraft - hydrostatische Druckunterschiede), das
Füllungsvolumen des betreffenden Flüssigkeitskompartments (Blutvolumen,  Abbildung), die Elastizitätsverhältnisse der betreffenden Gefäße
(Compliance).
Abbildung), die Elastizitätsverhältnisse der betreffenden Gefäße
(Compliance).
Dazu kommt die aktive Komponente des Myokards: Die
Herzaktivität folgt eigenen Gesetzmäßigkeiten (z.B.
Frank-Starling-Mechanimus), die bestimmen, wie gut es sich disatolisch
füllt und wie stark es während der Systole als Pumpe wirkt.
Der
Druckunterschied zwischen arteriellen (Versorgungs-) und venösen
(Abtransport-) Gefäßen beträgt etwa 10 kPa (75 mm Hg). Die Energie für
diesen Druckgradienten, der Blut durch die Haarnadelgefäße (Kapillaren)
treibt und damit den metabolischen Austausch sichert, stammt aus der
Herztätigkeit.
Im Folgenden werden die einzelnen Faktoren beschrieben, welche
das Zusammenwirken aktiver und passiver Komponenten für das Geschehen
im Blutkreislauf
(cardiovascular system)
ermöglichen: Füllung (Blutvolumen), Zusammenwirken von Dehnung und
Strömung (Hämodynamik), Füllung der Herzräume (Vorlast, zentraler
Venendruck, Pulmonaldruck), Orthostase, Arbeitskurve des Herzens,
arterieller Druck.
Verteilung des Blutvolumens
Das meiste Blut
befindet sich im Niederdrucksystem (Kapillaren bis rechtes Herz):
Kapillaren ~5%, Venolen und
Venen ~55%, Lungenkreislauf und Herzräume ~25% des gesamten
Blutvolumens. Aus diesem Reservoir strömt Blut zum rechten Herzen (venöser Rückstrom, venous return).

 Abbildung: Strömungsrate und Druckwerte vor und hinter der Pumpe
Abbildung: Strömungsrate und Druckwerte vor und hinter der Pumpe
Nach einer Vorlage in Herring / Paterson, Levick's Introduction to Cardiovascular Physiology, 6th ed. 2018
Das Pumpensymbol oben links steht für das Herz, die Pfeile für den Druck vor (Vorlast) und nach dem Herzen (Nachlast).
Steht die Pumpe still (Herzstillstand), ergibt sich in diesem
vereinfachten Kreislaufmodell für beide Drucke derselbe Wert
(systemischer Druck, mean circulatory pressure
MCP). Schaltet sich die Pumpe ein - zunächst auf einen niedrigen Wert
von 1 l/min, dann auf 5 l/min -, steigt der Druck auf der arteriellen
(geringe Compliance) stärker als er auf der venösen Seite (hohe
Compliance) abnimmt (grüne Kurven).
Das Einschalten
der Pumpe erhöht das arterielle und reduziert (etwa um denselben
Betrag) das venöse Blutvolumen. Der mittlere Druck auf der
Ausstromseite ist der arterielle Druck (hier
etwa 100 mmHg), auf der Einstromseite der zentrale Venendruck CVP (central venous pressure).
Sinkt das Herzminutenvolumen (z.B. bei Herzversagen), nimmt (ceteris
paribus) auch der arterielle Blutdruck ab, der mittlere venöse Druck
hingegen steigt (in Richtung MCP) an
 Als mittleren systemischen (statischen) Blutdruck (mean systemic filling pressure
MSFP, mean circulatory pressure MCP) bezeichnet man den Druck, der sich (abgesehen von hydrostatischen
Unterschieden) in allen Gefäßen nach einem kompletten Herzstillstand
(und bevor sekundäre Filtrationseffekte auftreten) einstellen würde.
(Eine kurze Zeitspanne nach dem "Shutdown" würde noch Blut von Arterien
in Kapillaren und Venen fabließen, bis sich die Drucke komplett
ausgeglichen haben und die Strömung den Wert 0 annimmt.)
Als mittleren systemischen (statischen) Blutdruck (mean systemic filling pressure
MSFP, mean circulatory pressure MCP) bezeichnet man den Druck, der sich (abgesehen von hydrostatischen
Unterschieden) in allen Gefäßen nach einem kompletten Herzstillstand
(und bevor sekundäre Filtrationseffekte auftreten) einstellen würde.
(Eine kurze Zeitspanne nach dem "Shutdown" würde noch Blut von Arterien
in Kapillaren und Venen fabließen, bis sich die Drucke komplett
ausgeglichen haben und die Strömung den Wert 0 annimmt.)
Dieser Druck entspricht der elastischen Gefäßdehnung durch den Inhalt (Blut) und beträgt etwa 7 mmHg oder rund 1 kPa
(passiver "Betriebsdruck" des gesamten Kreislaufs bei einem normalen
Blutvolumen und physiologischen Compliancewerten aller Gefäße). Sein Betrag nimmt mit der
Kreislauffüllung (Blutvolumen) zu und mit der Dehnbarkeit (Compliance) des
Gefäßsystems ab.
Dem allgemeinen Strömungsgesetz folgend, hängt der venöse Rückstrom vom
treibenden Druck ab, d.h. dem Unterschied des peripheren "Systemdrucks"
und dem diastolischen Druck im rechten Herzen. Die Pumpleistung
des Herzens hängt von der Vorlast ab.
Nach einer von Guyton entwickelten Projektion der Eigenschaften des Gefäßsystems einerseits,
des aktiven Herzens andererseits in eine Strömungs-Druck-Grafik kann
die Interaktion der beiden anschaulich dargestellt werden (Guyton's cross plot):
entwickelten Projektion der Eigenschaften des Gefäßsystems einerseits,
des aktiven Herzens andererseits in eine Strömungs-Druck-Grafik kann
die Interaktion der beiden anschaulich dargestellt werden (Guyton's cross plot):
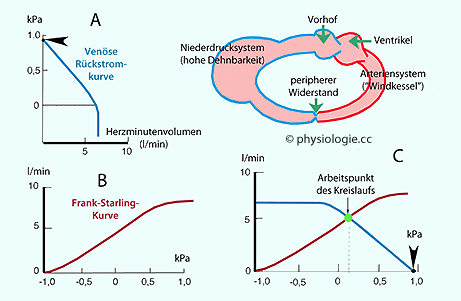
 Abbildung: Venöser Rückstrom gleich Herzzeitvolumen
Abbildung: Venöser Rückstrom gleich Herzzeitvolumen
Nach einer Vorlage in New Human Physiology
Der
schwarze Pfeilkopf in (A) und (C) gibt den Druck an, der sich akut bei
Herzstillstand im Kreislauf einstellen würde (systemischer oder statischer Blutdruck)
A: Druck-Strömungs-Kurve des venösen Systems. Der Druckunterschied von Niederdrucksystem zu Vorhof bestimmt die Blutströmung zum
Herzen. Diese Kurve ist in (C) mit Koordinatenwechsel dargestellt.
B: Druck-Strömungs-Kurve als Arbeitskurve des Herzens: Mit zunehmendem Füllungsdruck nimmt das Herzzeitvolumen zu: Frank-Starling-Mechanismus.
C: Nur im Schnittpunkt der beiden Kurven sind die Bedingungen
sowohl der venösen Strömung zum Herzen (blaue Kurve) als auch der Herzfunktion (rote Kurve) erfüllt; die strichlierte Linie
gibt den dabei herrschenden Druck im rechten Vorhof an.
Der Schnittpunkt der blauen Kurve mit der Druckachse (A, C) liegt bei ca. 1 kPa: statischer Blutdruck. Volumendehnbarkeit = Compliance

Die folgende  Abbildung zeigt, wie Veränderungen des Blutvolumens
einerseits, des Zustandes des Herzmuskels andererseits diesen
Schnittpunkt verlagern: Die grünen
Kurven zeigen den Normalzustand - "normal" = Starlingkurve,
"Normovolämie" = venöse Rückstromkurve, vascular function curve -, der Kurvenschnittpunkt liegt
bei einem Herzzeitvolumen von 5 l/min und einem Zentralvenendruck (Maß für die Vorlast des rechten Ventrikels) von etwa 2 mmHg.
Abbildung zeigt, wie Veränderungen des Blutvolumens
einerseits, des Zustandes des Herzmuskels andererseits diesen
Schnittpunkt verlagern: Die grünen
Kurven zeigen den Normalzustand - "normal" = Starlingkurve,
"Normovolämie" = venöse Rückstromkurve, vascular function curve -, der Kurvenschnittpunkt liegt
bei einem Herzzeitvolumen von 5 l/min und einem Zentralvenendruck (Maß für die Vorlast des rechten Ventrikels) von etwa 2 mmHg.
Die Rückstromkurve zeigt die Strömung (=Herzzeitvolumen, y-Achse) als Funktion des Zentralvenendrucks (right atrial pressure
RAP, x-Achse). Nimmt (ceteris paribus) der Betrag des
Zentralvenendrucks ab, nimmt der Druckgradient von der Peripherie
(MSFP) zum rechten Vorhof (RAP) zu. Damit steigt der venöse Rückstrom
von Blut zum Herzen (∆p = MSFP - RAP).

 Abbildung: Herzminutenvolumen als Funktion des zentralen Venendrucks (nach A. Guyton)
Abbildung: Herzminutenvolumen als Funktion des zentralen Venendrucks (nach A. Guyton)
Die Kurve des venösen Rückstroms ("Normovolämie": Venous return curve, vascular function curve) kreuzt diejenige der Herzleistung ("normal": Cardiac output curve) bei einem bestimmten Druck- (hier ~2 mmHg: Betrag des Zentralvenendrucks) und Strömungswert (hier ~5 l/min).
Steigender Zentralvenendruck reduziert den venösen Rückstrom (dieser wird Null bei ~7 mmHg, weil dann keine Druckdifferenz zum "Systemdruck" des Kreislaufs - mean circulatory pressure - mehr besteht) und steigert die Herzleistung (Frank-Starling-Mechanismus) - bis zu einem Plateau ab ~4 mmHg.
Bei
erhöhtem Blutvolumen ("Hypervolämie", z.B. durch rasche Infusion) liegen die Arbeitspunkte des Kreislaufs (blau) bei
höheren Werten für Zentralvenendruck und Herzminutenvolumen als bei
Normovolämie (hellgrüne Schnittpunkte). Die Steilheit
dieser Kurve bleibt durch Veränderung des Blutvolumens alleine
unbeeinflusst. Das gilt auch für Hypovolämie, bei der alle
Schnittpunktwerte erniedrigt wären (nicht gezeigt).
Bei
Herzversagen ("Schlagkraft eingeschränkt") ist die Leistungskurve des
Herzens in Richtung niedrigerer Förderleistungen verlagert

Nimmt das Blutvolumen zu (Hypervolämie, blaue Rückstromkurve),
verschiebt sich diese Kennkurve nach rechts und oben, weil der Kreislauf stärker
"aufgeblasen" ist (vgl. dort) - Resultat (Schnittpunkt der Kurven) ist typischerweise ein erhöhtes Herzzeitvolumen bei leicht erhöhtem Zentralvenendruck.
Die Steilheit der venösen Rückstromkurve (vascular function curve)
bleibt bei Veränderung des Blutvolumens oder Tonisierung der Venenwände
so gut wie konstant - sie wird nur im Diagramm zu reduzierten
(Hypovolämie oder Tonusverringerung) oder erhöhten Werten
(Volumenzunahme oder Venokonstriktion) verlagert ("parallelverschoben").
 Funktionell ausschlaggebend ist nicht das Blutvolumen als solches (wie es durch eine Indikatorverdünnungsmethode bestimmbar ist), sondern das effektive Blutvolumen (effective circulating volume -
Funktionell ausschlaggebend ist nicht das Blutvolumen als solches (wie es durch eine Indikatorverdünnungsmethode bestimmbar ist), sondern das effektive Blutvolumen (effective circulating volume -  s. dort).
Dabei handelt es sich um ein funktionell betontes Konzept, das die
Bedeutung der Regulation von Blutdruck und Durchblutung in den
Vordergrund rückt: Es ist dasjenige Volumen, dessen Größe über
verschiedene Rezeptoren im Körper (z.B. Barorezeptoren) indirekt
ermittelt wird und über neuroendokrine Systeme (Sympathikus,
verschiedene Hormone) regulatorisch wirksam wird.
s. dort).
Dabei handelt es sich um ein funktionell betontes Konzept, das die
Bedeutung der Regulation von Blutdruck und Durchblutung in den
Vordergrund rückt: Es ist dasjenige Volumen, dessen Größe über
verschiedene Rezeptoren im Körper (z.B. Barorezeptoren) indirekt
ermittelt wird und über neuroendokrine Systeme (Sympathikus,
verschiedene Hormone) regulatorisch wirksam wird.
Nimmt die Schlagkraft des Herzens ab (Kardiomyopathie - z.B. Ischämie, violette und rote
Starling-Kurve in der  Abbildung), sinkt einerseits das Herzzeitvolumen (weil das Myokard
geschwächt ist), andererseits erhöhen sich die Füllungsdrucke (weil
sich Blut in der Peripherie rückstaut).
Abbildung), sinkt einerseits das Herzzeitvolumen (weil das Myokard
geschwächt ist), andererseits erhöhen sich die Füllungsdrucke (weil
sich Blut in der Peripherie rückstaut).
 Veränderungen des Zentralvenendrucks müssen immer im Zusammenhang mit
der Gesamtsituation des Kreislaufs interpretiert werden (Zustand des
Herzmuskels vs. Zustand des Kreislaufs).
Veränderungen des Zentralvenendrucks müssen immer im Zusammenhang mit
der Gesamtsituation des Kreislaufs interpretiert werden (Zustand des
Herzmuskels vs. Zustand des Kreislaufs).
Die Körperlage beeinflusst die Drucke in den Gefäßen zusätzlich. Im Liegen beträgt der Venendruck entlang der
Körperachse 1-2 kPa (10-20 cm H2O oder rund 10 mm Hg); bei aufrechter Körperlage kommen orthostatische Druckunterschiede dazu.

 Näheres zu Schwerkraft und hydrostatischen Druckgradienten im Kreislauf s. dort
Näheres zu Schwerkraft und hydrostatischen Druckgradienten im Kreislauf s. dort
 Intravenöse Infusion: Die Höhe eines
Tropfers über der Infusionsstelle bestimmt den Infusionsdruck. So ergibt 20 cm Tropferhöhe bei einem
Venendruck von 15 cm Wassersäule 20-15 = 5 cm H2O treibenden Druck. Die Infusionsgeschwindigkeit hängt vom
Strömungswiderstand der Leitung ab; dieser wird mittels
Quetschrolle am Schlauch beeinflusst, hängt aber
auch vom Ende der Leitung in der Vene ab: Bilden sich
Thromben
Intravenöse Infusion: Die Höhe eines
Tropfers über der Infusionsstelle bestimmt den Infusionsdruck. So ergibt 20 cm Tropferhöhe bei einem
Venendruck von 15 cm Wassersäule 20-15 = 5 cm H2O treibenden Druck. Die Infusionsgeschwindigkeit hängt vom
Strömungswiderstand der Leitung ab; dieser wird mittels
Quetschrolle am Schlauch beeinflusst, hängt aber
auch vom Ende der Leitung in der Vene ab: Bilden sich
Thromben  , verlegen diese die Kanüle und die Tropfrate
nimmt während der Infusion ab.
, verlegen diese die Kanüle und die Tropfrate
nimmt während der Infusion ab.

Venengeflechte sind dynamische Volumenspeicher
Venen
speichern den größten Teil des Blutvolumens. Da ihre Wände relativ dünn
ausgebildet sind, können sie bei niedrigem Innendruck auch leicht
kollabieren. Das macht sich überall dort bemerkbar, wo der
hydrostatische Druck auf Grund der Körperposition niedrig ist, also in
Regionen, die - bezogen auf die Schwerkraft - jeweils "oben" zu
liegen kommen (vgl. hydrostatische Druckprofile).

 Abbildung: Druck-Volumen-Profil einer Vene im entspannten
(Querschnitte und obere Kurve) und kontrahierten Zustand (untere Kurve)
Abbildung: Druck-Volumen-Profil einer Vene im entspannten
(Querschnitte und obere Kurve) und kontrahierten Zustand (untere Kurve)
Nach Vanhoutte PM, Leusen I. The reactivity of isolated venous preparations to electrical stimulation. Pflügers Archiv: Eur J Physiol 1969; 306: 351-53
Die
Dehnbarkeit der Vene nimmt durch Kontraktion der Venenwand ab (Volumen
/ Druck), das durch die Vasokonstriktion verdrängte Volumen
(noradrenerge Aktivität) kommt dem venösen Rückstrom zum Herzen zugute
und wirkt damit kreislaufstützend.
Die Formveränderungen beim Kollaps (oben links) bedingen eine komplexe Hydrodynamik. Ab etwa 2 kPa venösem Druck ist das Venenprofil kreisrund (oben rechts)

I
n den jeweils "unten" gelegenen
Körpergebieten hingegen sind die Venen blutgefüllt - je weiter vom
hydrostatischen Indifferenzpunkt entfernt, umso stärker. (Der
hydrostatische Indifferenzpunkt ist die Stelle im Körper, bei welcher
der hydrostatische Druck im Gefäß bei Wechsel der Körperlage
unverändert bleibt - bei den großen Venen etwas unterhalb der
Zwerchfellkuppel, also im Bereich des Oberbauchs).
Dabei gilt das Siphonprinzip:
liegt in einem hydrostatisch verbundenen (offenen) Rohrsystem ein
Gefäßschenkel weiter oben, ist dort der Druck entsprechend reduziert -
und in einem weiter unten gelegenen ist der Druck erhöht (um jeweils ~1 kPa pro 0,1 m Höhenunterschied).
Die größte Dehnbarkeit (Compliance) der Venen zeigt sich bei einem gering positiven transmuralen Druck (~4 mmHg oder ~0,5 kPa): etwa 100 ml/mmHg - etwa das 50-fache der Compliance vergleichbar großer Arterien.
Ab transmuralen Drucken von 10-15 mmHg nimmt die Vene eine kreisrunde
Form an ( Abbildung). Die maschengitterartig angeordneten
Kollagenbündel in der Venenwand bieten ab diesem Druck einen zunehmen
rigiden Widerstand gegen weitere Dehnung, dementsprechend nimmt die
Compliance deutlich ab, die Volumen-Druck-Kurve wird zusehends steiler,
die Wand steifer - das ergibt einen automatischen Schutz vor zu starker
Blutfüllung und unterstützt zusammen mit dem Mechanismus der Muskelpumpe den Rückstrom zum Herzen, im Stehen insbesondere aus den Beinen.
Abbildung). Die maschengitterartig angeordneten
Kollagenbündel in der Venenwand bieten ab diesem Druck einen zunehmen
rigiden Widerstand gegen weitere Dehnung, dementsprechend nimmt die
Compliance deutlich ab, die Volumen-Druck-Kurve wird zusehends steiler,
die Wand steifer - das ergibt einen automatischen Schutz vor zu starker
Blutfüllung und unterstützt zusammen mit dem Mechanismus der Muskelpumpe den Rückstrom zum Herzen, im Stehen insbesondere aus den Beinen.
Zu diesem passiven Element kommt die Kontraktilität
der Venenwand: Die tunica media der Venen in Leber,
Gastrointestinaltrakt, Nieren (alle in der Nähe des venösen
hydrostatischen Indifferenzpunktes gelegen), aber auch in der Haut,
sind reichlich mit adrenergen Nervenfasern versorgt. Sympathische
Aktivität erhöht den Innendruck und treibt Blut zum Herzen, wirkt also
kreislaufaktivierend ( Abbildung), insbesondere in Stresssituationen.
Abbildung), insbesondere in Stresssituationen.
DeJager-Krogh-Mechanismus 
Neben dem Gefäßtonus hängt die Füllung von Venen vor allem vom
arteriellen Zustrom ab: Der DeJager-Krogh-Effekt (DeJager-Krogh-Mechanismus, DeJager-Krogh-Phänomen,  Abbildung)
besteht darin, dass eine - durch erhöhten Sympathikustonus bedingte -
Verengung arteriolärer Gefäße (Stresseffekt) und dadurch Reduktion des
Zuflusses zum nachgeschalteten venösen Gefäßgebiet (Venenplexus) zu
dessen Entspeicherung führt (vorher durch den Blutdruck angetriebene
Dehnung der Venenwände führt zu deren elastischem Zusammenziehen -
potenzielle Energie wird in kinetische Energie rückverwandelt). So wird
Blut Richtung Herz mobilisiert und steht zur Stabilisierung des
arteriellen Blutdrucks trotz funktioneller Hypovolämie zur Verfügung.
Abbildung)
besteht darin, dass eine - durch erhöhten Sympathikustonus bedingte -
Verengung arteriolärer Gefäße (Stresseffekt) und dadurch Reduktion des
Zuflusses zum nachgeschalteten venösen Gefäßgebiet (Venenplexus) zu
dessen Entspeicherung führt (vorher durch den Blutdruck angetriebene
Dehnung der Venenwände führt zu deren elastischem Zusammenziehen -
potenzielle Energie wird in kinetische Energie rückverwandelt). So wird
Blut Richtung Herz mobilisiert und steht zur Stabilisierung des
arteriellen Blutdrucks trotz funktioneller Hypovolämie zur Verfügung.
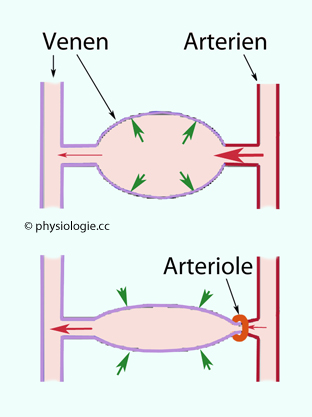
 Abbildung: DeJager-Krogh-Mechanismus
Abbildung: DeJager-Krogh-Mechanismus
Modifiziert nach Daugirdas JT, Dialysis hypotension: a hemodynamic analysis. Kidney Int 1991; 39: 233-46
Oben: Öffnen sich die Widerstandsgefäße
(arterioläre Vasodilatation), strömt mehr Blut ins Niederdrucksystem
ein (roter Pfeil rechts), Blut wird von Venen vermehrt gespeichert (grüne Pfeile) - die Vorlast für das Herz sinkt (Reduktion des Herzminutenvolumens).
Unten: Arterioläre Vasokonstriktion
verringert den Einstrom in das Kapillargebiet, der Dehnungsdruck nimmt
ab, die Venen retrahieren (elastisch - grüne Pfeile) und verlagern Blut
wird in Richtung Herz - die Vorlast für das Herz steigt (Erhöhung des Herzminutenvolumens)

Arteriolenweite
und Venenfüllung sind miteinander verknüpft - der Zustrom von Blut aus
den Arteriolen bestimmt die Füllung der nachfolgenden Venen, die bei
erhöhtem Einströmen von Blut einen Teil davon elastisch speichern (eine
Art "venöse Windkesselwirkung"):
Entspeicherung: Nimmt der arterielle Zufluss ab
(arterioläre Konstriktion), entspeichern die Venen aufgrund der
passiven Retraktion ihrer Wände (wie das Zusammenschnurren von
Gummibändern) einen Teil des vorher elastisch gespeicherten Blutes, das
Richtung Herz weiterströmt (potentielle wird zu kinetischer Energie). Dies dient der
Aufrechterhaltung des Herzzeitvolumens in kritischen
Kreislaufsituationen (DeJager-Krogh-Phänomen). Die Notwendige Kraft für die Kontraktion stammt aus der Gefäßwand. Dieser
Mechanismus kommt immer dann ins Spiel, wenn das Blutvolumen schlechter verfügbar wird oder rasch
absinkt (z.B. nach Blutverluist, im
Rahmen einer Hämodialyse usw).
Speicherung: Umgekehrt führt arterioläre Dilatation zu stärkerer Venenfüllung, dies erhöht die venöse Füllung und senkt den Rückstrom zum Herzen - kinetische wird zu potentieller Energie.
Auf diese Weise fungieren die Venen als dynamischer Zwischenspeicher.
Die notwendige Kraft für die Dilatation stammt (via Blutdruck) aus dem
Herzen.
Steuerung venöser Speichergefäße
Für die
Kreislaufwirksamkeit des venösen Blutspeichers ist sowohl der Betrag
des Blutvolumens (~7-8% der Körpermasse) als auch dessen Verteilung ausschlaggebend. Zwei Abschnitte
des Venensystems können besonders viel Blut speichern: Die
Venengeflechte der Haut und die der Baucheingeweide, letztere werden vom
Splanchnikusnerv versorgt (“Splanchnikusgebiet”:
Venen des Gastrointestinaltrakts, der Leber und Milz). Die Venen des
Splanchnikusgebietes enthalten im Ruhezustand etwa 20% des Blutvolumens
und haben zahlreiche α-Adrenozeptoren.
Bei Belastung bzw. Blutdruckabfall können sie kontrahieren (erhöhter
Sympathikustonus) und einen Teil des Blutes in den zentralen
(intrathorakalen) Blutkreislauf verschieben, was den Kreislauf
stabilisiert.
Dazu kommen die Venengeflechte der Skelettmuskulatur, die allerdings normalerweise immer dann gut entleert werden, wenn die betreffenden Muskeln aktiv sind ("Muskelpumpe").
Diese Venen sind kaum sympathisch versorgt; ihre Füllung wird indirekt
sympathisch beeinflusst, und zwar über den Zufluss durch präkapilläre
Widerstandsgefäße (DeJager-Krogh- Phänomen, s. oben).

 Abbildung: Die wichtigsten venösen Zuflussgebiete
Nach einer Vorlage bei Shepherd JT, Vanhoutte PM, The Human Cardiovascular System, Facts and Concepts. Raven Press NY 1979
Abbildung: Die wichtigsten venösen Zuflussgebiete
Nach einer Vorlage bei Shepherd JT, Vanhoutte PM, The Human Cardiovascular System, Facts and Concepts. Raven Press NY 1979
Kontraktion peripherer Venen (insbesondere im Splanchnikusgebiet) erhöht das zentrale Blutvolumen und Herzzeitvolumen.
Venengeflechte der Organe im Bauchraum (Splanchnikusgebiet, oben) reagieren vor allem auf "klassische" Kreislaufreflexe (z.B. Barorezeptorreflex), Venen in der Haut (Mitte) stehen vor allem im Dienst der Thermoregulation, Venen der Skelettmuskulatur (unten) werden durch die Muskelpumpe geleert (und haben kaum sympathische Innervation).
Alle diese Venengeflechte haben hohe
Speicherkapazität. Die Speicherung wird - außer über nervöse (sympathische) Einflüsse - über arteriellen Zufluss
(s.  Abbildung oben: DeJager-Krogh-Mechanismus) und mechanische Gegenkräfte (Druck von außen) reguliert
Abbildung oben: DeJager-Krogh-Mechanismus) und mechanische Gegenkräfte (Druck von außen) reguliert

Die Füllung der
Venen in Bauchraum und in der Haut wird sehr stark vom arteriellen Einstrom bestimmt:

Bei erhöhter Darmtätigkeit nimmt die Durchblutung im Splanchnicus-Gebiet zu (niedrige Sympathikus-Aktivität).

Steigt die Körpertemperatur an (+
Hautdurchblutung) oder kommt es zu vermehrter Muskelaktivität, wird die Durchblutung im Splanchnikusgebiet gedrosselt (+
Sympathikusaktivität).
Dazu kommt der Einfluss venenkontrahierender (Vasokonstriktoren) und/oder entspannender Faktoren (Vasodilatatoren).
Beispielsweise nimmt der Venentonus in den Beinen bei aufrechter
Körperlage reflektorisch zu, um die Speicherung von Blut in der unteren
Körperhälfte in dieser Situation zu minimieren.
Zwischen der Steuerung von Venen und arteriellen Widerstandsgefäßen gibt
es Unterschiede: Die meisten Venen haben ohne sympathischen Einfluss
kaum einen basalen Tonus; sie reagieren in den wenigsten Fällen auf
Dehnung ihrer Wand mit Kontraktion; und sie exprimieren Rezeptoren
unterschiedlich stark, z.B. wirkt Angiotensin II kaum auf Venen.
Zentraler Venendruck: Vorlast für das rechte Herz
Der zentrale Venendruck (ZVD) - der mittlere Blutdruck im Bereich
des rechten Atriums - dient Maß für die Vorlast für das rechte Herz. Sein Betrag hängt von der Körperlage ab: Da der hydrostatische Indifferenzpunkt
(aufrecht <-> liegend) des Venensystems unterhalb des Herzniveaus
liegt, ist er im Liegen höher als im Sitzen oder Stehen:
Zentraler Venendruck
(Mittelwert)
|
aufrecht
|
~0 (Außendruck)
|
liegend
|
um +4 mmHg (~0,5 kPa)
|
Der Zentralvenendruck schwankt um einen Mittelwert (Tabelle), die Oszillationen sind vor allem bedingt durch den Herzschlag (s. Venenpuls) und die Atmung, aber auch durch körperliche Aktivitäten. Sein mittlerer Betrag ist ein Maß für die Vorlast des rechten Ventrikels
und beträgt im Liegen wenige mm Hg
über dem Referenz (äußeren Luft-) druck, im Sitzen oder Stehen um
einige
mmHg weniger und beträgt dann ziemlich genau "Null", d.h. sein Betrag entspricht dem äußeren Bezugsdruck.
Bei Herzinsuffizienz kann der Zentralvenendruck bis auf ~20-30 mmHg
ansteigen, wenn das Herz das venöse Angebot nicht mehr bewältigt
(Überschreiten der Grenzen, innerhalb derer der
Frank-Starling-Mechanismus  wirkt).
wirkt).
 Interpretation des ZVD
Interpretation des ZVD:
Ein
hoher Zentralvenendruck kann zweierlei bedeuten:

Venensystem: Hohes venöses Volumenangebot, z.B. bei liegender Position (evt. auch Hypervolämie), aber auch

Myokardiale Schlagkraft:
Herzinsuffizienz (mangelhaftes
"Abpumpen" von Blut aus dem Niederdrucksystem).
Umgekehrt ist auch die
Interpretation
niedriger Druckwerte ambivalent: Diese können einerseits

eine hohe Herzleistung bedeuten (starker "Saugeffekt" der Ventrikel), andererseits aber auch

geringes
Volumenangebot (z.B. bei aufrechter Körperlage oder Hypovolämie, also
niedrigem Blutvolumen, z.B. bei Dehydration oder
Blutverlust).
Durch Beobachtung der Halsvenen kann der Betrag des Zentralvenendrucks grob
abgeschätzt werden: Bei Aufrichten des Oberkörpers auf ~45° sollten die
Jugularvenen kollabiert sein ( s.
dort); bleiben sie gefüllt, ist der
Zentralvenendruck erhöht. Auch der Kollaps der Venen am Handrücken bei
Anheben der Hand über Herzniveau (
s.
dort); bleiben sie gefüllt, ist der
Zentralvenendruck erhöht. Auch der Kollaps der Venen am Handrücken bei
Anheben der Hand über Herzniveau ( Abbildung unten) kann diagnostisch beurteilt werden.
Abbildung unten) kann diagnostisch beurteilt werden.
Für das linke Herz gilt Analoges, der Eingangsdruck wird klinisch als  PCWP = Pulmonary capillary wedge(d) pressure am Ausgang des Pulmonalkreislaufs ermittelt.
PCWP = Pulmonary capillary wedge(d) pressure am Ausgang des Pulmonalkreislaufs ermittelt.
Orthostase
Orthostase bedeutet aufrechte Körperhaltung (Stehen). Wechselt eine Person von Rückenlage (supine position)
zu aufrechter Körperposition (standing) - etwa beim morgendlichen Aufstehen -,
kommt es zu einer intensiven kardiovaskulären Belastung, da hydrostatische
Effekte zu einer raschen (Sekundenbereich) Umverteilung der Volumen-
und Druckverhältnisse im Kreislauf führen: Nur auf der Höhe der
entsprechenden hydrostatischen Indifferenzpunkte
(HIP) bleiben die jeweiligen Druckwerte unverändert, jeweils darüber
sinken sie ab, darunter steigen sie an - um 1 kPa (7,5 mmHg) je
Dezimeter Höhendifferenz.

 Abbildung: Druckverteilung im Liegen und Stehen
Abbildung: Druckverteilung im Liegen und Stehen
Nach einer Vorlage in Boron / Boulpaep: Concise Medical Physiology, Elsevier 2021
Arterielle
(rot) und venöse Drucke (blau) bei einer Person in Rückenlage (links)
und bei aufrechter Position (rechts). Die Unterschiedlichkeit des
arteriellen (Herzhöhe) und venösen hydrostatischen Indifferenzpunktes (Oberbauchniveau) ist nicht berücksichtigt.
Im Stehen addieren sich zu den systemischen Druckunterschieden
hydrostatische Druckgradienten. Der Betrag des jeweiligen
arterio-venösen Druckgradienten (violett markierte Flächen) ändert sich
nicht (Herzniveau: 93 mmHg, Kopf- und Fußniveau: 85 mmHg in diesem
Beispiel)
 Da die Aortenklappe etwa auf Höhe des arteriellen HIP liegt, bleibt die Nachlast (afterload) des linken Ventrikels beim Aufrichten des Körpers weitgehend unverändert; was passiert mit seiner Vorlast (preload)?
Diese ist durch die Füllung des Lungenkreislaufs bestimmt, und zwischen
diesem und dem (Hohl-)Venensystem liegt das rechte Herz. Für dessen
Füllung ist die Situation im Niederdrucksystem entscheidend. Der venöse
HIP liegt auf der Höhe des Oberbauchs; beim Aufstehen sinkt daher der
venöse Druck auf Herzhöhe (Zentralvenendruck) um etwa 0,5 kPa ab (s. oben), und das rechte Herz ist mit einem plötzlich reduzierten Blutangebot konfrontiert.
Das bedeutet: Das rechte Herz pumpt weniger Blut in die Lunge, die
Füllung des Lungenkreislaufs nimmt innerhalb weniger Sekunden merklich
ab, womit auch die Vorlast für den linken Ventrikel absinkt - bis zu
einem Punkt, an dem kreislauflabile Menschen präkollaptisch werden
können (zumal die Gehirndurchblutung aus hydrostatischen Gründen beim Aufrichten sofort absinkt).
Da die Aortenklappe etwa auf Höhe des arteriellen HIP liegt, bleibt die Nachlast (afterload) des linken Ventrikels beim Aufrichten des Körpers weitgehend unverändert; was passiert mit seiner Vorlast (preload)?
Diese ist durch die Füllung des Lungenkreislaufs bestimmt, und zwischen
diesem und dem (Hohl-)Venensystem liegt das rechte Herz. Für dessen
Füllung ist die Situation im Niederdrucksystem entscheidend. Der venöse
HIP liegt auf der Höhe des Oberbauchs; beim Aufstehen sinkt daher der
venöse Druck auf Herzhöhe (Zentralvenendruck) um etwa 0,5 kPa ab (s. oben), und das rechte Herz ist mit einem plötzlich reduzierten Blutangebot konfrontiert.
Das bedeutet: Das rechte Herz pumpt weniger Blut in die Lunge, die
Füllung des Lungenkreislaufs nimmt innerhalb weniger Sekunden merklich
ab, womit auch die Vorlast für den linken Ventrikel absinkt - bis zu
einem Punkt, an dem kreislauflabile Menschen präkollaptisch werden
können (zumal die Gehirndurchblutung aus hydrostatischen Gründen beim Aufrichten sofort absinkt).

 Abbildung: Hämodynamik in den Beinen bei aufrechter Körperhaltung
Nach einer Vorlage bei Mohrman DE / Heller LJ, Cardiovascular Physiology, 8th ed. McGraw Hill 2014
Abbildung: Hämodynamik in den Beinen bei aufrechter Körperhaltung
Nach einer Vorlage bei Mohrman DE / Heller LJ, Cardiovascular Physiology, 8th ed. McGraw Hill 2014
Im Stehen nimmt die Füllung der Venen zu, weil Blut aus dem arteriellen Kompartment nachfließt und die Venenwände dehnt (links).
Der hohe Kapillardruck auf Fußniveau führt zu Filtration in das Gewebe ("Knöchelödem", grüner Pfeil).
Bei Steigerung der Sympathikusaktivität kontrahieren sich die
Widerstandsgefäße, der Filtrationsdruck nimmt etwas ab, ohne
wesentlichen Einfluss auf Druck und Füllung in den Venen.
Muskelkontraktionen wirken sich intensiv auf Füllung und Drucke im
gesamten Gefäßsystem aus - sie nehmen ab, die Filtration sistiert.
Beendet man die Muskeltätigkeit, gleichen sich Füllungs- und Druckwerte allmählich den Ruhe-Stehwerten wieder an (rechts)

Die Muskelpumpe in den Beinen reduziert den Venendruck bei aufrechter Fortbewegung (z.B. im Gehen) von ~10-12 kPa (ruhiges Stehen ohne Muskelaktivität) auf ~3-4
kPa (der arteriovenöse Druckgradient steigt dadurch um mehr als 50%).
Außerdem sinkt der kapilläre Filtrationsdruck ganz wesentlich ab, was
die Entstehung (physiologischer) Knöchelödeme zu verhindern hilft.
Bei ruhigem Stehen beträgt der
venöse Druck im Unterschenkelbereich (je nach Körperlänge) ~70 mmHg (Fußrücken bis >90
mmHg), der arterielle Druck ist um ~100 mmHg höher
Auch im Liegen besteht ein Druckgradient von Fußvenen zum Herzen (venöser Rückstrom!)
|
Der
Rückstrom zum Herzen nimmt vorübergehend ab, wenn vermehrt
Blut in der Peripherie gespeichert wird - bis sich ein neues
Gleichgewicht einstellt. Dabei wird primär der Blutdruck so geregelt,
dass er im Normalbereich bleibt (Kreislaufreflexe).
Orthostatische  Belastung:
Richtet sich eine Person aus der liegenden Position auf und bleibt in
aufrechter Körperlage ruhig stehen, dann füllen sich die Venengeflechte
in den Beinen (von der arteriellen Seite her) mit zusätzlich Blut -
etwa 600-700 ml, die Hälfte davon innerhalb von 20-30 Sekunden. Ursache
ist der hydrostatische Druckgradient
im Stehen. Das bedeutet eine Reduktion des venösen Rückstroms zum
Herzen; Zentralvenendruck und Herzminutenvolumen nehmen deutlich ab (das Herzzeitvolumen von ~7,5 auf ~5 l/min, also etwa um ein Drittel).
Belastung:
Richtet sich eine Person aus der liegenden Position auf und bleibt in
aufrechter Körperlage ruhig stehen, dann füllen sich die Venengeflechte
in den Beinen (von der arteriellen Seite her) mit zusätzlich Blut -
etwa 600-700 ml, die Hälfte davon innerhalb von 20-30 Sekunden. Ursache
ist der hydrostatische Druckgradient
im Stehen. Das bedeutet eine Reduktion des venösen Rückstroms zum
Herzen; Zentralvenendruck und Herzminutenvolumen nehmen deutlich ab (das Herzzeitvolumen von ~7,5 auf ~5 l/min, also etwa um ein Drittel).
Innerhalb von 30-60 Sekunden sind die Venen in den Beinen - bedingt
durch den kontinuierlichen arteriellen Zustarom - so stark gefüllt,
dass die Venenklappen wieder geöffnet werden und eine kontinuierliche
(hydrostatisch offene) Blutsäule von den Füßen bis zum Herzen entsteht.
Nun ist der venösen Druck in den Venen im Fussbereich von ~10 auf ~90
mmHg angestiegen. Zwar ist zu Beginn der aufrechten Position kein Blut
retrograd in die Beine "gesackt" (intakte Venenklappen verhindern das),
aber das Blut findet rasch über die Arterien in das zusehends gefüllte
Venensystem der Beine.
Damit der Blutdruck dennoch stabil bleibt, müssen
Kompensationsmechanismen aktiviert werden: Erhöhter peripherer
Widerstand, gesteigerte Herzfrequenz (erhöhter Sympathikustonus). In
der Muskulatur und in der Haut wirkt darüber hinaus ein lokaler
Regulationsmechanismus: Dehnung der Venenwand bewirkt eine Kontraktion
der vorgeschalteten Widerstandsgefäße (Venoarteriolar response VAR,
auch Henriksen-Reflex genannt). Es wird geschätzt, dass die systemische
arterioläre Widerstandserhöhung bei Orthostase bis zu ~45% auf Effekte
des VAR zurückzuführen ist.
Funktioniert all das nicht ausreichend, sinkt die Hirndurchblutung so stark
ab (zerebrale Minderdurchblutung), dass Übelkeit, Symptome der
Verwirrtheit, schließlich Bewusstlosigkeit auftreten (Synkope  ). Der
Muskeltonus lässt nach, die betroffene Person sinkt ohnmächtig zusammen
(orthostatischer Kollaps). Die Synkope ist selbstlimitierend,
denn der Kollaps
). Der
Muskeltonus lässt nach, die betroffene Person sinkt ohnmächtig zusammen
(orthostatischer Kollaps). Die Synkope ist selbstlimitierend,
denn der Kollaps  löst das Problem: Die hydrostatische Belastung
verschwindet - Herzleistung, Blutdruck und Hirndurchblutung steigen an,
die Person erlangt rasch wieder das Bewusstsein.
löst das Problem: Die hydrostatische Belastung
verschwindet - Herzleistung, Blutdruck und Hirndurchblutung steigen an,
die Person erlangt rasch wieder das Bewusstsein.
 Venengeflechte mit dem größten physiologischen Speichervermögen (Volumencompliance:
Volumen bezogen auf den Füllungsdruck) befinden sich im Abdominalraum
(Splanchnikusgebiet) und in der Haut. Das Splanchnikusgebiet ist besonders postprandial gut
durchblutet (Verdauungsvorgänge); die Haut wiederum steht im Dienste der Thermoregulation
(Kühlung). Beide sind vom Sympathikus gesteuert: Hoher Sympathikustonus
führt zu Vasokonstriktion und senkt die Durchblutung, niedriger
Sympathikustonus erlaubt Vasodilatation (blutdruckpassiv) und läßt stärkere
Perfusion zu.
Venengeflechte mit dem größten physiologischen Speichervermögen (Volumencompliance:
Volumen bezogen auf den Füllungsdruck) befinden sich im Abdominalraum
(Splanchnikusgebiet) und in der Haut. Das Splanchnikusgebiet ist besonders postprandial gut
durchblutet (Verdauungsvorgänge); die Haut wiederum steht im Dienste der Thermoregulation
(Kühlung). Beide sind vom Sympathikus gesteuert: Hoher Sympathikustonus
führt zu Vasokonstriktion und senkt die Durchblutung, niedriger
Sympathikustonus erlaubt Vasodilatation (blutdruckpassiv) und läßt stärkere
Perfusion zu.
Ändert sich die Gesamtdurchblutung im Körper (verändertes Herzzeitvolumen), stellen
sich Widerstands- und Compliancewerte so ein, dass ein stabiler
Blutdruck resultiert. Der arterielle Blutdruck ist die primäre Regelgröße im Kreislauf.
Wasserimmersion
Eintauchen des Körpers in Wasser (Wasserimmersion)
verlagert ~700 ml Blut aus der Peripherie (Beine, Baucheingeweide) in
den Thorax, weitet das diastolische Herz um ~180 ml und erhöht den
arteriellen Blutdruck um ~10 mmHg. Das erklärt sich aus der
hydrostatischen Situation: Steht man z.B. bis zum Oberbauch in Wasser,
existiert nicht nur in den Venen, sondern auch außerhalb des Körpers
ein hydrostatisches Druckprofil - es komprimiert die Venen von außen,
und zwar umso stärker, je weiter unten sich die betrachtete Stelle
befindet.
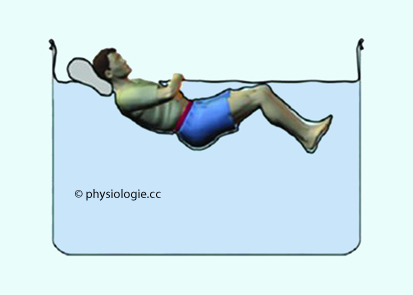
 Abbildung: Wasserimmersion
Nach Kermorgant M et al, Impacts of Simulated
Weightlessness by Dry Immersion on Optic Nerve Sheath Diameter and
Cerebral Autoregulation. Front Physiol 2017; 8: 780
Abbildung: Wasserimmersion
Nach Kermorgant M et al, Impacts of Simulated
Weightlessness by Dry Immersion on Optic Nerve Sheath Diameter and
Cerebral Autoregulation. Front Physiol 2017; 8: 780
Der Proband liegt in einer trockenen
"Tasche", die sich bildet, wenn er sich auf die auf dem Wasser liegende
(wasserdichte) Plane legt. So vermeidet man eine Aufweichung der Haut
bei längerer Immersion.
Die Indifferenztemperatur
(Temperatur, bei der der Körper weder auskühlt noch erhitzt wird) in
Wasser liegt beim Menschen bei 35 bis höchstens 36°C (abhängig von
Bewegung, Wasserströmung, Ausgangstemperatur des Körpers). Liegt die
Wassertemperatur niedriger, kühlt der Körper entsprechend rasch ab (der
konvektive Wärmetransfer ist in Wasser ~100-fach größer als in Luft)

Das kompensiert den Druckgradienten im Körper, die Venen
bleiben im wesentlichen gleich stark gefüllt. Taucht man bis zum Hals
in Wasser ein, dreht sich die Situation insoferne um, als der stärkere
Außendruck nunmehr überall die Venen komprimiert, deren Füllung nimmt
generell ab und das Herz wird stärker gedehnt.
Das führt wiederum über den
Frank-Starling-Mechanismus zu einer starken Blutfüllung der Lunge, was
sich bei der Atmung bemerkbar macht.
Das Reizmuster führt zu renaler Vasodilatation durch selektive Hemmung der sympathischen Aktivität in der Niere; weiters verminderte Vasopressinausschüttung und reduzierte Aktivität des RAAS; sowie erhöhte Ausschüttung natriuretischer Peptide und damit Salz- und Wasserausscheidung.
In längerer Schwerelosigkeit
ergibt sich eine ähnliche Umverteilung des Blutvolumens mit Natriurese
/ Diurese, Volumenverlust und Hypovolämie; zusammen mit einem
Nachlassen der reflektorischen Steuerungsstärke (innerhalb weniger
Tage: Auch bei Bettlägrigkeit zu beobachten) kommt es zu
"Dekonditioníerung" (Astronautensyndrom) - bei der Rückkehr zur Erde
zeigen sich ausgeprägte Probleme mit der Orthostase (Kollapsneigung).
Muskelpumpe
Die Durchblutung steigt besonders stark (bis ≥20-fach) in der Muskulatur bei körperlicher Arbeit;
die Venen der Muskulatur verfügen über Venenklappen, werden
durch den “Massageeffekt” der Muskeltätigkeit herzwärts entleert
(Muskelpumpe)
und speichern daher trotz erhöhter Perfusion wenig zusätzliches Blut.
 Dieser
Mechanismus der "Muskelpumpe" kann bis zu 50% der gesamten Energie für
den Transport des Blutes durch den Kreislauf ausmachen, unterstützt
also insbesondere bei körperlicher Belastung ganz wesentlich die
Fördertätigkeit des Herzens.
Dieser
Mechanismus der "Muskelpumpe" kann bis zu 50% der gesamten Energie für
den Transport des Blutes durch den Kreislauf ausmachen, unterstützt
also insbesondere bei körperlicher Belastung ganz wesentlich die
Fördertätigkeit des Herzens.
 Abbildung: Funktionsweise der "Muskelpumpe"
Abbildung: Funktionsweise der "Muskelpumpe"
Modifiziert nach einer Vorlage in Boron / Boulpaep, Medical Physiology, 1st ed. Saunders 2003
Kontrahiert
sich der Muskel, steigt der Druck im umschlossenen Venensegment und die
proximale (obere) Klappe öffnet, die distale (untere) schließt
druckpassiv. Blut wandert nach oben. Entspannt sich der Muskel wieder,
öffnet die untere Klappe und läßt weiter Blut einströmen.
Der
Venendruck kann bei ruhigem Stehen - hydrostatisch bedingt - bis auf ~100 mm Hg ansteigen

Der mechanische Ablauf
dieses zyklischen Vorgangs, der das abwechselnde Schließen und Öffnen
distaler und proximaler Klappen (und das Entleeren der zwischen ihnen
gelegenen Venensegmente) einschließt, ist im rechten Teil der der Abbildung
gezeigt.
Venenklappen finden sich überall in der Peripherie - außer in den Hohlvenen
(venae cavae), hier kann das Blut frei kopf- oder fußwärts strömen, - die
Druckverhältnisse liegen allerdings in der Regel so, dass sich das
Blut von peripher nach zentral (herzwärts) bewegt.
Die Folge ist, dass z.B. bei körperlicher Arbeit die zum Herzen
aufsteigende Blutmenge zunimmt (der venöse Bluttransport wird durch die
Muskelkontraktionen intensiviert), der Zerntralvenendruck ansteigt und damit das Schlagvolumen (Frank-Starling-Mechanismus).
 Zum venösen Rückstrom s. auch dort
Zum venösen Rückstrom s. auch dort
Eine Ausnahme kann kurzzeitig bei starkem Pressen bestehen (Valsalva-Versuch). Auch Husten
wirkt sich auf den Kreislauf aus: Bei einem Hustenstoß tritt im
Brustraum ein Überdruck bis zu 400 mmHg auf (mehr als eine halbe
Atmosphäre, oder 50 kPa). In solchen kurzen Phasen extrem hohen
intrathorakalen Drucks strömt das Blut in der unteren Hohlvene
abdominalwärts, also vom rechten Vorhof weg - die ventrikuläre Füllung
sinkt und damit die Auswurfleistung des Herzens (mögliche Synkope bei
längerem Pressen). Ähnliches gilt für respiratorische Zyklen:
Zusätzlich zur Muskelpumpe ist weiters der Einfluss der Atmung zu berücksichtigen ("Atempumpe"):
Im ausgeatmeten Zustand beträgt der intrathorakale Druck ca. -0,5 kPa,
im eingeatmeten -1,0 kPa (bei tiefer Inspiration ist der Druckabfall
intensiver). Dadurch fließt vermehrt Blut herzwärts ( Abbildung),
Zentralvenendruck, enddiastolisches Volumen und Schlagvolumen des
rechten Ventrikels nehmen zu.
Abbildung),
Zentralvenendruck, enddiastolisches Volumen und Schlagvolumen des
rechten Ventrikels nehmen zu.

 Abbildung: Atempumpe
Nach einer Vorlage bei http://humanphysiology.academy
Abbildung: Atempumpe
Nach einer Vorlage bei http://humanphysiology.academy
Einatmung (unteres Bild) erhöht das intrathorakale Volumen, der
Donders'sche Druck sinkt - etwa von -0,5 auf -1,0 kPa (also um ~4
mmHg); Gleichzeitig steigt der Druck im Bauchraum (die Zwerchfellkuppel
rückt abdominalwärts). Blut strömt vermehrt durch die untere Hohlvene
zum Herzen (Pfeil nach links)

 Inspiration intensiviert den Unterdruck im Donders'schen Raum
(Zwerchfellkuppel senkt sich, Interkostalmuskeln erweitern den
Brustkorb), das erhöht das Druckgefälle von der Peripherie
(systemischer Druck) zum Herzen (zentralvenöser Druck), und die
Blutströmung zum rechten Vorhof nimmt zu.
Inspiration intensiviert den Unterdruck im Donders'schen Raum
(Zwerchfellkuppel senkt sich, Interkostalmuskeln erweitern den
Brustkorb), das erhöht das Druckgefälle von der Peripherie
(systemischer Druck) zum Herzen (zentralvenöser Druck), und die
Blutströmung zum rechten Vorhof nimmt zu.
Der Beginn einer tiefen Inspiration senkt den Druck in der oberen Hohlvene, der venöse Rückstrom zum Herzen wird unterstützt
|
 Umgekehrt nimmt der Druck im Brustraum bei Ausatmung zu, der venöse
Druckgradient zum Herzen wird geringer und der venöse Rückstrom lässt
nach. Venenklappen (außer im V. cava-Bereich) verhindern einen retrograden Blutfluss.
Umgekehrt nimmt der Druck im Brustraum bei Ausatmung zu, der venöse
Druckgradient zum Herzen wird geringer und der venöse Rückstrom lässt
nach. Venenklappen (außer im V. cava-Bereich) verhindern einen retrograden Blutfluss.
Obwohl das rechtsventrikuläre Schlagvolumen bei Inspiration zunimmt,
sinkt das Schlagvolumen des linken Ventrikels gleichzeitig ab. Grund
ist die Tatsache, dass der Sogeffekt der Einatmung den pulmonalen
Blutpool vergrößert; der Druck in den Lungenvenen sinkt ab, und damit
auch das enddiastolische
Volumen und Schlagvolumen des linken Ventrikels. Die Auswurfleistung
des rechten und linken Ventrikels ändern sich mit der Atmung
gegenläufig:
|
Inspiration
|
Exspiration
|
Schlagvolumen rechter Ventrikel
|
↑
|
↓
|
Schlagvolumen linker Ventrikel
|
↓
|
↑
|
Die Reduktion des linksventrikulären
Schlagvolumens bei der Einatmung wird zum Teil durch respiratorische
Sinusarrhythmie kompensiert, die ja eine inspiratorische Beschleunigung
der Herzaktion bewirkt; insgesamt nimmt das cardiac output während der Einatmung ab, während der Ausatmung zu. Die Folge sind entsprechende Oszillationen des arteriellen Blutdrucks: Leicht erhöht exspiratorisch, leicht erniedrigt inspiratorisch.
Beobachtet man die Jugularvene bei einer Person in partieller Rückenlage ( vgl. dort), lässt sich die Jugularvene erkennen, deren Füllung mit dem Herzschlag oszilliert (Venenpuls,
vgl. dort), lässt sich die Jugularvene erkennen, deren Füllung mit dem Herzschlag oszilliert (Venenpuls,  s. dort):
Der Kollapspunkt (die Stelle, an welcher der transmurale Druck Null beträgt) trennt eine kopfwärts gelegene blutleere (Vene nicht
sichtbar) von einer kaudalen blutgefüllten Zone der Halsvene, und
wandert entsprechend dem Herzzyklus deutlich hin und her. Die
Druckschwankungen sind deutlich sichtbar, aber zu schwach, um palpiert
werden zu können (was man deutlich spüren kann, ist der Carotispuls).
s. dort):
Der Kollapspunkt (die Stelle, an welcher der transmurale Druck Null beträgt) trennt eine kopfwärts gelegene blutleere (Vene nicht
sichtbar) von einer kaudalen blutgefüllten Zone der Halsvene, und
wandert entsprechend dem Herzzyklus deutlich hin und her. Die
Druckschwankungen sind deutlich sichtbar, aber zu schwach, um palpiert
werden zu können (was man deutlich spüren kann, ist der Carotispuls).
Druck auf die Leber einer Person in
partieller Rückenlage befördert ausreichend venöses Blut in den
zentralen Venenbereich, um den Kollapspunkt der Jugularis nach
kopfwärts rücken zu lassen (hepato-jugularer Reflux).
Der Druck in der unteren Hohlvene schwankt im Ruhezustand zwischen ~0 und ~1 kPa, die Strömungsgeschwindigkeit des Blutes zwischen ~0 und ~20
cm/s ( Abbildung). Zwischen dem rechten Vorhof und der v. jugularis
liegen keine Venenklappen, diese Strecke bildet eine hydrostatisch
offene Strecke (bis zum Kollapspunkt).
Abbildung). Zwischen dem rechten Vorhof und der v. jugularis
liegen keine Venenklappen, diese Strecke bildet eine hydrostatisch
offene Strecke (bis zum Kollapspunkt).
Inspiration vergrößert den treibenden Druck für den Rückstrom des venösen Blutes
zum rechten Herzen beträchtlich (das kontrahierende Zwerchfell flacht
sich ab und drückt gegen den Bauchraum - hier steigt der Druck an, im
Brustraum sinkt er ab;  Abbildung).
Abbildung).
Richtet man sich
aus liegender Stellung auf, dann sinken die Druckwerte in Arterien und
Venen der oberen Körperregionen, während sie sich fußwärts erhöhen
(hydrostatische Druckschichtung); pro Meter Höhendifferenz beträgt der Druckunterschied 10 kPa (75 mm Hg). An der Stelle der hydrostatischen Indifferenz
bleiben die Druckwerte unverändert.
Für den
Wechsel vom Liegen zum Stehen befindet sich der arterielle
Indifferenzpunkt in Herzhöhe (kardiale Nachlast bei Lagewechsel
unverändert), der venöse in
Oberbauchhöhe (kardiale Vorlast sinkt beim Aufrichten des Körpers).
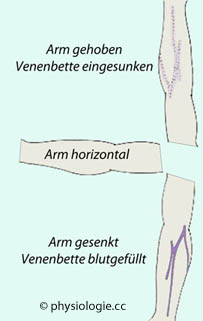
 Abbildung: Venenfüllung in Anhängigkeit von der Armlage (d.h. dem hydrostatischen Füllungsdruck)
Abbildung: Venenfüllung in Anhängigkeit von der Armlage (d.h. dem hydrostatischen Füllungsdruck)
Nach einer Vorlage bei Vick RL, Contemporary medical physiology, Addison-Wesley 1984
Sobald der
transmurale Druck negative Werte erreicht, kollabiert die Vene ("Venenbette eingesunken")

In der Praxis
der Blutdruckmessung wird meist wenig darauf geachtet, wo sich das
hydrostatische Indifferenzniveau des Arteriensystems befindet: Die
Manschette am Oberarm liegt automatisch etwa in Herzhöhe. Misst man
allerdings z.B. an Beinen oder Fingern, hängt der Druck sehr stark von
der Lage der Messstelle ab.
 Für
eine valide Blutdruckmessung ist es daher notwendig, die Messstelle auf
Herzhöhe zu positionieren, um hydrostatische Zusatzeffekte auf den
gemessenen Blutdruck zu vermeiden.
Für
eine valide Blutdruckmessung ist es daher notwendig, die Messstelle auf
Herzhöhe zu positionieren, um hydrostatische Zusatzeffekte auf den
gemessenen Blutdruck zu vermeiden.
Streckt
eine Person den Arm nach oben, sinken die hydrostatischen Drucke
entsprechend - die Venen kollabieren, der arterielle Druck im Bereich
der Hand sinkt auf ca. 30-50 mmHg
|
Ein orthostatischer Kollaps (auch: vaso-vagale Synkope)
tritt auf, wenn die Gehirndurchblutung bei aufrechter Körperlage auf
unter ~50% des Normalwertes absinkt. Dies ist meist durch ungenügendes
Blutangebot aus dem Venensystem und insuffizientes preload
des Herzens bedingt (die Kurve des venösen Rückstroms - blau in der
Abbildung oben - sinkt auf Werte, die als Herzminutenvolumen nicht
ausreichen, den arteriellen Blutdruck zu stabilisieren).
Eingeschränkte Wirkung der Muskelpumpe - bedingt durch defekte Venenklappen, Beinvenenthrombose etc. - kann zu chronisch-venöser Insuffizienz
führen. Der behinderte Rückfluss von Blut (venöse Abflussstörung)
steigert den Venendruck, behindert die Mikrozirkulation und bedingt
schließlich Varizenbildung. Die Symptome reichen von
bläulich-prominenten Venen (Stadium I) über bleibende Ödeme und
Pigmentierung der Haut (Stadium II) bis zur Geschwürbildung (Stadium
III).


 Herz und Blutgefäße sind hydromechanisch zum kardiovaskulären System zusammengeschlossen. In "Arbeitspunkten" (venös, arteriell) überschneiden sich ihre Druck-Volumen-Kurven (Guyton's cross plot).
Der
venöse Rückstrom ergibt sich aus der Differenz zwischen dem peripheren
"Systemdruck" (etwa im Bereich der Venolen) und dem diastolischen Druck
im rechten Herzen und bestimmt dessen Pumpleistung (Vorlast und Frank-Starling-Mechanimus).
Hypervolämie rückt den Arbeitspunkt zu erhöhtem Zentralvenendruck und
Herzminutenvolumen, bei Herzschwäche ist die Leistungskurve des Herzens
zu niedrigeren Förderleistungen verlagert Herz und Blutgefäße sind hydromechanisch zum kardiovaskulären System zusammengeschlossen. In "Arbeitspunkten" (venös, arteriell) überschneiden sich ihre Druck-Volumen-Kurven (Guyton's cross plot).
Der
venöse Rückstrom ergibt sich aus der Differenz zwischen dem peripheren
"Systemdruck" (etwa im Bereich der Venolen) und dem diastolischen Druck
im rechten Herzen und bestimmt dessen Pumpleistung (Vorlast und Frank-Starling-Mechanimus).
Hypervolämie rückt den Arbeitspunkt zu erhöhtem Zentralvenendruck und
Herzminutenvolumen, bei Herzschwäche ist die Leistungskurve des Herzens
zu niedrigeren Förderleistungen verlagert
 In unten
gelegenen Körperregionen sind die Venen umso stärker gefüllt, je weiter
sie vom venösen hydrostatischen Indifferenzpunkt (Oberbauchbereich) entfernt sind (jeweils ~1 kPa pro 0,1 m Höhenunterschied). Am besten dehnbar (das ~50-fache der arteriellen Compliance) sind Venen bei einem gering positiven transmuralen Druck (~4 mmHg oder ~0,5 kPa). Ab ~2 kPa
nehmen sie eine kreisrunde Form an und versteifen, die
Volumen-Druck-Kurve wird steiler - weitere Füllung wird verhindert, der
Mechanismus der Muskelpumpe unterstützt. Zusätzlich sind Venen
kontraktil: In Leber, Gastrointestinaltrakt, Nieren, Haut wirken
zahlreiche adrenerge Nervenfasern stark vasokonstriktorisch. Das erhöht den
Innendruck, treibt Blut zum Herzen, insbesondere in Stresssituationen In unten
gelegenen Körperregionen sind die Venen umso stärker gefüllt, je weiter
sie vom venösen hydrostatischen Indifferenzpunkt (Oberbauchbereich) entfernt sind (jeweils ~1 kPa pro 0,1 m Höhenunterschied). Am besten dehnbar (das ~50-fache der arteriellen Compliance) sind Venen bei einem gering positiven transmuralen Druck (~4 mmHg oder ~0,5 kPa). Ab ~2 kPa
nehmen sie eine kreisrunde Form an und versteifen, die
Volumen-Druck-Kurve wird steiler - weitere Füllung wird verhindert, der
Mechanismus der Muskelpumpe unterstützt. Zusätzlich sind Venen
kontraktil: In Leber, Gastrointestinaltrakt, Nieren, Haut wirken
zahlreiche adrenerge Nervenfasern stark vasokonstriktorisch. Das erhöht den
Innendruck, treibt Blut zum Herzen, insbesondere in Stresssituationen
 Neben dem
Gefäßtonus hängt die Füllung von Venen vom arteriellen Zustrom ab.
Öffnen die Widerstandsgefäße (arterioläre Vasodilatation), strömt mehr
Blut in Venen und wird dort vermehrt gespeichert (dynamischer Zwischenspeicher: kinetische wird zu
potentieller Energie), dies senkt den Rückstrom zum Herzen - die Vorlast des rechten Herzens nimmt ab (DeJager-Krogh- Mechanismus).
Arterioläre Vasokonstriktion wirkt umgekehrt, die Venen entspeichern
(potentielle wird zu kinetischer Energie) und erhöhen das
Herzminutenvolumen (insbesondere in kritischen Kreislaufsituationen) Neben dem
Gefäßtonus hängt die Füllung von Venen vom arteriellen Zustrom ab.
Öffnen die Widerstandsgefäße (arterioläre Vasodilatation), strömt mehr
Blut in Venen und wird dort vermehrt gespeichert (dynamischer Zwischenspeicher: kinetische wird zu
potentieller Energie), dies senkt den Rückstrom zum Herzen - die Vorlast des rechten Herzens nimmt ab (DeJager-Krogh- Mechanismus).
Arterioläre Vasokonstriktion wirkt umgekehrt, die Venen entspeichern
(potentielle wird zu kinetischer Energie) und erhöhen das
Herzminutenvolumen (insbesondere in kritischen Kreislaufsituationen)
 Die
meisten Venen haben ohne sympathischen Einfluss nur einen geringen
basalen Tonus und reagieren auf Dehnung kaum mit Kontraktion. Die Venengeflechte der Haut (Thermoregulation!) und der Baucheingeweide
(“Splanchnikusgebiet”) sind besonders gut dehnbar (Splanchnikusgebiet:
1/5 des Blutvolumens) und haben zahlreiche α-Adrenozeptoren. Venen im Splanchnikusgebiet reagieren auf klassische Kreislaufreflexe (z.B. Barorezeptorreflex) und
können in Stresssituationen (erhöhter Sympathikustonus) einen Teil des
Blutes zum Herzen verschieben, was den Kreislauf stabilisiert. Venengeflechte der Skelettmuskulatur sind ebenfalls gut dehnbar, aber kaum sympathisch versorgt: Sie werden
bei Muskelaktivität durch die "Muskelpumpe" automatisch geleert
(Venenklappen). Der Venentonus in den Beinen nimmt bei aufrechter
Körperlage reflektorisch zu, um die Speicherung von Blut in der unteren
Körperhälfte zu minimieren Die
meisten Venen haben ohne sympathischen Einfluss nur einen geringen
basalen Tonus und reagieren auf Dehnung kaum mit Kontraktion. Die Venengeflechte der Haut (Thermoregulation!) und der Baucheingeweide
(“Splanchnikusgebiet”) sind besonders gut dehnbar (Splanchnikusgebiet:
1/5 des Blutvolumens) und haben zahlreiche α-Adrenozeptoren. Venen im Splanchnikusgebiet reagieren auf klassische Kreislaufreflexe (z.B. Barorezeptorreflex) und
können in Stresssituationen (erhöhter Sympathikustonus) einen Teil des
Blutes zum Herzen verschieben, was den Kreislauf stabilisiert. Venengeflechte der Skelettmuskulatur sind ebenfalls gut dehnbar, aber kaum sympathisch versorgt: Sie werden
bei Muskelaktivität durch die "Muskelpumpe" automatisch geleert
(Venenklappen). Der Venentonus in den Beinen nimmt bei aufrechter
Körperlage reflektorisch zu, um die Speicherung von Blut in der unteren
Körperhälfte zu minimieren
 Der zentrale
Venendruck (CVP) ist der mittlere Blutdruck im Bereich der herznahen
thorakalen Venen / im rechten Vorhof. Er oszilliert mit Herzschlag und Atmung um einen
Mittelwert, dieser ist ein Maß für die Vorlast des rechten Ventrikels
(sein Betrag entspricht etwa dem barometrischen Druck). Hoher [CVP] kann zweierlei bedeuten: Hohes venöses Volumenangebot (z.B. liegende Position) oder geringe Herzleistung (Herzinsuffizienz); niedriger [CVP] geringes Volumenangebot (z.B. aufrechte Körperlage) oder hohe Herzleistung (Saugeffekt). Bei 45°-Lagerung des Oberkörpers sollten die Jugularvenen kollabiert sein, andernfalls ist der Zentralvenendruck erhöht Der zentrale
Venendruck (CVP) ist der mittlere Blutdruck im Bereich der herznahen
thorakalen Venen / im rechten Vorhof. Er oszilliert mit Herzschlag und Atmung um einen
Mittelwert, dieser ist ein Maß für die Vorlast des rechten Ventrikels
(sein Betrag entspricht etwa dem barometrischen Druck). Hoher [CVP] kann zweierlei bedeuten: Hohes venöses Volumenangebot (z.B. liegende Position) oder geringe Herzleistung (Herzinsuffizienz); niedriger [CVP] geringes Volumenangebot (z.B. aufrechte Körperlage) oder hohe Herzleistung (Saugeffekt). Bei 45°-Lagerung des Oberkörpers sollten die Jugularvenen kollabiert sein, andernfalls ist der Zentralvenendruck erhöht
 Orthostase
bedeutet aufrechte Körperhaltung (Stehen). Aufstehen ist eine
kardiovaskuläre Belastung: Über dem hydrostatischen Indifferenzpunkt sinken die
Druckwerte (1 kPa je dm Höhendifferenz), der Zentralvenendruck um ~0,5
kPa. Das rechte Herz pumpt weniger Blut, die Füllung des
Lungenkreislaufs sinkt, damit auch die
Vorlast für den linken Ventrikel - kreislauflabile Personen können
präkollaptisch werden, zumal die Gehirndurchblutung aus hydrostatischen
Gründen beim Aufrichten absinkt (orthostatischer Kollaps bei Halbierung
der Gehirndurchblutung). In den Beinen steigt der arterielle
Druck auf ~25 kPa, die Venen speichern zusätzliche 600-700 ml Blut, durch die Muskelpumpe im Gehen wird der venöse
Druck von ~10-12 auf ~3-4 kPa
reduziert (was auch die Entstehung von Knöchelödemen zu verhindern
hilft). Dehnung der
Venenwand bewirkt eine Kontraktion der vorgeschalteten
Widerstandsgefäße (Henriksen-Reflex), was fast die Hälfte der systemischen arteriolären Widerstandserhöhung bei Orthostase erklärt Orthostase
bedeutet aufrechte Körperhaltung (Stehen). Aufstehen ist eine
kardiovaskuläre Belastung: Über dem hydrostatischen Indifferenzpunkt sinken die
Druckwerte (1 kPa je dm Höhendifferenz), der Zentralvenendruck um ~0,5
kPa. Das rechte Herz pumpt weniger Blut, die Füllung des
Lungenkreislaufs sinkt, damit auch die
Vorlast für den linken Ventrikel - kreislauflabile Personen können
präkollaptisch werden, zumal die Gehirndurchblutung aus hydrostatischen
Gründen beim Aufrichten absinkt (orthostatischer Kollaps bei Halbierung
der Gehirndurchblutung). In den Beinen steigt der arterielle
Druck auf ~25 kPa, die Venen speichern zusätzliche 600-700 ml Blut, durch die Muskelpumpe im Gehen wird der venöse
Druck von ~10-12 auf ~3-4 kPa
reduziert (was auch die Entstehung von Knöchelödemen zu verhindern
hilft). Dehnung der
Venenwand bewirkt eine Kontraktion der vorgeschalteten
Widerstandsgefäße (Henriksen-Reflex), was fast die Hälfte der systemischen arteriolären Widerstandserhöhung bei Orthostase erklärt
 Wasserimmersion verlagert ~700 ml Blut aus der Peripherie (Beine,
Baucheingeweide) in den Thorax, weitet das diastolische Herz um ~180 ml
und erhöht den arteriellen Blutdruck um 1-2 kPa. Das Herz wird stärker
gefüllt, die Atmung erschwert. Hält dieses Reizmuster an, führt dies
reflektorisch zu renaler Vasodilatation und verminderter Sekretion von
Vasopressin, Angiotensin, Aldosteron, sowie erhöhter Ausschüttung
natriuretischer Peptide (Salz- und Wasserausscheidung). Ähnliche
Effekte resultieren aus Bettlägrigkeit und bedingen Probleme mit der
orthostatischen Regulation (Dekonditionierung, Kollapsneigung)
Wasserimmersion verlagert ~700 ml Blut aus der Peripherie (Beine,
Baucheingeweide) in den Thorax, weitet das diastolische Herz um ~180 ml
und erhöht den arteriellen Blutdruck um 1-2 kPa. Das Herz wird stärker
gefüllt, die Atmung erschwert. Hält dieses Reizmuster an, führt dies
reflektorisch zu renaler Vasodilatation und verminderter Sekretion von
Vasopressin, Angiotensin, Aldosteron, sowie erhöhter Ausschüttung
natriuretischer Peptide (Salz- und Wasserausscheidung). Ähnliche
Effekte resultieren aus Bettlägrigkeit und bedingen Probleme mit der
orthostatischen Regulation (Dekonditionierung, Kollapsneigung)
 Einatmung senkt den intrathorakalen (tiefe Inspiration senkt den Druck in der v. cava superior) und hebt den intraabdominellen Druck, Blut strömt vermehrt durch die untere
Hohlvene zum Herzen, das rechtsventrikuläre Schlagvoluemn nimmt zu
(Frank-Starling). Dennoch
sinkt das Schlagvolumen des linken Ventrikels, weil der Sogeffekt der
Einatmung den pulmonalen Blutpool vergrößert, den Druck in den
Lungenvenen senkt. Die Auswurfleistung des rechten und linken
Ventrikels ändern sich mit der Atmung gegenläufig. Insgesamt nimmt das
Herzminutenvolumen während der Einatmung ab, während der Ausatmung zu.
Die Folge sind Oszillationen des arteriellen Blutdrucks:
Leicht erhöht exspiratorisch, leicht erniedrigt inspiratorisch Einatmung senkt den intrathorakalen (tiefe Inspiration senkt den Druck in der v. cava superior) und hebt den intraabdominellen Druck, Blut strömt vermehrt durch die untere
Hohlvene zum Herzen, das rechtsventrikuläre Schlagvoluemn nimmt zu
(Frank-Starling). Dennoch
sinkt das Schlagvolumen des linken Ventrikels, weil der Sogeffekt der
Einatmung den pulmonalen Blutpool vergrößert, den Druck in den
Lungenvenen senkt. Die Auswurfleistung des rechten und linken
Ventrikels ändern sich mit der Atmung gegenläufig. Insgesamt nimmt das
Herzminutenvolumen während der Einatmung ab, während der Ausatmung zu.
Die Folge sind Oszillationen des arteriellen Blutdrucks:
Leicht erhöht exspiratorisch, leicht erniedrigt inspiratorisch
 Inspiration vergrößert den treibenden Druck für den Rückstrom des venösen Blutes zum rechten Herzen. Der
Druck in der v. cava inferior schwankt im Ruhezustand zwischen ~0 und
~1 kPa, die Strömungsgeschwindigkeit des Blutes zwischen ~0 und ~20
cm/s (Venenpuls). a: Druckansteg bei der
beginnenden Vorhofkontraktion; c: Vorwölben der geschlossenen AV-Klappe
während der Anspannungszeit; x: Verschiebung der
Ventilebene zur Herzspitze ("Sogeffekt" auf den Vorhof); v, y:
Abschluss des Ventilebenenmechanismus (AV-Klappe) Inspiration vergrößert den treibenden Druck für den Rückstrom des venösen Blutes zum rechten Herzen. Der
Druck in der v. cava inferior schwankt im Ruhezustand zwischen ~0 und
~1 kPa, die Strömungsgeschwindigkeit des Blutes zwischen ~0 und ~20
cm/s (Venenpuls). a: Druckansteg bei der
beginnenden Vorhofkontraktion; c: Vorwölben der geschlossenen AV-Klappe
während der Anspannungszeit; x: Verschiebung der
Ventilebene zur Herzspitze ("Sogeffekt" auf den Vorhof); v, y:
Abschluss des Ventilebenenmechanismus (AV-Klappe)
|

 Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.
Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.





 Venensystem
Venensystem
 DeJager-Krogh-Effekt: S. DeJager, August Krogh
DeJager-Krogh-Effekt: S. DeJager, August Krogh Verteilung des Blutvolumens
Verteilung des Blutvolumens  Dynamische Speicherung
Dynamische Speicherung  DeJager-Krogh- Mechanismus
DeJager-Krogh- Mechanismus  Steuerung venöser Speicherung
Steuerung venöser Speicherung  Vorlast für rechtes und linkes Herz: Zentraler Venendruck, PCWP
Vorlast für rechtes und linkes Herz: Zentraler Venendruck, PCWP  Orthostase
Orthostase  Wasserimmersion
Wasserimmersion  Muskelpumpe
Muskelpumpe  Atempumpe, Venenpuls
Atempumpe, Venenpuls  Hydrostatik, Orthostase
Hydrostatik, Orthostase Systemischer Blutdruck
Systemischer Blutdruck
 Core messages
Core messages
 Abbildung: Verteilung des Blutvolumens
Abbildung: Verteilung des Blutvolumens
 Abbildung), die Elastizitätsverhältnisse der betreffenden Gefäße
(Compliance).
Abbildung), die Elastizitätsverhältnisse der betreffenden Gefäße
(Compliance). 
 Abbildung: Strömungsrate und Druckwerte vor und hinter der Pumpe
Abbildung: Strömungsrate und Druckwerte vor und hinter der Pumpe Als mittleren systemischen (statischen) Blutdruck (mean systemic filling pressure
MSFP, mean circulatory pressure MCP) bezeichnet man den Druck, der sich (abgesehen von hydrostatischen
Unterschieden) in allen Gefäßen nach einem kompletten Herzstillstand
(und bevor sekundäre Filtrationseffekte auftreten) einstellen würde.
(Eine kurze Zeitspanne nach dem "Shutdown" würde noch Blut von Arterien
in Kapillaren und Venen fabließen, bis sich die Drucke komplett
ausgeglichen haben und die Strömung den Wert 0 annimmt.)
Als mittleren systemischen (statischen) Blutdruck (mean systemic filling pressure
MSFP, mean circulatory pressure MCP) bezeichnet man den Druck, der sich (abgesehen von hydrostatischen
Unterschieden) in allen Gefäßen nach einem kompletten Herzstillstand
(und bevor sekundäre Filtrationseffekte auftreten) einstellen würde.
(Eine kurze Zeitspanne nach dem "Shutdown" würde noch Blut von Arterien
in Kapillaren und Venen fabließen, bis sich die Drucke komplett
ausgeglichen haben und die Strömung den Wert 0 annimmt.) entwickelten Projektion der Eigenschaften des Gefäßsystems einerseits,
des aktiven Herzens andererseits in eine Strömungs-Druck-Grafik kann
die Interaktion der beiden anschaulich dargestellt werden (Guyton's cross plot):
entwickelten Projektion der Eigenschaften des Gefäßsystems einerseits,
des aktiven Herzens andererseits in eine Strömungs-Druck-Grafik kann
die Interaktion der beiden anschaulich dargestellt werden (Guyton's cross plot):
 Abbildung: Venöser Rückstrom gleich Herzzeitvolumen
Abbildung: Venöser Rückstrom gleich Herzzeitvolumen
 Abbildung zeigt, wie Veränderungen des Blutvolumens
einerseits, des Zustandes des Herzmuskels andererseits diesen
Schnittpunkt verlagern: Die grünen
Kurven zeigen den Normalzustand - "normal" = Starlingkurve,
"Normovolämie" = venöse Rückstromkurve, vascular function curve -, der Kurvenschnittpunkt liegt
bei einem Herzzeitvolumen von 5 l/min und einem Zentralvenendruck (Maß für die Vorlast des rechten Ventrikels) von etwa 2 mmHg.
Abbildung zeigt, wie Veränderungen des Blutvolumens
einerseits, des Zustandes des Herzmuskels andererseits diesen
Schnittpunkt verlagern: Die grünen
Kurven zeigen den Normalzustand - "normal" = Starlingkurve,
"Normovolämie" = venöse Rückstromkurve, vascular function curve -, der Kurvenschnittpunkt liegt
bei einem Herzzeitvolumen von 5 l/min und einem Zentralvenendruck (Maß für die Vorlast des rechten Ventrikels) von etwa 2 mmHg.


 Funktionell ausschlaggebend ist nicht das Blutvolumen als solches (wie es durch eine Indikatorverdünnungsmethode bestimmbar ist), sondern das effektive Blutvolumen (effective circulating volume -
Funktionell ausschlaggebend ist nicht das Blutvolumen als solches (wie es durch eine Indikatorverdünnungsmethode bestimmbar ist), sondern das effektive Blutvolumen (effective circulating volume -  s. dort).
Dabei handelt es sich um ein funktionell betontes Konzept, das die
Bedeutung der Regulation von Blutdruck und Durchblutung in den
Vordergrund rückt: Es ist dasjenige Volumen, dessen Größe über
verschiedene Rezeptoren im Körper (z.B. Barorezeptoren) indirekt
ermittelt wird und über neuroendokrine Systeme (Sympathikus,
verschiedene Hormone) regulatorisch wirksam wird.
s. dort).
Dabei handelt es sich um ein funktionell betontes Konzept, das die
Bedeutung der Regulation von Blutdruck und Durchblutung in den
Vordergrund rückt: Es ist dasjenige Volumen, dessen Größe über
verschiedene Rezeptoren im Körper (z.B. Barorezeptoren) indirekt
ermittelt wird und über neuroendokrine Systeme (Sympathikus,
verschiedene Hormone) regulatorisch wirksam wird.  Abbildung), sinkt einerseits das Herzzeitvolumen (weil das Myokard
geschwächt ist), andererseits erhöhen sich die Füllungsdrucke (weil
sich Blut in der Peripherie rückstaut).
Abbildung), sinkt einerseits das Herzzeitvolumen (weil das Myokard
geschwächt ist), andererseits erhöhen sich die Füllungsdrucke (weil
sich Blut in der Peripherie rückstaut). Veränderungen des Zentralvenendrucks müssen immer im Zusammenhang mit
der Gesamtsituation des Kreislaufs interpretiert werden (Zustand des
Herzmuskels vs. Zustand des Kreislaufs).
Veränderungen des Zentralvenendrucks müssen immer im Zusammenhang mit
der Gesamtsituation des Kreislaufs interpretiert werden (Zustand des
Herzmuskels vs. Zustand des Kreislaufs).
 Näheres zu Schwerkraft und hydrostatischen Druckgradienten im Kreislauf s. dort
Näheres zu Schwerkraft und hydrostatischen Druckgradienten im Kreislauf s. dort Intravenöse Infusion: Die Höhe eines
Tropfers über der Infusionsstelle bestimmt den Infusionsdruck. So ergibt 20 cm Tropferhöhe bei einem
Venendruck von 15 cm Wassersäule 20-15 = 5 cm H2O treibenden Druck. Die Infusionsgeschwindigkeit hängt vom
Strömungswiderstand der Leitung ab; dieser wird mittels
Quetschrolle am Schlauch beeinflusst, hängt aber
auch vom Ende der Leitung in der Vene ab: Bilden sich
Thromben
Intravenöse Infusion: Die Höhe eines
Tropfers über der Infusionsstelle bestimmt den Infusionsdruck. So ergibt 20 cm Tropferhöhe bei einem
Venendruck von 15 cm Wassersäule 20-15 = 5 cm H2O treibenden Druck. Die Infusionsgeschwindigkeit hängt vom
Strömungswiderstand der Leitung ab; dieser wird mittels
Quetschrolle am Schlauch beeinflusst, hängt aber
auch vom Ende der Leitung in der Vene ab: Bilden sich
Thromben  , verlegen diese die Kanüle und die Tropfrate
nimmt während der Infusion ab.
, verlegen diese die Kanüle und die Tropfrate
nimmt während der Infusion ab.
 Abbildung: Druck-Volumen-Profil einer Vene im entspannten
(Querschnitte und obere Kurve) und kontrahierten Zustand (untere Kurve)
Abbildung: Druck-Volumen-Profil einer Vene im entspannten
(Querschnitte und obere Kurve) und kontrahierten Zustand (untere Kurve)
 Abbildung). Die maschengitterartig angeordneten
Kollagenbündel in der Venenwand bieten ab diesem Druck einen zunehmen
rigiden Widerstand gegen weitere Dehnung, dementsprechend nimmt die
Compliance deutlich ab, die Volumen-Druck-Kurve wird zusehends steiler,
die Wand steifer - das ergibt einen automatischen Schutz vor zu starker
Blutfüllung und unterstützt zusammen mit dem Mechanismus der Muskelpumpe den Rückstrom zum Herzen, im Stehen insbesondere aus den Beinen.
Abbildung). Die maschengitterartig angeordneten
Kollagenbündel in der Venenwand bieten ab diesem Druck einen zunehmen
rigiden Widerstand gegen weitere Dehnung, dementsprechend nimmt die
Compliance deutlich ab, die Volumen-Druck-Kurve wird zusehends steiler,
die Wand steifer - das ergibt einen automatischen Schutz vor zu starker
Blutfüllung und unterstützt zusammen mit dem Mechanismus der Muskelpumpe den Rückstrom zum Herzen, im Stehen insbesondere aus den Beinen. Abbildung), insbesondere in Stresssituationen.
Abbildung), insbesondere in Stresssituationen. Abbildung)
besteht darin, dass eine - durch erhöhten Sympathikustonus bedingte -
Verengung arteriolärer Gefäße (Stresseffekt) und dadurch Reduktion des
Zuflusses zum nachgeschalteten venösen Gefäßgebiet (Venenplexus) zu
dessen Entspeicherung führt (vorher durch den Blutdruck angetriebene
Dehnung der Venenwände führt zu deren elastischem Zusammenziehen -
potenzielle Energie wird in kinetische Energie rückverwandelt). So wird
Blut Richtung Herz mobilisiert und steht zur Stabilisierung des
arteriellen Blutdrucks trotz funktioneller Hypovolämie zur Verfügung.
Abbildung)
besteht darin, dass eine - durch erhöhten Sympathikustonus bedingte -
Verengung arteriolärer Gefäße (Stresseffekt) und dadurch Reduktion des
Zuflusses zum nachgeschalteten venösen Gefäßgebiet (Venenplexus) zu
dessen Entspeicherung führt (vorher durch den Blutdruck angetriebene
Dehnung der Venenwände führt zu deren elastischem Zusammenziehen -
potenzielle Energie wird in kinetische Energie rückverwandelt). So wird
Blut Richtung Herz mobilisiert und steht zur Stabilisierung des
arteriellen Blutdrucks trotz funktioneller Hypovolämie zur Verfügung.
 Abbildung: DeJager-Krogh-Mechanismus
Abbildung: DeJager-Krogh-Mechanismus

 Abbildung: Die wichtigsten venösen Zuflussgebiete
Abbildung: Die wichtigsten venösen Zuflussgebiete Abbildung oben: DeJager-Krogh-Mechanismus) und mechanische Gegenkräfte (Druck von außen) reguliert
Abbildung oben: DeJager-Krogh-Mechanismus) und mechanische Gegenkräfte (Druck von außen) reguliert
 Bei erhöhter Darmtätigkeit nimmt die Durchblutung im Splanchnicus-Gebiet zu (niedrige Sympathikus-Aktivität).
Bei erhöhter Darmtätigkeit nimmt die Durchblutung im Splanchnicus-Gebiet zu (niedrige Sympathikus-Aktivität).  Steigt die Körpertemperatur an (+Hautdurchblutung) oder kommt es zu vermehrter Muskelaktivität, wird die Durchblutung im Splanchnikusgebiet gedrosselt (+Sympathikusaktivität).
Steigt die Körpertemperatur an (+Hautdurchblutung) oder kommt es zu vermehrter Muskelaktivität, wird die Durchblutung im Splanchnikusgebiet gedrosselt (+Sympathikusaktivität). wirkt).
wirkt). Interpretation des ZVD:
Interpretation des ZVD:
 Venensystem: Hohes venöses Volumenangebot, z.B. bei liegender Position (evt. auch Hypervolämie), aber auch
Venensystem: Hohes venöses Volumenangebot, z.B. bei liegender Position (evt. auch Hypervolämie), aber auch Myokardiale Schlagkraft: Herzinsuffizienz (mangelhaftes
"Abpumpen" von Blut aus dem Niederdrucksystem).
Myokardiale Schlagkraft: Herzinsuffizienz (mangelhaftes
"Abpumpen" von Blut aus dem Niederdrucksystem).  eine hohe Herzleistung bedeuten (starker "Saugeffekt" der Ventrikel), andererseits aber auch
eine hohe Herzleistung bedeuten (starker "Saugeffekt" der Ventrikel), andererseits aber auch  geringes
Volumenangebot (z.B. bei aufrechter Körperlage oder Hypovolämie, also
niedrigem Blutvolumen, z.B. bei Dehydration oder Blutverlust).
geringes
Volumenangebot (z.B. bei aufrechter Körperlage oder Hypovolämie, also
niedrigem Blutvolumen, z.B. bei Dehydration oder Blutverlust). s.
dort); bleiben sie gefüllt, ist der
Zentralvenendruck erhöht. Auch der Kollaps der Venen am Handrücken bei
Anheben der Hand über Herzniveau (
s.
dort); bleiben sie gefüllt, ist der
Zentralvenendruck erhöht. Auch der Kollaps der Venen am Handrücken bei
Anheben der Hand über Herzniveau ( Abbildung unten) kann diagnostisch beurteilt werden.
Abbildung unten) kann diagnostisch beurteilt werden. PCWP = Pulmonary capillary wedge(d) pressure am Ausgang des Pulmonalkreislaufs ermittelt.
PCWP = Pulmonary capillary wedge(d) pressure am Ausgang des Pulmonalkreislaufs ermittelt.
 Abbildung: Druckverteilung im Liegen und Stehen
Abbildung: Druckverteilung im Liegen und Stehen

 Abbildung: Hämodynamik in den Beinen bei aufrechter Körperhaltung
Abbildung: Hämodynamik in den Beinen bei aufrechter Körperhaltung

 Belastung:
Richtet sich eine Person aus der liegenden Position auf und bleibt in
aufrechter Körperlage ruhig stehen, dann füllen sich die Venengeflechte
in den Beinen (von der arteriellen Seite her) mit zusätzlich Blut -
etwa 600-700 ml, die Hälfte davon innerhalb von 20-30 Sekunden. Ursache
ist der hydrostatische Druckgradient
im Stehen. Das bedeutet eine Reduktion des venösen Rückstroms zum
Herzen; Zentralvenendruck und Herzminutenvolumen nehmen deutlich ab (das Herzzeitvolumen von ~7,5 auf ~5 l/min, also etwa um ein Drittel).
Belastung:
Richtet sich eine Person aus der liegenden Position auf und bleibt in
aufrechter Körperlage ruhig stehen, dann füllen sich die Venengeflechte
in den Beinen (von der arteriellen Seite her) mit zusätzlich Blut -
etwa 600-700 ml, die Hälfte davon innerhalb von 20-30 Sekunden. Ursache
ist der hydrostatische Druckgradient
im Stehen. Das bedeutet eine Reduktion des venösen Rückstroms zum
Herzen; Zentralvenendruck und Herzminutenvolumen nehmen deutlich ab (das Herzzeitvolumen von ~7,5 auf ~5 l/min, also etwa um ein Drittel).  ). Der
Muskeltonus lässt nach, die betroffene Person sinkt ohnmächtig zusammen
(orthostatischer Kollaps). Die Synkope ist selbstlimitierend,
denn der Kollaps
). Der
Muskeltonus lässt nach, die betroffene Person sinkt ohnmächtig zusammen
(orthostatischer Kollaps). Die Synkope ist selbstlimitierend,
denn der Kollaps  löst das Problem: Die hydrostatische Belastung
verschwindet - Herzleistung, Blutdruck und Hirndurchblutung steigen an,
die Person erlangt rasch wieder das Bewusstsein.
löst das Problem: Die hydrostatische Belastung
verschwindet - Herzleistung, Blutdruck und Hirndurchblutung steigen an,
die Person erlangt rasch wieder das Bewusstsein. Venengeflechte mit dem größten physiologischen Speichervermögen (Volumencompliance:
Volumen bezogen auf den Füllungsdruck) befinden sich im Abdominalraum
(Splanchnikusgebiet) und in der Haut. Das Splanchnikusgebiet ist besonders postprandial gut
durchblutet (Verdauungsvorgänge); die Haut wiederum steht im Dienste der Thermoregulation
(Kühlung). Beide sind vom Sympathikus gesteuert: Hoher Sympathikustonus
führt zu Vasokonstriktion und senkt die Durchblutung, niedriger
Sympathikustonus erlaubt Vasodilatation (blutdruckpassiv) und läßt stärkere
Perfusion zu.
Venengeflechte mit dem größten physiologischen Speichervermögen (Volumencompliance:
Volumen bezogen auf den Füllungsdruck) befinden sich im Abdominalraum
(Splanchnikusgebiet) und in der Haut. Das Splanchnikusgebiet ist besonders postprandial gut
durchblutet (Verdauungsvorgänge); die Haut wiederum steht im Dienste der Thermoregulation
(Kühlung). Beide sind vom Sympathikus gesteuert: Hoher Sympathikustonus
führt zu Vasokonstriktion und senkt die Durchblutung, niedriger
Sympathikustonus erlaubt Vasodilatation (blutdruckpassiv) und läßt stärkere
Perfusion zu.
 Abbildung: Wasserimmersion
Abbildung: Wasserimmersion
 Dieser
Mechanismus der "Muskelpumpe" kann bis zu 50% der gesamten Energie für
den Transport des Blutes durch den Kreislauf ausmachen, unterstützt
also insbesondere bei körperlicher Belastung ganz wesentlich die
Fördertätigkeit des Herzens.
Dieser
Mechanismus der "Muskelpumpe" kann bis zu 50% der gesamten Energie für
den Transport des Blutes durch den Kreislauf ausmachen, unterstützt
also insbesondere bei körperlicher Belastung ganz wesentlich die
Fördertätigkeit des Herzens.
 Abbildung: Funktionsweise der "Muskelpumpe"
Abbildung: Funktionsweise der "Muskelpumpe"
 Zum venösen Rückstrom s. auch dort
Zum venösen Rückstrom s. auch dort Abbildung),
Zentralvenendruck, enddiastolisches Volumen und Schlagvolumen des
rechten Ventrikels nehmen zu.
Abbildung),
Zentralvenendruck, enddiastolisches Volumen und Schlagvolumen des
rechten Ventrikels nehmen zu. 
 Abbildung: Atempumpe
Abbildung: Atempumpe
 Inspiration intensiviert den Unterdruck im Donders'schen Raum
(Zwerchfellkuppel senkt sich, Interkostalmuskeln erweitern den
Brustkorb), das erhöht das Druckgefälle von der Peripherie
(systemischer Druck) zum Herzen (zentralvenöser Druck), und die
Blutströmung zum rechten Vorhof nimmt zu.
Inspiration intensiviert den Unterdruck im Donders'schen Raum
(Zwerchfellkuppel senkt sich, Interkostalmuskeln erweitern den
Brustkorb), das erhöht das Druckgefälle von der Peripherie
(systemischer Druck) zum Herzen (zentralvenöser Druck), und die
Blutströmung zum rechten Vorhof nimmt zu. Umgekehrt nimmt der Druck im Brustraum bei Ausatmung zu, der venöse
Druckgradient zum Herzen wird geringer und der venöse Rückstrom lässt
nach. Venenklappen (außer im V. cava-Bereich) verhindern einen retrograden Blutfluss.
Umgekehrt nimmt der Druck im Brustraum bei Ausatmung zu, der venöse
Druckgradient zum Herzen wird geringer und der venöse Rückstrom lässt
nach. Venenklappen (außer im V. cava-Bereich) verhindern einen retrograden Blutfluss.
 Abbildung: Druck und Strömung in einer oberen Hohlvene (vena cava superior) während zweier Herzschläge
Abbildung: Druck und Strömung in einer oberen Hohlvene (vena cava superior) während zweier Herzschläge
 vgl. dort), lässt sich die Jugularvene erkennen, deren Füllung mit dem Herzschlag oszilliert (Venenpuls,
vgl. dort), lässt sich die Jugularvene erkennen, deren Füllung mit dem Herzschlag oszilliert (Venenpuls,  s. dort):
Der Kollapspunkt (die Stelle, an welcher der transmurale Druck Null beträgt) trennt eine kopfwärts gelegene blutleere (Vene nicht
sichtbar) von einer kaudalen blutgefüllten Zone der Halsvene, und
wandert entsprechend dem Herzzyklus deutlich hin und her. Die
Druckschwankungen sind deutlich sichtbar, aber zu schwach, um palpiert
werden zu können (was man deutlich spüren kann, ist der Carotispuls).
s. dort):
Der Kollapspunkt (die Stelle, an welcher der transmurale Druck Null beträgt) trennt eine kopfwärts gelegene blutleere (Vene nicht
sichtbar) von einer kaudalen blutgefüllten Zone der Halsvene, und
wandert entsprechend dem Herzzyklus deutlich hin und her. Die
Druckschwankungen sind deutlich sichtbar, aber zu schwach, um palpiert
werden zu können (was man deutlich spüren kann, ist der Carotispuls). Abbildung). Zwischen dem rechten Vorhof und der v. jugularis
liegen keine Venenklappen, diese Strecke bildet eine hydrostatisch
offene Strecke (bis zum Kollapspunkt).
Abbildung). Zwischen dem rechten Vorhof und der v. jugularis
liegen keine Venenklappen, diese Strecke bildet eine hydrostatisch
offene Strecke (bis zum Kollapspunkt). Abbildung).
Abbildung). 
 Abbildung: Venenfüllung in Anhängigkeit von der Armlage (d.h. dem hydrostatischen Füllungsdruck)
Abbildung: Venenfüllung in Anhängigkeit von der Armlage (d.h. dem hydrostatischen Füllungsdruck)
 Für
eine valide Blutdruckmessung ist es daher notwendig, die Messstelle auf
Herzhöhe zu positionieren, um hydrostatische Zusatzeffekte auf den
gemessenen Blutdruck zu vermeiden.
Für
eine valide Blutdruckmessung ist es daher notwendig, die Messstelle auf
Herzhöhe zu positionieren, um hydrostatische Zusatzeffekte auf den
gemessenen Blutdruck zu vermeiden.
 Herz und Blutgefäße sind hydromechanisch zum kardiovaskulären System zusammengeschlossen. In "Arbeitspunkten" (venös, arteriell) überschneiden sich ihre Druck-Volumen-Kurven (Guyton's cross plot).
Der
venöse Rückstrom ergibt sich aus der Differenz zwischen dem peripheren
"Systemdruck" (etwa im Bereich der Venolen) und dem diastolischen Druck
im rechten Herzen und bestimmt dessen Pumpleistung (Vorlast und Frank-Starling-Mechanimus).
Hypervolämie rückt den Arbeitspunkt zu erhöhtem Zentralvenendruck und
Herzminutenvolumen, bei Herzschwäche ist die Leistungskurve des Herzens
zu niedrigeren Förderleistungen verlagert
Herz und Blutgefäße sind hydromechanisch zum kardiovaskulären System zusammengeschlossen. In "Arbeitspunkten" (venös, arteriell) überschneiden sich ihre Druck-Volumen-Kurven (Guyton's cross plot).
Der
venöse Rückstrom ergibt sich aus der Differenz zwischen dem peripheren
"Systemdruck" (etwa im Bereich der Venolen) und dem diastolischen Druck
im rechten Herzen und bestimmt dessen Pumpleistung (Vorlast und Frank-Starling-Mechanimus).
Hypervolämie rückt den Arbeitspunkt zu erhöhtem Zentralvenendruck und
Herzminutenvolumen, bei Herzschwäche ist die Leistungskurve des Herzens
zu niedrigeren Förderleistungen verlagert  In unten
gelegenen Körperregionen sind die Venen umso stärker gefüllt, je weiter
sie vom venösen hydrostatischen Indifferenzpunkt (Oberbauchbereich) entfernt sind (jeweils ~1 kPa pro 0,1 m Höhenunterschied). Am besten dehnbar (das ~50-fache der arteriellen Compliance) sind Venen bei einem gering positiven transmuralen Druck (~4 mmHg oder ~0,5 kPa). Ab ~2 kPa
nehmen sie eine kreisrunde Form an und versteifen, die
Volumen-Druck-Kurve wird steiler - weitere Füllung wird verhindert, der
Mechanismus der Muskelpumpe unterstützt. Zusätzlich sind Venen
kontraktil: In Leber, Gastrointestinaltrakt, Nieren, Haut wirken
zahlreiche adrenerge Nervenfasern stark vasokonstriktorisch. Das erhöht den
Innendruck, treibt Blut zum Herzen, insbesondere in Stresssituationen
In unten
gelegenen Körperregionen sind die Venen umso stärker gefüllt, je weiter
sie vom venösen hydrostatischen Indifferenzpunkt (Oberbauchbereich) entfernt sind (jeweils ~1 kPa pro 0,1 m Höhenunterschied). Am besten dehnbar (das ~50-fache der arteriellen Compliance) sind Venen bei einem gering positiven transmuralen Druck (~4 mmHg oder ~0,5 kPa). Ab ~2 kPa
nehmen sie eine kreisrunde Form an und versteifen, die
Volumen-Druck-Kurve wird steiler - weitere Füllung wird verhindert, der
Mechanismus der Muskelpumpe unterstützt. Zusätzlich sind Venen
kontraktil: In Leber, Gastrointestinaltrakt, Nieren, Haut wirken
zahlreiche adrenerge Nervenfasern stark vasokonstriktorisch. Das erhöht den
Innendruck, treibt Blut zum Herzen, insbesondere in Stresssituationen Neben dem
Gefäßtonus hängt die Füllung von Venen vom arteriellen Zustrom ab.
Öffnen die Widerstandsgefäße (arterioläre Vasodilatation), strömt mehr
Blut in Venen und wird dort vermehrt gespeichert (dynamischer Zwischenspeicher: kinetische wird zu
potentieller Energie), dies senkt den Rückstrom zum Herzen - die Vorlast des rechten Herzens nimmt ab (DeJager-Krogh- Mechanismus).
Arterioläre Vasokonstriktion wirkt umgekehrt, die Venen entspeichern
(potentielle wird zu kinetischer Energie) und erhöhen das
Herzminutenvolumen (insbesondere in kritischen Kreislaufsituationen)
Neben dem
Gefäßtonus hängt die Füllung von Venen vom arteriellen Zustrom ab.
Öffnen die Widerstandsgefäße (arterioläre Vasodilatation), strömt mehr
Blut in Venen und wird dort vermehrt gespeichert (dynamischer Zwischenspeicher: kinetische wird zu
potentieller Energie), dies senkt den Rückstrom zum Herzen - die Vorlast des rechten Herzens nimmt ab (DeJager-Krogh- Mechanismus).
Arterioläre Vasokonstriktion wirkt umgekehrt, die Venen entspeichern
(potentielle wird zu kinetischer Energie) und erhöhen das
Herzminutenvolumen (insbesondere in kritischen Kreislaufsituationen) Die
meisten Venen haben ohne sympathischen Einfluss nur einen geringen
basalen Tonus und reagieren auf Dehnung kaum mit Kontraktion. Die Venengeflechte der Haut (Thermoregulation!) und der Baucheingeweide
(“Splanchnikusgebiet”) sind besonders gut dehnbar (Splanchnikusgebiet:
1/5 des Blutvolumens) und haben zahlreiche α-Adrenozeptoren. Venen im Splanchnikusgebiet reagieren auf klassische Kreislaufreflexe (z.B. Barorezeptorreflex) und
können in Stresssituationen (erhöhter Sympathikustonus) einen Teil des
Blutes zum Herzen verschieben, was den Kreislauf stabilisiert. Venengeflechte der Skelettmuskulatur sind ebenfalls gut dehnbar, aber kaum sympathisch versorgt: Sie werden
bei Muskelaktivität durch die "Muskelpumpe" automatisch geleert
(Venenklappen). Der Venentonus in den Beinen nimmt bei aufrechter
Körperlage reflektorisch zu, um die Speicherung von Blut in der unteren
Körperhälfte zu minimieren
Die
meisten Venen haben ohne sympathischen Einfluss nur einen geringen
basalen Tonus und reagieren auf Dehnung kaum mit Kontraktion. Die Venengeflechte der Haut (Thermoregulation!) und der Baucheingeweide
(“Splanchnikusgebiet”) sind besonders gut dehnbar (Splanchnikusgebiet:
1/5 des Blutvolumens) und haben zahlreiche α-Adrenozeptoren. Venen im Splanchnikusgebiet reagieren auf klassische Kreislaufreflexe (z.B. Barorezeptorreflex) und
können in Stresssituationen (erhöhter Sympathikustonus) einen Teil des
Blutes zum Herzen verschieben, was den Kreislauf stabilisiert. Venengeflechte der Skelettmuskulatur sind ebenfalls gut dehnbar, aber kaum sympathisch versorgt: Sie werden
bei Muskelaktivität durch die "Muskelpumpe" automatisch geleert
(Venenklappen). Der Venentonus in den Beinen nimmt bei aufrechter
Körperlage reflektorisch zu, um die Speicherung von Blut in der unteren
Körperhälfte zu minimieren Der zentrale
Venendruck (CVP) ist der mittlere Blutdruck im Bereich der herznahen
thorakalen Venen / im rechten Vorhof. Er oszilliert mit Herzschlag und Atmung um einen
Mittelwert, dieser ist ein Maß für die Vorlast des rechten Ventrikels
(sein Betrag entspricht etwa dem barometrischen Druck). Hoher [CVP] kann zweierlei bedeuten: Hohes venöses Volumenangebot (z.B. liegende Position) oder geringe Herzleistung (Herzinsuffizienz); niedriger [CVP] geringes Volumenangebot (z.B. aufrechte Körperlage) oder hohe Herzleistung (Saugeffekt). Bei 45°-Lagerung des Oberkörpers sollten die Jugularvenen kollabiert sein, andernfalls ist der Zentralvenendruck erhöht
Der zentrale
Venendruck (CVP) ist der mittlere Blutdruck im Bereich der herznahen
thorakalen Venen / im rechten Vorhof. Er oszilliert mit Herzschlag und Atmung um einen
Mittelwert, dieser ist ein Maß für die Vorlast des rechten Ventrikels
(sein Betrag entspricht etwa dem barometrischen Druck). Hoher [CVP] kann zweierlei bedeuten: Hohes venöses Volumenangebot (z.B. liegende Position) oder geringe Herzleistung (Herzinsuffizienz); niedriger [CVP] geringes Volumenangebot (z.B. aufrechte Körperlage) oder hohe Herzleistung (Saugeffekt). Bei 45°-Lagerung des Oberkörpers sollten die Jugularvenen kollabiert sein, andernfalls ist der Zentralvenendruck erhöht Orthostase
bedeutet aufrechte Körperhaltung (Stehen). Aufstehen ist eine
kardiovaskuläre Belastung: Über dem hydrostatischen Indifferenzpunkt sinken die
Druckwerte (1 kPa je dm Höhendifferenz), der Zentralvenendruck um ~0,5
kPa. Das rechte Herz pumpt weniger Blut, die Füllung des
Lungenkreislaufs sinkt, damit auch die
Vorlast für den linken Ventrikel - kreislauflabile Personen können
präkollaptisch werden, zumal die Gehirndurchblutung aus hydrostatischen
Gründen beim Aufrichten absinkt (orthostatischer Kollaps bei Halbierung
der Gehirndurchblutung). In den Beinen steigt der arterielle
Druck auf ~25 kPa, die Venen speichern zusätzliche 600-700 ml Blut, durch die Muskelpumpe im Gehen wird der venöse
Druck von ~10-12 auf ~3-4 kPa
reduziert (was auch die Entstehung von Knöchelödemen zu verhindern
hilft). Dehnung der
Venenwand bewirkt eine Kontraktion der vorgeschalteten
Widerstandsgefäße (Henriksen-Reflex), was fast die Hälfte der systemischen arteriolären Widerstandserhöhung bei Orthostase erklärt
Orthostase
bedeutet aufrechte Körperhaltung (Stehen). Aufstehen ist eine
kardiovaskuläre Belastung: Über dem hydrostatischen Indifferenzpunkt sinken die
Druckwerte (1 kPa je dm Höhendifferenz), der Zentralvenendruck um ~0,5
kPa. Das rechte Herz pumpt weniger Blut, die Füllung des
Lungenkreislaufs sinkt, damit auch die
Vorlast für den linken Ventrikel - kreislauflabile Personen können
präkollaptisch werden, zumal die Gehirndurchblutung aus hydrostatischen
Gründen beim Aufrichten absinkt (orthostatischer Kollaps bei Halbierung
der Gehirndurchblutung). In den Beinen steigt der arterielle
Druck auf ~25 kPa, die Venen speichern zusätzliche 600-700 ml Blut, durch die Muskelpumpe im Gehen wird der venöse
Druck von ~10-12 auf ~3-4 kPa
reduziert (was auch die Entstehung von Knöchelödemen zu verhindern
hilft). Dehnung der
Venenwand bewirkt eine Kontraktion der vorgeschalteten
Widerstandsgefäße (Henriksen-Reflex), was fast die Hälfte der systemischen arteriolären Widerstandserhöhung bei Orthostase erklärt Wasserimmersion verlagert ~700 ml Blut aus der Peripherie (Beine,
Baucheingeweide) in den Thorax, weitet das diastolische Herz um ~180 ml
und erhöht den arteriellen Blutdruck um 1-2 kPa. Das Herz wird stärker
gefüllt, die Atmung erschwert. Hält dieses Reizmuster an, führt dies
reflektorisch zu renaler Vasodilatation und verminderter Sekretion von
Vasopressin, Angiotensin, Aldosteron, sowie erhöhter Ausschüttung
natriuretischer Peptide (Salz- und Wasserausscheidung). Ähnliche
Effekte resultieren aus Bettlägrigkeit und bedingen Probleme mit der
orthostatischen Regulation (Dekonditionierung, Kollapsneigung)
Wasserimmersion verlagert ~700 ml Blut aus der Peripherie (Beine,
Baucheingeweide) in den Thorax, weitet das diastolische Herz um ~180 ml
und erhöht den arteriellen Blutdruck um 1-2 kPa. Das Herz wird stärker
gefüllt, die Atmung erschwert. Hält dieses Reizmuster an, führt dies
reflektorisch zu renaler Vasodilatation und verminderter Sekretion von
Vasopressin, Angiotensin, Aldosteron, sowie erhöhter Ausschüttung
natriuretischer Peptide (Salz- und Wasserausscheidung). Ähnliche
Effekte resultieren aus Bettlägrigkeit und bedingen Probleme mit der
orthostatischen Regulation (Dekonditionierung, Kollapsneigung) Einatmung senkt den intrathorakalen (tiefe Inspiration senkt den Druck in der v. cava superior) und hebt den intraabdominellen Druck, Blut strömt vermehrt durch die untere
Hohlvene zum Herzen, das rechtsventrikuläre Schlagvoluemn nimmt zu
(Frank-Starling). Dennoch
sinkt das Schlagvolumen des linken Ventrikels, weil der Sogeffekt der
Einatmung den pulmonalen Blutpool vergrößert, den Druck in den
Lungenvenen senkt. Die Auswurfleistung des rechten und linken
Ventrikels ändern sich mit der Atmung gegenläufig. Insgesamt nimmt das
Herzminutenvolumen während der Einatmung ab, während der Ausatmung zu.
Die Folge sind Oszillationen des arteriellen Blutdrucks:
Leicht erhöht exspiratorisch, leicht erniedrigt inspiratorisch
Einatmung senkt den intrathorakalen (tiefe Inspiration senkt den Druck in der v. cava superior) und hebt den intraabdominellen Druck, Blut strömt vermehrt durch die untere
Hohlvene zum Herzen, das rechtsventrikuläre Schlagvoluemn nimmt zu
(Frank-Starling). Dennoch
sinkt das Schlagvolumen des linken Ventrikels, weil der Sogeffekt der
Einatmung den pulmonalen Blutpool vergrößert, den Druck in den
Lungenvenen senkt. Die Auswurfleistung des rechten und linken
Ventrikels ändern sich mit der Atmung gegenläufig. Insgesamt nimmt das
Herzminutenvolumen während der Einatmung ab, während der Ausatmung zu.
Die Folge sind Oszillationen des arteriellen Blutdrucks:
Leicht erhöht exspiratorisch, leicht erniedrigt inspiratorisch Inspiration vergrößert den treibenden Druck für den Rückstrom des venösen Blutes zum rechten Herzen. Der
Druck in der v. cava inferior schwankt im Ruhezustand zwischen ~0 und
~1 kPa, die Strömungsgeschwindigkeit des Blutes zwischen ~0 und ~20
cm/s (Venenpuls). a: Druckansteg bei der
beginnenden Vorhofkontraktion; c: Vorwölben der geschlossenen AV-Klappe
während der Anspannungszeit; x: Verschiebung der
Ventilebene zur Herzspitze ("Sogeffekt" auf den Vorhof); v, y:
Abschluss des Ventilebenenmechanismus (AV-Klappe)
Inspiration vergrößert den treibenden Druck für den Rückstrom des venösen Blutes zum rechten Herzen. Der
Druck in der v. cava inferior schwankt im Ruhezustand zwischen ~0 und
~1 kPa, die Strömungsgeschwindigkeit des Blutes zwischen ~0 und ~20
cm/s (Venenpuls). a: Druckansteg bei der
beginnenden Vorhofkontraktion; c: Vorwölben der geschlossenen AV-Klappe
während der Anspannungszeit; x: Verschiebung der
Ventilebene zur Herzspitze ("Sogeffekt" auf den Vorhof); v, y:
Abschluss des Ventilebenenmechanismus (AV-Klappe)