

Eine Reise durch die Physiologie - Wie der Körper des Menschen funktioniert

Körperhaltung und Motorik



 Athetose: ἀ = un-, θετός < τιθέναι = veranlassen
Athetose: ἀ = un-, θετός < τιθέναι = veranlassen| Planung
und Feinsteuerung von Bewegungsabläufen bedürfen komplexer
Kontrollmechanismen. So ist den Ausgängen der Pyramidenbahn im
motorischen Cortex ein mehrgliedriger Mechanismus aus Basalganglien und motorischem Thalamus vorgeschaltet. Die Basalganglienkette schaltet einen direkten und einen indirekten Rückkopplungsweg der motorischen Kontrolle: -- Der direkte Weg bewirkt Disinhibition (Bewegungserleichterung), -- der indirekter Weg Inhibition (Bewegungshemmung). Beteiligte Transmitter sind Glutamat (exzitatorisch) und GABA (inhibitorisch). Zusätzlich sind dem Striatum dopaminerge Einflüsse aufgeschaltet (exzitatorisch und inhibitorisch). Die Funktion der Basalganglien lässt sich anhand von Funktionsstörungen ablesen, die Symptome wie (hyperton-hypokinetisch), Mb. ParkinsonHuntington-Chorea, Ballismus und Athetose (hypoton-hyperkinetischer Formenkreis) bewirken. |
 Dopaminrezeptor
Dopaminrezeptor
 Core messages
Core messages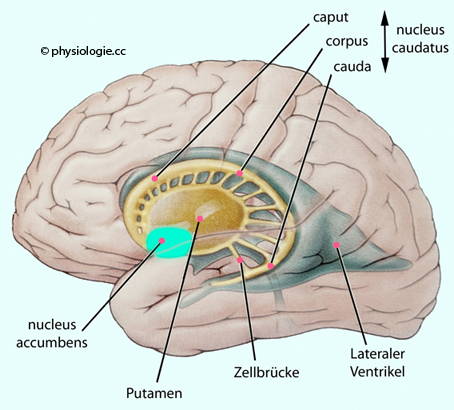
 Abbildung: Lage des Striatum
Abbildung: Lage des Striatum
 Abbildungen
Abbildungen  ).
). das Striatum (nucleus caudatus + Putamen + nucleus accumbens),
das Striatum (nucleus caudatus + Putamen + nucleus accumbens),  das Pallidum (globus pallidus),
das Pallidum (globus pallidus), der nucleus subthalamicus,
der nucleus subthalamicus, die substantia nigra (nucleus niger).
die substantia nigra (nucleus niger).
 Abbildung: Basalganglien
Abbildung: Basalganglien
 Abbildung).
Abbildung).
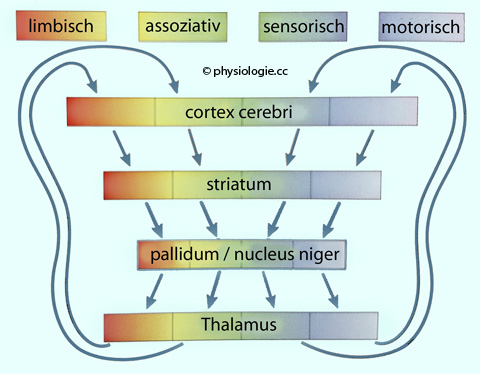
 Abbildung: Parallele Rückkopplungsschleifen zwischen Basalganglien, Thalamus und Großhirnrinde
Abbildung: Parallele Rückkopplungsschleifen zwischen Basalganglien, Thalamus und Großhirnrinde
 Abbildung) im Bereich der
Basalganglien äußern sich typischerweise in Bewegungsstörungen bzw. ihrer
willkürmotorischen Kontrolle.
Abbildung) im Bereich der
Basalganglien äußern sich typischerweise in Bewegungsstörungen bzw. ihrer
willkürmotorischen Kontrolle.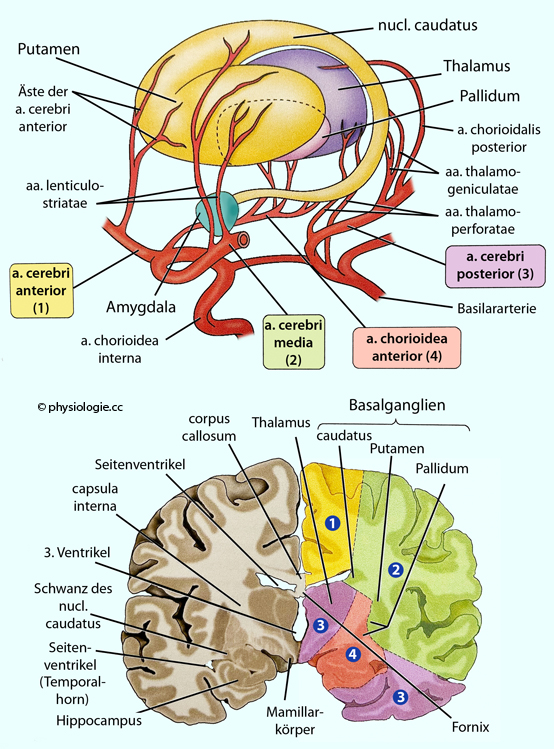
 Abbildung: Durchblutung tiefliegender Strukturen im Gehirn
Abbildung: Durchblutung tiefliegender Strukturen im Gehirn
 aus weiten Regionen der Großhirnrinde (inklusive limbischen Anteilen),
aus weiten Regionen der Großhirnrinde (inklusive limbischen Anteilen),  aus intralaminaren Kernen des Thalamus
aus intralaminaren Kernen des Thalamus und dopaminerge aus dem ventralen Mittelhirn.
und dopaminerge aus dem ventralen Mittelhirn. aus dem inneren Pallidum
aus dem inneren Pallidum  aus der pars reticulata der substantia
nigra.
aus der pars reticulata der substantia
nigra. 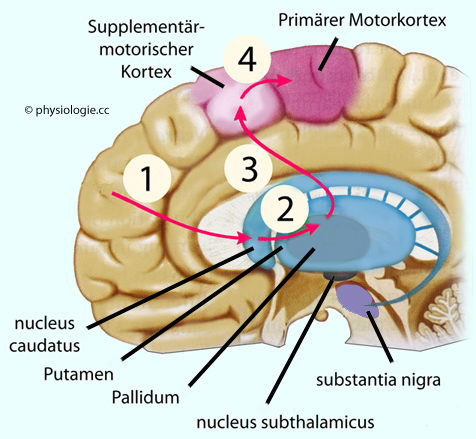
 Abbildung: Die Basalganglien sind in die transkortikale Bewegungsplanung eingebunden
Abbildung: Die Basalganglien sind in die transkortikale Bewegungsplanung eingebunden
 s. unten) auf.
s. unten) auf.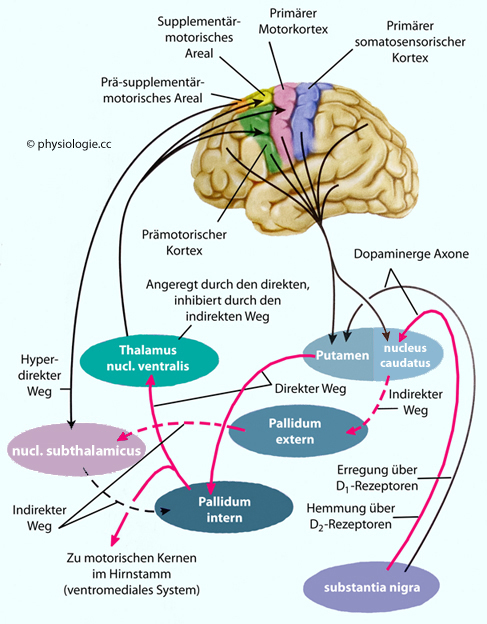
 Abbildung: Basalganglien
Abbildung: Basalganglien
 Direkter Weg: Er projiziert GABAerg aus dem Striatum in das innere Pallidum
(
Direkter Weg: Er projiziert GABAerg aus dem Striatum in das innere Pallidum
( Abbildung) und in die Substantia nigra (pars reticulata) und von
diesen beiden Stellen ebenfalls GABAerg in den Thalamus. Dies führt zu
einer Steigerung der Thalamusaktivität (Disinhibition: Zwei hemmende Neurone hintereinandergeschaltet).
Abbildung) und in die Substantia nigra (pars reticulata) und von
diesen beiden Stellen ebenfalls GABAerg in den Thalamus. Dies führt zu
einer Steigerung der Thalamusaktivität (Disinhibition: Zwei hemmende Neurone hintereinandergeschaltet). Indirekter Weg: Die GABAergen Neurone projizieren aus dem Striatum in das äußere Pallidum und von dort ebenfalls GABAerg in den nucleus subthalamicus
(
Indirekter Weg: Die GABAergen Neurone projizieren aus dem Striatum in das äußere Pallidum und von dort ebenfalls GABAerg in den nucleus subthalamicus
( Abbildung).
Von dort geht es glutamaterg zu den GABAergen Neuronen
des inneren Pallidum und der pars reticulata des nucleus niger. Der
indirekte Weg dämpft die Aktivität thalamischer Neuronen und dient
wahrscheinlch primär der Unterdrückung unerwünschter (unpassender)
Bewegungen.
Abbildung).
Von dort geht es glutamaterg zu den GABAergen Neuronen
des inneren Pallidum und der pars reticulata des nucleus niger. Der
indirekte Weg dämpft die Aktivität thalamischer Neuronen und dient
wahrscheinlch primär der Unterdrückung unerwünschter (unpassender)
Bewegungen.| Das Pallidum wird vom nucleus subthalamicus glutamaterg angeregt |
| Das Pallidum wird vom Striatum GABA-erg gehemmt |
 GABAerge Neuronen des Striatum (spiny projection neurons
SPNs) sind im Ruhezustand weitgehend inaktiv, während Zellen des globus
pallidus (pars interna) und der substantia nigra (pars reticulata) -
also inhibitorische Output-Neurone zum Thalamus - im Ruhezustand
tonisch aktiv sind. Unmittelbar vor einer Willkürbewegung regen
exzitatorische Projektionsneurone in Großhirnrinde und Thalamus SPNs
an, was wiederum deren Hemmung im direkten Pfad unterbindet und
Bewegungen "freigibt".
GABAerge Neuronen des Striatum (spiny projection neurons
SPNs) sind im Ruhezustand weitgehend inaktiv, während Zellen des globus
pallidus (pars interna) und der substantia nigra (pars reticulata) -
also inhibitorische Output-Neurone zum Thalamus - im Ruhezustand
tonisch aktiv sind. Unmittelbar vor einer Willkürbewegung regen
exzitatorische Projektionsneurone in Großhirnrinde und Thalamus SPNs
an, was wiederum deren Hemmung im direkten Pfad unterbindet und
Bewegungen "freigibt". Abbildung).
Der Vorteil ist eine kürzere Zugriffszeit als beim "klassischen"
indirekten Weg. Das kann z.B. in Gefahrensituationen sehr hilfreich
sein, wenn es darum geht, eine Bewegungsfolge plötzlich abzustoppen.
Abbildung).
Der Vorteil ist eine kürzere Zugriffszeit als beim "klassischen"
indirekten Weg. Das kann z.B. in Gefahrensituationen sehr hilfreich
sein, wenn es darum geht, eine Bewegungsfolge plötzlich abzustoppen. 1686 verfasste Thomas Sydenham Schriften über die Chorea minor (daher auch "Sydenham-Chorea"). Die substantia nigra wurde erstmals 1800 von Samuel Sömmerring identifiziert (daher auch die Bezeichnung "Sömmerring-Ganglion"). 1817 beschrieb James Parkinson die später (60 Jahre nach seinem Tod) nach ihm benannte Schüttellähmung. Die Chorea major ("Veitstanz") wurde 1872 von George Huntington beschrieben, nach ihm wird diese bis heute unheilbare Krankheit als Huntington-Chorea bezeichnet (s. unten).
1686 verfasste Thomas Sydenham Schriften über die Chorea minor (daher auch "Sydenham-Chorea"). Die substantia nigra wurde erstmals 1800 von Samuel Sömmerring identifiziert (daher auch die Bezeichnung "Sömmerring-Ganglion"). 1817 beschrieb James Parkinson die später (60 Jahre nach seinem Tod) nach ihm benannte Schüttellähmung. Die Chorea major ("Veitstanz") wurde 1872 von George Huntington beschrieben, nach ihm wird diese bis heute unheilbare Krankheit als Huntington-Chorea bezeichnet (s. unten).
 Körpermotorik (mit Betonung von Gesichts- und
Mundbewegungen), für die
Körpermotorik (mit Betonung von Gesichts- und
Mundbewegungen), für die 
 Kontrolle der Augenbewegungen (gesteuert vom
frontalen Augenfeld des Cortex), und
Kontrolle der Augenbewegungen (gesteuert vom
frontalen Augenfeld des Cortex), und 
 komplex-assoziative zur
Ausarbeitung motorischer Strategien im Rahmen von motivations- und
erkenntnisabhängigem Verhalten.
komplex-assoziative zur
Ausarbeitung motorischer Strategien im Rahmen von motivations- und
erkenntnisabhängigem Verhalten. 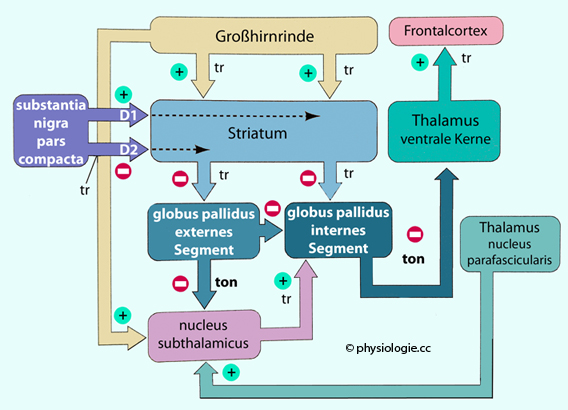
 Abbildung: Disinhibition durch Basalganglien via direkten und indirekten Pfad
Abbildung: Disinhibition durch Basalganglien via direkten und indirekten Pfad
 auf das Striatum zurück (
auf das Striatum zurück ( Abbildung).
Abbildung).
 Die pars reticulata (SNr) verfügt über GABAerge
Neuronen, diese projizieren auf den Thalamus (
Die pars reticulata (SNr) verfügt über GABAerge
Neuronen, diese projizieren auf den Thalamus ( Abbildung) und die
oberen Vierhügel (Augenbewegungen), und hemmen dopaminerge Aktivitäten
der pars compacta. Diese Neuronen sind spontanaktiv und üben
tonisch-inhibitorische Aktivität aus.
Abbildung) und die
oberen Vierhügel (Augenbewegungen), und hemmen dopaminerge Aktivitäten
der pars compacta. Diese Neuronen sind spontanaktiv und üben
tonisch-inhibitorische Aktivität aus.  Die pars compacta (SNc) sendet exzitatorische dopaminerge (D1)
Impulse an das Striatum (Nigro-striatales System), die in die Kontrolle der Feinmotorik
einfließen und motorische Lernvorgänge unterstützen. Wahrscheinlich ist
sie auch in die Schlaf-Wach-Regulation involviert.
Die pars compacta (SNc) sendet exzitatorische dopaminerge (D1)
Impulse an das Striatum (Nigro-striatales System), die in die Kontrolle der Feinmotorik
einfließen und motorische Lernvorgänge unterstützen. Wahrscheinlich ist
sie auch in die Schlaf-Wach-Regulation involviert.| Die substantia nigra hat dopaminerge Projektionen (D1-Rezeptoren) auf das Striatum Ungenügende Wirkung dieser Fasern (Dopaminmangel) verursacht Parkinson-Symptome |

 Abbildung: Amygdala und Basalganglien
Abbildung: Amygdala und Basalganglien
 Abbildung), und beide projizieren - direkt und indirekt - auf den Hippokampus,
der Erinnerungsinhalte verfügbar hält, bis sie kortikal "abgespeichert"
sind. Das bedeutet, dass die Amygdala Lernprozesse in den Basalganglien
beeinflusst.
Abbildung), und beide projizieren - direkt und indirekt - auf den Hippokampus,
der Erinnerungsinhalte verfügbar hält, bis sie kortikal "abgespeichert"
sind. Das bedeutet, dass die Amygdala Lernprozesse in den Basalganglien
beeinflusst.  Die Funktionsschleifen in den Basalganglien werden durch
“Berieselungssysteme” moduliert, z.B. durch die nigro-striatalen
Bahnen. Diese benutzen Dopamin als Transmitter, ihr Ausfall führt zum
Parkinson-Syndrom.
Die Funktionsschleifen in den Basalganglien werden durch
“Berieselungssysteme” moduliert, z.B. durch die nigro-striatalen
Bahnen. Diese benutzen Dopamin als Transmitter, ihr Ausfall führt zum
Parkinson-Syndrom. Dopaminrezeptoren befinden sich an entsprechenden Nervenzellen (Striatum, limbisches System, nucl. accumbens, Groß- und Kleinhirnhirnrinde). Teils regen sie über ein Gs-Protein die Adenylatzyklase an (D1-Gruppe: D1, D5), teils hemmen sie diese über ein Gi-Protein (D2-Gruppe: D2, D3, D4).
 D1-Dopaminrezeptoren regen striatale Output-Neurone im direkten Weg an,
hemmen GABAerge Neurone in innerem Globus pallidus (GPi) und der substantia nigra pars reticulata (SNr).
D1-Dopaminrezeptoren regen striatale Output-Neurone im direkten Weg an,
hemmen GABAerge Neurone in innerem Globus pallidus (GPi) und der substantia nigra pars reticulata (SNr). Im indirekten Weg bewirkt Aktivierung von D2-Dopaminrezeptoren die Hemmung striataler Output-Neurone zum äußeren Globus pallidus (GPe) und Hemmung von glutamatergen Neuronen im nucleus subthalamicus (STN), und GABAerger Neurone im inneren globus pallidus und dem retikulären Teil der substantia nigra.
Im indirekten Weg bewirkt Aktivierung von D2-Dopaminrezeptoren die Hemmung striataler Output-Neurone zum äußeren Globus pallidus (GPe) und Hemmung von glutamatergen Neuronen im nucleus subthalamicus (STN), und GABAerger Neurone im inneren globus pallidus und dem retikulären Teil der substantia nigra.
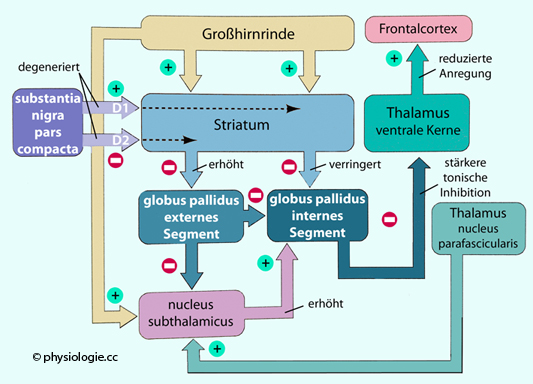
 Abbildung: Verändertes Gleichgewicht im Basalgangliensystem bei Mb. Parkinson
Abbildung: Verändertes Gleichgewicht im Basalgangliensystem bei Mb. Parkinson
 Das Parkinson-Syndrom
Das Parkinson-Syndrom  ist
die häufigste Basalganglienerkrankung.
Ursache ist eine Degeneration dopaminerger Efferenzen aus dem nucleus
niger, ihre Wirkung auf den globus pallidus nimmt ab. Der direkte Pfad
der Inhibition der ventralen Thalamuskerne wird verstärkt, der motorische Cortex schwächer angeregt (
ist
die häufigste Basalganglienerkrankung.
Ursache ist eine Degeneration dopaminerger Efferenzen aus dem nucleus
niger, ihre Wirkung auf den globus pallidus nimmt ab. Der direkte Pfad
der Inhibition der ventralen Thalamuskerne wird verstärkt, der motorische Cortex schwächer angeregt ( Abbildung), es kommt zu “Einfrieren”
von Bewegungen (Akinese), erhöhtem
Muskeltonus (Rigor) und Zittern der Finger bzw. Hände (Ruhetremor).
Abbildung), es kommt zu “Einfrieren”
von Bewegungen (Akinese), erhöhtem
Muskeltonus (Rigor) und Zittern der Finger bzw. Hände (Ruhetremor).  Eine
Substitutionstherapie mit der Vorstufe L-DOPA (Levodopa) oder Dopamin-Agonisten
ist möglich, weiters die Gabe von Anticholinergika, um der
dopaminmangelbedingten Enthemmung des cholinergen Systems
entgegenzuwirken.
Eine
Substitutionstherapie mit der Vorstufe L-DOPA (Levodopa) oder Dopamin-Agonisten
ist möglich, weiters die Gabe von Anticholinergika, um der
dopaminmangelbedingten Enthemmung des cholinergen Systems
entgegenzuwirken.  Parkinsonartige Symptome können auch durch
Medikamente (Neuroleptika) hervorgerufen werden.
Parkinsonartige Symptome können auch durch
Medikamente (Neuroleptika) hervorgerufen werden.| Mb. Parkinson beruht auf dem Untergang dopaminerger Neurone in der substantia nigra |
 , Tourette-Syndrom
, Tourette-Syndrom  , Aufmerksamkeitsdefizit / Hyperaktivität (ADHD, Attention deficit hyperactivity disorder) u.a. in Verbindung gebracht.
, Aufmerksamkeitsdefizit / Hyperaktivität (ADHD, Attention deficit hyperactivity disorder) u.a. in Verbindung gebracht.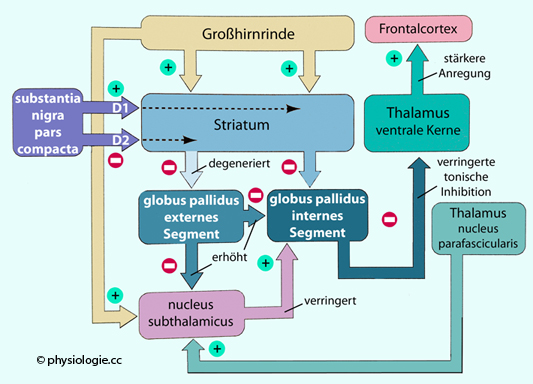
 Abbildung: Verändertes Gleichgewicht im Basalgangliensystem bei Chorea Huntington
Abbildung: Verändertes Gleichgewicht im Basalgangliensystem bei Chorea Huntington
 Die autosomal-dominant vererbliche
Huntington-Chorea
Die autosomal-dominant vererbliche
Huntington-Chorea  (Huntington's disease) geht u.a. mit Degeneration GABAerger Nerven, die vom
Striatum izum Pallidum ziehen (
(Huntington's disease) geht u.a. mit Degeneration GABAerger Nerven, die vom
Striatum izum Pallidum ziehen ( Abbildung), sowie auch cholinerger
Interneurone einher. Die Krankheit
beginnt mit Bewegungsunruhe (Extremitäten, Mimik, später Kopf und
Rumpf), die sich später zu plötzlich einsetzendem, unwillkürlichen Bewegungen steigern (choreatische Hyperkinesie: kurze, irreguläre Bewegungen, welche die Willkürmotorik unterbrechen). Im weiteren Verlauf kann es zu Akinesie und Rigor kommen.
Abbildung), sowie auch cholinerger
Interneurone einher. Die Krankheit
beginnt mit Bewegungsunruhe (Extremitäten, Mimik, später Kopf und
Rumpf), die sich später zu plötzlich einsetzendem, unwillkürlichen Bewegungen steigern (choreatische Hyperkinesie: kurze, irreguläre Bewegungen, welche die Willkürmotorik unterbrechen). Im weiteren Verlauf kann es zu Akinesie und Rigor kommen.  Athetose
Athetose  ist eine relativ häufig auftretende extrapyramidal-motorische Störung,
bedingt durch Defekte im Bereich der Basalganglien, insbesondere des Striatum (Pallidum), die oft auf perinatale
Schädigungen zurückzuführen sind.
Zu den Symptomen gehören u.a. langsame,
schraubende Bewegungen der Gliedmaßen und des Rumpfes, stolpernder
Gang, Überstreckungen, Spreizung der Finger, Grimassieren bei
geöffnetem Mund.
ist eine relativ häufig auftretende extrapyramidal-motorische Störung,
bedingt durch Defekte im Bereich der Basalganglien, insbesondere des Striatum (Pallidum), die oft auf perinatale
Schädigungen zurückzuführen sind.
Zu den Symptomen gehören u.a. langsame,
schraubende Bewegungen der Gliedmaßen und des Rumpfes, stolpernder
Gang, Überstreckungen, Spreizung der Finger, Grimassieren bei
geöffnetem Mund.  Ballismus
Ballismus  tritt meist (infolge Blutung in einen nucl.
subthalamicus) einseitig als Hemiballismus auf (oder nur eine Extremität betreffend: Monoballismus) und bedingt
“schleudernde” Bewegungen im Arm-, Bein-, Schulter- oder Beckengürtelbereich.
tritt meist (infolge Blutung in einen nucl.
subthalamicus) einseitig als Hemiballismus auf (oder nur eine Extremität betreffend: Monoballismus) und bedingt
“schleudernde” Bewegungen im Arm-, Bein-, Schulter- oder Beckengürtelbereich.  Die Basalganglien (Striatum, Pallidum, nucleus subthalamicus) dienen
motorischer Feinabstimmung. Sie hemmen Neurone in Thalamus und Hirnstamm
Die Basalganglien (Striatum, Pallidum, nucleus subthalamicus) dienen
motorischer Feinabstimmung. Sie hemmen Neurone in Thalamus und Hirnstamm Das Striatum wird glutamaterg angeregt (Sensorik, Großhirnrinde) und
inhibiert GABAerg Pallidum und substantia nigra. Die substantia nigra
hemmt das Striatum (nigro-striatales System: bei Ausfall oder
Dopaminmangel Parkinson-Syndrom) und hebt seinerseits die Hemmung des
Thalamus durch GABAerge Neurone (inneres
Pallidum, substantia nigra pars reticulata) auf (Disinhibition)
Das Striatum wird glutamaterg angeregt (Sensorik, Großhirnrinde) und
inhibiert GABAerg Pallidum und substantia nigra. Die substantia nigra
hemmt das Striatum (nigro-striatales System: bei Ausfall oder
Dopaminmangel Parkinson-Syndrom) und hebt seinerseits die Hemmung des
Thalamus durch GABAerge Neurone (inneres
Pallidum, substantia nigra pars reticulata) auf (Disinhibition) Die Basalganglien haben zwei Ausgangssysteme: Die Basalganglien haben zwei Ausgangssysteme:-- Der GABAerge direkte Weg projiziert aus dem Striatum in das innere Pallidum und in die Substantia nigra (pars reticulata) und von hier (ebenfalls GABAerg) zu motorischen Thalamuskernen, die dadurch disinhibiert (aktiviert) werden -- Indirekter Weg: GABAerge Projektionen aus dem Striatum in das äußere Pallidum und von dort - ebenfalls GABAerg - in den nucleus subthalamicus. Dieser regt das Pallidum glutamaterg an, und dieses hemmt motorische Thalamuskerne  Die substantia nigra beeinflusst die Steuerung von Augenbewegungen,
motorische Planung, Lernen und Motivation. Sie steht unter der
Kontrolle des Striatums, auf das sie dopaminerg zurückprojiziert. Ihre
spontanaktive pars reticulata hemmt Thalamus, obere Vierhügel und pars
compacta. Diese erregt dopaminerg das Striatum (nigro-striatales System)
Die substantia nigra beeinflusst die Steuerung von Augenbewegungen,
motorische Planung, Lernen und Motivation. Sie steht unter der
Kontrolle des Striatums, auf das sie dopaminerg zurückprojiziert. Ihre
spontanaktive pars reticulata hemmt Thalamus, obere Vierhügel und pars
compacta. Diese erregt dopaminerg das Striatum (nigro-striatales System) Dopaminrezeptoren befinden sich auf zahlreichen Neuronen (Striatum,
limbisches System, nucl. accumbens, Groß- und Kleinhirnhirnrinde).
Teils regen sie die Adenylatzyklase an (D1-Gruppe), teils hemmen sie
diese (D2-Gruppe). Sie sind wichtig für Verhaltensmotorik, räumliches
Gedächtnis, Kognition, Gedächtnis, Lernen, Motivation, Lustempfinden,
Steuerung neuroendokriner Signale, zerebrales Belohnungssystem
Dopaminrezeptoren befinden sich auf zahlreichen Neuronen (Striatum,
limbisches System, nucl. accumbens, Groß- und Kleinhirnhirnrinde).
Teils regen sie die Adenylatzyklase an (D1-Gruppe), teils hemmen sie
diese (D2-Gruppe). Sie sind wichtig für Verhaltensmotorik, räumliches
Gedächtnis, Kognition, Gedächtnis, Lernen, Motivation, Lustempfinden,
Steuerung neuroendokriner Signale, zerebrales Belohnungssystem Mb. Parkionson, Huntington-Chorea, Athetose und Ballismus liegen Ausfallserscheinungen im Basalgangliensystem zugrunde Mb. Parkionson, Huntington-Chorea, Athetose und Ballismus liegen Ausfallserscheinungen im Basalgangliensystem zugrunde
|
