




 Atmung und Hämoglobin, Blutgaswerte
Atmung und Hämoglobin, Blutgaswerte
 bradytroph: βραδυ- = langsam, τροφή = Ernährung
bradytroph: βραδυ- = langsam, τροφή = Ernährung| Hämoglobin
bringt Sauerstoff in das Gewebe; hier entsteht Kohlendioxid, das den pH-Wert
senkt und zum Teil physikalisch gelöst, zum Teil als Bicarbonat, zum
Teil an Hämoglobin gebunden zur Lunge transportiert wird. Blutgastransport und
Säure-Basen-Haushalt sind eng miteinander verknüpft. Bei der Blutgasanalyse werden die Werte für pCO2, pH, pO2 sowie Blutpuffer (Pufferbasen, buffer bases) bestimmt.
Dabei nimmt Bicarbonat die erste Stelle ein (~50% der pufferfähigen
Valenzen), gefolgt von Hämoglobin, Plasmaproteinen und Phosphat. Was den O2-Bedarf betrifft, haben verschiedene Gewebe unterschiedlichen spezifischen Sauerstoffverbrauch (ml O2 pro Minute pro 100 Gramm Gewebe) - umso größer, je höher der normierte Energieumsatz ist. Spitzenreiter ist das Myokard, das bei körperlicher Ausbelastung mehr als 50 ml/min/100g O2-Verbrauch erreichen kann; der Skelettmuskel schafft höchstens 15, die Gehirnrinde 10, die Nierenrinde 7, die Leber 5 ml/min/100g. Der Stoffwechsel ist säureüberschüssig; in erster Linie entfernt der Körper saure Valenzen über CO2, also die Atmung (etwa 15 Mol pro Tag). Andere ("nichtflüchtige") Säuren werden metabolisiert bzw. über die Nieren ausgeschieden (0,07 M/d - im Vergleich zur Kohlensäureabatmung knapp 0,5%). Das Hämoglobin ist wegen seiner Säuretransportfunktion ein wichtiger Player im Säure-Basen-Haushalt. Seine Pufferfähigkeit nimmt zu, wenn es Sauerstoff abgibt (Haldane-Effekt) - damit entlastet es die anderen Pufferbasen und trägt die Hauptlast (2/3) der physiologischen pH-Kompensation. |
 Referenzwertetabelle
Referenzwertetabelle  Spezifischer Sauerstoffverbrauch
Spezifischer Sauerstoffverbrauch  Pufferung
Pufferung  pO2 im Gewebe
pO2 im Gewebe
 Core messages
Core messages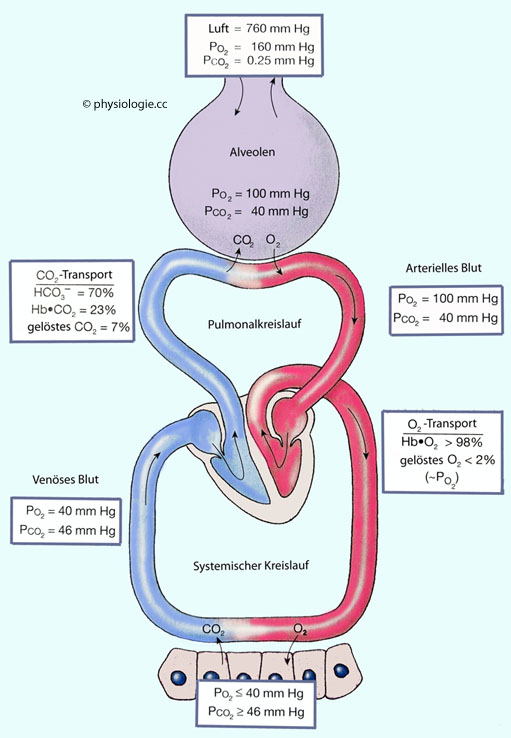
 Abbildung: Gastransport durch den Körper
Abbildung: Gastransport durch den Körper
| Einatemluft (Seehöhe, trocken) |
21 kPa |
159 mmHg |
| Alveolärer pO2 |
13,3 kPa |
100 mmHg |
| Arterieller pO2 | 12,5 kPa (11,2-13,9) |
94 mmHg (84-104) |
| Alveolo-arterieller pO2-Grandient |
<2 kPa |
<15 mmHg |
| Arterielle Sauerstoffsättigung |
>97% |
|
| Arterieller Sauerstoffgehalt |
200 ml/l |
20 ml/dl |
| pCO2 Einatemluft |
0,03 kPa |
0,2 mmHg |
| pCO2 Alveolarluft / arterielles Blut |
5,3 kPa (4,7-6,1) |
40 mmHg (35-45) |
| Arterieller CO2-Gehalt | 480 ml/l |
48 ml/dl |
| Arterieller [H+] / pH |
35-45 nM |
7,35-7,45 |
| Gemischt-venöser pO2 (Ruhe) |
5,3 kPa |
40 mmHg |
| Gemischt-venöser O2-Gehalt (Ruhe) | 150 ml/l |
15 ml/dl |
| Gemischt-venöse O2-Sättigung | 75% |
|
| Gemischt-venöser pCO2 (Ruhe) | 6,1 kPa |
46 mmHg |
| Gemischt-venöser CO2-Gehalt (Ruhe) | 520 ml/l |
52 ml/dl |
| Arterieller [HCO3-] |
24 mM (21-27) |
 Zu den Atemgas-Bindungscharakteristika des Hämoglobins s. dort
Zu den Atemgas-Bindungscharakteristika des Hämoglobins s. dort
 Abbildung: Vergleich Sauerstoffverbrauch vs. Herzminutenvolumen
Abbildung: Vergleich Sauerstoffverbrauch vs. Herzminutenvolumen
| Spezifischer O2-Verbrauch in Ruhe: ~4 ml/min/kg |
 : 1,34 ml O2
/ g Hb) =200 ml Sauerstoff pro Liter Blut (20 Vol%).
: 1,34 ml O2
/ g Hb) =200 ml Sauerstoff pro Liter Blut (20 Vol%).
 Abbildung: Minütlicher Sauerstoffverbrauch von jeweils 100g Gewebe
Abbildung: Minütlicher Sauerstoffverbrauch von jeweils 100g Gewebe Graue und weiße Substanz im Gehirn
Graue und weiße Substanz im Gehirn Herzmuskel bei körperlicher Ruhe und bei Maximalbelastung
Herzmuskel bei körperlicher Ruhe und bei Maximalbelastung Niere: Rinde, äußere und innere Markzone
Niere: Rinde, äußere und innere Markzone Leber
Leber Milz
Milz Muskel im Ruhezustand und bei maximaler Belastung
Muskel im Ruhezustand und bei maximaler Belastung
 (d.h.
Energieverbrauch) ab: So beträgt der spezifische Sauerstoffverbrauch
(d.h.
Energieverbrauch) ab: So beträgt der spezifische Sauerstoffverbrauch  im Gehirn 3,5 ml O2 /min/100g - mit einer 10fachen Diskrepanz zwischen Rinde (~10 ml/min/100g) und weißer Substanz (~1 ml/min/100g)
im Gehirn 3,5 ml O2 /min/100g - mit einer 10fachen Diskrepanz zwischen Rinde (~10 ml/min/100g) und weißer Substanz (~1 ml/min/100g) im Herzmuskel 10 ml O2 /min/100g
bei körperlicher Ruhe, der Wert kann bei Ausbelastung mehr als 5-fach
steigen (>50 ml/min/100g)
im Herzmuskel 10 ml O2 /min/100g
bei körperlicher Ruhe, der Wert kann bei Ausbelastung mehr als 5-fach
steigen (>50 ml/min/100g) in der Nierenrinde ~7 ml O2 /min/100g, im Nierenmark wesentlich weniger (die Nieren beanspruchen ~7% des gesamten Ruhe-Sauerstoffverbrauchs des Körpers)
in der Nierenrinde ~7 ml O2 /min/100g, im Nierenmark wesentlich weniger (die Nieren beanspruchen ~7% des gesamten Ruhe-Sauerstoffverbrauchs des Körpers) die Leber hat einen fünfmal höheren Wert (~5 ml/min/100g) als die Milz, was sich mit ihrer hohen metabolischen Aktivität erklärt
die Leber hat einen fünfmal höheren Wert (~5 ml/min/100g) als die Milz, was sich mit ihrer hohen metabolischen Aktivität erklärt im ruhenden Skelettmuskel 0,3 ml/min/100g, bei Aktivität steigt der Wert auf bis zu 15 ml O2 /min/100g (bis 50fach!) - das ist möglich, weil
sowohl die Durchblutung (bis 20-fach) als auch die arterio-venöse
Sauerstoffdifferenz (bis 3-fach) zunehmen (bei hochtrainierten Sportlern sind noch höhere Steigerungen der Durchblutung möglich)
im ruhenden Skelettmuskel 0,3 ml/min/100g, bei Aktivität steigt der Wert auf bis zu 15 ml O2 /min/100g (bis 50fach!) - das ist möglich, weil
sowohl die Durchblutung (bis 20-fach) als auch die arterio-venöse
Sauerstoffdifferenz (bis 3-fach) zunehmen (bei hochtrainierten Sportlern sind noch höhere Steigerungen der Durchblutung möglich) Auch bei maximaler Ausbelastung liegt der Wert in der Muskulatur nur
um die Hälfte höher als beim Herzmuskel während körperlicher Ruhe - das
maximal belastete Myokard verbraucht pro Gewichtseinheit fast 4mal so
viel Sauerstoff wie ein maximal aktiver Skelettmuskel.
Auch bei maximaler Ausbelastung liegt der Wert in der Muskulatur nur
um die Hälfte höher als beim Herzmuskel während körperlicher Ruhe - das
maximal belastete Myokard verbraucht pro Gewichtseinheit fast 4mal so
viel Sauerstoff wie ein maximal aktiver Skelettmuskel. Beim Abbau von Biomolekülen im Körper entstehen neben Kohlendioxid (CO2) auch andere Stoffe, die in wässriger Lösung Wasserstoffionen (H+) liefern und daher als Säuren bezeichnet werden. Um eine Übersäuerung des Körpers zu verhindern, müssen diese aus dem Körper entfernt werden. Die
Lunge ist das wichtigste säureausscheidende Organ, da sie mit der Ausatemluft große Mengen CO2 eliminiert:
Beim Abbau von Biomolekülen im Körper entstehen neben Kohlendioxid (CO2) auch andere Stoffe, die in wässriger Lösung Wasserstoffionen (H+) liefern und daher als Säuren bezeichnet werden. Um eine Übersäuerung des Körpers zu verhindern, müssen diese aus dem Körper entfernt werden. Die
Lunge ist das wichtigste säureausscheidende Organ, da sie mit der Ausatemluft große Mengen CO2 eliminiert: H+ + HCO3-
H+ + HCO3- Bicarbonat
(HCO3-): Der Bicarbonatwert ist ein Maß für die Gesamt-Pufferkapazität
des Blutes. Er kann vor allem durch die Nierenfunktion verändert werden
Bicarbonat
(HCO3-): Der Bicarbonatwert ist ein Maß für die Gesamt-Pufferkapazität
des Blutes. Er kann vor allem durch die Nierenfunktion verändert werden
 Hämoglobin
Hämoglobin  in
den roten Blutkörperchen. Besonders wichtig, da es physiologischerweise zwei
Drittel der Pufferwirkung im Blut übernimmt (Haldane-Effekt
in
den roten Blutkörperchen. Besonders wichtig, da es physiologischerweise zwei
Drittel der Pufferwirkung im Blut übernimmt (Haldane-Effekt  )
) Plasmaeiweiße (Albumin und Globuline), die wie jedes Protein puffernd wirken
Plasmaeiweiße (Albumin und Globuline), die wie jedes Protein puffernd wirken Phosphat, vorwiegend intrazellulär
Phosphat, vorwiegend intrazellulär
 Der Däne August Krogh
erhielt 1920 den Nobelpreis für Physiologie oder Medizin für "die
Entdeckung des kapillarmotorischen Regulationsmechanismus". Mittels
eines von ihm entwickelten Geräts zur Messung von Gaspartialdrucken in
sehr kleinen Gewebeproben (Mikrotonometrie) konnte er die Wanderung von
Atemgasen entlang von Partialdruckgradienten nachweisen und zeigen,
dass dieser Austausch nicht ein aktiver Prozess ist, sondern auf
Diffusion beruht. Damit widersprach er der damaligen Lehrmeinung, die
u.a. von John Haldane vertreten wurde. Zusammen mit Christian Bohr und Karl Hasselbalch
konnte er weiters feststellen, dass Kohlendioxid die Sauerstoffaufnahme
des Hämoglobins reduziert. Den Nobelpreis brachten ihm seine
Erkenntnisse zur Steuerung der Kapillardurchblutung in Abhängigkeit
vom lokalen Bedarf ein.
Der Däne August Krogh
erhielt 1920 den Nobelpreis für Physiologie oder Medizin für "die
Entdeckung des kapillarmotorischen Regulationsmechanismus". Mittels
eines von ihm entwickelten Geräts zur Messung von Gaspartialdrucken in
sehr kleinen Gewebeproben (Mikrotonometrie) konnte er die Wanderung von
Atemgasen entlang von Partialdruckgradienten nachweisen und zeigen,
dass dieser Austausch nicht ein aktiver Prozess ist, sondern auf
Diffusion beruht. Damit widersprach er der damaligen Lehrmeinung, die
u.a. von John Haldane vertreten wurde. Zusammen mit Christian Bohr und Karl Hasselbalch
konnte er weiters feststellen, dass Kohlendioxid die Sauerstoffaufnahme
des Hämoglobins reduziert. Den Nobelpreis brachten ihm seine
Erkenntnisse zur Steuerung der Kapillardurchblutung in Abhängigkeit
vom lokalen Bedarf ein.
 Abbildung: Krogh'scher Zylinder
Abbildung: Krogh'scher Zylinder
 ,
,  Abbildung): Die höchsten pO2-Werte finden sich in der Nähe des arteriellen Kapillarschenkels, die niedrigsten in der Peripherie um dessen venöses Ende.
Abbildung): Die höchsten pO2-Werte finden sich in der Nähe des arteriellen Kapillarschenkels, die niedrigsten in der Peripherie um dessen venöses Ende. Beispielsweise ist der Sauerstoffpartialdruck in
den besonders intensiv perfundierten Geweben der corpora carotica /
aortica (Messung des arteriellen Sauerstoffpartialdrucks!) und der
Nierenrinde (Perfusion hauptsächlich funktionell!) nahe an den
arteriellen Werten (um 100 mm Hg), während
Beispielsweise ist der Sauerstoffpartialdruck in
den besonders intensiv perfundierten Geweben der corpora carotica /
aortica (Messung des arteriellen Sauerstoffpartialdrucks!) und der
Nierenrinde (Perfusion hauptsächlich funktionell!) nahe an den
arteriellen Werten (um 100 mm Hg), während  der Körperdurchschnitt
bei 40-50 mmHg liegt - entsprechend einer Ausnützung des arteriellen
Sauerstoffangebots von etwa einem Drittel (
der Körperdurchschnitt
bei 40-50 mmHg liegt - entsprechend einer Ausnützung des arteriellen
Sauerstoffangebots von etwa einem Drittel ( s. O2-Bindungskurve des Hämoglobins).
In dieser "mittleren" Zone liegt z.B. weißes Fettgewebe (~50 mmHg).
s. O2-Bindungskurve des Hämoglobins).
In dieser "mittleren" Zone liegt z.B. weißes Fettgewebe (~50 mmHg).
 Besonders hypoxisch wird Gewebe, das den meisten Sauerstoff vom
Hämoglobin abzieht - etwa intensiv aktive Muskulatur.
Besonders hypoxisch wird Gewebe, das den meisten Sauerstoff vom
Hämoglobin abzieht - etwa intensiv aktive Muskulatur. Bei mangelhafter Durchblutung der Mikrozirkulation kann es an Stellen mit dem niedrigsten pO2
kritisch werden, wenn die Nachfrage der Zellen für längere Zeit höher
ist als das Sauerstoffangebot. Je nach Stoffwechselintensität und
spezifischem Sauerstoffbedarf (s. oben) treten Beeinträchtigungen des
Stoffwechsels und Gewebeschäden relativ früh auf, wie z.B. im
ischämischen Gehirn oder Herzmuskel ("tachytrophes" Gewebe) oder erst
verzögert, wie z.B. bei einem abgetrennten Finger ("bradytrophes" Gewebe).
Bei mangelhafter Durchblutung der Mikrozirkulation kann es an Stellen mit dem niedrigsten pO2
kritisch werden, wenn die Nachfrage der Zellen für längere Zeit höher
ist als das Sauerstoffangebot. Je nach Stoffwechselintensität und
spezifischem Sauerstoffbedarf (s. oben) treten Beeinträchtigungen des
Stoffwechsels und Gewebeschäden relativ früh auf, wie z.B. im
ischämischen Gehirn oder Herzmuskel ("tachytrophes" Gewebe) oder erst
verzögert, wie z.B. bei einem abgetrennten Finger ("bradytrophes" Gewebe). 
| Blutgasanalyse nennt man die Bestimmung der Blutwerte, die zur Beurteilung des
Säure-Basen-Status notwendig sind. |

 Abbildung: Entnahme arteriellen Blutes
Abbildung: Entnahme arteriellen Blutes 


| Gemessene Größe | Normalwert (gerundet) |
| pH-Wert (actual-pH) | 7,4 (7,35 - 7,45) |
| pCO2 (actual-pCO2) | 40 mm Hg (35-45 mm Hg) |
| pO2 |
100 mm Hg (>80 mm Hg) abhängig von Alter, Meereshöhe,.. |
 Bicarbonatgehalt ... ~24 mM
Bicarbonatgehalt ... ~24 mM 
 Pufferbasenwert ... ~48 mM (Basenabweichung 0 mM)
Pufferbasenwert ... ~48 mM (Basenabweichung 0 mM)
 Der Sauerstoffbedarf der Körpers beträgt durchschnittlich ≥4 ml/kg/min (bei 70 kg KG ~0,3 l/min). Arterielles Blut ist so gut wie vollständig O2-gesättigt und transportiert bei
~150 g Hämoglobin pro Liter Blut ~20 Vol-% O2 (200 ml/l) (Hüfner-Zahl : 1,34 ml O2 / g Hb).
Im Ruhezustand konsumiert der Körper ~5 Vol-% (arterio-venöse
Sauerstoffdifferenz) der arteriell angebotenen 20 Vol-%, das venöse
Blut bringt ~15 Vol-% zur Lunge zurück (Sauerstoffreserve für
körperliche Belastung), das Hämoglobin ist in venösem Mischblut zu ~75% sauerstoffgesättigt Der Sauerstoffbedarf der Körpers beträgt durchschnittlich ≥4 ml/kg/min (bei 70 kg KG ~0,3 l/min). Arterielles Blut ist so gut wie vollständig O2-gesättigt und transportiert bei
~150 g Hämoglobin pro Liter Blut ~20 Vol-% O2 (200 ml/l) (Hüfner-Zahl : 1,34 ml O2 / g Hb).
Im Ruhezustand konsumiert der Körper ~5 Vol-% (arterio-venöse
Sauerstoffdifferenz) der arteriell angebotenen 20 Vol-%, das venöse
Blut bringt ~15 Vol-% zur Lunge zurück (Sauerstoffreserve für
körperliche Belastung), das Hämoglobin ist in venösem Mischblut zu ~75% sauerstoffgesättigt Spezifischer Sauerstoffverbrauch bezieht sich auf jeweils 100 g Gewebe (Herzmuskel bis 50, Nierenrinde ~7, Leber ~5, Gehirn 3,5, ruhender Skelettmuskel 0,3, aktiver Skelettmuskel bis 15 ml O2 /min/100g ml/min - maximal belastetes Myokard verbraucht pro Gewichtseinheit fast 4mal so viel Sauerstoff wie maximal aktiver Skelettmuskel) Spezifischer Sauerstoffverbrauch bezieht sich auf jeweils 100 g Gewebe (Herzmuskel bis 50, Nierenrinde ~7, Leber ~5, Gehirn 3,5, ruhender Skelettmuskel 0,3, aktiver Skelettmuskel bis 15 ml O2 /min/100g ml/min - maximal belastetes Myokard verbraucht pro Gewichtseinheit fast 4mal so viel Sauerstoff wie maximal aktiver Skelettmuskel) Der Katabolismus produziert Säuren, diese werden aus dem Körper entfernt - überwiegend in Form von CO2 (der pH-Wert des Blutes beeinflusst die Atmung) sowie (soferne angebracht) nichtflüchtige Säurevalenzen mit dem Harn. Blut ist wegen seines Gehalts an Pufferbasen (~48 mM: Bicarbonat, Hämoglobin, Plasmaproteine, Phosphat) leicht alkalisch (pH=7,4). Abweichungen des pH-Werts im Blut werden durch Kompensation (Wiederherstellung des Puffergleichgewichts) korrigiert Der Katabolismus produziert Säuren, diese werden aus dem Körper entfernt - überwiegend in Form von CO2 (der pH-Wert des Blutes beeinflusst die Atmung) sowie (soferne angebracht) nichtflüchtige Säurevalenzen mit dem Harn. Blut ist wegen seines Gehalts an Pufferbasen (~48 mM: Bicarbonat, Hämoglobin, Plasmaproteine, Phosphat) leicht alkalisch (pH=7,4). Abweichungen des pH-Werts im Blut werden durch Kompensation (Wiederherstellung des Puffergleichgewichts) korrigiert Um
Blutkapillaren gibt es im Gewebe Zonen gleichen
Sauerstoffpartialdrucks, entsprechend der Entfernung vom arteriellen
bzw. venösen Ende der Kapillare (Krogh'sche Zylinder). In der Leber
sind Lobuli entsprechend dem jeweiligen pO2 metabolisch organisiert Um
Blutkapillaren gibt es im Gewebe Zonen gleichen
Sauerstoffpartialdrucks, entsprechend der Entfernung vom arteriellen
bzw. venösen Ende der Kapillare (Krogh'sche Zylinder). In der Leber
sind Lobuli entsprechend dem jeweiligen pO2 metabolisch organisiert Blutgasanalyse
nennt man die Bestimmung der Blutwerte, die zur Beurteilung des
Säure-Basen-Status notwendig sind. Durch Einstechen in Ohrläppchen oder
Fingerbeere gewonnenes "Kapillarblut" ist arterielles Blut (es wird in
heparinisierte Proberöhrchen - "Kapillaren" - aufgezogen und spätestens
nach einer Stunde gemessen): pO2 ~100 mmHg, pCO2 ~40 mmHg. Respiratorische Störungen verändern zunächst den pCO2
im Blut, metabolische Störungen bewirken eine Abweichung der
Pufferkapazität. Die Basenabweichung (BE) gibt an, ob zu viel (+:
Alkalose) oder zu wenig (-: Azidose) Pufferbasen im Blut vorhanden
sind. Respiratorische Störungen können von der Niere metabolisch
kompensiert werden, die Atmung kann an der Kompensation metabolischer
Störungen teilnehmen. Mit dem pH-Wert ändern sich oft auch
Elektrolytwerte, zu deren Messung verwendet man meist ionensensitive
Elektroden Blutgasanalyse
nennt man die Bestimmung der Blutwerte, die zur Beurteilung des
Säure-Basen-Status notwendig sind. Durch Einstechen in Ohrläppchen oder
Fingerbeere gewonnenes "Kapillarblut" ist arterielles Blut (es wird in
heparinisierte Proberöhrchen - "Kapillaren" - aufgezogen und spätestens
nach einer Stunde gemessen): pO2 ~100 mmHg, pCO2 ~40 mmHg. Respiratorische Störungen verändern zunächst den pCO2
im Blut, metabolische Störungen bewirken eine Abweichung der
Pufferkapazität. Die Basenabweichung (BE) gibt an, ob zu viel (+:
Alkalose) oder zu wenig (-: Azidose) Pufferbasen im Blut vorhanden
sind. Respiratorische Störungen können von der Niere metabolisch
kompensiert werden, die Atmung kann an der Kompensation metabolischer
Störungen teilnehmen. Mit dem pH-Wert ändern sich oft auch
Elektrolytwerte, zu deren Messung verwendet man meist ionensensitive
Elektroden |
