




 pH-Wert, Metabolismus und Organfunktionen
pH-Wert, Metabolismus und Organfunktionen
 metabolisch: μετα = (her)um, βάλλειν = werfen
metabolisch: μετα = (her)um, βάλλειν = werfen| Organe / Gewebe sind metabolisch, mechanisch, neuroendokrin oder immunologisch miteinander verknüpft. Beispiele: -- Fettsäuren dienen Skelett- und Herzmuskel, Glucose vor allem dem Gehirn als Energiequelle; diese Substrate werden von der Leber nachgeliefert -- Atmung, Nieren-, Leber-, Pankreas-, Magen- und Darmfunktion stimmen ihre Funktionen bei der Balancierung des pH-Wertes aufeinander ab; interorganischer Austausch betrifft vor allem Kohlendioxid, Ammonium, Harnstoff, Bicarbonat -- Haut, Schleimhäute und lymphatische Organe kooperieren bei der Abwehr potentieller Infektionserreger Ein klinisch besonders relevanter Begleiteffekt ist die Wirkung des pH-Wertes auf den Kaliumspiegel: Steigt bei azidotischer Stoffwechsellage die H+-Ionenkonzentration (sinkt der pH-Wert) in den Zellen (z.B. Myozyten), kompromittiert das - über verschiedene Wirkungen - die Fähigkeit der Zelle, Kaliumionen aufzunehmen. Das senkt den intrazellulären, und hebt den extrazellulären Kaliumspiegel (Hyperkaliämie). Azidose steigert, Alkalose senkt den Kaliumspiegel im Blut - eine Infusion von Pufferbasen senkt den Kaliumspiegel. Deshalb erübrigt sich oft die Behandlung einer Hyperkaliämie bei Azidose: Die Normalisierung des pH befördert automatisch Kalium aus dem Extra- in den Intrazellulärraum. |
 Extrazellulärer vs. intrazellulärer pH pH und Kaliumwert
Extrazellulärer vs. intrazellulärer pH pH und Kaliumwert
 vgl. dort
vgl. dort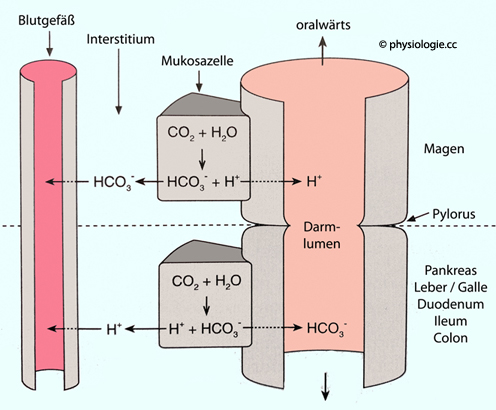
 Abbildung: Säurebilanz des gastrointestinalen Systems
Abbildung: Säurebilanz des gastrointestinalen Systems
 intrazellulär: Zytoplasma (pH=7,2), Lysosomen (pH=5-6), Mitochondrien (pH=8)
intrazellulär: Zytoplasma (pH=7,2), Lysosomen (pH=5-6), Mitochondrien (pH=8)  extrazellulär: Blutplasma (pH=7,3), Pankreassaft (pH=8,2), Magenlumen (pH bis ~1).
extrazellulär: Blutplasma (pH=7,3), Pankreassaft (pH=8,2), Magenlumen (pH bis ~1). , Weitertransport,
Ausscheidung). Dabei kommt es zur Kooperation zwischen verschiedenen
Geweben und Organen.
, Weitertransport,
Ausscheidung). Dabei kommt es zur Kooperation zwischen verschiedenen
Geweben und Organen.  Leber
Leber  Nieren
Nieren Fettgewebe
Fettgewebe Muskulatur
Muskulatur Herz
Herz Gehirn
Gehirn 
 Abbildung: Metabolische Verbindung zwischen Herzmuskel, Nervensystem, Fett- und Muskelgewebe
Abbildung: Metabolische Verbindung zwischen Herzmuskel, Nervensystem, Fett- und Muskelgewebe
 Insbesondere die Energieversorgung des Gehirns hängt primär von
laufender Versorgung mit Glucose (und Ketonkörpern
Insbesondere die Energieversorgung des Gehirns hängt primär von
laufender Versorgung mit Glucose (und Ketonkörpern  ) ab, es ist ein
reiner Verbraucher; das andere Extrem ist das Fettgewebe, das den
größten Speicher von Stoffwechselenergie darstellt (Energiebedarf für
mehrere Wochen,
) ab, es ist ein
reiner Verbraucher; das andere Extrem ist das Fettgewebe, das den
größten Speicher von Stoffwechselenergie darstellt (Energiebedarf für
mehrere Wochen,  s. dort).
s. dort). Stellt
die Leber auf Hungerstoffwechsel um (Substratmangel wie im Hunger, oder
mangelnder Eintritt von Substrat in die Zellen wie bei Diabetes
mellitus), entstehen aus Fetten
Ketonkörper
(Acetessigsäure, Beta-Hydroxy-Buttersäure). Diese können vom
Nervengewebe zur Energiegewinnung herangezogen werden, nachdem eine
entsprechende Umstellung (Expression der nötigen Enzyme) erfolgt
ist.
Stellt
die Leber auf Hungerstoffwechsel um (Substratmangel wie im Hunger, oder
mangelnder Eintritt von Substrat in die Zellen wie bei Diabetes
mellitus), entstehen aus Fetten
Ketonkörper
(Acetessigsäure, Beta-Hydroxy-Buttersäure). Diese können vom
Nervengewebe zur Energiegewinnung herangezogen werden, nachdem eine
entsprechende Umstellung (Expression der nötigen Enzyme) erfolgt
ist. Abbildung): Dringen vermehrt H+-Ionen
aus dem Interstitium in Zellen ein, verringern sie z.B. an Muskelzellen
den Na-K-2Cl-Symport zusammen mit der Na-K-ATPase und senken so die
Kaliumaufnahme. Gleichzeitig treiben sie K+ von seiner Bindung an Protein und in den Extrazellulärraum. Resultat ist ein Anstieg des extrazellulären Kaliumspiegels.
Abbildung): Dringen vermehrt H+-Ionen
aus dem Interstitium in Zellen ein, verringern sie z.B. an Muskelzellen
den Na-K-2Cl-Symport zusammen mit der Na-K-ATPase und senken so die
Kaliumaufnahme. Gleichzeitig treiben sie K+ von seiner Bindung an Protein und in den Extrazellulärraum. Resultat ist ein Anstieg des extrazellulären Kaliumspiegels.
 Abbildung: Wie Azidose den Serum-K-Spiegel hebt
Abbildung: Wie Azidose den Serum-K-Spiegel hebt
 Das bedeutet z.B., dass eine Reduktion des pH-Wertes im Blut von 7,4
auf 7,0 einen Serum-Kaliumwert von 4,5 auf etwa 6,5 erhöhen würde.
Das bedeutet z.B., dass eine Reduktion des pH-Wertes im Blut von 7,4
auf 7,0 einen Serum-Kaliumwert von 4,5 auf etwa 6,5 erhöhen würde.
 Im Magen sezernieren Belegzellen (parietal cells) -
getrennt - H-Ionen und Chloridionen. Dabei wird ein
pH-Gradient von >6 überwunden, d.h. ein Unterschied in der
Protonenkonzentration von bis zu über 1 zu einer Million. Dies ist
einer der größten Konzentrationsunterschiede, die über eine Biomembran
aufgebaut werden kann.
Im Magen sezernieren Belegzellen (parietal cells) -
getrennt - H-Ionen und Chloridionen. Dabei wird ein
pH-Gradient von >6 überwunden, d.h. ein Unterschied in der
Protonenkonzentration von bis zu über 1 zu einer Million. Dies ist
einer der größten Konzentrationsunterschiede, die über eine Biomembran
aufgebaut werden kann. Die Nieren sind an der nicht-respiratorischen Regulation des
pH-Gleichgewichts prominent beteiligt (tubuläre Mechanismen), so dass
sich Nierenerkrankungen in vielfacher Weise im Säure-Basen-Haushalt
bemerkbar machen können - z.B. tubuläre Azidose.
Die Nieren sind an der nicht-respiratorischen Regulation des
pH-Gleichgewichts prominent beteiligt (tubuläre Mechanismen), so dass
sich Nierenerkrankungen in vielfacher Weise im Säure-Basen-Haushalt
bemerkbar machen können - z.B. tubuläre Azidose.
 Der pH-Wert beträgt im Zytoplasma 7,2, in Lysosomen 5-6, Mitochondrien
~8, Blutplasma 7,3, arteriellem Blut 7,4, Pankreassaft 8,2, Magensekret ~1 Der pH-Wert beträgt im Zytoplasma 7,2, in Lysosomen 5-6, Mitochondrien
~8, Blutplasma 7,3, arteriellem Blut 7,4, Pankreassaft 8,2, Magensekret ~1  Metabolische Interdependenz besteht zwischen allen Geweben, vor allem Leber, Nieren, Fettgewebe, Muskulatur, Gehirn: Muskelgewebe
konsumiert Fettsäuren und Glucose, das
Gehirn Glucose, alle auch fallweise Ketonkörper. Die Leber bildet postabsorptiv
aus Fettsäuren und Glycerin (aus Fettgewebe) sowie
Aminosäuren Glucose; Acetessigsäure und ß-Hydroxy-Buttersäure werden
nach
Expression der nötigen Enzyme (längerer Hungerzustand) zur
Energiegewinnung herangezogen (vor allem im Gehirn) und belasten den
Stoffwechsel (metabolische Azidose). Die Niere scheidet saure Nicht-CO2-Valenzen aus (Ammonium, Sulfat, Phosphat) Metabolische Interdependenz besteht zwischen allen Geweben, vor allem Leber, Nieren, Fettgewebe, Muskulatur, Gehirn: Muskelgewebe
konsumiert Fettsäuren und Glucose, das
Gehirn Glucose, alle auch fallweise Ketonkörper. Die Leber bildet postabsorptiv
aus Fettsäuren und Glycerin (aus Fettgewebe) sowie
Aminosäuren Glucose; Acetessigsäure und ß-Hydroxy-Buttersäure werden
nach
Expression der nötigen Enzyme (längerer Hungerzustand) zur
Energiegewinnung herangezogen (vor allem im Gehirn) und belasten den
Stoffwechsel (metabolische Azidose). Die Niere scheidet saure Nicht-CO2-Valenzen aus (Ammonium, Sulfat, Phosphat) Wenn Wasserstoffionen vermehrt in Zellen eindringen (Azidose), reduzieren sie deren Kaliumaufnahme (Na/K-Pumpe, Na/K/2Cl-Symport) und
verdängen K+ von der Bindung an Protein. K+ gelangt vermehrt in
den Extrazellulärraum, wo der Kaliumspiegel ansteigt (Hyperkaliämie). Insgesamt gilt: Änderungen des Blut-pH um [0,1] verändern den Kaliumspiegel um ~0,5 mM
(z.B. Blut-pH 7,4 → 7,0: Serum-Kalium 4,5 → 6,5 mM). Wird die Azidose behoben, nimmt der Kaliumspiegel entsprechend ab Wenn Wasserstoffionen vermehrt in Zellen eindringen (Azidose), reduzieren sie deren Kaliumaufnahme (Na/K-Pumpe, Na/K/2Cl-Symport) und
verdängen K+ von der Bindung an Protein. K+ gelangt vermehrt in
den Extrazellulärraum, wo der Kaliumspiegel ansteigt (Hyperkaliämie). Insgesamt gilt: Änderungen des Blut-pH um [0,1] verändern den Kaliumspiegel um ~0,5 mM
(z.B. Blut-pH 7,4 → 7,0: Serum-Kalium 4,5 → 6,5 mM). Wird die Azidose behoben, nimmt der Kaliumspiegel entsprechend ab Im Magen überwinden Belegzellen einen pH-Gradienten von >6 (Anstieg der [H+] um >106).
Die Nieren regulieren den pH über tubuläre Mechanismen. Der pH wirkt
sich auf den Calciumhaushalt aus: Je niedriger (höhere [H+],
desto weniger Ca++ bindet an Protein (Konkurrenz um anionische Bindungsvalenzen), der Anteil freier Ca++-Ionen (biologisch aktiv) nimmt zu Im Magen überwinden Belegzellen einen pH-Gradienten von >6 (Anstieg der [H+] um >106).
Die Nieren regulieren den pH über tubuläre Mechanismen. Der pH wirkt
sich auf den Calciumhaushalt aus: Je niedriger (höhere [H+],
desto weniger Ca++ bindet an Protein (Konkurrenz um anionische Bindungsvalenzen), der Anteil freier Ca++-Ionen (biologisch aktiv) nimmt zu |
