

Eine Reise durch die Physiologie - Wie der Körper des Menschen funktioniert

Hirnentwicklung,
Lernen, neuronale Plastizität
© H. Hinghofer-Szalkay
 Ammonshorn (cornu Ammonis): Nach dem ägyptischen Gott Amun, der u.a. in der Form eines Widders verehrt wurde
Ammonshorn (cornu Ammonis): Nach dem ägyptischen Gott Amun, der u.a. in der Form eines Widders verehrt wurde
(Endo)Cannabinoide: ἔνδον = innen, cannabis sativa = Hanf
Engramm: ἔν = hinein, γράμμα = Geschriebenes
Gyrus dentatus: Seine Fortsätze geben ihm eine "gezähnte" Form* (dentatus)
Hippocampus: ἵππος= Pferd, καμπή = Krümmung (Seepferdchen, Meeresmonster)
Korsakoff-Syndrom: Sergei Korsakow
Netrine: netr (Sanskrit) = Führer
Papez-Kreis: James Papez
Pawlow-Versuch: Iwan P. Pawlow
Reelin: Nach dem torkelnden (to reel) Gang Reelin-mutierter Mäuse
Schaffer-Kollaterale: Károly Schaffer
Semaphorine: σημα = Zeichen, φορός = Träger
Wernicke-Enzephalopathie: Carl Wernicke
Sinnesmeldungen werden kortikal für Sekundenbruchteile als sensorisches Gedächtnis gespeichert. Anschließend halten Neuronengruppen im Präfrontalhirn Gedächtnisinhalte über
reziproke Verbindungen mit sekundären Rindenfeldern verfügbar (Kurzzeitgedächtnis), während Verbindungen zur formatio reticularis zusätzlichen Informationsfluss über den Thalamus reduzieren und die Kapazität des Kurzzeitgedächtnisses limitieren (Fokussierung der Aufmerksamkeit).
Ein Teil der im Kurzzeitgedächtnis gehaltenen Information wird dauerhaft gespeichert (Langzeitgedächtnis). Dieses teilt man ein in ein

-- deklaratives (explizites, bewusstes) Gedächtnis, vorwiegend im Temporallappen (Hippocampus) gespeichert (semantisch - Fakten, Bedeutungen; episodisch - was, wann, wo, warum), und ein

-- nicht-deklaratives (implizites) - "wissen wie". Das prozedurale Gedächtnis betrifft motorische Fertigkeiten und wird vorwiegend vom Striatum (nucleus caudatus und Putamen) gespeichert (das Kleinhirn verwaltet motorische Reflexe).
Der Hippocampus speichert mit Hilfe reziproker Verbindungen mit dem gyrus parahippocampalis kontextuelle und episodische Gedächtnisinhalte
und baut deklaratives Gedächtnis auf. Dazu bedarf es synaptischer
Verstärkungen (Langzeitpotenzierung) und Neubildungen (Synapsen,
lernfähige Kreisschaltungen).
Glutamatrezeptoren
(NMDAR) spielen für die Gedächtnisbildung eine Schlüsselrolle: Sie sind
"Koinzidenzdetektoren" - sie öffnen, wenn sowohl der präsynaptische als
auch der postsynaptische Teil der Synapse gleichzeitig oder knapp
nacheinander aktiviert wird. Je häufiger das vorkommt, desto intensiver
ist der synaptische Effekt (spike-timing dependent plasticity).
Längerfristige Veränderungen können sowohl im Sinne einer Verstärkung (Langzeitpotenzierung) oder Abschwächung der Synapsenwirkung erfolgen (Langzeitdepression).
|
Überblick  Arten von Gedächtnis
Arten von Gedächtnis  Synaptische Plastizität, Langzeitpotenzierung / Langzeitdepression
Synaptische Plastizität, Langzeitpotenzierung / Langzeitdepression  Hippocampus und Erinnerung
Hippocampus und Erinnerung  Weitere am Gedächtnis beteiligte Hirnregionen
Weitere am Gedächtnis beteiligte Hirnregionen  Arten des Lernens
Arten des Lernens

Netrine / Semaphorine  Gyrus parahippocampalis
Gyrus parahippocampalis  Koinzidenzdetektion
Koinzidenzdetektion  Entorhinaler Cortex
Entorhinaler Cortex  Langzeitpotenzierung
Langzeitpotenzierung  Langzeitdepression
Langzeitdepression
 Praktische Aspekte
Praktische Aspekte  Core messages
Core messages
Bis zum 5. Schwangerschaftsmonat bildet der Fetus besonders viele neue Neurone aus (pro Minute bis zu eine Viertelmillion). Damit ihre Axone zu
ihren Zielneuronen finden, muss eine räumlich-zeitlich
abgestimmte Expression molekularer Signale stattfinden: Netrine sorgen für das richtige Auswachsen embyonaler Neurone; Semaphorine üben steuernde und organisierende Wirkungen aus; Zelladhäsionsmoleküle helfen bei der gegenseitigen Fixierung von Leit- und geführten Zellen.
 Das korrekte Auswachsen von Axonen wird durch spezielle chemotrope Proteine gesteuert, deren
Das korrekte Auswachsen von Axonen wird durch spezielle chemotrope Proteine gesteuert, deren Konzentrationsgradient
auf die Bewegung bzw. Wachstumsrichtung von Zielzellen entweder anziehend (attraction) oder abweisend wirken (repulsion). Sie werden z.T. sezerniert und werden über
Rezeptoren an der Zellmembran von Zielzellen erkannt und
beeinflusst die Richtung ihrer Fortbewegung bzw. ihres Vorwachsens.
Netrine 
ähneln in ihrem Aufbau dem
extrazellulären Matrixprotein Laminin und helfen den Wachstumskegeln vorwachsender Neuriten, ihre synaptischen Ziele zu finden.
Semaphorine  leiten nicht nur - sowohl efferente als auch afferente - Axone bei
Entwicklung und Heilung, sondern erfüllen auch Aufgaben im Rahmen von
Immunfunktionen und Knochenwachstum.
leiten nicht nur - sowohl efferente als auch afferente - Axone bei
Entwicklung und Heilung, sondern erfüllen auch Aufgaben im Rahmen von
Immunfunktionen und Knochenwachstum.
Bei der Geburt ist bereits der vollständige Satz von fast 100 Milliarden Nervenzellen
gegeben, die Vernetzung untereinander muss sich allerdings über viele
Jahre weiterentwickeln.
Um die auf das Gehirn ständig einströmende Flut an Information sinnvoll
zu organisieren, ist es notwendig, diese nicht nur von Augenblick zu
Augenblick zu verwalten (etwa durch Auslösung von Reflexen), sondern
einen Teil auch so abzuspeichern, dass Spuren solcher Information
("Engramme", Erfahrungen) zu einem späteren Zeitpunkt in aktuelle
Entscheidungsfindungsprozesse einfließen können. Diese Fähigkeit,
Information aufzunehmen (encoding), zu speichern (storage), zu vertiefen (consolidation) und schließlich abzurufen (retrieval), wird als Gedächtnis bezeichnet.
Diese Fähigkeiten sind über weite Teile des Gehirns verteilt. Eine zentrale Rolle spielt das limbische System, insbesondere der Hippocampus;
aber auch Teile des Frontal-, Parietal- und Temporalcortex
(deklaratives Gedächtnis) sowie Basalganglien und Kleinhirn
(prozedurales Gedächtnis) sind beteiligt und kooperieren bei den
verschiedenen Manifestationen des Lernens und Erinnerns.
Bezogen auf die Dauer (Nachhaltigkeit) unterscheidet man
Kurz- (sensorisches, Arbeits-) und Langzeitgedächtnis (sekundär,
tertiär), letzteres mit expliziten (deklarativen) und impliziten
Anteilen:
Arten von Gedächtnis
Kurzzeitgedächtnis  Langzeitgedächtnis
Langzeitgedächtnis
Das
Gehirn verfügt über mehrere unterschiedliche Gedächtnissysteme. Wie
weiter unten genauer geschildert, haben das hippocampale System
(Hippocampus und umliegender entorhinaler Cortex) entscheidende
Bedeutung für deklaratives / episodisches, die Mandelkerne
für emotionales Gedächtnis, das Striatum für prozedurales / implizites
Gedächtnis. Das Präfrontalhirn kümmert sich um Aspekte des
Arbeitsgedächtnisses ("Faktenwissen"), ventral-laterale Regionen um die
Speicherung und das Aufrufen von Gedächtnisinhalten. Prozedurale
Aspekte (Bewegungsmuster) werden in motorischen Gehirnarealen
(Mortorcortex, Kleinhirn) gespeichert und verwaltet.
Ein anderer Aspekt gruppiert nach der Zeitspanne der Speicherung und Abrufbarkeit von Gedächtnisinhalten und -leistungen:
Kurzzeitgedächtnis
 Information von den Sinnesorganen gelangt zunächst in das Kurzzeitgedächtnis. Es wird vom sensorimotorischen sowie präfrontalen Cortex verwaltet; zum Aufbau des Gedächtnisses (Lernprozess) ist die Hippocampusformation unverzichtbar.
Information von den Sinnesorganen gelangt zunächst in das Kurzzeitgedächtnis. Es wird vom sensorimotorischen sowie präfrontalen Cortex verwaltet; zum Aufbau des Gedächtnisses (Lernprozess) ist die Hippocampusformation unverzichtbar.
 Abbildung: Erinnerungen speichernde Gehirnregionen
Nach einer Vorlage bei qbi.uq.edu.au/brain-basics
Abbildung: Erinnerungen speichernde Gehirnregionen
Nach einer Vorlage bei qbi.uq.edu.au/brain-basics
Kurzfristiges Arbeitsgedächtnis wird im Präfrontalhirn verwaltet.
Explizites (deklaratives,
episodisches) und semantisches Gedächtnis (Faktenwissen) werden
von Neocortex, Mandelkernen (amygdalae) und Hippocampus deponiert und
sind hier abrufbar.
Implizites
(nicht-deklaratives, insbesondere motorisches) Gedächtnis ruht in
Zentren der Bewegungskontrolle (Basalganglien, Kleinhirn)

Im
sensorischen (ikonographischen) Gedächtnis werden
Sinnesmeldungen für einige Sekundenbruchteile gespeichert (sensory buffers). Man schätzt,
dass für einen Erinnerungsvorgang 10 bis 100 Millionen Nervenzellen
aktiviert werden. Dabei wird z.B. ein visuelles Informationspaket, das
im Okzipitallappen (Sehrinde) auftaucht, parietal auf "wo" und temporal
auf "was" analysiert, bevor es weiter zum Präfrontalhirn gelangt, wo
das Kurzzeitgedächtnis verwaltet wird.
Das Eintreffen aktueller Gedächtnisinhalte im Präfrontalcortex aktiviert hier Neuronengruppen, die über reziproke Verbindungen mit sekundären Rindenfeldern die Repräsentation der
betreffenden Gedächtnisinhalte verfügbar halten. Direkte Verbindungen
der präfrontalen Rinde zur formatio reticularis sorgen dafür, dass der
Informationsfluss über den Thalamus währenddessen gedämpft wird
(limitierte Kapazität des Kurzzeitgedächtnisses). Diese Fokussierung fördert selektive Aufmerksamkeit.
Störungen bedingen
leichte Ablenkbarkeit, verminderte Speicherkapazität und erschwertes
Lernen.
Das
bewusste Arbeitsgedächtnis tritt erstmals 7-12 Monate postpartal auf
und entwickelt sich bis zur Adoleszenz.
 Ein Teil
der im Kurzzeitgedächtnis gehaltenen Information gelangt in das Arbeitsgedächtnis (working memory),
das Information für kurze Zeit speichert (z.B. Autonummer)
und für den Zeitraum einer betreffenden Tätigkeit andauert. Unter der Anleitung einer zentralen "Zuordnungsstation" (central executive) wird der Informationsstrom weitergeleitet - insbesondere zum dorsolateralen Präfrontalcortex, der für das Arbeitsgedächtnis essentiell ist.
Ein Teil
der im Kurzzeitgedächtnis gehaltenen Information gelangt in das Arbeitsgedächtnis (working memory),
das Information für kurze Zeit speichert (z.B. Autonummer)
und für den Zeitraum einer betreffenden Tätigkeit andauert. Unter der Anleitung einer zentralen "Zuordnungsstation" (central executive) wird der Informationsstrom weitergeleitet - insbesondere zum dorsolateralen Präfrontalcortex, der für das Arbeitsgedächtnis essentiell ist.
Beispielsweise erhöht das Merken von Worten die Aktivität im linken präfrontalen sowie dem linken parahippocampalen Cortex; das Merken von Bildern stimuliert diese Hirnteile - die offenbar für die Konsolidierung des Gedächtnisses erforderlich sind - beidseitig.
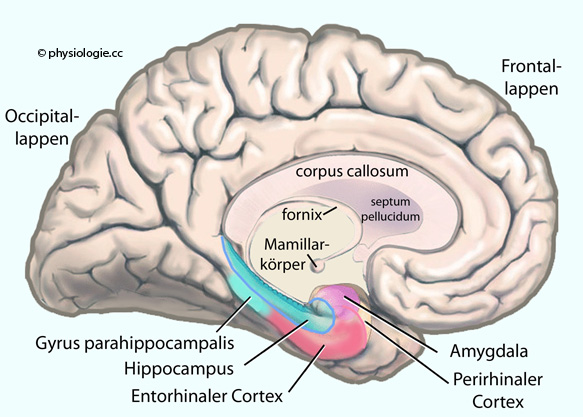
 Abbildung: Mediale Anteile des Temporallappens (linke Hirnhälfte)
Abbildung: Mediale Anteile des Temporallappens (linke Hirnhälfte)
Nach einer Vorlage bei Hocquet G, Class Incremental
Continual Learning in Deep Natural Networks. Artificial Intelligence.
Université Paris-Saclay 2021
Der parahippocampale
Cortex verarbeitet, integriert und speichert räumliche ("wo") und zeitliche
("wann") Sinnesinformationen und ist eine Drehscheibe für den Aufbau
kontextueller Aspekte. Er bereitet räumliches Gedächtnis vor,
analysiert und erkennt dreidimensionale und zeitliche Zusammenhänge auf der Basis
multisensorischer Informationen.
Der Hippocampus
spielt eine zentrale Rolle für Aufbau, Strukturierung, Speicherung und
Wiederauffinden expliziter und räumlicher Gedächtnisinhalte. So können
Sinnesinformationen geordnet, Gedächtnis konsolidiert, Kontexte
hergestellt, Assoziationen hergestellt, Muster erkannt und gespeichert
werden. Der Hippocampus
hilft, neue Inhalte in das Langzeitgedächtnis überzuführen und sich an
sie zu erinnern. Er assisiiert auch bei der Navigation des Körpers in
seiner Umwelt.
An all diesen Vorgängen ist der entorhinale Cortex
als Schaltstelle zwischen Hippocampus und Neocortex beteiligt. Über
Perforansfasern verarbeitet und übermittelt er einerseits
Informationen zum Hippocampus, andererseits leitet er Gedächtnisinhalte
an den Neocortex weiter und verstärkt neuronale Verbindungen mit diesem
 Das als gyrus parahippocampalis bezeichnete corticale Gewebe ist ein Teil des limbischen Systems und liegt hinter dem Temporalpol an der Innenseite des Temporallappens (
Das als gyrus parahippocampalis bezeichnete corticale Gewebe ist ein Teil des limbischen Systems und liegt hinter dem Temporalpol an der Innenseite des Temporallappens ( Abbildung). Er empfängt, verarbeitet und interpretiert ihm über verschiedene Pfade zuströmende (vor allem visuelle) Sinnesinformationen und fügt sie in komplexere Zusammenhänge ein.
Abbildung). Er empfängt, verarbeitet und interpretiert ihm über verschiedene Pfade zuströmende (vor allem visuelle) Sinnesinformationen und fügt sie in komplexere Zusammenhänge ein.
Das Arbeitsgedächtnis ist eine wesentliche Komponente des Kurzzeitgedächtnisses
|
Gegebenenfalls werden die abgebildeten Eindrücke konsolidiert und in länger anhaltende Gedächtnisspeicher (z.B. bei optischen Eindrücken in den
visuellen Cortex) überführt - es entstehen physiologische
Veränderungen, die dem Langzeitgedächtnis zugrundeliegen.
Solche "Gedächtnisspuren" wurden im Rahmen eines neuropsychologischen Konzepts der 1920-er Jahre als Engramme bezeichnet. Nunmehr ist es klar, dass das limbische System - hier insbesondere die Hippocampusformation - eine zentrale Rolle bei Entstehung und Verwaltung des Gedächtnisses spielt.
bezeichnet. Nunmehr ist es klar, dass das limbische System - hier insbesondere die Hippocampusformation - eine zentrale Rolle bei Entstehung und Verwaltung des Gedächtnisses spielt.
Der Überführung von
Gedächtnisinhalten in das Langzeitgedächtnis liegt u.a. Langzeitpotenzierung synaptischer Verschaltungen in der Gehirnrinde zugrunde (s. weiter unten).
Das Langzeitgedächtnis
speichert vorwiegend Information, die voraussichtlich auch in der Zukunft bedeutsam ist. (Man schätzt, dass
das Beherrschen einer Sprache das Speichern von ~105
Informationselementen erfordert.) Sitz des Langzeitgedächtnisses ist die
Großhirnrinde, vorwiegend in Regionen, in welche
der betreffende Sinneseindruck projiziert wurde (z.B. das Okzipitalhirn
bei Erinnerungen an visuelle Inhalte).
 Das sekundäre
Gedächtnis hat große Kapazität und speichert Information über längere Zeit (Minuten bis Jahre). Der Zugriff kann
länger dauern (”Einfallen“ z.B. von Prüfungsstoff durch
”Nachdenken“).
Das sekundäre
Gedächtnis hat große Kapazität und speichert Information über längere Zeit (Minuten bis Jahre). Der Zugriff kann
länger dauern (”Einfallen“ z.B. von Prüfungsstoff durch
”Nachdenken“).
 Das tertiäre Gedächtnis speichert lebenslang (z.B. eigener Name) und ist durch raschen Zugriff
gekennzeichnet (kein langes Nachdenken nötig).
Das tertiäre Gedächtnis speichert lebenslang (z.B. eigener Name) und ist durch raschen Zugriff
gekennzeichnet (kein langes Nachdenken nötig).
Das Langzeitgedächtnis wird in einen deklarativen (expliziten) und einen nicht-deklarativen (impliziten) Anteil untergliedert:

 Abbildung: Formen und Sitz des Langzeitgedächtnisses
Kombiniert nach Vorlagen in Breedlove & Watson,
Behavioral Neuroscience 8th ed. Sinauer / Oxford 2018, und Kandel
/ Schwartz / Jessell (eds): Principles of Neural Science, 4th ed.
McGraw-Hill, 2000
Abbildung: Formen und Sitz des Langzeitgedächtnisses
Kombiniert nach Vorlagen in Breedlove & Watson,
Behavioral Neuroscience 8th ed. Sinauer / Oxford 2018, und Kandel
/ Schwartz / Jessell (eds): Principles of Neural Science, 4th ed.
McGraw-Hill, 2000
Das explizite Gedächtnis erlaubt sie Erinnerung an bewusst gesammelte Erfahrungen (was?) und geht bei Amnesie verloren, das implizite
betrifft "unbewusstes Gedächtnis"und beeinflusst Motorik und Verhalten.
Gedächtnisinhalte - z.B. Fakten über eine Stadt - können unabhängig von
Situationen abgerufen werden, in denen sie erworben wurden. Prozedurale
Gedächtnisinhalte gehören zum nicht-deklarativen Gedächtnis
("Verhaltensgedächtnis": wie
werden Dinge erledigt?) und betreffen integrierte Information aus
mehreren Ereignissen, in denen sie erlangt wurden, z.B. wie man ein
Fahrrad fährt

 Deklaratives
Deklaratives (
explizites, bewusstes) Gedächtnis (
Wissensgedächtnis) ermöglicht die Wiedergabe von Fakten und Episoden (
"wissen, dass"). Diese Inhalte werden vorwiegend im (mittleren)
Temporalhirn
(insbesondere dem
Hippocampus) gespeichert (elektrische Reizung des Temporalhirns kann vergessen
geglaubte Erinnerungen aktivieren).
Beidseitige Läsionen des Hippocampus
führen zu antegrader Amnesie, d.h. neue Gedächtnisinhalte können nicht
mehr gespeichert werden.
Man unterscheidet im Rahmen explizierter Gedächtnisinhalte
 semantisches
semantisches (konzeptbasiertes: Fakten, Bedeutungen),
 episodisches
episodisches (autobiografischen: Kontext - was, wann, wo, warum),
 räumliches
räumliches (Orte) - eine Domäne des entorhinalen Cortex,
 soziales
soziales Gedächtnis (Personen) - insbesondere durch CA2-Neuronen.
 Nicht-deklaratives
Nicht-deklaratives (
implizites, nicht-bewusstes) Gedächtnis (
Verhaltensgedächtnis) ermöglicht, zu
"wissen, wie".
Dazu zählt auch die (unbewusst gesteuerte) korrekte Grammatik der
Sprache. Sitz des impliziten Gedächtnisses sind insbesondere das
Kleinhirn (motorische Fähigkeiten) und die
Mandelkerne (emotionale Reaktionen).
Das
prozedurale Gedächtnis lernt und speichert Bewegungsabläufe (motorische Fertigkeiten -
skill memory) vor allem im Bereich der Basalganglien (
Striatum) - das Kleinhirn konzentriert sich auf die Präzision der Bewegungsdurchführung.
Klassische
Konditionierung beeinflusst Reflexe in einer Weise, dass sie durch erlernte Verknüpfungen ausgelöst werden können (Pawlow-Versuch

).
Basalganglien und Kleinhirn beteiligen sich an der Bildung des impliziten Gedächtnisses
|
Unbewusste
Hinweisreize werden im gesamten Neocortex verwaltet
(Priming, Bahnung: Ein Reiz - Wort, Bild, Geruch u.a. - aktiviert assoziativ implizite Gedächtnisinhalte).
 Das Wiederabrufen von (Erinnern
an) im Langzeitgedächtnis gespeicherte(r) Information benötigt
gerichtete Aufmerksamkeit. Dieser Vorgang ermöglicht den Zugang zum
Gedächtnisinhalt, aber auch dessen (unbewusste) Bearbeitung.
Wiederholtes "Erinnern" kann die dentsprechenden Inhalte verstärken, aber auch verformen.
So werden die Gedächtnisinhalte bei wiederholtem Erinnerungsvorgang
zusehends verfälscht (Zeugenaussagen vor Gericht: Je länger das
Ereignis in der Vergangenheit liegt, desto stärker sind die
betreffenden Erinnerungsinhalte unbewusst verändert).
Das Wiederabrufen von (Erinnern
an) im Langzeitgedächtnis gespeicherte(r) Information benötigt
gerichtete Aufmerksamkeit. Dieser Vorgang ermöglicht den Zugang zum
Gedächtnisinhalt, aber auch dessen (unbewusste) Bearbeitung.
Wiederholtes "Erinnern" kann die dentsprechenden Inhalte verstärken, aber auch verformen.
So werden die Gedächtnisinhalte bei wiederholtem Erinnerungsvorgang
zusehends verfälscht (Zeugenaussagen vor Gericht: Je länger das
Ereignis in der Vergangenheit liegt, desto stärker sind die
betreffenden Erinnerungsinhalte unbewusst verändert).
Zusammengefasst:
 Das Arbeitsgedächtnis nutzt frontale und parietale Rindengebiete
Das Arbeitsgedächtnis nutzt frontale und parietale Rindengebiete
 Lernen und Erinnern erfordert die Kooperation zahlreicher Hirnregionen
Lernen und Erinnern erfordert die Kooperation zahlreicher Hirnregionen
 Unterschiedliche Formen des Gedächtnisses beruhen auf der Leistung
unterschiedlicher (wenn auch überlappender) Hirnregionen
Unterschiedliche Formen des Gedächtnisses beruhen auf der Leistung
unterschiedlicher (wenn auch überlappender) Hirnregionen
 Jede dieser Hirnregionen beteiligt sich an unterschiedlichen Gedächtnisleistungen.
Jede dieser Hirnregionen beteiligt sich an unterschiedlichen Gedächtnisleistungen.
Synaptische Plastizität und Lernprozesse
Neuronale Plastizität: Dem Aufbau von Erinnerungsspuren im Gehirn liegen neuronale Remodellierungsvorgänge zugrunde. Gedächtnisinhalte werden mittels Veränderung synaptischer Gewichtungen (physiologische Veränderungen), Ausbildung neuer Synapsen und Neuronen (strukturelle Veränderungen) gespeichert. Lernen und Gedächtnis beruhen auf der Modifizierung der synaptischen
Übertragung in neuronalen Netzen.
Glutamatrezeptoren werden pro Stunde mehrmals recycelt (im
Synapsenbereich endozytiert und durch Exozytose wieder in die
postsynaptische Membran eingelagert). Dieses Gleichgewicht kann Veränderungen unterliegen, wodurch die Synapsenwirkung verstärkt oder abgeschwächt wird (synaptische Plastizität):
 Werden
mehr Rezeptoren in die Synapse eingebaut als aus ihr entfernt, dann
wächst die Rezeptorzahl und damit das Ausmaß der Depolarisation (EPSP)
pro Quantum freigesetzten Glutamins;
Werden
mehr Rezeptoren in die Synapse eingebaut als aus ihr entfernt, dann
wächst die Rezeptorzahl und damit das Ausmaß der Depolarisation (EPSP)
pro Quantum freigesetzten Glutamins;
 umgekehrt nimmt die Amplitude des EPSP ab, wenn mehr Rezeptoren endo- als exozytiert werden.
umgekehrt nimmt die Amplitude des EPSP ab, wenn mehr Rezeptoren endo- als exozytiert werden.
Man unterscheidet kurzzeitige, Millisekunden bis Minuten währende (short-term synaptic plasticity) von langfristiger synaptischer Plastizität (long-term synaptic plasticity),
die von Stunden bis zum ganzen Leben der Person andauert.
 Langzeiteffekte können die Stärke der Synapsenwirkung anhaltend erhöhen (LTP: Verstärkung) oder reduzieren (LTD: Abschwächung). Dahinter stecken unterschiedliche
Mechanismen, Synapsen und Transduktionswege; die Bezeichnung bezieht
sich lediglich auf die Richtung des erzielten Effekts.
Langzeiteffekte können die Stärke der Synapsenwirkung anhaltend erhöhen (LTP: Verstärkung) oder reduzieren (LTD: Abschwächung). Dahinter stecken unterschiedliche
Mechanismen, Synapsen und Transduktionswege; die Bezeichnung bezieht
sich lediglich auf die Richtung des erzielten Effekts.
LTP / LTD sind Mechanismen, die im Rahmen des Zusammenwirkens zeitlich
naheliegender Ereignisse und deren Verknüpfung eine Rolle spielen. Dazu
dienen neuronale Funktionskreise, die als Koinzidenzdetektoren
bezeichnet werden.
 Unter Koinzidenzdetektion (coincidence detection)
bzw. Koinzidenzdetektor versteht man eine neuronale Schaltung, welche
aus unterschiedlichen Quellen stammende, aber zeitlich eng
zusammentreffende Signale erkennt und so codiert, dass sie als
Grundlage für Gedächtnis und Erinnerung dienen können.
Koinzidenzdetektion unterstützt die Assoziation getrennter
Gedächtnisinhalte und verringert den Einfluss von Stör- und
Unschärfeeinflüssen.
Unter Koinzidenzdetektion (coincidence detection)
bzw. Koinzidenzdetektor versteht man eine neuronale Schaltung, welche
aus unterschiedlichen Quellen stammende, aber zeitlich eng
zusammentreffende Signale erkennt und so codiert, dass sie als
Grundlage für Gedächtnis und Erinnerung dienen können.
Koinzidenzdetektion unterstützt die Assoziation getrennter
Gedächtnisinhalte und verringert den Einfluss von Stör- und
Unschärfeeinflüssen.
Synaptische
Plastizität ist ein Kennzeichen der Dynamik neurophysiologischer
Signalverarbeitung. Ein führendes Beispiel sind glutamaterge
Ionenkanäle im hippocampalen System - NMDA-Rezeptor
(NMDAR, N-methyl-d-aspartate receptor) und AMPA-Rezeptor (AMPAR, α-amino- 3-hydroxy-5-methyl- 4-isoxazolepropionic acid receptor) - an dendritischen Dornenfortsätzen (dendritic spines) ( Abbildung):
Abbildung):
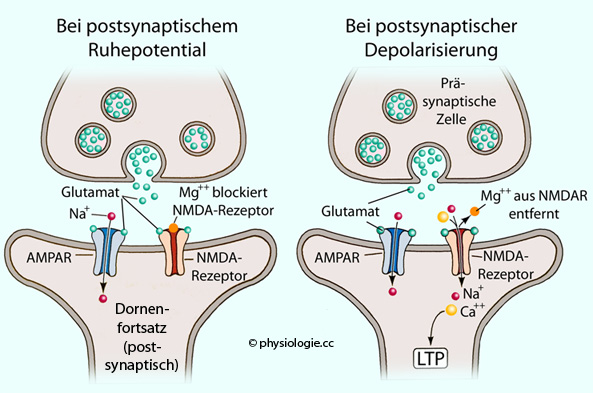
 Abbildung: NMDA-Kanäle als Koinzidenzdetektoren
Nach
einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Abbildung: NMDA-Kanäle als Koinzidenzdetektoren
Nach
einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Der postsynaptische NMDA-Rezeptor ist ein "Koinzidenzdetektor"
- er öffnet nur, wenn Glutamat (aus präsynaptischer Aktivierung) gebunden und gleichzeitig die
postsynaptische Membran (aus postsynaptischer Aktivierung) ausreichend depolarisiert ist.
Dadurch lösen sich Magnesiumionen
vom Kanal (der Magnesiumblock wird aufgehoben) und diffundieren in den Extrazellulärraum, der Kanal ist
für Einstrom von Natrium- und Calciumionen frei. Erhöhte Ca++-Konzentration
in der postsynaptischen Zelle triggert Veränderungen, die hier zu
Langzeitpotenzierung (LTP) führen, die Stärke des synaptischen Effekts
(Synapsenstärke) nimmt zu

 Der NMDA-Rezeptor ist ein molekularer Koinzidenzdetektor, seine Öffnung hängt von zwei Bedingungen ab:
Der NMDA-Rezeptor ist ein molekularer Koinzidenzdetektor, seine Öffnung hängt von zwei Bedingungen ab:
 Gibt die präsynaptische Endigung den Neurotransmitter Glutamat frei und
bindet dieses an den NMDAR, dann erlangt dieser nur dann seine
"OFFEN"-Konfiguration,
Gibt die präsynaptische Endigung den Neurotransmitter Glutamat frei und
bindet dieses an den NMDAR, dann erlangt dieser nur dann seine
"OFFEN"-Konfiguration,
 wenn die postsynaptische Zelle gleichzeitig
depolarisiert ist - denn dann verschwindet der Magnesiumblock und die
NMDAR lassen den Einstrom von Na+ und Ca++ zu (
wenn die postsynaptische Zelle gleichzeitig
depolarisiert ist - denn dann verschwindet der Magnesiumblock und die
NMDAR lassen den Einstrom von Na+ und Ca++ zu ( Abbildung). Depolarisierung postsynaptischer Neuronen kann z.B. an Pyramidenzellen im Hippocampus durch Schaffer'sche Kollateralen hervorgerufen werden.
Abbildung). Depolarisierung postsynaptischer Neuronen kann z.B. an Pyramidenzellen im Hippocampus durch Schaffer'sche Kollateralen hervorgerufen werden.
Der Calciumeinstrom in dendritische Dornenfortsätze triggert anschließend eine Reihe nachhaltiger
Veränderungen im postsynaptischen Apparat. Starke Erhöhung der zytosolischen [Ca++] aktiviert Proteinkinasen - u.a. CaMKII -, welche AMPA-Rezeptoren phosphorylieren und ihre vermehrte Einlagerung in die postsynaptische Membran fördern ("AMPAfizierung"). Das verstärkt bei Erregung
der Synapse den Na
+-Einstrom durch AMPAR und induziert
Langzeitpotenzierung.
Außer NMDAR gibt es weiterer Beispiele für molekulare Koinzidenzdetektoren, z.B.
 Inositol-3-Phosphat Rezeptoren: Diese aktivieren intrazelluläre Ca++-Speicher bei synchronem Auftreten von IP3 (Zeichen der Rezeptoraktivierung) und Ca++ (postsynaptische Aktivität) oder
Inositol-3-Phosphat Rezeptoren: Diese aktivieren intrazelluläre Ca++-Speicher bei synchronem Auftreten von IP3 (Zeichen der Rezeptoraktivierung) und Ca++ (postsynaptische Aktivität) oder
 Phospholipase C
an Synapsen in Hippocampus, Neocortex, Basalganglien, Kleinhirn
(Postsynaptische Depolarisierung fördert hier die Freisetzung von Endocannabinoiden, welche retrograd inhibitorische postsynaptische Ströme blockieren: Depolarization-induced suppression of inhibition). PLC moduliert diesen Mechanismus als Koinzidenzdetektor; die Endocannabinoidfreisetzung ist verstärkt, wenn Depolarisierung und Rezeptoraktivierung zusammenwirken.
Phospholipase C
an Synapsen in Hippocampus, Neocortex, Basalganglien, Kleinhirn
(Postsynaptische Depolarisierung fördert hier die Freisetzung von Endocannabinoiden, welche retrograd inhibitorische postsynaptische Ströme blockieren: Depolarization-induced suppression of inhibition). PLC moduliert diesen Mechanismus als Koinzidenzdetektor; die Endocannabinoidfreisetzung ist verstärkt, wenn Depolarisierung und Rezeptoraktivierung zusammenwirken.
AMPAR bewegen sich zwischen einem endosomalen Speicherpool und der Zellmembran (Recycling,  Abbildung unten). Vermehrte subsynaptische Einlagerung von AMPAR wirkt zugunsten synaptischer
Langzeitpotenzierung (LTP), vermehrte Endozytose (Abnahme der Zahl aktiver AMPAR) in Richtung
Langzeitdepression (LTD).
Abbildung unten). Vermehrte subsynaptische Einlagerung von AMPAR wirkt zugunsten synaptischer
Langzeitpotenzierung (LTP), vermehrte Endozytose (Abnahme der Zahl aktiver AMPAR) in Richtung
Langzeitdepression (LTD).
Präsynaptische Aktionspotentialsalven führen zu Glutamatfreisetzung und postsynaptischen EPSPs durch Kationeneinstrom
An nicht
aktivierten glutamatergen Synapsen sind die NMDA-Rezeptoren durch
Magnesiumionen blockiert
Vordepolarisation öffnet NMDA-Rezeptoren, Ca++ strömt ein. Ca++-aktivierbare
Proteinkinase phosphoryliert AMPA-Rezeptoren, die in die
postsynaptische Membran eingelagert werden ("AMPAfizierung"), Na+ strömt ein und verstärkt die Depolarisation (Langzeitpotenzierung LTP)
|
Der Koinzidenzdetektor-
Mechanismus verstärkt Reaktionen
auf wiederholt stattgefundene Reizmuster. Die Intensität des Calciumeinstroms durch den NMDA-Rezeptor zeigt das Ausmaß der prä- / postsynaptischen Coaktivierung an: Je öfter der präsynaptische und
postsynaptische Teil gleichzeitig (oder knapp nacheinander)
aktiviert sind, desto intensiver ist die
Auswirkung auf die Synapse und deren Kapazität (synaptische Potenzierung) - man spricht auch von spike-timing dependent plasticity (STDP).
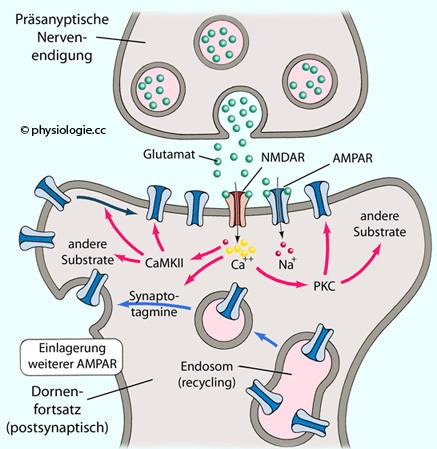
 Abbildung: Mechanismen synaptischer Langzeitpotenzierung
Nach
einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Abbildung: Mechanismen synaptischer Langzeitpotenzierung
Nach
einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Bei
Freisetzung von Glutamat aus präsynaptischen Vesikeln öffnet der
NMDA-Rezeptor (NMDAR) nur dann, wenn der postsynaptische Dornenfortsatz
ausreichend depolarisiert ist. Wenn dies zutrifft, diffundiert Ca++
in die postsynaptische Zelle (dendritischer Dornenfortsatz).
Calciumionen im postsynaptischen Zytosol aktivieren dort Proteinkinasen
- wie CaMKII und PKC. Diese phosphorylieren diverse Zielproteine, und AMPA-Rezeptor (AMPAR)- hältige Membran aus Reserve-Endosomen wird - unter der Mitwirkung von Synaptotagminen - in die Zellmembran integriert. Anschließend wandern die Rezeptoren in die Synapsenregion.
Das Ergebnis
ist eine Erhöhung der AMPAR-Zahl in der subsynaptischen Membran des
betreffenden Dornenfortsatzes und dessen Empfindlichkeit für Glutamat
(Langzeitpotenzierung)
 Langzeitpotenzierung (LTP, long-term potentiation -
Langzeitpotenzierung (LTP, long-term potentiation -  Abbildung) ist eine Zunahme der Synapsenstärke infolge starker Reizung des postsynaptischen Neurons (Aktionspotentiale in Abständen von <20 ms für eine Dauer von mindestens 100 ms), die für mindestens eine Stunde anhält (sie kann auch wesentlich länger wirken - Tage, Wochen, Monate oder auch lebenslang). Die
Wirkung hält nur dann lange an, wenn sie nicht nur auf der Aktivierung
von Enzymketten (rascher Abbau der Produkte), sondern auch
der Neubildung von Proteinen beruht (Genexpression, folgende
Abbildung) ist eine Zunahme der Synapsenstärke infolge starker Reizung des postsynaptischen Neurons (Aktionspotentiale in Abständen von <20 ms für eine Dauer von mindestens 100 ms), die für mindestens eine Stunde anhält (sie kann auch wesentlich länger wirken - Tage, Wochen, Monate oder auch lebenslang). Die
Wirkung hält nur dann lange an, wenn sie nicht nur auf der Aktivierung
von Enzymketten (rascher Abbau der Produkte), sondern auch
der Neubildung von Proteinen beruht (Genexpression, folgende  Abbildung).
Abbildung).
Voraussetzung für
Langzeitpotenzierung ist eine ausreichende Depolarisierung dendritischer Dornfortsätze (dendritic spines) der
Empfängerzelle, die durch hohe Reizfrequenz erreicht werden kann;
einzelne oder niedrigfrequente Stimuli sind dazu nicht in der Lage.
Eine
Schlüsselrolle spielt dabei [Ca++] in Zytosol - ist die Konzentration hoch, werden vor allem Kinasen, ist sie niedrig, vor allem
Phosphatasen aktiviert (Kinasen fördern die AMPAfizierung, Phosphatasen reduzieren sie).
Intrazelluläre Ca++-Ionen aktivieren zahlreiche Enzyme, u.a. Calmodulin; Ca++-Calmodulin
ist der entscheidende Signalstoff für die Langzeitpotenzierung: Es
aktiviert weitere Enzyme, wie Adenylylcyclase (Adenylatzyklase) und die
Ca++-Calmodulin-abhängige Proteinkinase (CaM-Kinase II), die sich selbst phosphoryliert. Ca++-Calmodulin ist der Signalstoff für die Langzeitpotenzierung: Es aktiviert weitere Enzyme, wie die Ca++-Calmodulin-abhängige Proteinkinase C (PKC), NO-Synthase (NO wirkt möglicherweise als retrograder Signalstoff), und die CaM-Kinase II (CaMKII), die sich selbst phosphoryliert (dadurch halten ihre Wirkungen lange an). CaM-Kinase II phosphoryliert
AMPA-Rezeptoren, MAP-Kinasen (diese beteiligen sich am Aufbau von
Dendriten) oder auch NMDA-Rezeptoren (weiterer Calciumeinstrom).
cAMP katalysiert die Aktivität der Proteinkinase A (PKA);
diese phosphoryliert AMPA-Rezeptoren, und diese bleiben länger geöffnet,
wenn sie Glutamat binden - die Synapse bleibt länger aktiviert, die
postsynaptische Zelle länger depolarisiert; dies trägt zur
Langzeitpotenzierung bei.
Nach
Bindung des Transmitters, Ca++-Einstrom und Aktivierung von Kinasen (Proteinkinasen A und C, Calmodulin) wird CREB aktiviert, im Zellkern die Transkription entsprechender Gene und die Synthese
für den Synapseneffekt kritischer Proteine beeinflusst
(Rezeptormoleküle, Transmitter, Strukturproteine). Dadurch wird der Effekt einer Synapsenaktivierung und auch die Synapsenzahl modifiziert. CREB
ist ein weiteres Zielprotein für die Langzeitpotenzierung, es lagert
sich an CRE (cAMP-responsives Element) der DNA und steuert dadurch
Schritte der Proteinsynthese ( Abbildung).
Abbildung).
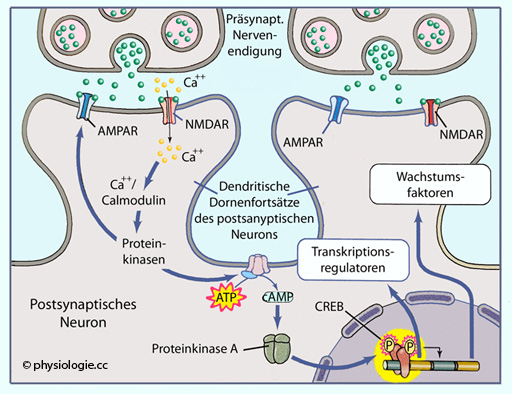
 Abbildung: Mechanismen langanhaltender Veränderungen postsynaptischer Signalübertragung bei Langzeitpotenzierung
Nach
einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Abbildung: Mechanismen langanhaltender Veränderungen postsynaptischer Signalübertragung bei Langzeitpotenzierung
Nach
einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Proteinkinase A aktiviert im Rahmen der späten Komponente der Langzeitpotenzierung den Transkriptionsregulator CREB. Dadurch werden mehrere Gene exprimiert, welche die PKA-Aktivität sowie Synapsenstruktur dauerhaft verändern
Dendritische Dornfortsätze können je nach Beanspruchung der
synaptischen Apparate ihre Größe, Gestalt und Zahl verändern. Neben
diesen postsynaptischen
Veränderungen können im Rahmen von Langzeitpotenzierung /
Langzeitdepression auch präsynaptische Anpassung auftreten (z.B.
durch Stickstoffmonoxid), etwa durch Veränderung der freigesetzten Glutamatmenge.
Langzeitpotenzierung wurde beim Primatengehirn zuerst bei Neuronen des (auf die
Speicherung von Gedächtnisinhalten spezialisierten) Hippocampus
beobachtet, dient aber überall im Nervensystem der Bildung von
Erinnerungsspuren bzw. Modifikation bestehender
Gedächtnisinhalte.
Synapsen können an Größe gewinnen oder einbüßen. Weiters können neue
Synapsen ausgebildet werden, oder ihr Verbindungsmuster wird geändert.
Resultat sind veränderte postsynaptische Potentiale und/oder neue
Erregungsmuster an synaptischen Arrangements.
Das Gleichgewicht der AMPA-Bestückung an der subsynaptischen Membran
von dendritioschen Dornenfortsätzen kann sich auch zugunsten einer
Verringerung der Rezeptorzahl verschieben und synaptische Abschwächung
(Langzeitdepression) bewirken:
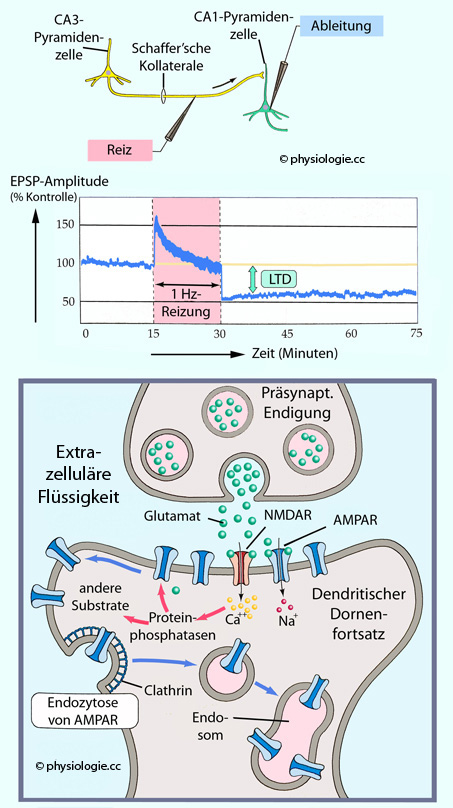
 Abbildung: Synaptische Langzeitdepression im Hippocampus
Nach
einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Abbildung: Synaptische Langzeitdepression im Hippocampus
Nach
einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Oben:
Die Schaffer'sche Kollaterale einer CA3-Pyramidenzelle im Hippocampus
wird elektrisch gereizt und die Reaktion einer von der Kollaterale
beeinflussten CA1-Pyramidenzelle registriert. Jeder Reiz löst ein
exzitatorisches postsynaptisches Potential (eine vorübergehende
Depolarisierung) aus.
Mitte:
Registrierung der resultierenden EPSP-Größen vor, während und nach
niedrigfrequenter (1 Hz) Reizung für eine Dauer von15 Minuten. Die
Stimulation erhöht während der Reizperiode die Größe der EPSPs zunächst
um 50%, dieser Effekt klingt noch während der Stimulation rasch ab.
Nach der Reizung ist die Amplitude weiterer EPSPs auf etwa die Hälfte
reduziert. Dieser Effekt (LTD = Langzeitdepression) hält für mehrere
Stunden an.
Unten:
Mechanismen der erfolgten LTD. Während der Stimulationsperiode hat der
nur geringe postsynaptische Anstieg der Calciumkonzentration vor allem
Proteinphosphatasen angeregt, was zu einer Internalisierung von AMPAR
aus der subsynaptischen Membran in Richtung Speichervesikel (Endosomen,
sorting endosomes) führt und die Empfindlichkeit der CA1-Zelle gegenüber von Schaffer'schen Kollateralen freigesetztem Glutamat reduziert.
 Zum Clathrinmechanismus s. dort
Zum Clathrinmechanismus s. dort

 Niedrige Aktionspotentialfrequenz an postsynaptischen Dendriten bewirkt hier Langzeitdepression (LTD, long-term
depression). Diese währt für einige Stunden oder länger (Tage, Wochen). AMPAR werden vermehrt endozytiert, bewirkt durch Phosphatasen wie
Calcineurin oder Proteinphosphatase 1 (PP1) (
Niedrige Aktionspotentialfrequenz an postsynaptischen Dendriten bewirkt hier Langzeitdepression (LTD, long-term
depression). Diese währt für einige Stunden oder länger (Tage, Wochen). AMPAR werden vermehrt endozytiert, bewirkt durch Phosphatasen wie
Calcineurin oder Proteinphosphatase 1 (PP1) ( Abbildung). Die
Rezeptoren werden in der Zelle gespeichert oder abgebaut.
Abbildung). Die
Rezeptoren werden in der Zelle gespeichert oder abgebaut.
Langzeitpotenzierung
und -depression treten an zahlreichen Orten im ZNS auf (Mandelkerne, Hippocampus,
Frontal- und Okzipitalhirn, Kleinhirn). In der Kleinhirnrinde funktioniert LTD NMDAR-unabhängig über metabotrope
Glutamatrezeptoren (mGluR).
Zusammen mit aktivitätsabhängiger Bildung von
Wachstumsfaktoren (z.B. BDNF) ist das Wechselspiel fördernder und hemmender Effekte auf die Synapsenstärke eine
Grundlagen für die Dynamik von Gedächtnis und Erinnerungsvermögen.
 Das Wechselspiel von LTP und LTD dient der
Feineinstellung ("Schärfung") von Gedächtnismustern.
Das Wechselspiel von LTP und LTD dient der
Feineinstellung ("Schärfung") von Gedächtnismustern.
 Nach
wiederholter gleichzeitiger Erregung
des prä- und postsynaptischen Neurons (Koinzidenz) ist die synaptische
Übertragungen verstärkt. Calciumionen aktivieren Proteinkinasen, Phospholipasen und neuronale
NO-Synthase (nNOS), was u.a. zu Verstärkung der Synapsenwirkung und auch Erhöhung der Synapsenzahl führt. Im postsynaptischen Teil werden
AMPA-Rezeptoren in die Membran eingebaut, die synaptische Kapazität
steigt (Langzeitpotenzierung: "Neurons that fire together wire together"). Langzeitpotenzierung erhöht in Pyramidenzellen die Amplitude erregender
postsynaptischer Potentiale (EPSPs) über Stunden bis Tage.
Nach
wiederholter gleichzeitiger Erregung
des prä- und postsynaptischen Neurons (Koinzidenz) ist die synaptische
Übertragungen verstärkt. Calciumionen aktivieren Proteinkinasen, Phospholipasen und neuronale
NO-Synthase (nNOS), was u.a. zu Verstärkung der Synapsenwirkung und auch Erhöhung der Synapsenzahl führt. Im postsynaptischen Teil werden
AMPA-Rezeptoren in die Membran eingebaut, die synaptische Kapazität
steigt (Langzeitpotenzierung: "Neurons that fire together wire together"). Langzeitpotenzierung erhöht in Pyramidenzellen die Amplitude erregender
postsynaptischer Potentiale (EPSPs) über Stunden bis Tage.
 Werden der prä- und postsynaptische Teil hingegen desynchron oder nur schwach aktiviert
(fehlende oder unzureichende Koinzidenz), werden AMPA-Rezeptoren internalisiert
(endozytiert), die Synapseneffizienz nimmt ab, und es kann zur
Zurückbildung der Synapse kommen (Langzeitdepression: "Neurons that fire out of sync lose their link").
Werden der prä- und postsynaptische Teil hingegen desynchron oder nur schwach aktiviert
(fehlende oder unzureichende Koinzidenz), werden AMPA-Rezeptoren internalisiert
(endozytiert), die Synapseneffizienz nimmt ab, und es kann zur
Zurückbildung der Synapse kommen (Langzeitdepression: "Neurons that fire out of sync lose their link").
Synaptische Veränderungen können über längere Zeit funktionelle und morphologische Spuren im neuronalen Netzwerk hinterlassen (Gedächtnis). Synaptische Veränderungen erfolgen
 präsynaptisch - Variation der Menge des pro Aktionspotential ausgeschütteten und / oder wiederaufgenommenen Transmitters, und / oder
präsynaptisch - Variation der Menge des pro Aktionspotential ausgeschütteten und / oder wiederaufgenommenen Transmitters, und / oder
 postsynaptisch - bezüglich Transmittereffekt (Zahl und/oder Empfindlichkeit der Rezeptoren) und Transmitterabbau.
postsynaptisch - bezüglich Transmittereffekt (Zahl und/oder Empfindlichkeit der Rezeptoren) und Transmitterabbau.
 Gliazellen sind an synaptischer Plastizität (Zu- oder Abnahme der Synapsendichte) beteiligt. So können Astrozyten und Mikrogliazellen
die Stellen markieren, an denen synaptische Veränderungen
(Synaptogenese oder Synapsenelimination mit nachfolgender Phagozytose)
erfolgen sollen (
Gliazellen sind an synaptischer Plastizität (Zu- oder Abnahme der Synapsendichte) beteiligt. So können Astrozyten und Mikrogliazellen
die Stellen markieren, an denen synaptische Veränderungen
(Synaptogenese oder Synapsenelimination mit nachfolgender Phagozytose)
erfolgen sollen ( Abbildung).
Abbildung).
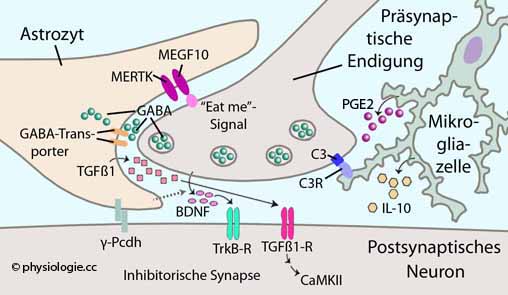
 Abbildung: Einfluss von Gliazellen auf Synaptogenese und -elimination
Abbildung: Einfluss von Gliazellen auf Synaptogenese und -elimination
Nach Um JW, Roles of Glial Cells in Sculpting Inhibitory Synapses and Neural Circuits. Front Mol Neurosci 2017; 10 (article 381)
Astrozyten und Mikrogliazellen mediieren sowohl Vermehrung als auch Reduktion GABAerger Synapsen über mehrere Mechanismen:
Astrozyten bilden TGFß1, dieses regt die Bildung inhibitorischer Synapsen via CaMKII
an. Die Synapsenbildung wird weiters reguliert über astrozytäres
Protocadherin (γ-Pcdh - Protocadherine sind die größte Untergruppe in
der Cadherin-Superfamilie und vermitteln homophile Zelladhäsion), GABA-Transporter und den BDNF-TrkB (Tropomyosin Rezeptorkinase B) -Weg.
Elimination der Synapsen kann durch Astrozyten
ausgelöst werden - über ein "Eat me"-Signal via das Regulatorptotein
MEGF10 und die Proteinkinase MERTK - oder durch Mikroglia (über
Erkennung der C3-Expression durch C3-Rezeptoren und anschließende
Phagozytose). Mikroglia produziert u.a. PGE2 (stimuliert Astrozytenproliferation und Entzündungsvorgänge) und IL-10 (neuroprotektiver Effekt)

Lernvorgänge verändern weiters die Myelinisierung vermehrt aktivierter Nervenfasern durch Oligodendrozyten (activity dependent plasticity): OPCs (oligodendron precursor cells)
verfügen über NMDA- und AMPA-Rezeptoren und reagieren auf erhöhte
Freisetzung von Glutamat (und ATP) mit Proliferation und Ausreifung zu
Oligodendozyten. Vermehrte neuronale Aktivität (z.B. motorisches
Lernen) führt zu einer Verkürzung der Myelinsegmente und damit
Erweiterung der Ranvier'schen Schnürringe, altes Myelin zieht sich zurück und neues wird abgelagert (remodeling), was eine Präzisierung motorischer Vorgänge bewirken kann. Auch unterstützen Oligodendrozyten den Stoffwechsel der Neuriten.
 Zu synaptischen Vernetzungsmolekülen und deren Dynamik s. dort
Zu synaptischen Vernetzungsmolekülen und deren Dynamik s. dort
Retrograde Wirkung
(Rückwirkung auf die Präsynapse): Signalmoleküle wie BDNF, NO oder (Endo-) Cannabinoide
 werden vom angeregten postsynaptischen Apparat freigesetzt
und diffundieren zum präsynaptischen Teil, binden hier an entsprechende
Rezeptoren und modulieren die Transmitterfreisetzung - z.B. durch
Einfluss auf den Calciumeinstrom. Nimmt dieser zu, werden Vesikel
mobilisiert, die Transmitterfreisetzung vermehrt und die synaptische
Effizienz gesteigert.
werden vom angeregten postsynaptischen Apparat freigesetzt
und diffundieren zum präsynaptischen Teil, binden hier an entsprechende
Rezeptoren und modulieren die Transmitterfreisetzung - z.B. durch
Einfluss auf den Calciumeinstrom. Nimmt dieser zu, werden Vesikel
mobilisiert, die Transmitterfreisetzung vermehrt und die synaptische
Effizienz gesteigert.
Stickstoffmonoxid wirkt als retrograder Neurotransmitter
|
Frühe und späte Langzeitpotenzierung (LTP): LTP mit einer Effektdauer von 1-3 Stunden erfolgt unabhängig von Transkriptions- und Translationsänderungen (frühe - early - Langzeitpotenzierung, E-LTP), solche mit über 3 Stunden anhaltender Wirkung ist generell abhängig von veränderter Genexpression (späte - late - Langzeitpotenzierung, L-LTP).
Die
Abhängigkeit des synaptischen Effekts von der Reizstärke ist über
unterschiedliche Enzymaktivierung im postsynaptischen Apparat
erklärbar ( Abbildung): Hochfrequente Stimulierung der Synapse aktiviert über
starken Calciumeinstrom (intrazellulärer Ca++-Spiegel über 5 µM) Kinasen und
AMPA-Rezeptoren, was zu Verstärkung der Synapsenwirkung führt (LTP
erklärt sich auch über vermehrte AMPAR-Zahl).
Abbildung): Hochfrequente Stimulierung der Synapse aktiviert über
starken Calciumeinstrom (intrazellulärer Ca++-Spiegel über 5 µM) Kinasen und
AMPA-Rezeptoren, was zu Verstärkung der Synapsenwirkung führt (LTP
erklärt sich auch über vermehrte AMPAR-Zahl).
 Abbildung: Wie Ca++ sowohl LTP als auch LTD triggern kann
Nach Bear / Connors / Paradiso, Neuroscience - Exploring the Brain, 4th Ed. Williams & Wilkins 2015
Abbildung: Wie Ca++ sowohl LTP als auch LTD triggern kann
Nach Bear / Connors / Paradiso, Neuroscience - Exploring the Brain, 4th Ed. Williams & Wilkins 2015
Hohe Ca++-Spiegel
aktivieren eher Kinasen, was AMPA-Rezeptoren phosphoryliert und die
Synapsenkapazität steigert.
Umgekehrt fördert niedriger Ca++-Spiegel im postsynaptischen Neuron Phosphatasen und dephosporyliert damit AMPA-Rezeptoren

Umgekehrt: Ist der postsynaptische Calciumspiegel niedrig (~1 µM), dann
tritt die Wirkung von Phosphatasen in den Vordergrund; AMPAR werden
dephosphoryliert und verlieren ihre Wirksamkeit, ihre Anzahl in der subsynaptischen Membran nimmt ab (LTD).
Die Lage einer Synapse am Dendritenbaum und ihre Zeitfenster für LTD/LTP (timing rules) bestimmen die zeit- und ortsabhängige synaptische Plastizität: Diese
hängt mit der Dynamik des Membranpotentials an den betreffenden Zellen
zusammen (Aktionspotentiale sind meist durch starke exzitatorische
Wirkungen an Dendriten verursacht; vom Axonhügel ausgehend laufen sie einerseits
über das Axon peripherwärts, andererseits "retrograd" über Soma und
Dendritenbaum und beeinflussen dort den Zustand postsynaptischer
Synapsenappparate). Lokale Potentialschwankungen hingegen klingen in ihrer Nachbarschaft rasch ab, z.B. auf den halben Betrag in 100 µm Entfernung.
 Das bedeutet, dass nahe an aktivierten Synapsen gelegene andere
Synapsen an LTP- und LTD-Prozessen mitbeteiligt sind (diese Synapsen
"lernen mit"), während weiter entfernt liegende von solchen lokalen
Vorgängen unbeeinflusst bleiben (Selektivität).
Das bedeutet, dass nahe an aktivierten Synapsen gelegene andere
Synapsen an LTP- und LTD-Prozessen mitbeteiligt sind (diese Synapsen
"lernen mit"), während weiter entfernt liegende von solchen lokalen
Vorgängen unbeeinflusst bleiben (Selektivität).
Auch die Morphologie ( Abbildung) spielt eine Rolle:
Abbildung) spielt eine Rolle:
 Abbildung: Calciumverteilung in einem dendritischen Dornenfortsatz
Nach Blackstone C, Sheng M, Postsynaptic calcium signaling microdomains in neurons. Front Biosci 2002; 7: d872-85
Abbildung: Calciumverteilung in einem dendritischen Dornenfortsatz
Nach Blackstone C, Sheng M, Postsynaptic calcium signaling microdomains in neurons. Front Biosci 2002; 7: d872-85
Kopfteil (spine head)
und Halsteil eines Dornenfortsatzes (dendritic spine)
- letzterer mit vergleichsweise hoher elektrischer
Impedanz, die den Kopfteil elektrisch weitgehend isoliert - bilden
(ähnlich einer
Zellorganelle) ein funktionelles Kompartiment. Eintreffende
Depolarisationen werden nicht wesentlich abgeschwächt, die
Ionenbewegungen durch die Membran des Kopfteils haben hier - lokal
begrenzt - vergleichsweise große Wirkung. Calciumionen spielen als
second messenger eine wichtige Rolle, sie bilden funktionelle
"Mikrodomänen" im Zytoplasma des Dornenfortsatzes. Der Calciumpool des
endoplasmatischen Retikulums erstreckt sich durch die ganze Zelle
(Austausch über den Halsteil angedeutet).
Zeitliche Koinzidenzen prä- und postsynaptischer Aktivierung werden zu synaptischer Plastizität im Sinne von Potenzierung und Depression (d.h. Lernvorgängen) umgesetzt
B, endogener Calciumpuffer  IP3R, IP3-Rezeptor
IP3R, IP3-Rezeptor  mGluR, metabotroper Glutamatrezeptor
mGluR, metabotroper Glutamatrezeptor  PMCA, Plasmamembran Ca++-ATPase
PMCA, Plasmamembran Ca++-ATPase  SERCA regelt das Wiederauffüllen des Calciumspeichers im endoplasmatischen Retikulum)
SERCA regelt das Wiederauffüllen des Calciumspeichers im endoplasmatischen Retikulum)  SOC, store-operated calcium channel (für die Aufnahme von Calciumionen)
SOC, store-operated calcium channel (für die Aufnahme von Calciumionen)  VDCC, voltage-dependent calcium channel. Calciumionen
triggern eine Kaskade intrazellulärer Folgevorgänge, inklusive die
Aktivierung von Kinasen, was schließlich zur Verstärkung der
synaptischen Übertragung führt
VDCC, voltage-dependent calcium channel. Calciumionen
triggern eine Kaskade intrazellulärer Folgevorgänge, inklusive die
Aktivierung von Kinasen, was schließlich zur Verstärkung der
synaptischen Übertragung führt

Veränderungen des Dornenfortsatzes von Dendriten ("Halsteil", spine neck)
könnte z.B. die Diffusion von Calciumionen im Dendriten und damit die
oben beschriebenen synaptischen Vorgänge beeinflussen ("biochemische
Kompartimentierung"). Lokale synaptische Vorgänge wirken sich hier
intensiv aus, die Koinzidenzdetektion findet mit hoher Effizienz statt.
Spannungsschwankungen bleiben im Wesentlichen auf den Kopfteil beschränkt und wirken sich wegen des hohen Widerstandes im Halsteil über diesen hinaus kaum auf den Hauptast des Dendriten aus.
Dendritenfortsätze können endoplasmatisches Retikulum (das Calcium speichert)
aktiv in den Kopfteil ziehen und auf diese Weise calciumabhängige Prozesse steuern (Purkinje-Zellen).
Reelin  : Eine wichtige Rolle für die Langzeitpotenzierung spielt das große (388 kD) Glykoprotein Reelin,
das der Gedächtnisverfestigung und der ontogenetischen
Organisation der Neuronenzellschichten im Hippocampus dient.
Es
beeinflusst Migration und Interaktion von Nervenzellen und regt die
Ausbildung von dendritischen Fortsätzen an. Ein Mangel an Reelin
scheint für die Entwicklung verschiedener neuropathologischer
Zustandsbilder eine Rolle zu spielen.
: Eine wichtige Rolle für die Langzeitpotenzierung spielt das große (388 kD) Glykoprotein Reelin,
das der Gedächtnisverfestigung und der ontogenetischen
Organisation der Neuronenzellschichten im Hippocampus dient.
Es
beeinflusst Migration und Interaktion von Nervenzellen und regt die
Ausbildung von dendritischen Fortsätzen an. Ein Mangel an Reelin
scheint für die Entwicklung verschiedener neuropathologischer
Zustandsbilder eine Rolle zu spielen.
Lernprozesse beeinflussen also interneuronale Verbindungen in dynamischer Weise: Dendriten
sprossen aus oder bilden sich zurück, synaptische Übertragung wird
effizienter oder schwächer.
Zusätzlich zu der neuronalen Dynamik kommen
auch Einflüsse der Blutversorgung: Kapillaren können neu aussprossen,
andere wieder verschwinden. Wiederholte Reizung neuronaler Schaltkreise
führt im Allgemeinen zu Verbesserung der zugrunde liegenden
Kommunikation von Nervenzellen und der Perfusion des betroffenen
Gebietes.
Überreizung
hingegen kann gegenteilige Effekte auslösen, wie Neurotoxizität und
Verringerung der lokalen Durchblutung.
Neuriten, Gliazellen und Gefäße
kooperieren und beeinflussen sich gegenseitig.
Hippocampusformation und Gedächtnis

vgl.
dort
Die sogenannte Hippocampusformation  (folgende Abbildungen) im medialen Temporallappen umfasst den gyrus dentatus, den Hippocampus ("Ammonshorn", cornu ammonis) und das Subiculum.
(folgende Abbildungen) im medialen Temporallappen umfasst den gyrus dentatus, den Hippocampus ("Ammonshorn", cornu ammonis) und das Subiculum.
 Der gyrus dentatus
Der gyrus dentatus  gilt als die Eingangspforte für das Hippocampussystem, Afferenzen stammen aus dem entorhinalen Cortex via Perforansfasern. Er enthält Körnerzellen (granular cells), die glutamaterg und auch GABAerg auf Pyramidenzellen des Ammonshorns projizieren. Der gyrus dentatus übernimmt eine Vorverarbeitung eintreffender Informationen, die je nach ihrer Bedeutung und Neuigkeit bewertet und separiert (spezialisiert) verarbeitet werden (pattern separation). Der gyrus dentatus hilft bei Mustererkennung, getrennter Verarbeitung, Orientierung im Raum, Aufrufen von Gedächtnisinhalten.
gilt als die Eingangspforte für das Hippocampussystem, Afferenzen stammen aus dem entorhinalen Cortex via Perforansfasern. Er enthält Körnerzellen (granular cells), die glutamaterg und auch GABAerg auf Pyramidenzellen des Ammonshorns projizieren. Der gyrus dentatus übernimmt eine Vorverarbeitung eintreffender Informationen, die je nach ihrer Bedeutung und Neuigkeit bewertet und separiert (spezialisiert) verarbeitet werden (pattern separation). Der gyrus dentatus hilft bei Mustererkennung, getrennter Verarbeitung, Orientierung im Raum, Aufrufen von Gedächtnisinhalten.
Die subgranuläre Zone des dreischichtigen gyrus dentatus ist vermutlich zu Neurogenese aus Stammzellen auch bei erwachsenen Menschen fähig (pro Tag mehrere hundert neue Nervenzellen).
 Der Hippocampus
- ein 5 cm langer Streifen allocorticaler grauer Substanz im gyrus parahippocampalis,
dessen Form im Querschnitt an das gekrümmte Horn eines Schafbocks
erinnert und deswegen auch als Ammonshorn (CA:
cornu ammonis) bezeichnet wird - ist zentral an der Überführung von
Inhalten des Kurzzeit- zu solchen des Langzeitgedächtnisses beteiligt.
Weiters baut er räumliches Gedächtnis auf, was für die Bewegung des
Körpers im Raum (Navigation) wesentlich ist. Seine mit dem Code CA
bezeichneten Neurone (
Der Hippocampus
- ein 5 cm langer Streifen allocorticaler grauer Substanz im gyrus parahippocampalis,
dessen Form im Querschnitt an das gekrümmte Horn eines Schafbocks
erinnert und deswegen auch als Ammonshorn (CA:
cornu ammonis) bezeichnet wird - ist zentral an der Überführung von
Inhalten des Kurzzeit- zu solchen des Langzeitgedächtnisses beteiligt.
Weiters baut er räumliches Gedächtnis auf, was für die Bewegung des
Körpers im Raum (Navigation) wesentlich ist. Seine mit dem Code CA
bezeichneten Neurone ( Abbildung unten) kooperieren in Kreisschaltungen in einer Weise, welche synaptische Langzeitverstärkung (LTP, long term potentiation) und Gedächtniskonsolidierung unterstützt.
Abbildung unten) kooperieren in Kreisschaltungen in einer Weise, welche synaptische Langzeitverstärkung (LTP, long term potentiation) und Gedächtniskonsolidierung unterstützt.
 Das Subiculum
ist der unterste Anteil der Hippocampusformation. Es ist vermutlich am
Arbeitsgedächtnis, vielleicht auch an der hypothalamisch-hypophysären
Regulation beteiligt.
Das Subiculum
ist der unterste Anteil der Hippocampusformation. Es ist vermutlich am
Arbeitsgedächtnis, vielleicht auch an der hypothalamisch-hypophysären
Regulation beteiligt.
In der Nachbarschaft der Hippocampusformation liegen der entorhinale Cortex (dieser wird der Hippocampusformation oft auch zugezählt), das Prä- (Brodmann 27) und Parasubiculum (Brodmann 49).
Für den Aufbau von Gedächtnisinhalten benötigt man synaptische Verstärkungen und das Etablieren neuer Synapsen (Synaptogenese), unterstützt
durch Kreisschaltungen, wie
sie
im Hippocampusvorluegen. Dabei führt die Koinzidenz von
Erregungsmustern zu synaptischer Verstärkung und Aufbau perpetuierter
Funktionskreise, die beim "Erinnern" mobilisiert werden können.
So bewirkt in einer typischen in-vivo-Versuchssituation wiederholte elektrische Reizung (in Abständen von 10 bis 30 Sekunden) einer
einzelnen
Schaffer'schen Kollaterale (präsynaptisch) an einer zugeordneten
CA1-Zelle (postsynaptisch) immer wieder EPSPs identer Stärke (kein
Lerneffekt). Depolarisiert man aber das CA1-Neuron über einen
zusätzlichen Reiz, nimmt die EPSP-Amplitude bei gleichzeitiger Reizung
der Schaffer'schen Kollaterale deutlich zu (Langzeitpotenzierung, Lerneffekt).
fMRI-Studien
haben gezeigt, dass Aktivierung und Stoffwechsel des Hippocampus mit
der Zahl der Assoziationen von Gedächtnisinhalten zunimmt. Der
Hippocampus (vor allem dessen posteriore Anteile) ist am Auffinden
epidodischer, semantischer wie auch autobiographischer
Gedächtnisinhalte beteiligt - dabei reaktiviert er Inhalte des
Langzeitgedächtnisses. Die Mobilisiereung von Teilaspekten einer Erinnerung
können ein umfassenderes Gedächtnismuster aktivieren (pattern completion).
Der Hippocampus
erhält Information aus Hirnregionen, die sich mit
Objekterkennung und -zuordnung befassen (visuell, akustisch), stellt
räumlich-zeitliche Zusammenhänge her und steuert entsprechende
affektive und Verhaltensreaktionen. Dabei greifen sie auf die Aktivität
von Zellen zurück, welche die Orientierung unterstützen (grid cells, place cells).
Auch scheint der Hippocampus an Zukunftsplanungen beteiligt zu sein
(Verknüpfung von Elementen aus dem Repertoire von Gedächtnisinhalten
bei mentaler Projektion auf zukünftige Problemlösungen).

 Abbildung: Hippocampusformation
Abbildung: Hippocampusformation
Nach einer Vorlage in Banich / Compton, Cognitive Neuroscience, 4th ed. 2018, Cambridge Univ. Press
Ein
Hippocampuspräparat (links) erinnert in seiner Form an die Gestalt
eines Seepferdchens (rechts) - daher der Name. Der "Kopf" entspricht dem Gebiet um den
gyrus dentatus, der "Schwanz" dem entorhinalen Cortex

Wie kann das Gehirn neu ankommende
Information speichern und Gedächtnisinhalte
organisieren? Wiederholte Anregung interneuronaler synaptischer Verbindungen kann durch Stärkung des synaptischen Effekts zum Aufbau von "Gedächtnispuren"
führen. Dabei ist der Hippocampus für das Wiedererkennen und Merken
neuer Eindrücke essentiell, vor allem für das explizite Gedächtnis.
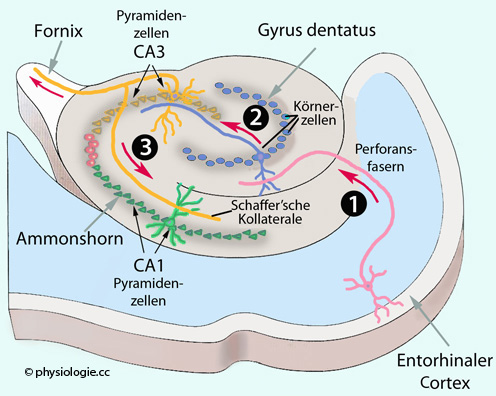

 Abbildung: Hippocampusformation und "trisynaptischer Schaltkreis"
Modifiziert nach einer Vorlage in Bear / Connors / Paradiso, Neuroscience - Exploring the Brain, 4th Ed Williams & Wilkins 2015
Abbildung: Hippocampusformation und "trisynaptischer Schaltkreis"
Modifiziert nach einer Vorlage in Bear / Connors / Paradiso, Neuroscience - Exploring the Brain, 4th Ed Williams & Wilkins 2015
Im Hippocampus sind zwei Schichten grauer Substanz umeinandergewickelt: Der gyrus dentatus und das Ammonshorn (Cornu Ammonis, CA). Zentral ist ein aus drei Neuronen aufgebauter Schaltkreis, von dem man annimmt, dass er episodisches Gedächtnis ermöglicht (trisynaptic loop).
Der Eingang in das System sind Axone aus dem entorhinalen Cortex (1: Perforansfasern, rosa dargestellt). Diese regen Körnerzellen (granule cells) (blau dargestellt) des gyrus dentatus an. Deren Axone (Moosfasern) regen CA3-Zellen im Ammonshorn an (2). Die Axone der CA3-Zellen (gelb dargestellt) ziehen über den Fornix aus dem Hippocampus; Kollateralen davon (Schaffer-Kollateralen) regen wiederum CA1-Neurone im Ammonshorn an (3).
Das Ammonshorn besteht aus mehreren Feldern (hippocampal subfields):
 CA1-Neurone (grün dargestellt) entsenden Neurone in das Subiculum (zwischen entorhinalem Cortex und CA1 gelegen). CA1-Neurone zeigen Langzeitpotenzierung
- Dendriten aktivierter Pyramidenzellen lagern AMPA-Rezeptoren in ihre Membran ein und verstärken hier die
Synapsenwirkung zusammen mit (dort schon vorhandenen)
NMDA-Rezeptoren. Diese Dendriten bilden eine dicke Schichte (stratum radiatum) der CA1-Region, hier wirken Synapsen von
Schaffer'schen Kollateralen (Axone aus der CA3-Region).
CA1-Neurone (grün dargestellt) entsenden Neurone in das Subiculum (zwischen entorhinalem Cortex und CA1 gelegen). CA1-Neurone zeigen Langzeitpotenzierung
- Dendriten aktivierter Pyramidenzellen lagern AMPA-Rezeptoren in ihre Membran ein und verstärken hier die
Synapsenwirkung zusammen mit (dort schon vorhandenen)
NMDA-Rezeptoren. Diese Dendriten bilden eine dicke Schichte (stratum radiatum) der CA1-Region, hier wirken Synapsen von
Schaffer'schen Kollateralen (Axone aus der CA3-Region).
 CA2-Neurone liegen zwischen CA1 und CA3. Auch sie erhalten Afferenzen über Perforans-Fasern.
CA2-Neurone liegen zwischen CA1 und CA3. Auch sie erhalten Afferenzen über Perforans-Fasern.
 CA3-Neurone erhalten Afferenzen über Moosfasern der Körnerzellen im
gyrus dentatus und über Perforansfasern aus dem entorhinalen Cortex.
Ihre Axone projizieren auf CA1 und CA2 über Schaffer'sche
Kollateralen, sowie auf CA3 zurück.
CA3-Neurone erhalten Afferenzen über Moosfasern der Körnerzellen im
gyrus dentatus und über Perforansfasern aus dem entorhinalen Cortex.
Ihre Axone projizieren auf CA1 und CA2 über Schaffer'sche
Kollateralen, sowie auf CA3 zurück.
 CA4 gilt als polymorphe Schichte des gyrus dentatus.
CA4 gilt als polymorphe Schichte des gyrus dentatus.
Der gyrus dentatus bildet lebenslang Nervenzellen nach (Neurogenese, adult neurogenesis). Solche jungen Neuriten sind plastischer als "alte" und zeigen verstärkte Langzeitpotenzierung

Synaptische Plastizität ist überall im Gehirn nachweisbar, sie ist an der CA3-CA1-
Synapse besonders intensiv untersucht worden. In CA1 erfolgt
Langzeitpotenzierung an NMDA- / AMPA-Synapsen: Letztere werden bei
niedriger Aktivität an der Synapse alleine angeregt (NMDA-Rezeptoren
sind Magnesium-blockiert). Bei
intensiver Glutamatausschüttung hingegen wird die postsynaptische
Membran ausreichend depolarisiert (Natriumeinstrom durch AMPA), um den
Block aufzuheben, und die NMDA-Kanäle lassen Calciumionen in die
postsynaptische Zelle, mit der Folge aktivierter Proteinkinasen, Aktivierung von CREB und
Einbau zahlreicher weiterer AMPA-Rezeptoren. Die Synapse wird
empfindlicher gegenüber Glutamat.
Neben
exzitatorischen Neuronen finden sich verschiedene inhibierende Interneurone, die Vorwärts- und Rückwärts-Hemmung aufbauen und
rhythmische Aktivitätsmuster generieren. Modifikationen sind jederzeit
möglich, die Verbindungen dynamisch veränderbar. Das in der Abbildung
gezeigte Modellnetzwerk dient als Grundlage für das Verständnis der Gedächtnisbildung.
CA1 ist der wichtigste
Ursprungsort der Efferenzen aus dem Hippocampus; deren Axone
projizieren z.T. auf den entorhinalen Cortex (tiefere Schichten) zurück
- direkt oder über Umschaltung im Subiculum ( Abbildung unten). CA3-Neuronen
(Pyramidenzellen) bilden auch untereinander starke exzitatorische
Konnexe. Auch das dient offenbar der Verstärkung von Gedächtnisspuren,
kann aber bei Übererregung zur Auslösung von Krämpfen führen.
Auch erhält CA3 anregende Projektionen aus der kleinen benachbarten CA2-Region;
diese wiederum wird aus dem entorhinalen Cortex (lamina II) direkt und
indirekt (über gyrus dentatus und CA3) angeregt, erhält aber auch
Impulse aus dem Hypothalamus (nucl.
paraventricularis und supraopticus). Die CA2-Region speichert soziale
Erinnerungen (Personenerkennung); ihre Neurone exprimieren intensiv
Rezeptoren für Oxytozin und Vasopressin.
All diese
Kreisschaltungen dienen offenbar der Speicherung und Verwertung von
Gedächtnisinhalten. Eine zentrale Bedeutung hat der NMDA-Rezeptor mit seinen besonderen Eigenschaften. Er findet sich vor allem in der CA1-Region des Hippocampus.
Abbildung unten). CA3-Neuronen
(Pyramidenzellen) bilden auch untereinander starke exzitatorische
Konnexe. Auch das dient offenbar der Verstärkung von Gedächtnisspuren,
kann aber bei Übererregung zur Auslösung von Krämpfen führen.
Auch erhält CA3 anregende Projektionen aus der kleinen benachbarten CA2-Region;
diese wiederum wird aus dem entorhinalen Cortex (lamina II) direkt und
indirekt (über gyrus dentatus und CA3) angeregt, erhält aber auch
Impulse aus dem Hypothalamus (nucl.
paraventricularis und supraopticus). Die CA2-Region speichert soziale
Erinnerungen (Personenerkennung); ihre Neurone exprimieren intensiv
Rezeptoren für Oxytozin und Vasopressin.
All diese
Kreisschaltungen dienen offenbar der Speicherung und Verwertung von
Gedächtnisinhalten. Eine zentrale Bedeutung hat der NMDA-Rezeptor mit seinen besonderen Eigenschaften. Er findet sich vor allem in der CA1-Region des Hippocampus.
 Der Hippocampus ist unverzichtbar für die Bildung und Rekapitulation
räumlicher, kontextueller und episodischer Gedächtnisinhalte. Er repräsentiert vom entorhinalen Cortex des gyrus parahippocampalis zugeleitete (Abbildungen) räumlich
organisierte sensorische Information in kontextspezifischer Weise.
Der Hippocampus ist unverzichtbar für die Bildung und Rekapitulation
räumlicher, kontextueller und episodischer Gedächtnisinhalte. Er repräsentiert vom entorhinalen Cortex des gyrus parahippocampalis zugeleitete (Abbildungen) räumlich
organisierte sensorische Information in kontextspezifischer Weise.
 Zur Bedeutung des Hippocampus für Gedächtnis und Raumorientierung s. dort
Ohne die Aktivität des Hippocampus sind das Selbst und seine Umgebung betreffende Fakten nicht aufrufbar.
Der Hippocampus nimmt eine zentrale Stellung für Verbindungen ein, die zum Entstehen von Erinnerung notwendig sind. Er verfügt über reziproke Verbindungen mit dem parahippocampalen Cortex,
der aus so gut wie allen kortikalen Assoziationsarealen Informationen
über die aktuelle Situation der Person erhält.
Zur Bedeutung des Hippocampus für Gedächtnis und Raumorientierung s. dort
Ohne die Aktivität des Hippocampus sind das Selbst und seine Umgebung betreffende Fakten nicht aufrufbar.
Der Hippocampus nimmt eine zentrale Stellung für Verbindungen ein, die zum Entstehen von Erinnerung notwendig sind. Er verfügt über reziproke Verbindungen mit dem parahippocampalen Cortex,
der aus so gut wie allen kortikalen Assoziationsarealen Informationen
über die aktuelle Situation der Person erhält.
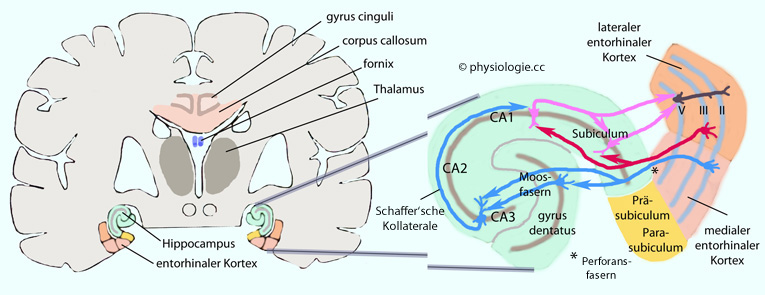
 Abbildung: Schaltungen in Subiculum und hippocampalem System
Nach Yu
et al. A circuit view of deep brain stimulation in Alzheimer’s disease
and the possible mechanisms. Molecular Neurodegeneration (2019) 14:33
Abbildung: Schaltungen in Subiculum und hippocampalem System
Nach Yu
et al. A circuit view of deep brain stimulation in Alzheimer’s disease
and the possible mechanisms. Molecular Neurodegeneration (2019) 14:33
Links: Schnitt (Frontalebene) durch das Gehirn mit Hippocampus und entorhinalem Cortex im medialen Temporalhirn.
Rechts: Hippocampus-Netzwerk. Das
Subiculum liegt zwischen gyrus dentatus und entorhinalem Cortex und
verbindet den Hippocampus mit dem gyrus parahippocampalis; vermutlich
trifft es die endgültige Entscheidung über die Informationsverwaltung
des Hippocampus. Dessen Rindengebiete werden - nach den vorwiegenden
Zellen - mit CA1 bis CA4 bezeichnet (CA, Cornu Ammonis).
Perforansfasern sind
Axone von Neuronen in Schichte II des entorhinalen Cortex, die
über Moosfasern (z.T. indirekt: Umschaltung im gyrus dentatus, der als
Teil des Hippocampus gilt) auf CA3-Neurone projizieren
("trisynaptischer" exzitatorischer Pfad, blau); und solche von
Pyramidenzellen in Schichte III, die direkt auf CA1-Neurone projizieren
(rot).
Neurone von CA1 und dem Subiculum wiederum projizieren zurück auf
Schichte V des entorhinalen Cortex (violett). Auf diese Weise entsteht
eine Ringschaltung; mit dem
entorhinalen Cortex bestehen sowohl afferente als auch efferente Verbindungen

Vom Ammonshorn ziehen Bahnen zum Subiculum
und von dort zum entorhinalen Cortex. Die Funktion
solcher Verschaltungen ist einerseits die
Etablierung von Gedächtnisspuren (synaptische Potenzierung),
andererseits Musterabgleichung und Erinnerung an bereits gespeicherte Gedächtniselemente.
 Der Moosfaserpfad (Axone von Körnerzellen im gyrus dentatus) vermittelt bei hochfrequenter Reizung starken Ca++-Einstrom in präsynaptische Endigungen, Aktivierung der Proteinkinase A, erhöhte Glutamatfreisetzung
und EPSP-Verstärkung an Synapsen zu CA3-Zellen.
Der Moosfaserpfad (Axone von Körnerzellen im gyrus dentatus) vermittelt bei hochfrequenter Reizung starken Ca++-Einstrom in präsynaptische Endigungen, Aktivierung der Proteinkinase A, erhöhte Glutamatfreisetzung
und EPSP-Verstärkung an Synapsen zu CA3-Zellen.
 Beim Mechanismus über Schaffer'sche Kollaterale
handelt es sich hingegen um assoziative Verstärkung, d.h. prä- und
postsynaptische Erregung müssen zeitlich zusammenwirken
("Koinzidenzdetektor": NMDA-Öffnung bei gleichzeitiger Aktivierung von
AMPA-Kanälen -
Beim Mechanismus über Schaffer'sche Kollaterale
handelt es sich hingegen um assoziative Verstärkung, d.h. prä- und
postsynaptische Erregung müssen zeitlich zusammenwirken
("Koinzidenzdetektor": NMDA-Öffnung bei gleichzeitiger Aktivierung von
AMPA-Kanälen -  Abbildung).
Input-Spezifität:
Der Lernvorgang am CA1-Neuron betrifft nur den trainierten Synapsenapparat: Wiederholte Reizung anderer Eingänge an die CA1-Zelle haben auf die synaptische Kapazität des konditionierten Systems keinen Einfluss.
Abbildung).
Input-Spezifität:
Der Lernvorgang am CA1-Neuron betrifft nur den trainierten Synapsenapparat: Wiederholte Reizung anderer Eingänge an die CA1-Zelle haben auf die synaptische Kapazität des konditionierten Systems keinen Einfluss.
Zirkuläre Verschaltungen (Papez-Kreise): Kreisschaltungen sind z.B. Hippocampus → Fornix → Mamillarkörper → fasciculus mamillothalamicus → nuclei anteriores thalami → tractus thalamocingularis → gyrus cinguli → Hippocampus, wie z.B. zu granulären Zellen im gyrus dentatus zu Moosfasern zu CA3-Zellen und schließlich Schaffer'schen Kollateralen zu CA1-Zellen.
Regenerierung des Neuronenpools: Der Hippocampus bildet
laufend neue Neurone - die jungen Nervenzellen sind außerordentlich erregbar und bilden zahlreiche synaptische Kontakte aus, die der Ausbildung neuer Engramme dienen. Dazu
synchronisieren sich Zellen des Hippocampus und der
parahippocampalen Region, es bilden sich Zellgruppen aus, deren
synaptische Organisation komplexe Gedächtnisfunktionen ermöglicht (z.B.
Ortserkennung: Ortszellen, Ortsfelder).
Versuchstiere
mit genetisch veränderten Komponenten der zur Ausprägung von Erinnerung
und Gedächtnis nötigen Elemente (z.B. mutierte Calmodulinkinase CaMKII,
s. Abbildungen unten) sind zu entsprechenden Erinnerungen (z.B. räumliche Orientierung) nicht mehr fähig.
Weitere am Gedächtnis beteiligte Hirnregionen
Der
Hippocampus konsolidiert und speichert Gedächtnisinhalte, ist aber
nicht alleine für Erinnerung und Lernen zuständig; dies sind Leistungen
mehrerer Gehirnabschnitte, und das Bewusstsein bedarf nicht
notwendigerweise hippocampaler Aktivität. Lernen und Erinnern stehen
auch unter dem Einfluss nichthippocampaler Gehirngebiete:
 Limbischer, wie die Mandelkerne (Gedächtnis und Emotionen);
Limbischer, wie die Mandelkerne (Gedächtnis und Emotionen);
 neokortikaler,
wie das ventrale visuelle System (Verarbeitung und Zugriff), die
vordere Temporalregion (Speicherung semantischer Information) oder das
Präfrontalhirn (Beurteilung, Fokussierung, Handlungsstrategie);
neokortikaler,
wie das ventrale visuelle System (Verarbeitung und Zugriff), die
vordere Temporalregion (Speicherung semantischer Information) oder das
Präfrontalhirn (Beurteilung, Fokussierung, Handlungsstrategie);
 subkortikaler, wie die Basalganglien (motorische Geschicklichkeit).
Gedächtnis wird nicht nur nach seiner Art typisiert (s. oben), sondern auch nach Stadien seiner Bearbeitung. Gedächtnisinhalte müssen gebildet (coding) und anschließend gespeichert werden (storage), wobei sie stabilisiert bzw. verstärkt werden können (consolidation). Und um sie nutzbar zu machen, werden sie abgerufen (retrieval). In welchen Teilen des Gehirns laufen diese verschiedenen Vorgänge ab?
subkortikaler, wie die Basalganglien (motorische Geschicklichkeit).
Gedächtnis wird nicht nur nach seiner Art typisiert (s. oben), sondern auch nach Stadien seiner Bearbeitung. Gedächtnisinhalte müssen gebildet (coding) und anschließend gespeichert werden (storage), wobei sie stabilisiert bzw. verstärkt werden können (consolidation). Und um sie nutzbar zu machen, werden sie abgerufen (retrieval). In welchen Teilen des Gehirns laufen diese verschiedenen Vorgänge ab?
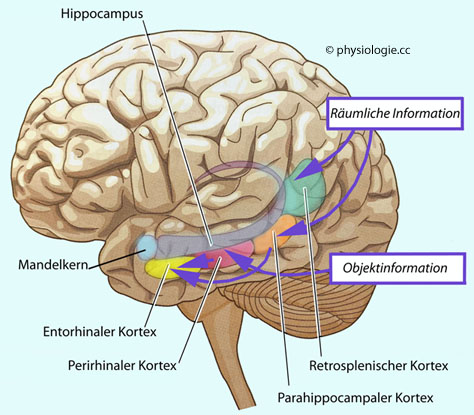
 Abbildung: An der Gedächtnisbildung beteiligte Regionen im mittleren Temporalhirn
Nach einer Vorlage in Banich / Compton, Cognitive Neuroscience, 4th ed. 2018, Cambridge Univ. Press
Abbildung: An der Gedächtnisbildung beteiligte Regionen im mittleren Temporalhirn
Nach einer Vorlage in Banich / Compton, Cognitive Neuroscience, 4th ed. 2018, Cambridge Univ. Press
Verschiedene Cortexareale sind auf unterschiedliche Gedächtnisleistungen spezialisiert: Der
retrosplenische und parahippocampale Cortex bearbeiten räumliche
Information, der perirhinale Cortex Information über Gegenstände, der
entorhinale von der Modalität unabhängige semantische Information

Gedächtnis
entsteht vor allem in zwei Hirnregionen: Im mittleren Temporallappen
(Hippocampus und assoziierte Hirngebiete,  Abbildung) und im Präfrontalcortex. An den Hippocampus grenzen
Abbildung) und im Präfrontalcortex. An den Hippocampus grenzen
 der retrosplenische Cortex
(entspricht Brodmann 29 und 30), ein assoziatives Rindengebiet, das
hinter dem Splenium des corpus callosum liegt und sich an episodischem
Gedächtnis, Raumanalyse und Körpernavigation ("ich" vs. "Umwelt")
beteiligt;
der retrosplenische Cortex
(entspricht Brodmann 29 und 30), ein assoziatives Rindengebiet, das
hinter dem Splenium des corpus callosum liegt und sich an episodischem
Gedächtnis, Raumanalyse und Körpernavigation ("ich" vs. "Umwelt")
beteiligt;
 der parahippocampale Cortex, zusammen mit dem retrosplenischen dient er offenbar vor allem der Projektion räumlicher Hinweise zur Gedächtnisbildung. Seine parahippocampal place area
(PPA) speichert und erkennt Umweltmuster (Räume, Landschaften), andere
Teile - vor allem im rechten gyrus parahippocampalis - erkennen soziale
Kontexte (z.B. Ironie, Sarkasmus);
der parahippocampale Cortex, zusammen mit dem retrosplenischen dient er offenbar vor allem der Projektion räumlicher Hinweise zur Gedächtnisbildung. Seine parahippocampal place area
(PPA) speichert und erkennt Umweltmuster (Räume, Landschaften), andere
Teile - vor allem im rechten gyrus parahippocampalis - erkennen soziale
Kontexte (z.B. Ironie, Sarkasmus);
 der perirhinale Cortex (Brodmann 35 / 36) verarbeitet Information über Objekte und ihre Identität;
der perirhinale Cortex (Brodmann 35 / 36) verarbeitet Information über Objekte und ihre Identität;
 der entorhinale Cortex
(Brodmann 28 / 34) erhält und verwaltet Informationen, die über
getrennte Modalitäten hinausgehen können und sowohl räumliche als auch
zeitliche Komponenten haben.
Gedächtniscodierung erfolgt auch im Präfrontalhirn, vor allem in dessen ventrolateralem Cortex, wobei hier die Bedeutung der Information für die jeweils aktuelle Situation bewertet wird (Auswahl, Handlungsrelevanz). Der dorsolaterale Präfrontalcortex beteiligt sich mit Vergleich und allfälliger Umordnung von Relevanzen (Handlungsreihenfolge). Dabei besteht Lateralisierung: So wird der linke Präfrontalcortex bei verbalen
der entorhinale Cortex
(Brodmann 28 / 34) erhält und verwaltet Informationen, die über
getrennte Modalitäten hinausgehen können und sowohl räumliche als auch
zeitliche Komponenten haben.
Gedächtniscodierung erfolgt auch im Präfrontalhirn, vor allem in dessen ventrolateralem Cortex, wobei hier die Bedeutung der Information für die jeweils aktuelle Situation bewertet wird (Auswahl, Handlungsrelevanz). Der dorsolaterale Präfrontalcortex beteiligt sich mit Vergleich und allfälliger Umordnung von Relevanzen (Handlungsreihenfolge). Dabei besteht Lateralisierung: So wird der linke Präfrontalcortex bei verbalen (Sprache), der
rechte bei nonverbalen Abläufen der Erinnerung (z.B. Gesichtserkennung) aktiviert.
Der präfromtale Cortex unterstützt das Aufrufen von Gedächtnisinhalten,
die er organisiert, selektioniert und evaluiert. Auch für die
(strategische) Unterdrückung von Erinnerungen spielt der Präfrontalcortex eine wichtige Rolle (inhibitorische Kontrolle).

 Abbildung: Netzwerke für Lernen und Gedächtnis
Nach einer Vorlage in Banich / Compton, Cognitive Neuroscience, 4th ed. 2018, Cambridge Univ. Press
Abbildung: Netzwerke für Lernen und Gedächtnis
Nach einer Vorlage in Banich / Compton, Cognitive Neuroscience, 4th ed. 2018, Cambridge Univ. Press
Unterschiedliche
kortikale Areale liefern verschiedene Aspekte des Gedächtsnisses: Das
hippocampale System konzentriert sich auf deklaratives und
episodisches, der Mandelkern auf emotionales, das Striatum auf
prozedurales / implizites Gedächtnis.
Der dorsolaterale Präfrontalcortex kümmert sich vor allem um
Arbeitsgedächtnis, der ventrolaterale um Speicherung / Erinnern,
zusammen mit dem Partietalcortex. Gebiete wie der untere Temporalcortex
vermitteln sensorische, der motorische Cortex Bewegungserinnerungen

Das Präfrontalhirn kümmert sich um
strategische Aspekte des Gedächtnisses: Organisation, Selektion,
Evaluation der Inhalte. Dabei spielt die Seite eine Rolle: Der linke posteriore Präfrontalcortex ist bei verbalen Aufgaben aktiv (z.B. Worterkennung), der rechte bei nicht-verbalen (z.B. Gesichtserkennung). Auch für die Unterdrückung des Aufrufens von Gedächtnisinhalten spielt der präfrontale Cortex eine Rolle (inhibitorische Kontrollfunktion).
Das Parietalhirn steuert
ebenfalls zum Gedächtnis bei - vor allem was die "innere
Repräsentierung" des Körpers betrifft -, wenn auch bei Läsionen keine
gravierenden Lern- und Merkstörungen beobachtet werden (ähnlich wie
beim Präfrontalhirn).
Motorischer Cortex und Basalganglien schließlich (insbesondere das Striatum: Putamen, globus pallidus,  Abbildung) sind in motorische Lern-, Merk- und Gedächtnisabläufe involviert. Zu entsprechenden Fähigkeiten des Kleinhirns s. dort.
Abbildung) sind in motorische Lern-, Merk- und Gedächtnisabläufe involviert. Zu entsprechenden Fähigkeiten des Kleinhirns s. dort.
Arten des Lernens
Beim
Lernen geht es nicht nur um das Speichern von Information, sondern auch
um die Auswirkung davon, etwa das Erwerben von Fähigkeiten. Werden
Tatsachen oder Fähigkeiten erlernt, ohne dass Reize bzw.
Verhaltensweisen verknüpft werden müssen (Konditionierung), spricht man
von nicht-assoziativem Lernen. Geht es darum, eine Verbindung zwischen einem Reiz (stimulus) und einer Reaktion (response) herzustellen, spricht man von assoziativem Lernen.
Das Erlernte kann im Bereich bewusster Verarbeitung liegen (wobei man das deklarative
Gedächtnis beansprucht), oder die untersuchten Reiz-Reaktions-
Verknüpfungen laufen auf un(ter)bewusster Ebene ab. Aus
neurophysiologischer Sicht kann man dann Lernerfolge einerseits an vegetativen Reaktionen auf auslösende Reize ablesen, wie das bei der klassischen Konditionierung geschieht; oder es geht um motorische Abläufe, die bei der operanten Konditionierung beeinflusst werden sollen.
 Abbildung: Klassische Konditionierung
Nach einer Vorlage bei Myers DG, DeWall CN, Psychology in Everyday Life, 4th ed. 2017
Abbildung: Klassische Konditionierung
Nach einer Vorlage bei Myers DG, DeWall CN, Psychology in Everyday Life, 4th ed. 2017
Der
unkonditionierte Reiz (Blick auf / Duft und Geschmack von Futter) ist
derjenige, der natürlicherweise den Salivationsreflex auslöst und zur
unkonditionierten Reaktion (Speichelfluss) führt.
Die Konditionierung besteht darin, wiederholt auf einen neutralen Reiz (hier: akustisch) den unkonditionierten Reiz folgen zu lassen.
Nach
erfolgreicher Konditionierung reicht der neutrale Reiz alleine zur
Reflexaktivierung, er wird dadurch zum "konditionierten" Reiz

 Klassische Konditionierung (
Klassische Konditionierung ( Abbildung): Hier geht es darum, eine neuronale Verknüpfung zwischen einem neutralen Sinnesreiz und einem knapp darauf folgenden unkonditionierten Reiz (unconditioned stimulus) herzustellen. Als unkonditioniert bezeichnet man einen Reiz, der zu einer physiologisch "vorprogrammierten" Antwort führt (z.B. Perzipierung von Futter → Salivation).
Abbildung): Hier geht es darum, eine neuronale Verknüpfung zwischen einem neutralen Sinnesreiz und einem knapp darauf folgenden unkonditionierten Reiz (unconditioned stimulus) herzustellen. Als unkonditioniert bezeichnet man einen Reiz, der zu einer physiologisch "vorprogrammierten" Antwort führt (z.B. Perzipierung von Futter → Salivation).
Ist die neuronale Verknüpfung erfolgreich erfolgt, reicht der neutrale Reiz alleine aus, eine entsprechende Antwort auszulösen ( Abbildung). Man sagt, der neutrale Reiz ist zu einem "konditionierten" geworden und löst eine konditionierte Reaktion (conditioned response) aus.
Abbildung). Man sagt, der neutrale Reiz ist zu einem "konditionierten" geworden und löst eine konditionierte Reaktion (conditioned response) aus.
Das klassische Beispiel dafür ist der von Ivan Pawlow
beobachtete Konditionierungseffekt ("Pawlow'scher Hund": Versuchstier reagiert mit Speichelfluss auf einen neutralen Reiz alleine, wenn er der Fütterung regelmäßig vorausgegangen ist).
 Operante Konditionierung: Von verschiedenen Verhaltensweisen (z.B. nach Futter suchen, zu einem Lichtsignal laufen,..) führt nur eine (z.B. Drücken eines Schalters) zum Erfolg (z.B. Fütterung). Das
lernt das Versuchstier nach dem Prinzip von Versuch und Irrtum. Das
Versuchsdesign kann auch bestimmte Verhaltensweisen bestrafen (z.B.
Stromschlag). Belohnung führt zu positiver, Bestrafung zu negativer Konditionierung.
Operante Konditionierung: Von verschiedenen Verhaltensweisen (z.B. nach Futter suchen, zu einem Lichtsignal laufen,..) führt nur eine (z.B. Drücken eines Schalters) zum Erfolg (z.B. Fütterung). Das
lernt das Versuchstier nach dem Prinzip von Versuch und Irrtum. Das
Versuchsdesign kann auch bestimmte Verhaltensweisen bestrafen (z.B.
Stromschlag). Belohnung führt zu positiver, Bestrafung zu negativer Konditionierung.
Wichtig für den Lernerfolg (Herstellen neuronaler Verknüpfungen) ist,
dass die Belohnung oder Bestrafung unmittelbar auf die zu lernende
Verhaltensweise folgt (räumliche und zeitliche Nähe: Kontiguität),
optimalerweise sollte der zeitliche Abstand etwa eine halbe Sekunde
betragen. Auch muss die Kombination für das Versuchstier verlässlich
sein (Kausalzusammenhang, Kontingenz). Kommt es zu einer Dissoziation dieser Verknüpfung, "verlernt" das Tier die Verknüpfung wieder (Extinktion). Extinktion, Sensitivierung (Verstärkung einer physiologischen Reaktion, z.B. bei hoher Reizintensität) oder Habituation
(Gewöhnung an bestimmte Reize, Abnahme der physiologischen Reaktion)
sind Anpassungsprozesse, die im Rahmen des assoziativen Lernens
auftreten können.
Klassische und operante Konditionierung spielen auch im alltäglichen Leben
des Menschen in verschiedenster Form eine Rolle, ohne dass die Betroffenen sich
dessen bewusst sein müssen.
 Über zerebelläre Konditionierungsmechanismen s. dort
Über zerebelläre Konditionierungsmechanismen s. dort

Gedächtnisstörungen
(Amnesien) können den Übertritt ins Langzeitgedächtnis betreffen
(anterograde Amnesie): Durch Erkrankungen wie das Korsakoff- oder Wernicke-Korsakoff-Syndrom
 (infolge Hirnschädigung, Thiaminmangel, Alkoholabusus u.a.) oder schockartige Ereignisse (Unfall,
Blutung) verklingen neue Gedächtnisinhalte spurlos. Der Patient ist ab
dem auslösenden Ereignis unfähig, sich Neues zu merken; soeben Erlebtes wird gleich wieder vergessen.
(infolge Hirnschädigung, Thiaminmangel, Alkoholabusus u.a.) oder schockartige Ereignisse (Unfall,
Blutung) verklingen neue Gedächtnisinhalte spurlos. Der Patient ist ab
dem auslösenden Ereignis unfähig, sich Neues zu merken; soeben Erlebtes wird gleich wieder vergessen.
Eine Degeneration der Mamillarkörper - die über die Fornix Impulse aus dem Subiculum erhalten und über den tractus mamillothalamicus
mit dem Thalamus, sowie mittels des tractus mamillotegmentalis mit der
Mittelhirnhaube verbunden sind - kommt u.a. bei Alkoholabusus vor,
dabei kann es zu gravierendem Gedächtnisverlust kommen; die genaue
Funktion der Mamillarkörper ist noch unbekannt.
Durch
Gehirnerschütterung, Gehirnschlag oder ähnliche Akutereignisse kann das Langzeitgedächtnis angegriffen sein (retrograde Amnesie).
Je schwerer die Schädigung, umso weiter in die Vergangenheit greift das
zurückgreifende Vergessen. Retrograde Amnesien sind oft mit antegraden
kombiniert. Amnesien können sich mit Besserung des Zustandes weitgehend
wieder zurückbilden, scheinbar verlorene Gedächtnisinhalte wieder
auffindbar werden.

  Das Kurzzeitgedächtnis speichert via limbisches System Sinnesmeldungen
in der Gehirnrinde. Zunächst entstehen sensorische Zwischenspeicher in
Form berarbeiteter Informationspakete (z.B. visuelle "Wo"-Inhalte im
Parietalhirn, "Was"-Inhalte im Temporalhirn)
Das Kurzzeitgedächtnis speichert via limbisches System Sinnesmeldungen
in der Gehirnrinde. Zunächst entstehen sensorische Zwischenspeicher in
Form berarbeiteter Informationspakete (z.B. visuelle "Wo"-Inhalte im
Parietalhirn, "Was"-Inhalte im Temporalhirn)
 Als Komponente des
Kurzzeitgedächtnisses speichert das Arbeitsgedächtnis für Sekunden sensorische Information in
einem Informationspuffer. Dabei steigt die Aktivität des Parahippocampus
und des Präfrontalhirns Als Komponente des
Kurzzeitgedächtnisses speichert das Arbeitsgedächtnis für Sekunden sensorische Information in
einem Informationspuffer. Dabei steigt die Aktivität des Parahippocampus
und des Präfrontalhirns
 Das Langzeitgedächtnis sitzt vor allem in Regionen, in welche der
betreffende Sinneseindruck projiziert wurde. Das sekundäre Gedächtnis
verfügt über große Kapazität und speichert über Jahre, der Zugriff
erfolgt über ”Nachdenken“. Inhalte im tertiären Gedächtnis sind sofort
verfügbar und gehen normalerweise nicht verloren
Das Langzeitgedächtnis sitzt vor allem in Regionen, in welche der
betreffende Sinneseindruck projiziert wurde. Das sekundäre Gedächtnis
verfügt über große Kapazität und speichert über Jahre, der Zugriff
erfolgt über ”Nachdenken“. Inhalte im tertiären Gedächtnis sind sofort
verfügbar und gehen normalerweise nicht verloren
 Deklaratives (explizites, bewusstes) Gedächtnis (Wissensgedächtnis)
speichert Fakten und Episoden, es wird im Temporallappen gespeichert.
Nicht-deklaratives (implizites, nicht-bewusstes) Gedächtnis
(Bewegungsabläufe - prozedurales Gedächtnis, Sprachgrammatik) wird in
Kleinhirn und Basalganglien gespeichert
Deklaratives (explizites, bewusstes) Gedächtnis (Wissensgedächtnis)
speichert Fakten und Episoden, es wird im Temporallappen gespeichert.
Nicht-deklaratives (implizites, nicht-bewusstes) Gedächtnis
(Bewegungsabläufe - prozedurales Gedächtnis, Sprachgrammatik) wird in
Kleinhirn und Basalganglien gespeichert
 Der Hippocampus ermöglicht das Entstehen von Erinnerungen. Dazu ist er
reziprok mit dem parahippocampalen Cortex verbunden - dieser bezieht
aktuelle Informationen aus kortikalen Assoziationsarealen - und ist in
die limbische Kreisschaltung ("Papez-Kreise") eingebaut, die zum Merken
und Erinnern notwendige Mechanismen aufbaut. Der Hippocampus erneuert
laufend seinen Neuronenpool, junge Neurone sind sehr erregbar und
bilden fortlaufend synaptische Kontakte aus, insbesondere
zur parahippocampalen Region. Junge Zellgruppen erfüllen dynamische
Gedächtnisfunktionen, z.B. zur Erkennung von Orten in der Umgebung
(Ortszellen,
Ortsfelder)
Der Hippocampus ermöglicht das Entstehen von Erinnerungen. Dazu ist er
reziprok mit dem parahippocampalen Cortex verbunden - dieser bezieht
aktuelle Informationen aus kortikalen Assoziationsarealen - und ist in
die limbische Kreisschaltung ("Papez-Kreise") eingebaut, die zum Merken
und Erinnern notwendige Mechanismen aufbaut. Der Hippocampus erneuert
laufend seinen Neuronenpool, junge Neurone sind sehr erregbar und
bilden fortlaufend synaptische Kontakte aus, insbesondere
zur parahippocampalen Region. Junge Zellgruppen erfüllen dynamische
Gedächtnisfunktionen, z.B. zur Erkennung von Orten in der Umgebung
(Ortszellen,
Ortsfelder)
 Das Speichern neuer Gedächtnisinhalte erfordert Neuroplastizität:
Präsynaptisch kann sich die freigesetzte / wiederaufgenommene
Transmittermenge (pro Aktionspotential), postsynaptisch der
Transmittereffekt (Zahl / Empfindlichkeit der Rezeptoren) bzw. -abbau
verändern; mit der Rezeptorzahl steigt der Effekt
(z.B. EPSP) pro Quantum freigesetzten Transmitters. Synapsen können
wachsen oder schrumpfen, verschwinden oder neu gebildet, ihr
Verbindungsmuster kann geändert werden
Das Speichern neuer Gedächtnisinhalte erfordert Neuroplastizität:
Präsynaptisch kann sich die freigesetzte / wiederaufgenommene
Transmittermenge (pro Aktionspotential), postsynaptisch der
Transmittereffekt (Zahl / Empfindlichkeit der Rezeptoren) bzw. -abbau
verändern; mit der Rezeptorzahl steigt der Effekt
(z.B. EPSP) pro Quantum freigesetzten Transmitters. Synapsen können
wachsen oder schrumpfen, verschwinden oder neu gebildet, ihr
Verbindungsmuster kann geändert werden
 Gliazellen beteiligen sich an Lernvorgängen: Astrozyten können Stellen
synaptischer Veränderung markieren, Oligodendrozyten die Myelinisierung verändern Gliazellen beteiligen sich an Lernvorgängen: Astrozyten können Stellen
synaptischer Veränderung markieren, Oligodendrozyten die Myelinisierung verändern
 Langzeitpotenzierung ist eine Zunahme der Synapsenstärke für mindestens
eine Stunde. Präsynaptische Aktionspotentialsalven führen zu
Glutamatfreisetzung und postsynaptischen EPSPs durch Kationeneinstrom.
An nicht aktivierten glutamatergen Synapsen sind die NMDA-Rezeptoren
durch Magnesiumionen blockiert. Vordepolarisation öffnet sie und Ca++
strömt ein, worauf Proteinkinase AMPA-Rezeptoren phosphoryliert, die in
die postsynaptische Membran eingeklagert werden ("AMPAfizierung"), Na+-Einstrom und Depolarisation verstärken (Langzeitpotenzierung LTP)
Langzeitpotenzierung ist eine Zunahme der Synapsenstärke für mindestens
eine Stunde. Präsynaptische Aktionspotentialsalven führen zu
Glutamatfreisetzung und postsynaptischen EPSPs durch Kationeneinstrom.
An nicht aktivierten glutamatergen Synapsen sind die NMDA-Rezeptoren
durch Magnesiumionen blockiert. Vordepolarisation öffnet sie und Ca++
strömt ein, worauf Proteinkinase AMPA-Rezeptoren phosphoryliert, die in
die postsynaptische Membran eingeklagert werden ("AMPAfizierung"), Na+-Einstrom und Depolarisation verstärken (Langzeitpotenzierung LTP)
 Wiederholte gleichzeitiger Erregung des prä- und postsynaptischen
Neurons (Koinzidenz: "Neurons that fire together wire together")
verstärkt entsprechende synaptische Verschaltungen für Tage bis Wochen.
Proteinkinasen, Phospholipasen und neuronale NO-Synthase erhöhen
Synapsenwirkung und -zahl, die synaptische Kapazität steigt
Wiederholte gleichzeitiger Erregung des prä- und postsynaptischen
Neurons (Koinzidenz: "Neurons that fire together wire together")
verstärkt entsprechende synaptische Verschaltungen für Tage bis Wochen.
Proteinkinasen, Phospholipasen und neuronale NO-Synthase erhöhen
Synapsenwirkung und -zahl, die synaptische Kapazität steigt
 Klassische Konditionierung
beruht auf der Verknüpfung eines (neutralen) Reizes (z.B. Glockenton)
mit einem knapp darauf folgenden unkonditionierten Reiz, der zu einer
Reflexantwort führt (z.B. Futter). Der neutrale Reiz reicht dann aus,
eine Antwort auszulösen: Er ist zu einem "konditionierten" geworden und
löst eine konditionierte Reaktion aus Klassische Konditionierung
beruht auf der Verknüpfung eines (neutralen) Reizes (z.B. Glockenton)
mit einem knapp darauf folgenden unkonditionierten Reiz, der zu einer
Reflexantwort führt (z.B. Futter). Der neutrale Reiz reicht dann aus,
eine Antwort auszulösen: Er ist zu einem "konditionierten" geworden und
löst eine konditionierte Reaktion aus
 Operante Konditionierung
ergibt sich, wenn von verschiedenen Verhaltensweisen nur eine zum
Erfolg führt (Versuch und Irrtum). Belohnung führt zu positiver,
Bestrafung zu negativer Konditionierung Operante Konditionierung
ergibt sich, wenn von verschiedenen Verhaltensweisen nur eine zum
Erfolg führt (Versuch und Irrtum). Belohnung führt zu positiver,
Bestrafung zu negativer Konditionierung
|

 Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.
Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.




 Ammonshorn (cornu Ammonis): Nach dem ägyptischen Gott Amun, der u.a. in der Form eines Widders verehrt wurde
Ammonshorn (cornu Ammonis): Nach dem ägyptischen Gott Amun, der u.a. in der Form eines Widders verehrt wurde

 Arten von Gedächtnis
Arten von Gedächtnis  Synaptische Plastizität, Langzeitpotenzierung / Langzeitdepression
Synaptische Plastizität, Langzeitpotenzierung / Langzeitdepression  Hippocampus und Erinnerung
Hippocampus und Erinnerung  Weitere am Gedächtnis beteiligte Hirnregionen
Weitere am Gedächtnis beteiligte Hirnregionen  Arten des Lernens
Arten des Lernens

 Gyrus parahippocampalis
Gyrus parahippocampalis  Koinzidenzdetektion
Koinzidenzdetektion  Entorhinaler Cortex
Entorhinaler Cortex  Langzeitpotenzierung
Langzeitpotenzierung  Langzeitdepression
Langzeitdepression
 Core messages
Core messages Das korrekte Auswachsen von Axonen wird durch spezielle chemotrope Proteine gesteuert, deren Konzentrationsgradient auf die Bewegung bzw. Wachstumsrichtung von Zielzellen entweder anziehend (attraction) oder abweisend wirken (repulsion). Sie werden z.T. sezerniert und werden über
Rezeptoren an der Zellmembran von Zielzellen erkannt und
beeinflusst die Richtung ihrer Fortbewegung bzw. ihres Vorwachsens.
Das korrekte Auswachsen von Axonen wird durch spezielle chemotrope Proteine gesteuert, deren Konzentrationsgradient auf die Bewegung bzw. Wachstumsrichtung von Zielzellen entweder anziehend (attraction) oder abweisend wirken (repulsion). Sie werden z.T. sezerniert und werden über
Rezeptoren an der Zellmembran von Zielzellen erkannt und
beeinflusst die Richtung ihrer Fortbewegung bzw. ihres Vorwachsens. ähneln in ihrem Aufbau dem extrazellulären Matrixprotein Laminin und helfen den Wachstumskegeln vorwachsender Neuriten, ihre synaptischen Ziele zu finden.
ähneln in ihrem Aufbau dem extrazellulären Matrixprotein Laminin und helfen den Wachstumskegeln vorwachsender Neuriten, ihre synaptischen Ziele zu finden. leiten nicht nur - sowohl efferente als auch afferente - Axone bei
Entwicklung und Heilung, sondern erfüllen auch Aufgaben im Rahmen von
Immunfunktionen und Knochenwachstum.
leiten nicht nur - sowohl efferente als auch afferente - Axone bei
Entwicklung und Heilung, sondern erfüllen auch Aufgaben im Rahmen von
Immunfunktionen und Knochenwachstum. Langzeitgedächtnis
Langzeitgedächtnis Information von den Sinnesorganen gelangt zunächst in das Kurzzeitgedächtnis. Es wird vom sensorimotorischen sowie präfrontalen Cortex verwaltet; zum Aufbau des Gedächtnisses (Lernprozess) ist die Hippocampusformation unverzichtbar.
Information von den Sinnesorganen gelangt zunächst in das Kurzzeitgedächtnis. Es wird vom sensorimotorischen sowie präfrontalen Cortex verwaltet; zum Aufbau des Gedächtnisses (Lernprozess) ist die Hippocampusformation unverzichtbar.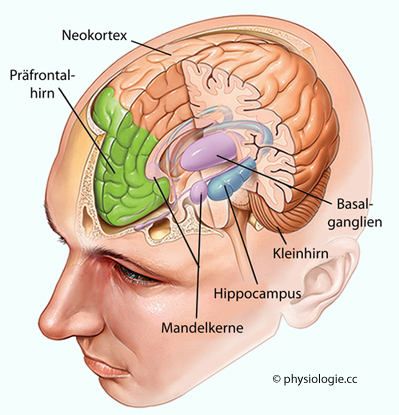
 Abbildung: Erinnerungen speichernde Gehirnregionen
Abbildung: Erinnerungen speichernde Gehirnregionen
 Ein Teil
der im Kurzzeitgedächtnis gehaltenen Information gelangt in das Arbeitsgedächtnis (working memory),
das Information für kurze Zeit speichert (z.B. Autonummer)
und für den Zeitraum einer betreffenden Tätigkeit andauert. Unter der Anleitung einer zentralen "Zuordnungsstation" (central executive) wird der Informationsstrom weitergeleitet - insbesondere zum dorsolateralen Präfrontalcortex, der für das Arbeitsgedächtnis essentiell ist.
Ein Teil
der im Kurzzeitgedächtnis gehaltenen Information gelangt in das Arbeitsgedächtnis (working memory),
das Information für kurze Zeit speichert (z.B. Autonummer)
und für den Zeitraum einer betreffenden Tätigkeit andauert. Unter der Anleitung einer zentralen "Zuordnungsstation" (central executive) wird der Informationsstrom weitergeleitet - insbesondere zum dorsolateralen Präfrontalcortex, der für das Arbeitsgedächtnis essentiell ist.
 Abbildung: Mediale Anteile des Temporallappens (linke Hirnhälfte)
Abbildung: Mediale Anteile des Temporallappens (linke Hirnhälfte) Das als gyrus parahippocampalis bezeichnete corticale Gewebe ist ein Teil des limbischen Systems und liegt hinter dem Temporalpol an der Innenseite des Temporallappens (
Das als gyrus parahippocampalis bezeichnete corticale Gewebe ist ein Teil des limbischen Systems und liegt hinter dem Temporalpol an der Innenseite des Temporallappens ( Abbildung). Er empfängt, verarbeitet und interpretiert ihm über verschiedene Pfade zuströmende (vor allem visuelle) Sinnesinformationen und fügt sie in komplexere Zusammenhänge ein.
Abbildung). Er empfängt, verarbeitet und interpretiert ihm über verschiedene Pfade zuströmende (vor allem visuelle) Sinnesinformationen und fügt sie in komplexere Zusammenhänge ein.  bezeichnet. Nunmehr ist es klar, dass das limbische System - hier insbesondere die Hippocampusformation - eine zentrale Rolle bei Entstehung und Verwaltung des Gedächtnisses spielt.
bezeichnet. Nunmehr ist es klar, dass das limbische System - hier insbesondere die Hippocampusformation - eine zentrale Rolle bei Entstehung und Verwaltung des Gedächtnisses spielt. Das sekundäre
Gedächtnis hat große Kapazität und speichert Information über längere Zeit (Minuten bis Jahre). Der Zugriff kann
länger dauern (”Einfallen“ z.B. von Prüfungsstoff durch
”Nachdenken“).
Das sekundäre
Gedächtnis hat große Kapazität und speichert Information über längere Zeit (Minuten bis Jahre). Der Zugriff kann
länger dauern (”Einfallen“ z.B. von Prüfungsstoff durch
”Nachdenken“).  Das tertiäre Gedächtnis speichert lebenslang (z.B. eigener Name) und ist durch raschen Zugriff
gekennzeichnet (kein langes Nachdenken nötig).
Das tertiäre Gedächtnis speichert lebenslang (z.B. eigener Name) und ist durch raschen Zugriff
gekennzeichnet (kein langes Nachdenken nötig).
 Abbildung: Formen und Sitz des Langzeitgedächtnisses
Abbildung: Formen und Sitz des Langzeitgedächtnisses
 Deklaratives (explizites, bewusstes) Gedächtnis (Wissensgedächtnis) ermöglicht die Wiedergabe von Fakten und Episoden ("wissen, dass"). Diese Inhalte werden vorwiegend im (mittleren) Temporalhirn
(insbesondere dem Hippocampus) gespeichert (elektrische Reizung des Temporalhirns kann vergessen
geglaubte Erinnerungen aktivieren).
Deklaratives (explizites, bewusstes) Gedächtnis (Wissensgedächtnis) ermöglicht die Wiedergabe von Fakten und Episoden ("wissen, dass"). Diese Inhalte werden vorwiegend im (mittleren) Temporalhirn
(insbesondere dem Hippocampus) gespeichert (elektrische Reizung des Temporalhirns kann vergessen
geglaubte Erinnerungen aktivieren).  semantisches (konzeptbasiertes: Fakten, Bedeutungen),
semantisches (konzeptbasiertes: Fakten, Bedeutungen),  episodisches (autobiografischen: Kontext - was, wann, wo, warum),
episodisches (autobiografischen: Kontext - was, wann, wo, warum),  räumliches (Orte) - eine Domäne des entorhinalen Cortex,
räumliches (Orte) - eine Domäne des entorhinalen Cortex, soziales Gedächtnis (Personen) - insbesondere durch CA2-Neuronen.
soziales Gedächtnis (Personen) - insbesondere durch CA2-Neuronen.  Nicht-deklaratives (implizites, nicht-bewusstes) Gedächtnis (Verhaltensgedächtnis) ermöglicht, zu "wissen, wie".
Dazu zählt auch die (unbewusst gesteuerte) korrekte Grammatik der
Sprache. Sitz des impliziten Gedächtnisses sind insbesondere das Kleinhirn (motorische Fähigkeiten) und die Mandelkerne (emotionale Reaktionen).
Das prozedurale Gedächtnis lernt und speichert Bewegungsabläufe (motorische Fertigkeiten - skill memory) vor allem im Bereich der Basalganglien (Striatum) - das Kleinhirn konzentriert sich auf die Präzision der Bewegungsdurchführung.
Nicht-deklaratives (implizites, nicht-bewusstes) Gedächtnis (Verhaltensgedächtnis) ermöglicht, zu "wissen, wie".
Dazu zählt auch die (unbewusst gesteuerte) korrekte Grammatik der
Sprache. Sitz des impliziten Gedächtnisses sind insbesondere das Kleinhirn (motorische Fähigkeiten) und die Mandelkerne (emotionale Reaktionen).
Das prozedurale Gedächtnis lernt und speichert Bewegungsabläufe (motorische Fertigkeiten - skill memory) vor allem im Bereich der Basalganglien (Striatum) - das Kleinhirn konzentriert sich auf die Präzision der Bewegungsdurchführung. ).
). Das Wiederabrufen von (Erinnern
an) im Langzeitgedächtnis gespeicherte(r) Information benötigt
gerichtete Aufmerksamkeit. Dieser Vorgang ermöglicht den Zugang zum
Gedächtnisinhalt, aber auch dessen (unbewusste) Bearbeitung.
Wiederholtes "Erinnern" kann die dentsprechenden Inhalte verstärken, aber auch verformen.
So werden die Gedächtnisinhalte bei wiederholtem Erinnerungsvorgang
zusehends verfälscht (Zeugenaussagen vor Gericht: Je länger das
Ereignis in der Vergangenheit liegt, desto stärker sind die
betreffenden Erinnerungsinhalte unbewusst verändert).
Das Wiederabrufen von (Erinnern
an) im Langzeitgedächtnis gespeicherte(r) Information benötigt
gerichtete Aufmerksamkeit. Dieser Vorgang ermöglicht den Zugang zum
Gedächtnisinhalt, aber auch dessen (unbewusste) Bearbeitung.
Wiederholtes "Erinnern" kann die dentsprechenden Inhalte verstärken, aber auch verformen.
So werden die Gedächtnisinhalte bei wiederholtem Erinnerungsvorgang
zusehends verfälscht (Zeugenaussagen vor Gericht: Je länger das
Ereignis in der Vergangenheit liegt, desto stärker sind die
betreffenden Erinnerungsinhalte unbewusst verändert). Das Arbeitsgedächtnis nutzt frontale und parietale Rindengebiete
Das Arbeitsgedächtnis nutzt frontale und parietale Rindengebiete Lernen und Erinnern erfordert die Kooperation zahlreicher Hirnregionen
Lernen und Erinnern erfordert die Kooperation zahlreicher Hirnregionen Unterschiedliche Formen des Gedächtnisses beruhen auf der Leistung
unterschiedlicher (wenn auch überlappender) Hirnregionen
Unterschiedliche Formen des Gedächtnisses beruhen auf der Leistung
unterschiedlicher (wenn auch überlappender) Hirnregionen Jede dieser Hirnregionen beteiligt sich an unterschiedlichen Gedächtnisleistungen.
Jede dieser Hirnregionen beteiligt sich an unterschiedlichen Gedächtnisleistungen. Werden
mehr Rezeptoren in die Synapse eingebaut als aus ihr entfernt, dann
wächst die Rezeptorzahl und damit das Ausmaß der Depolarisation (EPSP)
pro Quantum freigesetzten Glutamins;
Werden
mehr Rezeptoren in die Synapse eingebaut als aus ihr entfernt, dann
wächst die Rezeptorzahl und damit das Ausmaß der Depolarisation (EPSP)
pro Quantum freigesetzten Glutamins;  umgekehrt nimmt die Amplitude des EPSP ab, wenn mehr Rezeptoren endo- als exozytiert werden.
umgekehrt nimmt die Amplitude des EPSP ab, wenn mehr Rezeptoren endo- als exozytiert werden.  Langzeiteffekte können die Stärke der Synapsenwirkung anhaltend erhöhen (LTP: Verstärkung) oder reduzieren (LTD: Abschwächung). Dahinter stecken unterschiedliche
Mechanismen, Synapsen und Transduktionswege; die Bezeichnung bezieht
sich lediglich auf die Richtung des erzielten Effekts.
Langzeiteffekte können die Stärke der Synapsenwirkung anhaltend erhöhen (LTP: Verstärkung) oder reduzieren (LTD: Abschwächung). Dahinter stecken unterschiedliche
Mechanismen, Synapsen und Transduktionswege; die Bezeichnung bezieht
sich lediglich auf die Richtung des erzielten Effekts.  Unter Koinzidenzdetektion (coincidence detection)
bzw. Koinzidenzdetektor versteht man eine neuronale Schaltung, welche
aus unterschiedlichen Quellen stammende, aber zeitlich eng
zusammentreffende Signale erkennt und so codiert, dass sie als
Grundlage für Gedächtnis und Erinnerung dienen können.
Koinzidenzdetektion unterstützt die Assoziation getrennter
Gedächtnisinhalte und verringert den Einfluss von Stör- und
Unschärfeeinflüssen.
Unter Koinzidenzdetektion (coincidence detection)
bzw. Koinzidenzdetektor versteht man eine neuronale Schaltung, welche
aus unterschiedlichen Quellen stammende, aber zeitlich eng
zusammentreffende Signale erkennt und so codiert, dass sie als
Grundlage für Gedächtnis und Erinnerung dienen können.
Koinzidenzdetektion unterstützt die Assoziation getrennter
Gedächtnisinhalte und verringert den Einfluss von Stör- und
Unschärfeeinflüssen.  Abbildung):
Abbildung):
 Abbildung: NMDA-Kanäle als Koinzidenzdetektoren
Abbildung: NMDA-Kanäle als Koinzidenzdetektoren
 Der NMDA-Rezeptor ist ein molekularer Koinzidenzdetektor, seine Öffnung hängt von zwei Bedingungen ab:
Der NMDA-Rezeptor ist ein molekularer Koinzidenzdetektor, seine Öffnung hängt von zwei Bedingungen ab:  Gibt die präsynaptische Endigung den Neurotransmitter Glutamat frei und
bindet dieses an den NMDAR, dann erlangt dieser nur dann seine
"OFFEN"-Konfiguration,
Gibt die präsynaptische Endigung den Neurotransmitter Glutamat frei und
bindet dieses an den NMDAR, dann erlangt dieser nur dann seine
"OFFEN"-Konfiguration,  wenn die postsynaptische Zelle gleichzeitig
depolarisiert ist - denn dann verschwindet der Magnesiumblock und die
NMDAR lassen den Einstrom von Na+ und Ca++ zu (
wenn die postsynaptische Zelle gleichzeitig
depolarisiert ist - denn dann verschwindet der Magnesiumblock und die
NMDAR lassen den Einstrom von Na+ und Ca++ zu ( Abbildung). Depolarisierung postsynaptischer Neuronen kann z.B. an Pyramidenzellen im Hippocampus durch Schaffer'sche Kollateralen hervorgerufen werden.
Abbildung). Depolarisierung postsynaptischer Neuronen kann z.B. an Pyramidenzellen im Hippocampus durch Schaffer'sche Kollateralen hervorgerufen werden. Inositol-3-Phosphat Rezeptoren: Diese aktivieren intrazelluläre Ca++-Speicher bei synchronem Auftreten von IP3 (Zeichen der Rezeptoraktivierung) und Ca++ (postsynaptische Aktivität) oder
Inositol-3-Phosphat Rezeptoren: Diese aktivieren intrazelluläre Ca++-Speicher bei synchronem Auftreten von IP3 (Zeichen der Rezeptoraktivierung) und Ca++ (postsynaptische Aktivität) oder  Phospholipase C
an Synapsen in Hippocampus, Neocortex, Basalganglien, Kleinhirn
(Postsynaptische Depolarisierung fördert hier die Freisetzung von Endocannabinoiden, welche retrograd inhibitorische postsynaptische Ströme blockieren: Depolarization-induced suppression of inhibition). PLC moduliert diesen Mechanismus als Koinzidenzdetektor; die Endocannabinoidfreisetzung ist verstärkt, wenn Depolarisierung und Rezeptoraktivierung zusammenwirken.
Phospholipase C
an Synapsen in Hippocampus, Neocortex, Basalganglien, Kleinhirn
(Postsynaptische Depolarisierung fördert hier die Freisetzung von Endocannabinoiden, welche retrograd inhibitorische postsynaptische Ströme blockieren: Depolarization-induced suppression of inhibition). PLC moduliert diesen Mechanismus als Koinzidenzdetektor; die Endocannabinoidfreisetzung ist verstärkt, wenn Depolarisierung und Rezeptoraktivierung zusammenwirken. Abbildung unten). Vermehrte subsynaptische Einlagerung von AMPAR wirkt zugunsten synaptischer
Langzeitpotenzierung (LTP), vermehrte Endozytose (Abnahme der Zahl aktiver AMPAR) in Richtung
Langzeitdepression (LTD).
Abbildung unten). Vermehrte subsynaptische Einlagerung von AMPAR wirkt zugunsten synaptischer
Langzeitpotenzierung (LTP), vermehrte Endozytose (Abnahme der Zahl aktiver AMPAR) in Richtung
Langzeitdepression (LTD).

 Abbildung: Mechanismen synaptischer Langzeitpotenzierung
Abbildung: Mechanismen synaptischer Langzeitpotenzierung Langzeitpotenzierung (LTP, long-term potentiation -
Langzeitpotenzierung (LTP, long-term potentiation -  Abbildung) ist eine Zunahme der Synapsenstärke infolge starker Reizung des postsynaptischen Neurons (Aktionspotentiale in Abständen von <20 ms für eine Dauer von mindestens 100 ms), die für mindestens eine Stunde anhält (sie kann auch wesentlich länger wirken - Tage, Wochen, Monate oder auch lebenslang). Die
Wirkung hält nur dann lange an, wenn sie nicht nur auf der Aktivierung
von Enzymketten (rascher Abbau der Produkte), sondern auch
der Neubildung von Proteinen beruht (Genexpression, folgende
Abbildung) ist eine Zunahme der Synapsenstärke infolge starker Reizung des postsynaptischen Neurons (Aktionspotentiale in Abständen von <20 ms für eine Dauer von mindestens 100 ms), die für mindestens eine Stunde anhält (sie kann auch wesentlich länger wirken - Tage, Wochen, Monate oder auch lebenslang). Die
Wirkung hält nur dann lange an, wenn sie nicht nur auf der Aktivierung
von Enzymketten (rascher Abbau der Produkte), sondern auch
der Neubildung von Proteinen beruht (Genexpression, folgende  Abbildung).
Abbildung).  Abbildung).
Abbildung).
 Abbildung: Mechanismen langanhaltender Veränderungen postsynaptischer Signalübertragung bei Langzeitpotenzierung
Abbildung: Mechanismen langanhaltender Veränderungen postsynaptischer Signalübertragung bei Langzeitpotenzierung

 Abbildung: Synaptische Langzeitdepression im Hippocampus
Abbildung: Synaptische Langzeitdepression im Hippocampus  Zum Clathrinmechanismus s. dort
Zum Clathrinmechanismus s. dort
 Niedrige Aktionspotentialfrequenz an postsynaptischen Dendriten bewirkt hier Langzeitdepression (LTD, long-term
depression). Diese währt für einige Stunden oder länger (Tage, Wochen). AMPAR werden vermehrt endozytiert, bewirkt durch Phosphatasen wie
Calcineurin oder Proteinphosphatase 1 (PP1) (
Niedrige Aktionspotentialfrequenz an postsynaptischen Dendriten bewirkt hier Langzeitdepression (LTD, long-term
depression). Diese währt für einige Stunden oder länger (Tage, Wochen). AMPAR werden vermehrt endozytiert, bewirkt durch Phosphatasen wie
Calcineurin oder Proteinphosphatase 1 (PP1) ( Abbildung). Die
Rezeptoren werden in der Zelle gespeichert oder abgebaut.
Abbildung). Die
Rezeptoren werden in der Zelle gespeichert oder abgebaut.  Das Wechselspiel von LTP und LTD dient der
Feineinstellung ("Schärfung") von Gedächtnismustern.
Das Wechselspiel von LTP und LTD dient der
Feineinstellung ("Schärfung") von Gedächtnismustern. Nach
wiederholter gleichzeitiger Erregung
des prä- und postsynaptischen Neurons (Koinzidenz) ist die synaptische
Übertragungen verstärkt. Calciumionen aktivieren Proteinkinasen, Phospholipasen und neuronale
NO-Synthase (nNOS), was u.a. zu Verstärkung der Synapsenwirkung und auch Erhöhung der Synapsenzahl führt. Im postsynaptischen Teil werden
AMPA-Rezeptoren in die Membran eingebaut, die synaptische Kapazität
steigt (Langzeitpotenzierung: "Neurons that fire together wire together"). Langzeitpotenzierung erhöht in Pyramidenzellen die Amplitude erregender
postsynaptischer Potentiale (EPSPs) über Stunden bis Tage.
Nach
wiederholter gleichzeitiger Erregung
des prä- und postsynaptischen Neurons (Koinzidenz) ist die synaptische
Übertragungen verstärkt. Calciumionen aktivieren Proteinkinasen, Phospholipasen und neuronale
NO-Synthase (nNOS), was u.a. zu Verstärkung der Synapsenwirkung und auch Erhöhung der Synapsenzahl führt. Im postsynaptischen Teil werden
AMPA-Rezeptoren in die Membran eingebaut, die synaptische Kapazität
steigt (Langzeitpotenzierung: "Neurons that fire together wire together"). Langzeitpotenzierung erhöht in Pyramidenzellen die Amplitude erregender
postsynaptischer Potentiale (EPSPs) über Stunden bis Tage. Werden der prä- und postsynaptische Teil hingegen desynchron oder nur schwach aktiviert
(fehlende oder unzureichende Koinzidenz), werden AMPA-Rezeptoren internalisiert
(endozytiert), die Synapseneffizienz nimmt ab, und es kann zur
Zurückbildung der Synapse kommen (Langzeitdepression: "Neurons that fire out of sync lose their link").
Werden der prä- und postsynaptische Teil hingegen desynchron oder nur schwach aktiviert
(fehlende oder unzureichende Koinzidenz), werden AMPA-Rezeptoren internalisiert
(endozytiert), die Synapseneffizienz nimmt ab, und es kann zur
Zurückbildung der Synapse kommen (Langzeitdepression: "Neurons that fire out of sync lose their link"). präsynaptisch - Variation der Menge des pro Aktionspotential ausgeschütteten und / oder wiederaufgenommenen Transmitters, und / oder
präsynaptisch - Variation der Menge des pro Aktionspotential ausgeschütteten und / oder wiederaufgenommenen Transmitters, und / oder postsynaptisch - bezüglich Transmittereffekt (Zahl und/oder Empfindlichkeit der Rezeptoren) und Transmitterabbau.
postsynaptisch - bezüglich Transmittereffekt (Zahl und/oder Empfindlichkeit der Rezeptoren) und Transmitterabbau. Gliazellen sind an synaptischer Plastizität (Zu- oder Abnahme der Synapsendichte) beteiligt. So können Astrozyten und Mikrogliazellen
die Stellen markieren, an denen synaptische Veränderungen
(Synaptogenese oder Synapsenelimination mit nachfolgender Phagozytose)
erfolgen sollen (
Gliazellen sind an synaptischer Plastizität (Zu- oder Abnahme der Synapsendichte) beteiligt. So können Astrozyten und Mikrogliazellen
die Stellen markieren, an denen synaptische Veränderungen
(Synaptogenese oder Synapsenelimination mit nachfolgender Phagozytose)
erfolgen sollen ( Abbildung).
Abbildung). 
 Abbildung: Einfluss von Gliazellen auf Synaptogenese und -elimination
Abbildung: Einfluss von Gliazellen auf Synaptogenese und -elimination
 werden vom angeregten postsynaptischen Apparat freigesetzt
und diffundieren zum präsynaptischen Teil, binden hier an entsprechende
Rezeptoren und modulieren die Transmitterfreisetzung - z.B. durch
Einfluss auf den Calciumeinstrom. Nimmt dieser zu, werden Vesikel
mobilisiert, die Transmitterfreisetzung vermehrt und die synaptische
Effizienz gesteigert.
werden vom angeregten postsynaptischen Apparat freigesetzt
und diffundieren zum präsynaptischen Teil, binden hier an entsprechende
Rezeptoren und modulieren die Transmitterfreisetzung - z.B. durch
Einfluss auf den Calciumeinstrom. Nimmt dieser zu, werden Vesikel
mobilisiert, die Transmitterfreisetzung vermehrt und die synaptische
Effizienz gesteigert.
 Abbildung): Hochfrequente Stimulierung der Synapse aktiviert über
starken Calciumeinstrom (intrazellulärer Ca++-Spiegel über 5 µM) Kinasen und
AMPA-Rezeptoren, was zu Verstärkung der Synapsenwirkung führt (LTP
erklärt sich auch über vermehrte AMPAR-Zahl).
Abbildung): Hochfrequente Stimulierung der Synapse aktiviert über
starken Calciumeinstrom (intrazellulärer Ca++-Spiegel über 5 µM) Kinasen und
AMPA-Rezeptoren, was zu Verstärkung der Synapsenwirkung führt (LTP
erklärt sich auch über vermehrte AMPAR-Zahl). 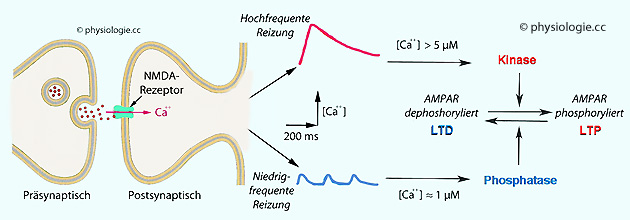
 Abbildung: Wie Ca++ sowohl LTP als auch LTD triggern kann
Abbildung: Wie Ca++ sowohl LTP als auch LTD triggern kann
 Das bedeutet, dass nahe an aktivierten Synapsen gelegene andere
Synapsen an LTP- und LTD-Prozessen mitbeteiligt sind (diese Synapsen
"lernen mit"), während weiter entfernt liegende von solchen lokalen
Vorgängen unbeeinflusst bleiben (Selektivität).
Das bedeutet, dass nahe an aktivierten Synapsen gelegene andere
Synapsen an LTP- und LTD-Prozessen mitbeteiligt sind (diese Synapsen
"lernen mit"), während weiter entfernt liegende von solchen lokalen
Vorgängen unbeeinflusst bleiben (Selektivität).  Abbildung) spielt eine Rolle:
Abbildung) spielt eine Rolle:
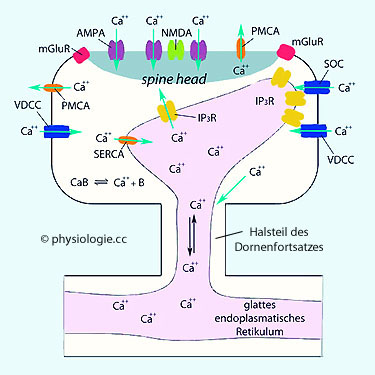
 Abbildung: Calciumverteilung in einem dendritischen Dornenfortsatz
Abbildung: Calciumverteilung in einem dendritischen Dornenfortsatz IP3R, IP3-Rezeptor
IP3R, IP3-Rezeptor  mGluR, metabotroper Glutamatrezeptor
mGluR, metabotroper Glutamatrezeptor  PMCA, Plasmamembran Ca++-ATPase
PMCA, Plasmamembran Ca++-ATPase  SERCA regelt das Wiederauffüllen des Calciumspeichers im endoplasmatischen Retikulum)
SERCA regelt das Wiederauffüllen des Calciumspeichers im endoplasmatischen Retikulum)  SOC, store-operated calcium channel (für die Aufnahme von Calciumionen)
SOC, store-operated calcium channel (für die Aufnahme von Calciumionen)  VDCC, voltage-dependent calcium channel. Calciumionen
triggern eine Kaskade intrazellulärer Folgevorgänge, inklusive die
Aktivierung von Kinasen, was schließlich zur Verstärkung der
synaptischen Übertragung führt
VDCC, voltage-dependent calcium channel. Calciumionen
triggern eine Kaskade intrazellulärer Folgevorgänge, inklusive die
Aktivierung von Kinasen, was schließlich zur Verstärkung der
synaptischen Übertragung führt
 : Eine wichtige Rolle für die Langzeitpotenzierung spielt das große (388 kD) Glykoprotein Reelin,
das der Gedächtnisverfestigung und der ontogenetischen
Organisation der Neuronenzellschichten im Hippocampus dient.
Es
beeinflusst Migration und Interaktion von Nervenzellen und regt die
Ausbildung von dendritischen Fortsätzen an. Ein Mangel an Reelin
scheint für die Entwicklung verschiedener neuropathologischer
Zustandsbilder eine Rolle zu spielen.
: Eine wichtige Rolle für die Langzeitpotenzierung spielt das große (388 kD) Glykoprotein Reelin,
das der Gedächtnisverfestigung und der ontogenetischen
Organisation der Neuronenzellschichten im Hippocampus dient.
Es
beeinflusst Migration und Interaktion von Nervenzellen und regt die
Ausbildung von dendritischen Fortsätzen an. Ein Mangel an Reelin
scheint für die Entwicklung verschiedener neuropathologischer
Zustandsbilder eine Rolle zu spielen. vgl. dort
vgl. dort (folgende Abbildungen) im medialen Temporallappen umfasst den gyrus dentatus, den Hippocampus ("Ammonshorn", cornu ammonis) und das Subiculum.
(folgende Abbildungen) im medialen Temporallappen umfasst den gyrus dentatus, den Hippocampus ("Ammonshorn", cornu ammonis) und das Subiculum.  Der gyrus dentatus
Der gyrus dentatus  gilt als die Eingangspforte für das Hippocampussystem, Afferenzen stammen aus dem entorhinalen Cortex via Perforansfasern. Er enthält Körnerzellen (granular cells), die glutamaterg und auch GABAerg auf Pyramidenzellen des Ammonshorns projizieren. Der gyrus dentatus übernimmt eine Vorverarbeitung eintreffender Informationen, die je nach ihrer Bedeutung und Neuigkeit bewertet und separiert (spezialisiert) verarbeitet werden (pattern separation). Der gyrus dentatus hilft bei Mustererkennung, getrennter Verarbeitung, Orientierung im Raum, Aufrufen von Gedächtnisinhalten.
gilt als die Eingangspforte für das Hippocampussystem, Afferenzen stammen aus dem entorhinalen Cortex via Perforansfasern. Er enthält Körnerzellen (granular cells), die glutamaterg und auch GABAerg auf Pyramidenzellen des Ammonshorns projizieren. Der gyrus dentatus übernimmt eine Vorverarbeitung eintreffender Informationen, die je nach ihrer Bedeutung und Neuigkeit bewertet und separiert (spezialisiert) verarbeitet werden (pattern separation). Der gyrus dentatus hilft bei Mustererkennung, getrennter Verarbeitung, Orientierung im Raum, Aufrufen von Gedächtnisinhalten. Der Hippocampus
- ein 5 cm langer Streifen allocorticaler grauer Substanz im gyrus parahippocampalis,
dessen Form im Querschnitt an das gekrümmte Horn eines Schafbocks
erinnert und deswegen auch als Ammonshorn (CA:
cornu ammonis) bezeichnet wird - ist zentral an der Überführung von
Inhalten des Kurzzeit- zu solchen des Langzeitgedächtnisses beteiligt.
Weiters baut er räumliches Gedächtnis auf, was für die Bewegung des
Körpers im Raum (Navigation) wesentlich ist. Seine mit dem Code CA
bezeichneten Neurone (
Der Hippocampus
- ein 5 cm langer Streifen allocorticaler grauer Substanz im gyrus parahippocampalis,
dessen Form im Querschnitt an das gekrümmte Horn eines Schafbocks
erinnert und deswegen auch als Ammonshorn (CA:
cornu ammonis) bezeichnet wird - ist zentral an der Überführung von
Inhalten des Kurzzeit- zu solchen des Langzeitgedächtnisses beteiligt.
Weiters baut er räumliches Gedächtnis auf, was für die Bewegung des
Körpers im Raum (Navigation) wesentlich ist. Seine mit dem Code CA
bezeichneten Neurone ( Abbildung unten) kooperieren in Kreisschaltungen in einer Weise, welche synaptische Langzeitverstärkung (LTP, long term potentiation) und Gedächtniskonsolidierung unterstützt.
Abbildung unten) kooperieren in Kreisschaltungen in einer Weise, welche synaptische Langzeitverstärkung (LTP, long term potentiation) und Gedächtniskonsolidierung unterstützt. Das Subiculum
ist der unterste Anteil der Hippocampusformation. Es ist vermutlich am
Arbeitsgedächtnis, vielleicht auch an der hypothalamisch-hypophysären
Regulation beteiligt.
Das Subiculum
ist der unterste Anteil der Hippocampusformation. Es ist vermutlich am
Arbeitsgedächtnis, vielleicht auch an der hypothalamisch-hypophysären
Regulation beteiligt.
 Abbildung: Hippocampusformation
Abbildung: Hippocampusformation
 Der im medialen Temporallappen gelegene entorhinale Cortex ist
ein Teil des (dreischichtigen, entwicklungsgeschichtlich älteren)
Allocortex und ist mit Gedächtnisaufbau, örtlicher und zeitlicher
Orientierung beschäftigt. Funktionell ist er zwischen Hippocampus und
Neocortex geschaltet. Seine Neuriten bilden Synapsen mit Zellen des
gyrus dentatus (
Der im medialen Temporallappen gelegene entorhinale Cortex ist
ein Teil des (dreischichtigen, entwicklungsgeschichtlich älteren)
Allocortex und ist mit Gedächtnisaufbau, örtlicher und zeitlicher
Orientierung beschäftigt. Funktionell ist er zwischen Hippocampus und
Neocortex geschaltet. Seine Neuriten bilden Synapsen mit Zellen des
gyrus dentatus ( Abbildung unten) und bauen Langzeitpotenzierung auf.
Abbildung unten) und bauen Langzeitpotenzierung auf. Abbildung) und CA1-Neuronen des Ammonshorns
Abbildung) und CA1-Neuronen des Ammonshorns (eines Teils des Hippocampus, in der medialen Wand des Temporallappens) erreichen:
(eines Teils des Hippocampus, in der medialen Wand des Temporallappens) erreichen:  aus lamina II direkt sowie und über Zwischenschaltung im gyrus dentatus und
aus lamina II direkt sowie und über Zwischenschaltung im gyrus dentatus und aus lamina III direkt.
aus lamina III direkt. zu
CA1-Zellen → Fasern zu Subiculum → Fasern zurück zum entorhinalen Cortex.
CA3-Zellen haben auto-assoziative Verstärkungskollateralen.
zu
CA1-Zellen → Fasern zu Subiculum → Fasern zurück zum entorhinalen Cortex.
CA3-Zellen haben auto-assoziative Verstärkungskollateralen. Abbildung: Hippocampusformation und "trisynaptischer Schaltkreis"
Abbildung: Hippocampusformation und "trisynaptischer Schaltkreis" CA1-Neurone (grün dargestellt) entsenden Neurone in das Subiculum (zwischen entorhinalem Cortex und CA1 gelegen). CA1-Neurone zeigen Langzeitpotenzierung
- Dendriten aktivierter Pyramidenzellen lagern AMPA-Rezeptoren in ihre Membran ein und verstärken hier die
Synapsenwirkung zusammen mit (dort schon vorhandenen)
NMDA-Rezeptoren. Diese Dendriten bilden eine dicke Schichte (stratum radiatum) der CA1-Region, hier wirken Synapsen von
Schaffer'schen Kollateralen (Axone aus der CA3-Region).
CA1-Neurone (grün dargestellt) entsenden Neurone in das Subiculum (zwischen entorhinalem Cortex und CA1 gelegen). CA1-Neurone zeigen Langzeitpotenzierung
- Dendriten aktivierter Pyramidenzellen lagern AMPA-Rezeptoren in ihre Membran ein und verstärken hier die
Synapsenwirkung zusammen mit (dort schon vorhandenen)
NMDA-Rezeptoren. Diese Dendriten bilden eine dicke Schichte (stratum radiatum) der CA1-Region, hier wirken Synapsen von
Schaffer'schen Kollateralen (Axone aus der CA3-Region).  CA2-Neurone liegen zwischen CA1 und CA3. Auch sie erhalten Afferenzen über Perforans-Fasern.
CA2-Neurone liegen zwischen CA1 und CA3. Auch sie erhalten Afferenzen über Perforans-Fasern. CA3-Neurone erhalten Afferenzen über Moosfasern der Körnerzellen im
gyrus dentatus und über Perforansfasern aus dem entorhinalen Cortex.
Ihre Axone projizieren auf CA1 und CA2 über Schaffer'sche
Kollateralen, sowie auf CA3 zurück.
CA3-Neurone erhalten Afferenzen über Moosfasern der Körnerzellen im
gyrus dentatus und über Perforansfasern aus dem entorhinalen Cortex.
Ihre Axone projizieren auf CA1 und CA2 über Schaffer'sche
Kollateralen, sowie auf CA3 zurück. CA4 gilt als polymorphe Schichte des gyrus dentatus.
CA4 gilt als polymorphe Schichte des gyrus dentatus.

 Abbildung unten). CA3-Neuronen
(Pyramidenzellen) bilden auch untereinander starke exzitatorische
Konnexe. Auch das dient offenbar der Verstärkung von Gedächtnisspuren,
kann aber bei Übererregung zur Auslösung von Krämpfen führen.
Abbildung unten). CA3-Neuronen
(Pyramidenzellen) bilden auch untereinander starke exzitatorische
Konnexe. Auch das dient offenbar der Verstärkung von Gedächtnisspuren,
kann aber bei Übererregung zur Auslösung von Krämpfen führen.  Der Hippocampus ist unverzichtbar für die Bildung und Rekapitulation
räumlicher, kontextueller und episodischer Gedächtnisinhalte. Er repräsentiert vom entorhinalen Cortex des gyrus parahippocampalis zugeleitete (Abbildungen) räumlich
organisierte sensorische Information in kontextspezifischer Weise.
Der Hippocampus ist unverzichtbar für die Bildung und Rekapitulation
räumlicher, kontextueller und episodischer Gedächtnisinhalte. Er repräsentiert vom entorhinalen Cortex des gyrus parahippocampalis zugeleitete (Abbildungen) räumlich
organisierte sensorische Information in kontextspezifischer Weise.  Zur Bedeutung des Hippocampus für Gedächtnis und Raumorientierung s. dort
Zur Bedeutung des Hippocampus für Gedächtnis und Raumorientierung s. dort
 Abbildung: Schaltungen in Subiculum und hippocampalem System
Abbildung: Schaltungen in Subiculum und hippocampalem System
 Der Moosfaserpfad (Axone von Körnerzellen im gyrus dentatus) vermittelt bei hochfrequenter Reizung starken Ca++-Einstrom in präsynaptische Endigungen, Aktivierung der Proteinkinase A, erhöhte Glutamatfreisetzung
und EPSP-Verstärkung an Synapsen zu CA3-Zellen.
Der Moosfaserpfad (Axone von Körnerzellen im gyrus dentatus) vermittelt bei hochfrequenter Reizung starken Ca++-Einstrom in präsynaptische Endigungen, Aktivierung der Proteinkinase A, erhöhte Glutamatfreisetzung
und EPSP-Verstärkung an Synapsen zu CA3-Zellen.  Beim Mechanismus über Schaffer'sche Kollaterale
handelt es sich hingegen um assoziative Verstärkung, d.h. prä- und
postsynaptische Erregung müssen zeitlich zusammenwirken
("Koinzidenzdetektor": NMDA-Öffnung bei gleichzeitiger Aktivierung von
AMPA-Kanälen -
Beim Mechanismus über Schaffer'sche Kollaterale
handelt es sich hingegen um assoziative Verstärkung, d.h. prä- und
postsynaptische Erregung müssen zeitlich zusammenwirken
("Koinzidenzdetektor": NMDA-Öffnung bei gleichzeitiger Aktivierung von
AMPA-Kanälen -  Abbildung).
Abbildung).  Limbischer, wie die Mandelkerne (Gedächtnis und Emotionen);
Limbischer, wie die Mandelkerne (Gedächtnis und Emotionen);  neokortikaler,
wie das ventrale visuelle System (Verarbeitung und Zugriff), die
vordere Temporalregion (Speicherung semantischer Information) oder das
Präfrontalhirn (Beurteilung, Fokussierung, Handlungsstrategie);
neokortikaler,
wie das ventrale visuelle System (Verarbeitung und Zugriff), die
vordere Temporalregion (Speicherung semantischer Information) oder das
Präfrontalhirn (Beurteilung, Fokussierung, Handlungsstrategie);  subkortikaler, wie die Basalganglien (motorische Geschicklichkeit).
subkortikaler, wie die Basalganglien (motorische Geschicklichkeit).
 Abbildung: An der Gedächtnisbildung beteiligte Regionen im mittleren Temporalhirn
Abbildung: An der Gedächtnisbildung beteiligte Regionen im mittleren Temporalhirn
 Abbildung) und im Präfrontalcortex. An den Hippocampus grenzen
Abbildung) und im Präfrontalcortex. An den Hippocampus grenzen  der retrosplenische Cortex
(entspricht Brodmann 29 und 30), ein assoziatives Rindengebiet, das
hinter dem Splenium des corpus callosum liegt und sich an episodischem
Gedächtnis, Raumanalyse und Körpernavigation ("ich" vs. "Umwelt")
beteiligt;
der retrosplenische Cortex
(entspricht Brodmann 29 und 30), ein assoziatives Rindengebiet, das
hinter dem Splenium des corpus callosum liegt und sich an episodischem
Gedächtnis, Raumanalyse und Körpernavigation ("ich" vs. "Umwelt")
beteiligt; der parahippocampale Cortex, zusammen mit dem retrosplenischen dient er offenbar vor allem der Projektion räumlicher Hinweise zur Gedächtnisbildung. Seine parahippocampal place area
(PPA) speichert und erkennt Umweltmuster (Räume, Landschaften), andere
Teile - vor allem im rechten gyrus parahippocampalis - erkennen soziale
Kontexte (z.B. Ironie, Sarkasmus);
der parahippocampale Cortex, zusammen mit dem retrosplenischen dient er offenbar vor allem der Projektion räumlicher Hinweise zur Gedächtnisbildung. Seine parahippocampal place area
(PPA) speichert und erkennt Umweltmuster (Räume, Landschaften), andere
Teile - vor allem im rechten gyrus parahippocampalis - erkennen soziale
Kontexte (z.B. Ironie, Sarkasmus); der perirhinale Cortex (Brodmann 35 / 36) verarbeitet Information über Objekte und ihre Identität;
der perirhinale Cortex (Brodmann 35 / 36) verarbeitet Information über Objekte und ihre Identität;  der entorhinale Cortex
(Brodmann 28 / 34) erhält und verwaltet Informationen, die über
getrennte Modalitäten hinausgehen können und sowohl räumliche als auch
zeitliche Komponenten haben.
der entorhinale Cortex
(Brodmann 28 / 34) erhält und verwaltet Informationen, die über
getrennte Modalitäten hinausgehen können und sowohl räumliche als auch
zeitliche Komponenten haben. 
 Abbildung: Netzwerke für Lernen und Gedächtnis
Abbildung: Netzwerke für Lernen und Gedächtnis
 Abbildung) sind in motorische Lern-, Merk- und Gedächtnisabläufe involviert. Zu entsprechenden Fähigkeiten des Kleinhirns s. dort.
Abbildung) sind in motorische Lern-, Merk- und Gedächtnisabläufe involviert. Zu entsprechenden Fähigkeiten des Kleinhirns s. dort.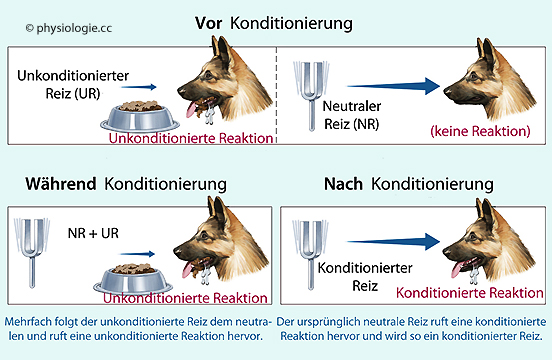
 Abbildung: Klassische Konditionierung
Abbildung: Klassische Konditionierung
 Klassische Konditionierung (
Klassische Konditionierung ( Abbildung): Hier geht es darum, eine neuronale Verknüpfung zwischen einem neutralen Sinnesreiz und einem knapp darauf folgenden unkonditionierten Reiz (unconditioned stimulus) herzustellen. Als unkonditioniert bezeichnet man einen Reiz, der zu einer physiologisch "vorprogrammierten" Antwort führt (z.B. Perzipierung von Futter → Salivation).
Abbildung): Hier geht es darum, eine neuronale Verknüpfung zwischen einem neutralen Sinnesreiz und einem knapp darauf folgenden unkonditionierten Reiz (unconditioned stimulus) herzustellen. Als unkonditioniert bezeichnet man einen Reiz, der zu einer physiologisch "vorprogrammierten" Antwort führt (z.B. Perzipierung von Futter → Salivation). Abbildung). Man sagt, der neutrale Reiz ist zu einem "konditionierten" geworden und löst eine konditionierte Reaktion (conditioned response) aus.
Abbildung). Man sagt, der neutrale Reiz ist zu einem "konditionierten" geworden und löst eine konditionierte Reaktion (conditioned response) aus. Operante Konditionierung: Von verschiedenen Verhaltensweisen (z.B. nach Futter suchen, zu einem Lichtsignal laufen,..) führt nur eine (z.B. Drücken eines Schalters) zum Erfolg (z.B. Fütterung). Das
lernt das Versuchstier nach dem Prinzip von Versuch und Irrtum. Das
Versuchsdesign kann auch bestimmte Verhaltensweisen bestrafen (z.B.
Stromschlag). Belohnung führt zu positiver, Bestrafung zu negativer Konditionierung.
Operante Konditionierung: Von verschiedenen Verhaltensweisen (z.B. nach Futter suchen, zu einem Lichtsignal laufen,..) führt nur eine (z.B. Drücken eines Schalters) zum Erfolg (z.B. Fütterung). Das
lernt das Versuchstier nach dem Prinzip von Versuch und Irrtum. Das
Versuchsdesign kann auch bestimmte Verhaltensweisen bestrafen (z.B.
Stromschlag). Belohnung führt zu positiver, Bestrafung zu negativer Konditionierung.  (infolge Hirnschädigung, Thiaminmangel, Alkoholabusus u.a.) oder schockartige Ereignisse (Unfall,
Blutung) verklingen neue Gedächtnisinhalte spurlos. Der Patient ist ab
dem auslösenden Ereignis unfähig, sich Neues zu merken; soeben Erlebtes wird gleich wieder vergessen.
(infolge Hirnschädigung, Thiaminmangel, Alkoholabusus u.a.) oder schockartige Ereignisse (Unfall,
Blutung) verklingen neue Gedächtnisinhalte spurlos. Der Patient ist ab
dem auslösenden Ereignis unfähig, sich Neues zu merken; soeben Erlebtes wird gleich wieder vergessen.
 Das Kurzzeitgedächtnis speichert via limbisches System Sinnesmeldungen
in der Gehirnrinde. Zunächst entstehen sensorische Zwischenspeicher in
Form berarbeiteter Informationspakete (z.B. visuelle "Wo"-Inhalte im
Parietalhirn, "Was"-Inhalte im Temporalhirn)
Das Kurzzeitgedächtnis speichert via limbisches System Sinnesmeldungen
in der Gehirnrinde. Zunächst entstehen sensorische Zwischenspeicher in
Form berarbeiteter Informationspakete (z.B. visuelle "Wo"-Inhalte im
Parietalhirn, "Was"-Inhalte im Temporalhirn) Als Komponente des
Kurzzeitgedächtnisses speichert das Arbeitsgedächtnis für Sekunden sensorische Information in
einem Informationspuffer. Dabei steigt die Aktivität des Parahippocampus
und des Präfrontalhirns
Als Komponente des
Kurzzeitgedächtnisses speichert das Arbeitsgedächtnis für Sekunden sensorische Information in
einem Informationspuffer. Dabei steigt die Aktivität des Parahippocampus
und des Präfrontalhirns Das Langzeitgedächtnis sitzt vor allem in Regionen, in welche der
betreffende Sinneseindruck projiziert wurde. Das sekundäre Gedächtnis
verfügt über große Kapazität und speichert über Jahre, der Zugriff
erfolgt über ”Nachdenken“. Inhalte im tertiären Gedächtnis sind sofort
verfügbar und gehen normalerweise nicht verloren
Das Langzeitgedächtnis sitzt vor allem in Regionen, in welche der
betreffende Sinneseindruck projiziert wurde. Das sekundäre Gedächtnis
verfügt über große Kapazität und speichert über Jahre, der Zugriff
erfolgt über ”Nachdenken“. Inhalte im tertiären Gedächtnis sind sofort
verfügbar und gehen normalerweise nicht verloren Deklaratives (explizites, bewusstes) Gedächtnis (Wissensgedächtnis)
speichert Fakten und Episoden, es wird im Temporallappen gespeichert.
Nicht-deklaratives (implizites, nicht-bewusstes) Gedächtnis
(Bewegungsabläufe - prozedurales Gedächtnis, Sprachgrammatik) wird in
Kleinhirn und Basalganglien gespeichert
Deklaratives (explizites, bewusstes) Gedächtnis (Wissensgedächtnis)
speichert Fakten und Episoden, es wird im Temporallappen gespeichert.
Nicht-deklaratives (implizites, nicht-bewusstes) Gedächtnis
(Bewegungsabläufe - prozedurales Gedächtnis, Sprachgrammatik) wird in
Kleinhirn und Basalganglien gespeichert Der Hippocampus ermöglicht das Entstehen von Erinnerungen. Dazu ist er
reziprok mit dem parahippocampalen Cortex verbunden - dieser bezieht
aktuelle Informationen aus kortikalen Assoziationsarealen - und ist in
die limbische Kreisschaltung ("Papez-Kreise") eingebaut, die zum Merken
und Erinnern notwendige Mechanismen aufbaut. Der Hippocampus erneuert
laufend seinen Neuronenpool, junge Neurone sind sehr erregbar und
bilden fortlaufend synaptische Kontakte aus, insbesondere
zur parahippocampalen Region. Junge Zellgruppen erfüllen dynamische
Gedächtnisfunktionen, z.B. zur Erkennung von Orten in der Umgebung
(Ortszellen,
Ortsfelder)
Der Hippocampus ermöglicht das Entstehen von Erinnerungen. Dazu ist er
reziprok mit dem parahippocampalen Cortex verbunden - dieser bezieht
aktuelle Informationen aus kortikalen Assoziationsarealen - und ist in
die limbische Kreisschaltung ("Papez-Kreise") eingebaut, die zum Merken
und Erinnern notwendige Mechanismen aufbaut. Der Hippocampus erneuert
laufend seinen Neuronenpool, junge Neurone sind sehr erregbar und
bilden fortlaufend synaptische Kontakte aus, insbesondere
zur parahippocampalen Region. Junge Zellgruppen erfüllen dynamische
Gedächtnisfunktionen, z.B. zur Erkennung von Orten in der Umgebung
(Ortszellen,
Ortsfelder) Das Speichern neuer Gedächtnisinhalte erfordert Neuroplastizität:
Präsynaptisch kann sich die freigesetzte / wiederaufgenommene
Transmittermenge (pro Aktionspotential), postsynaptisch der
Transmittereffekt (Zahl / Empfindlichkeit der Rezeptoren) bzw. -abbau
verändern; mit der Rezeptorzahl steigt der Effekt
(z.B. EPSP) pro Quantum freigesetzten Transmitters. Synapsen können
wachsen oder schrumpfen, verschwinden oder neu gebildet, ihr
Verbindungsmuster kann geändert werden
Das Speichern neuer Gedächtnisinhalte erfordert Neuroplastizität:
Präsynaptisch kann sich die freigesetzte / wiederaufgenommene
Transmittermenge (pro Aktionspotential), postsynaptisch der
Transmittereffekt (Zahl / Empfindlichkeit der Rezeptoren) bzw. -abbau
verändern; mit der Rezeptorzahl steigt der Effekt
(z.B. EPSP) pro Quantum freigesetzten Transmitters. Synapsen können
wachsen oder schrumpfen, verschwinden oder neu gebildet, ihr
Verbindungsmuster kann geändert werden Gliazellen beteiligen sich an Lernvorgängen: Astrozyten können Stellen
synaptischer Veränderung markieren, Oligodendrozyten die Myelinisierung verändern
Gliazellen beteiligen sich an Lernvorgängen: Astrozyten können Stellen
synaptischer Veränderung markieren, Oligodendrozyten die Myelinisierung verändern Langzeitpotenzierung ist eine Zunahme der Synapsenstärke für mindestens
eine Stunde. Präsynaptische Aktionspotentialsalven führen zu
Glutamatfreisetzung und postsynaptischen EPSPs durch Kationeneinstrom.
An nicht aktivierten glutamatergen Synapsen sind die NMDA-Rezeptoren
durch Magnesiumionen blockiert. Vordepolarisation öffnet sie und Ca++
strömt ein, worauf Proteinkinase AMPA-Rezeptoren phosphoryliert, die in
die postsynaptische Membran eingeklagert werden ("AMPAfizierung"), Na+-Einstrom und Depolarisation verstärken (Langzeitpotenzierung LTP)
Langzeitpotenzierung ist eine Zunahme der Synapsenstärke für mindestens
eine Stunde. Präsynaptische Aktionspotentialsalven führen zu
Glutamatfreisetzung und postsynaptischen EPSPs durch Kationeneinstrom.
An nicht aktivierten glutamatergen Synapsen sind die NMDA-Rezeptoren
durch Magnesiumionen blockiert. Vordepolarisation öffnet sie und Ca++
strömt ein, worauf Proteinkinase AMPA-Rezeptoren phosphoryliert, die in
die postsynaptische Membran eingeklagert werden ("AMPAfizierung"), Na+-Einstrom und Depolarisation verstärken (Langzeitpotenzierung LTP) Wiederholte gleichzeitiger Erregung des prä- und postsynaptischen
Neurons (Koinzidenz: "Neurons that fire together wire together")
verstärkt entsprechende synaptische Verschaltungen für Tage bis Wochen.
Proteinkinasen, Phospholipasen und neuronale NO-Synthase erhöhen
Synapsenwirkung und -zahl, die synaptische Kapazität steigt
Wiederholte gleichzeitiger Erregung des prä- und postsynaptischen
Neurons (Koinzidenz: "Neurons that fire together wire together")
verstärkt entsprechende synaptische Verschaltungen für Tage bis Wochen.
Proteinkinasen, Phospholipasen und neuronale NO-Synthase erhöhen
Synapsenwirkung und -zahl, die synaptische Kapazität steigt Klassische Konditionierung
beruht auf der Verknüpfung eines (neutralen) Reizes (z.B. Glockenton)
mit einem knapp darauf folgenden unkonditionierten Reiz, der zu einer
Reflexantwort führt (z.B. Futter). Der neutrale Reiz reicht dann aus,
eine Antwort auszulösen: Er ist zu einem "konditionierten" geworden und
löst eine konditionierte Reaktion aus
Klassische Konditionierung
beruht auf der Verknüpfung eines (neutralen) Reizes (z.B. Glockenton)
mit einem knapp darauf folgenden unkonditionierten Reiz, der zu einer
Reflexantwort führt (z.B. Futter). Der neutrale Reiz reicht dann aus,
eine Antwort auszulösen: Er ist zu einem "konditionierten" geworden und
löst eine konditionierte Reaktion aus Operante Konditionierung
ergibt sich, wenn von verschiedenen Verhaltensweisen nur eine zum
Erfolg führt (Versuch und Irrtum). Belohnung führt zu positiver,
Bestrafung zu negativer Konditionierung
Operante Konditionierung
ergibt sich, wenn von verschiedenen Verhaltensweisen nur eine zum
Erfolg führt (Versuch und Irrtum). Belohnung führt zu positiver,
Bestrafung zu negativer Konditionierung