

Eine Reise durch die Physiologie - Wie der Körper des Menschen funktioniert


 Nichtparenchymzellen
Nichtparenchymzellen
 Asialoglykoprotein: Glykoprotein, von dem Sialinsäure entfernt wurde (kommt im Speichel vor; σίαλον = Speichel)
Asialoglykoprotein: Glykoprotein, von dem Sialinsäure entfernt wurde (kommt im Speichel vor; σίαλον = Speichel)| Die Leber verfügt - außer Hepatozyten - über ein System nicht-parenchymatöser Zellen,
die über parakrine Signalstoffe (z.B.
Wachstumsfaktoren) und Zellkontakte (untereinander und mit
Hepatozyten) Funktionen wie Wachstum, Regeneration, Stoffwechsel und
Immunaktivität der Leber kontrollieren. Zu diesem System gehören sinusoidale Endothelzellen, Kupffer-sche Sternzellen und Itozellen (Stellatumzellen). Endothelzellen können Makromoleküle binden und aus dem Blut entfernen; sie präsentieren über MHC-I- und MHC-II-Moleküle zelluläre Antigene an T-Zellen. Kupffer-Zellen phagozytieren sehr effizient Bakterien und beteiligen sich an der Antigenpräsentation; sie nehmen auch Toxine, Immunkomplexe, Zelltrümmer und Viren auf und sezernieren dabei Zytokine, welche die Bildung von Akutphasen-Proteinen (CRP, Fibrinogen, Coeruloplasmin, Haptoglobin, Ferritin..) auslösen. Stellatumzellen (Ito-Zellen) liegen perisinusoidal, sind kontraktil und beeinflussen die Perfusion. Sie speichern Fett und Vitamin A, und beteiligen sich an Immunreaktionen (Antigenpräsentation, Stimulierung von natürlichen Killerzellen). Sie sind durch Zytokine aktivierbar und beteiligen sich im Falle von Vergiftungen oder Verletzungen an Heilungs- und Fibrosierungsprozessen. |
 Endothel
Endothel  Kupfferzellen
Kupfferzellen  Ito- (Stellatum-) zellen
Ito- (Stellatum-) zellen  C-reaktives Protein
C-reaktives Protein Akutphasenproteine
Akutphasenproteine
 Core messages
Core messages bezeichneten Hepatozyten (die organspezifische metabolische Aufgaben
erfüllen) finden sich im Lebergewebe auch andere Zellen (Endothel,
Kupffer'sche Sternzellen u.a.), die als "Nichtparenchym"
zusammengefasst werden.
bezeichneten Hepatozyten (die organspezifische metabolische Aufgaben
erfüllen) finden sich im Lebergewebe auch andere Zellen (Endothel,
Kupffer'sche Sternzellen u.a.), die als "Nichtparenchym"
zusammengefasst werden.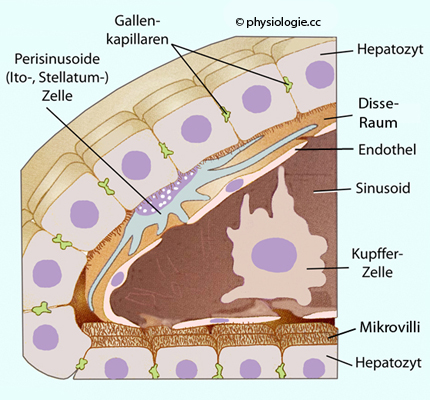
 Abbildung: Lebersinusoid
Abbildung: Lebersinusoid (nicht gezeigt) im Disse'schen Raum liegen den Sternzellen oder Endothelzellen direkt
an; sie verfügen über Granula, die Proteasen und Perforin enthalten und
tragen zur Virusbekämpfung, Tumorzellbeseitigung und Aktivierung
von Kupffer-Zellen bei.
(nicht gezeigt) im Disse'schen Raum liegen den Sternzellen oder Endothelzellen direkt
an; sie verfügen über Granula, die Proteasen und Perforin enthalten und
tragen zur Virusbekämpfung, Tumorzellbeseitigung und Aktivierung
von Kupffer-Zellen bei.
 können mit Ito-Zellen sowie mit
Mikrovilli der Hepatozyten direkten Kontakt aufnehmen, was dem
immunologischen Informationsaustausch dient.
können mit Ito-Zellen sowie mit
Mikrovilli der Hepatozyten direkten Kontakt aufnehmen, was dem
immunologischen Informationsaustausch dient.
 Abbildung: Funktion von Stellatumzellen (Ito-Zellen)
Abbildung: Funktion von Stellatumzellen (Ito-Zellen)
 Bei traumatischen Einflüssen kommt es zu Umwandlung
parenchymaler Zellen (Hepatozyten, Cholangiozyten) in nichtparenchymale
(Myofibroblasten). Ferner können sich (mobile) Knochenmarks- und portale
Blastenzellen in Myofibroblasten
verwandeln (diese sind kontraktil, bilden intensiv Kollagen und sind in
Wundheilungsvorgänge involiert)
Bei traumatischen Einflüssen kommt es zu Umwandlung
parenchymaler Zellen (Hepatozyten, Cholangiozyten) in nichtparenchymale
(Myofibroblasten). Ferner können sich (mobile) Knochenmarks- und portale
Blastenzellen in Myofibroblasten
verwandeln (diese sind kontraktil, bilden intensiv Kollagen und sind in
Wundheilungsvorgänge involiert) Auch der umgekehrte Weg (mesenchymal
zu parenchymal) ist möglich (
Auch der umgekehrte Weg (mesenchymal
zu parenchymal) ist möglich ( Abbildung).
Abbildung). (diskontinuierliche Kapillarwände). Sie können Makromoleküle binden und aus dem Blut entfernen. Dazu verfügen sie über verschiedene Rezeptoren, wie für Fc-Abschnitte von Immunkomplexen, für Asialoglykoproteine
(diskontinuierliche Kapillarwände). Sie können Makromoleküle binden und aus dem Blut entfernen. Dazu verfügen sie über verschiedene Rezeptoren, wie für Fc-Abschnitte von Immunkomplexen, für Asialoglykoproteine
 (werden Sialinsäurereste von Plasma-Glykoproteinen abgespalten, so
werden letztere über den Asialoproteinrezeptor in der Leber aufgenommen
und abgebaut -
(werden Sialinsäurereste von Plasma-Glykoproteinen abgespalten, so
werden letztere über den Asialoproteinrezeptor in der Leber aufgenommen
und abgebaut -  s. dort), oder für LDL-Apoproteine.
s. dort), oder für LDL-Apoproteine. 
 Abbildung: Feinstruktur der Leber mit Sinusoid, Kupffer-Zellen, Ito- (=Stellatum-) Zellen
Abbildung: Feinstruktur der Leber mit Sinusoid, Kupffer-Zellen, Ito- (=Stellatum-) Zellen

 Abbildung: Antwort von Akutphasenproteinen im Blut auf mäßigen Entzündungsreiz
Abbildung: Antwort von Akutphasenproteinen im Blut auf mäßigen Entzündungsreiz
 Abbildung):
Abbildung):
 Einige Indikatorproteine reagieren rasch und intensiv (Anstieg bis
300-fach: z.B. C-reaktives Protein), die Konzentration nähert sich nach
wenigen Tagen wieder dem Kontrollwert an;
Einige Indikatorproteine reagieren rasch und intensiv (Anstieg bis
300-fach: z.B. C-reaktives Protein), die Konzentration nähert sich nach
wenigen Tagen wieder dem Kontrollwert an;  einige langsamer und moderat
(z.B. Fibrinogen), ihre Konzentration bleibt über Wochen erhöht; wieder
andere zeigen ein vorübergehendes (~10 Tage) Absinken ihrer
Plasmakonzentration (z.B. Albumin).
einige langsamer und moderat
(z.B. Fibrinogen), ihre Konzentration bleibt über Wochen erhöht; wieder
andere zeigen ein vorübergehendes (~10 Tage) Absinken ihrer
Plasmakonzentration (z.B. Albumin).  Akutphasenproteine werden von der Leber auf Zytokinreize hin (IL-1, IL6, TNF) als Zeichen einer systemischen
Entzündungsreaktion kurz nach Beginn einer Infektion gebildet und in den
Kreislauf sezerniert.
Akutphasenproteine fördern die Opsonisierung und wirken als Gerinnungsfaktoren, Komplementfaktoren,
Transport- und metallbindende Proteine, Proteasen oder Protease-Inhibitoren.
Akutphasenproteine werden von der Leber auf Zytokinreize hin (IL-1, IL6, TNF) als Zeichen einer systemischen
Entzündungsreaktion kurz nach Beginn einer Infektion gebildet und in den
Kreislauf sezerniert.
Akutphasenproteine fördern die Opsonisierung und wirken als Gerinnungsfaktoren, Komplementfaktoren,
Transport- und metallbindende Proteine, Proteasen oder Protease-Inhibitoren. das C-reaktive Protein (CRP), das an Pathogene bindet und opsonisierend wirkt (die Phagozytose steigert),
das C-reaktive Protein (CRP), das an Pathogene bindet und opsonisierend wirkt (die Phagozytose steigert), MBL, das an mikrobielle Membranen bindet und Komplement aktiviert,
MBL, das an mikrobielle Membranen bindet und Komplement aktiviert,  Fibrinogen, das die Thrombenbildung anregt und dadurch Pathogene fixiert,
Fibrinogen, das die Thrombenbildung anregt und dadurch Pathogene fixiert, Coeruloplasmin, das freie Radikale (die im Rahmen von Entzündungen entstehen) binden kann,
Coeruloplasmin, das freie Radikale (die im Rahmen von Entzündungen entstehen) binden kann, Haptoglobin, das frei gewordenes Hämoglobin bindet (und dadurch die Niere schont),
Haptoglobin, das frei gewordenes Hämoglobin bindet (und dadurch die Niere schont), Ferritin, das Eisen bindet (und dadurch den Bakterien entzieht),
Ferritin, das Eisen bindet (und dadurch den Bakterien entzieht), Hepcidin, das die intestinale Eisenresorption hemmt,
Hepcidin, das die intestinale Eisenresorption hemmt, Thrombopoetin, das die Bildung von Thrombozyten anregt (dieses Hormon wird außer von der Leber auch von den Nieren gebildet).
Thrombopoetin, das die Bildung von Thrombozyten anregt (dieses Hormon wird außer von der Leber auch von den Nieren gebildet). Akutphasenproteine Nach Bröker / Schütt / Fleischer, Grundwissen Immunologie, 4. Aufl. Springer 2019 |
||
| Protein |
Funktion |
Gruppe |
| Fibrinogen Prothrombin |
Koagulation, Gewebereparatur |
Gerinnungs- faktoren |
| C1-C9 MBL |
Opsonisierung |
Komplement- faktoren |
| Präkallikrein |
Vasodilatation, Permeabilität |
Kallikrein-Kinin- System |
| α1-Antitrypsin |
Hemmung der Proteolyse |
Proteinase- inhibitoren |
| CRP |
Opsonisierung Komplement- aktivierung |
Opsonine |
| Coeruloplasmin Haptoglobin Serumamyloid A |
Radikalfänger, Hämoglobin- transporter, Cholesterin- transporter |
Transporter |
 Zur Interaktion von Darm (Resorption), Leber (Speicherung), Knochenmark (Erythropoese), Milz (Ery-Abbau) und Nieren (Erythropoetin) s. auch dort
Zur Interaktion von Darm (Resorption), Leber (Speicherung), Knochenmark (Erythropoese), Milz (Ery-Abbau) und Nieren (Erythropoetin) s. auch dort sind im Disse-Raum um die Sinus angeordnete (perisinuisoidale) Perizyten, die mit 1,4% der Lebermasse zahlenmäßig 5-8% aller Zellen in der Leber ausmachen. Welche Funktionen sie im ungereizten "Ruhezustand" erfüllen, ist zum Teil unklar. Sie synthetisieren geringe Mengen einer gelartigen Stützstruktur (extrazelluläre Matrix) - bestehend aus Kollagen (Typ IV), Glykoproteinen (Fibronectin, Laminin) und Proteoglykanen -, die gut permeabel ist und den Stoffaustausch (auch von Makromolekülen) zwischen Hepatozyten und Blutbahn kaum behindert. Weiters speichern Stellatumzellen Fett und Vitamin A (50-80% des gesamten Körperspeichers an Retinlyester). Vielleicht beteiligen
sie sich an der Antigenpräsentation, wahrscheinlich können sie natürliche Killerzellen (NK-Zellen) stimulieren.
sind im Disse-Raum um die Sinus angeordnete (perisinuisoidale) Perizyten, die mit 1,4% der Lebermasse zahlenmäßig 5-8% aller Zellen in der Leber ausmachen. Welche Funktionen sie im ungereizten "Ruhezustand" erfüllen, ist zum Teil unklar. Sie synthetisieren geringe Mengen einer gelartigen Stützstruktur (extrazelluläre Matrix) - bestehend aus Kollagen (Typ IV), Glykoproteinen (Fibronectin, Laminin) und Proteoglykanen -, die gut permeabel ist und den Stoffaustausch (auch von Makromolekülen) zwischen Hepatozyten und Blutbahn kaum behindert. Weiters speichern Stellatumzellen Fett und Vitamin A (50-80% des gesamten Körperspeichers an Retinlyester). Vielleicht beteiligen
sie sich an der Antigenpräsentation, wahrscheinlich können sie natürliche Killerzellen (NK-Zellen) stimulieren.  CRP im Serum
CRP im Serum 
 Nichtparenchymzellen (6-7% der Lebermasse, ~40% aller Zellen in der Leber) sind Endothelzellen, Kupffer-Zellen,
Stellatum-(Ito-) Zellen, dendritische Zellen, Cholangiozyten,
Lymphozyten. Sie
entfernen Mikroorganismen, Toxine und untergehende Erythrozyten aus dem
Blut. Über parakrine Faktoren beeinflussen sie Stoffwechsel,
Wachstum und Transportfunktionen der Hepatozyten. Endothelzellen und Ito-Zellen präsentieren zusammen mit Hepatozyten Antigene. Stoffe können frei zwischen Blut und Disse-Raum passieren; Lymphozyten haben direkte Kontakte zu Leberzellen und Ito-Zellen (immunologischer Informationsaustausch) Nichtparenchymzellen (6-7% der Lebermasse, ~40% aller Zellen in der Leber) sind Endothelzellen, Kupffer-Zellen,
Stellatum-(Ito-) Zellen, dendritische Zellen, Cholangiozyten,
Lymphozyten. Sie
entfernen Mikroorganismen, Toxine und untergehende Erythrozyten aus dem
Blut. Über parakrine Faktoren beeinflussen sie Stoffwechsel,
Wachstum und Transportfunktionen der Hepatozyten. Endothelzellen und Ito-Zellen präsentieren zusammen mit Hepatozyten Antigene. Stoffe können frei zwischen Blut und Disse-Raum passieren; Lymphozyten haben direkte Kontakte zu Leberzellen und Ito-Zellen (immunologischer Informationsaustausch)  Endothelzellen (2,8% der Lebermasse) kleiden die Lebersinusoide aus (diskontinuierlicher Kapillartyp mit Fenestrierungen), bilden vasoaktive Substanzen (Endothelin, NO) und haben zahlreiche Rezeptoren, z.B. für Immunkomplexe (Fc-Teil), Asialoglykoproteine, LDL-Apoprotein. Über MHC präsentieren sie zelluläre Antigene an T-Zellen, solche mit passenden Rezeptoren werden zu reifen CD4- und CD8-Zellen. Zytokine aus Stellatum-, Kupffer- und dendritischen Zellen wirken auf diese Vorgänge modifizierend ein Endothelzellen (2,8% der Lebermasse) kleiden die Lebersinusoide aus (diskontinuierlicher Kapillartyp mit Fenestrierungen), bilden vasoaktive Substanzen (Endothelin, NO) und haben zahlreiche Rezeptoren, z.B. für Immunkomplexe (Fc-Teil), Asialoglykoproteine, LDL-Apoprotein. Über MHC präsentieren sie zelluläre Antigene an T-Zellen, solche mit passenden Rezeptoren werden zu reifen CD4- und CD8-Zellen. Zytokine aus Stellatum-, Kupffer- und dendritischen Zellen wirken auf diese Vorgänge modifizierend ein Kupffersche
Sternzellen (2,1% der Lebermasse) sind Makrophagen (80-90% der
stationären Makrophagen des gesamten retikulohistiozytären Systems),
sie bauen Bakterien aus dem Darm ab (z.B. E coli), nehmen Toxine, Immunkomplexe, Zelltrümmer und Viren auf. Bei Kontakt mit Toxinen sezernieren sie Zytokine (IL-6, TNF - Akutphasenantwort: CRP, Fibrinogen, Coeruloplasmin, Haptoglobin, Ferritin) und produzieren Wasserstoffperoxid, Kollagenase, Prostaglandine. Sie spalten Hämoglobin, bauen Häm zu Bilirubin ab, Eisen wird recycelt. Weiters präsentieren Kupfferzellen Antigene, sind über zytoplasmatische Fortsätze mit Endothelzellen verbunden (sie beeinflussen die Blutströmung im Sinusoid) und tauschen mit allen Zellarten Information aus. Auch synthetisieren sie Komponenten der extrazellulären Matrix Kupffersche
Sternzellen (2,1% der Lebermasse) sind Makrophagen (80-90% der
stationären Makrophagen des gesamten retikulohistiozytären Systems),
sie bauen Bakterien aus dem Darm ab (z.B. E coli), nehmen Toxine, Immunkomplexe, Zelltrümmer und Viren auf. Bei Kontakt mit Toxinen sezernieren sie Zytokine (IL-6, TNF - Akutphasenantwort: CRP, Fibrinogen, Coeruloplasmin, Haptoglobin, Ferritin) und produzieren Wasserstoffperoxid, Kollagenase, Prostaglandine. Sie spalten Hämoglobin, bauen Häm zu Bilirubin ab, Eisen wird recycelt. Weiters präsentieren Kupfferzellen Antigene, sind über zytoplasmatische Fortsätze mit Endothelzellen verbunden (sie beeinflussen die Blutströmung im Sinusoid) und tauschen mit allen Zellarten Information aus. Auch synthetisieren sie Komponenten der extrazellulären Matrix  Stellatumzellen
(Stern-, Ito-Zellen) im Disse-Raum machen mit 1,4% der Lebermasse 5-8%
aller Leberzellen aus. Ihre Fortsätze umfassen Lebersinusoide. Sie speichern Fett und
Vitamin A (50-80% des im Körper gespeicherten Retinylesters);
wahrscheinlich können sie NK-Zellen anregen. Aktiviert werden sie durch
Zytokine bei Gewebeschädigung; dabei proliferieren sie zu kontraktilen
Zellen und beteiligen sich an der Wundheilung (Synthese extrazellulärer Matrix). Leberspezifische
NK-Zellen liegen Sternzellen oder Endothelzellen direkt an und tragen
zu Virusbekämpfung und Aktivierung von Kupffer-Zellen bei Stellatumzellen
(Stern-, Ito-Zellen) im Disse-Raum machen mit 1,4% der Lebermasse 5-8%
aller Leberzellen aus. Ihre Fortsätze umfassen Lebersinusoide. Sie speichern Fett und
Vitamin A (50-80% des im Körper gespeicherten Retinylesters);
wahrscheinlich können sie NK-Zellen anregen. Aktiviert werden sie durch
Zytokine bei Gewebeschädigung; dabei proliferieren sie zu kontraktilen
Zellen und beteiligen sich an der Wundheilung (Synthese extrazellulärer Matrix). Leberspezifische
NK-Zellen liegen Sternzellen oder Endothelzellen direkt an und tragen
zu Virusbekämpfung und Aktivierung von Kupffer-Zellen bei |
