

Eine Reise durch die Physiologie - Wie der Körper des Menschen funktioniert


 Bedarf an
Mineralstoffen, Spurenelementen, Vitaminen
Bedarf an
Mineralstoffen, Spurenelementen, Vitaminen
© H. Hinghofer-Szalkay
 Askorbinsäure: Verhindert Skorbut
Askorbinsäure: Verhindert Skorbut
Fluor: fluere = fließen (Fluorite wurden Metallerzen zugesetzt, um deren Schmelzpunkt zu erniedrigen)
Folsäure: folium (lat) = Blatt
Jod: ιώο-ειδης = veilchenfarbig, violett
Kalium: القلية "al-qalya", Pflanzenasche
Calcium, Calciferol: Calcium (calx = Kalk), φέρειν = tragen, bringen
Magnesium: μαγνησιη λιθός = Magnetstein
Natrium: ناترون "natrun“, Natron
Pantothensäure: παντό = (über)all (kommt in den meisten Nahrungsmitteln vor)
Phosphor: φως-φóρος = lichttragend
Selen: σελήνη = Mond (Berzelius: Ähnlichkeit zur Erde (Tellur)
Struma: lat. struma = Drüsenschwellung (am Hals)
Thiamin: θείον = Schwefel (schwefelhaltiges Vitamin)
Die notwendige Zufuhr von Vitaminen, Spurenelementen
(<0,01% der Körpermasse) und
Mineralien liegt im Bereich von einigen Mikrogramm bis zu einigen Gramm
pro Tag. Der Bedarf ist jeweils abhängig von Körpergröße, Gesundheitszustand, Aktivitätsgrad, Geschlecht, Alter und psychischer
Belastung.
Die Resorption
ist häufig an Begleitfaktoren geknüpft und mehrfach
reguliert, wie z.B. von Eisen, das übrigens weder mit
Stuhl noch mit Harn ausgeschieden wird (sondern mit Blutverlust).
Natrium ist das Leit-Kation des extrazellulären, Kalium des
intrazellulären Kompartiments; Calcium ist u.a. als intrazellulärer
Signalstoff lebenswichtig und befindet sich - wie Phosphor, der u.a. für energiereiche Phosphate, Nukleinsäuren und Phospholipide benötigt wird - zum
Großteil in den Knochen; Magnesium wird von hunderten Enzymen benötigt; Spurenelemente haben typischerweise spezifische Kofunktionen.
Wasserlösliche Vitamine werden bei überhöhter Zufuhr leicht wieder
ausgeschieden; fettlösliche hingegen (für ihre Aufnahme ist eine intakte
Fettresorption notwendig) reichern sich im
Fettgewebe an und können leicht überdosiert werden.
|
Mineralstoffe  Spurenelemente
Spurenelemente
 Vitamine
Vitamine
 Core messages
Core messages
Mikronährstoffe sind Mineralien, Spurenelemente und Vitamine
Der Darm resorbiert
(neben Kohlenhydraten, Fetten, Protein und Nukleinsäuren) Vitamine, Mineralien, Spurenelemente (wie z.B. Zink) und alles, was in
der Nahrung in resorbierbarer Form sonst noch vorhanden ist (Gewürz-
und Farbstoffe, Konservierungsstoffe, Hormone, Medikamente,
verschiedenste Chemikalien).

 Abbildung: Täglicher Bedarf einer erwachsenen Person an Mineralstoffen, Spurenelementen und Vitaminen
Nach Hinghofer-Szalkay H, Aspekte einer physiologischen Ernährungsweise. Wien Med Wschr 1980; 130: 69-73
Abbildung: Täglicher Bedarf einer erwachsenen Person an Mineralstoffen, Spurenelementen und Vitaminen
Nach Hinghofer-Szalkay H, Aspekte einer physiologischen Ernährungsweise. Wien Med Wschr 1980; 130: 69-73
Mineralstoffe (blau): Durchschnittlicher täglicher Austausch mit der Umwelt im Gramm-Bereich (Phosphor 2g/d;
Kalium, Chlor, Natrium, Calcium jeweils ≥1 g/d; Magnesium ~0,5 g/d)
Vitamine (grün): Bedarf im Bereich zwischen ~80 mg/d und ~3 µg/d
Spurenelemente (rot): Bedarf im Bereich zwischen ~10 mg/d
und ~10 µg/d

Mineralstoffe und Spurenelemente werden
von den Dünndarmschleimhaut unterschiedlich stark resorbiert
(verschiedene Bioverfügbarkeit), zum Teil abhängig von Anwesenheit und
Zustandsform anderer Nährstoffe.
Referenzwerte
der deutschen, österreichischen und schweizerischen Gesellschaften für
Ernährung werden als DACH-Referenzwerte bezeichnet. Im folgenden Text
werden die seit 2008 in der EU geltenden RDA-Werte (EU-RDA) genannt.
 Zur Definition von RDA-Werten s. auch dort
Zur Definition von RDA-Werten s. auch dort
 Mineralstoffe
Mineralstoffe

 Abbildung: Prozentueller Anteil der Elemente am Körpergewicht
Abbildung: Prozentueller Anteil der Elemente am Körpergewicht
Nach einer Vorlage bei science.jrank.org
Der hohe Anteil der Sauerstoffmasse am Körpergewicht erklärt sich durch die Tatsache, dass der Körper zu ~60% aus Wasser besteht

Natrium (Atommasse 23) ist das Leitkation des Extrazellulärraums (~140
mM/l). Von leichter Hyponatriämie spricht man bei Serumspiegeln zwischen 120 und 130 mM/l, von schwerer Hyponatriämie bei niedrigeren Werten. Hypernatriämie liegt bei Werten ab 150 mM/l vor.
Das Atomgewicht von Natrium beträgt 23, das von Chlorid 35,5; 1
molKochsalz sind 58,5 g (Umrechnung Masse Na zu NaCl: 1 zu 2,5). 140
mM bedeuten 8,19 g NaCl pro Liter; weitere gelöste Substanzen in der
extrazellulären Flüssigkeit erhöhen deren osmotischen Gehalt.
 5 g Kochsalz bedeuten 2,3 g Natrium.
5 g Kochsalz bedeuten 2,3 g Natrium.
Der Körper enthält freies Na+ zu etwa 2/3 als NaCl, 1/3 als NaHCO3.
Die Menge freien Natriums (2 moloder ~46 g bei einem Gewicht von ~70
kg) bestimmt über die Osmoregulation Blut- und interstitielles Volumen.
Etwa die gleiche Menge liegt im Knochen gespeichert vor, dieses Natrium
ist nicht direkt verfügbar bzw. osmoregulatorisch aktiv. Die gesamte
Natriummenge im Körper wird auf ca. 100 g geschätzt.
 Eine "physiologische (isotone) Kochsalzlösung" (Grundlage für Infusionslösungen) ist 0,9%-ig, d.h. 1 Liter enthält 9 g NaCl.
Eine "physiologische (isotone) Kochsalzlösung" (Grundlage für Infusionslösungen) ist 0,9%-ig, d.h. 1 Liter enthält 9 g NaCl.
Die physiologische Bandbreite der täglichen Natriumzufuhr ist relativ gering:
 Einerseits sollten mindestens einige mg/kg Körpergewicht täglich
zugeführt
werden, um das extrazelluläre Volumen stabil zu halten - chronische
Unterversorgung mit Kochsalz führt (auch bei maximaler
Aldosteronwirkung) zu Hypotonizität, Hypovolämie und Hypotonie,
schließlich zu Kreislaufversagen
Einerseits sollten mindestens einige mg/kg Körpergewicht täglich
zugeführt
werden, um das extrazelluläre Volumen stabil zu halten - chronische
Unterversorgung mit Kochsalz führt (auch bei maximaler
Aldosteronwirkung) zu Hypotonizität, Hypovolämie und Hypotonie,
schließlich zu Kreislaufversagen
 Andererseits können größere Mengen die Osmo- und Volumenregulation überfordern, da der Körper nicht auf die Ausscheidung von hochkonzentriertem Salz angepasst ist. Zwar kann die Niere die Ausscheidung der Zufuhr anpassen (je mehr
Kochsalz zugeführt wird, desto geringer ist die
Aldosteronbildung, und es wird mehr Natrium
ausgeschieden), aber dies funktioniert nur in einem relativ begrenzten Osmolaritätsbereich.
Andererseits können größere Mengen die Osmo- und Volumenregulation überfordern, da der Körper nicht auf die Ausscheidung von hochkonzentriertem Salz angepasst ist. Zwar kann die Niere die Ausscheidung der Zufuhr anpassen (je mehr
Kochsalz zugeführt wird, desto geringer ist die
Aldosteronbildung, und es wird mehr Natrium
ausgeschieden), aber dies funktioniert nur in einem relativ begrenzten Osmolaritätsbereich.
 Der tägliche Bedarf an Natrium
wird mit 1 bis 3 Gramm (entspricht ~2-7 g Kochsalz) angegeben; nach
der Empfehlung der Deutschen Gesellschaft für Ernährung sollten
erwachsene Personen nicht mehr als 6 g Kochsalz täglich konsumieren (Referenzwert: 1,5 g Natrium / Tag).
Der tägliche Bedarf an Natrium
wird mit 1 bis 3 Gramm (entspricht ~2-7 g Kochsalz) angegeben; nach
der Empfehlung der Deutschen Gesellschaft für Ernährung sollten
erwachsene Personen nicht mehr als 6 g Kochsalz täglich konsumieren (Referenzwert: 1,5 g Natrium / Tag).
 Die tägliche Aufnahme von Chlorid (Atommasse 35,5) ergibt sich im Wesentlichen aus der Kochsalzaufnahme (Empfehlung Erwachsene: 3,2 g Cl/d).
Die tägliche Aufnahme von Chlorid (Atommasse 35,5) ergibt sich im Wesentlichen aus der Kochsalzaufnahme (Empfehlung Erwachsene: 3,2 g Cl/d).
 EU-RDA für Chlorid: 800 mg
EU-RDA für Chlorid: 800 mg
Meerwasser hat eine viermal höhere Kochsalzkonzentration als
extrazelluläre Flüssigkeit. Trinkt man derart konzentrierte Salzlösung
ohne Zusatz von Wasser, ist die Konzentrationsfähigkeit der
menschlichen Niere überfordert - hypertone Dehydration und
lebensbedrohliches Kreislaufversagen sind die Folge.
 3 g NaCl / kg KG / Tag (also bei 70 kg Körpergewicht etwa 210 g/d) ist eine potenziell tödliche Dosis.
3 g NaCl / kg KG / Tag (also bei 70 kg Körpergewicht etwa 210 g/d) ist eine potenziell tödliche Dosis.
 Referenzwerte (Blutserum)
Natrium 136-145 mM
Kalium 3,5-5,0 mM
Chlorid 99-109mM
Referenzwerte (Blutserum)
Natrium 136-145 mM
Kalium 3,5-5,0 mM
Chlorid 99-109mM
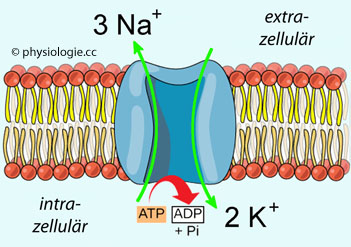

Abbildung: Na-K-ATPase
Nach einer Vorlage in cnx.org
Dieser
ABC-Transporter tauscht Natrium unter Energieverbrauch (ATP-Abbau)
gegen Kalium, im Verhältnis 3 zu 2 - er ladet die Membran direkt
elektrisch auf (innen negativ, elektrogene Wirkung). Dieser Effekt auf das Membranpotential ist allerdings gering (~10%), der führende Beitrag zum Ruhepotential ist das Bestreben von Kalium, die Zelle zu verlassen (innen ~150 mM, außen ~4 mM,  s. dort)
s. dort)

Kalium
(Atommasse 39) ist das wichtigste intrazelluläre Kation (98%
intrazellulär) und an zahlreichen physiologischen Prozessen beteiligt,
wie
Kalium ist das Leit-Kation der
intrazellulären Flüssigkeit (~150 mM oder 5,5 g pro kg). Der
Kaliumgehalt des Körpers beträgt um die 50 mM/kg Körpergewicht: Bei Frauen ~44 mM/kg (Fettzellen haben geringen Flüssigkeitsgehalt), gut trainierte Männer kommen auf ~58 mM/kg (hoher Muskelanteil), über 65-Jährige auf ~47 mM/kg (reduzierte Muskelmasse). 1 mM = 39 mg, daher ergibt sich ein durchschnittlicher Kaliumgehalt im Körper einer erwachsenen Person von etwa 150 Gramm (120-190 g).
Die Ausscheidung erfolgt zu 85-95% über den Harn, zu 5-15% über die Faeces.
 Der tägliche Bedarf an Kalium
liegt möglicherweise höher als die
übliche Aufnahme von 2,0-3,5 g/d (0,75-1,25 mM/kg/d) - empfohlen werden 4,7 g/d (120 mM/d). Referenzwert: 4 g Kalium täglich.
Der tägliche Bedarf an Kalium
liegt möglicherweise höher als die
übliche Aufnahme von 2,0-3,5 g/d (0,75-1,25 mM/kg/d) - empfohlen werden 4,7 g/d (120 mM/d). Referenzwert: 4 g Kalium täglich.
 EU-RDA für Kalium: 2000 mg
EU-RDA für Kalium: 2000 mg
Kaliumreich sind z.B. (gerundete Zahlenwerte in mg/100g)
 Hülsenfrüchte (Linsen 800, Erbsen 900, weiße Bohnen 1300, Sojabohnen 1700)
Hülsenfrüchte (Linsen 800, Erbsen 900, weiße Bohnen 1300, Sojabohnen 1700)
 Nüsse (500-600)
Nüsse (500-600)
 Gemüse (z.B. Spargel 200, Kartoffeln 400, Spinat 600)
Gemüse (z.B. Spargel 200, Kartoffeln 400, Spinat 600)
 Vollmilchschokolade 400, Kakaopulver 1500
Vollmilchschokolade 400, Kakaopulver 1500
 Getreidepridukte (Reis 150, div. Brotsorten 240-440, Kleie über 1000)
Getreidepridukte (Reis 150, div. Brotsorten 240-440, Kleie über 1000)
 manche Obstsorten (über 300: Bananen, Schwarze Johannisbeeren, Honigmelone)
manche Obstsorten (über 300: Bananen, Schwarze Johannisbeeren, Honigmelone)
 Fisch (220-440), Fleisch (250-420)
Fisch (220-440), Fleisch (250-420)
 Zur Regulation der intestinalen Kaliumresorption s. dort
Zur Regulation der intestinalen Kaliumresorption s. dort

Zur Dynamik des Kaliums in der
Niere s.
dort
 Zur Physiologie des Natriums und Kaliums (Leitkation der intrazellulären Flüssigkeit: ~30 l bei ~70 kg KG) s. u.a. II.9, X.6, XII.8.
Zur Physiologie des Natriums und Kaliums (Leitkation der intrazellulären Flüssigkeit: ~30 l bei ~70 kg KG) s. u.a. II.9, X.6, XII.8.
Calcium (Ca++)
Calcium (Atommasse 40) trägt erheblich zur Körpermasse bei (etwa 1,4% - bis zu 1,9% - des Gewichts, d.h. bei einer 70 kg schweren Person rund 1200 Gramm (~30,000 mmol) - davon befinden sich mehr als 99% als strukturelle Komponente
("anorganischer" Bestandteil: apatitähnliche, stark druckbelastbare
Kristallstrukturen) in Knochen und Zähnen (Hydroxylapatit: Ca10(PO4)6(OH)2).
 Abbildung:
Abbildung: Calc
iumbilanz einer erwachsenen Person
Nach einer Vorlage bei Hilal-Dandan / Brunton, Goodman
& Gilman's Manual of Pharmacology and Therapeutics, 2nd ed., McGraw
Hill Education 2014
Im steady state entspricht die mit Stuhl und Harn abgegebene der alimentär aufgenommenen Menge (in diesem Beispiel 800 mg/d).
Mit dem Knochensystem werden täglich etwa 300 mg ausgetauscht

Calcium spielt in zahlreichen Bereichen eine entscheidende Rolle:
 Bestandteil des Knochens. Die Einlagerung / Mobilisierung von Calciumionen in den / aus dem riesigen Knochenspeicher (etwa 1,2 kg oder 3.104 mmol) steht unter mehrfacher hormoneller Kontrolle, der Austausch mit dem Körper beträgt ungefähr 300 mg in 24 Stunden (
Bestandteil des Knochens. Die Einlagerung / Mobilisierung von Calciumionen in den / aus dem riesigen Knochenspeicher (etwa 1,2 kg oder 3.104 mmol) steht unter mehrfacher hormoneller Kontrolle, der Austausch mit dem Körper beträgt ungefähr 300 mg in 24 Stunden ( Abbildung).
Abbildung).
 Extrazellulär: Cofaktor für die Blutgerinnung (Faktoren XII, XI, X, II, Fibrin), Stabilisierung des Ruhepotentials (Erregbarkeit von Neuronen, neuromuskulären Endplatten)
Extrazellulär: Cofaktor für die Blutgerinnung (Faktoren XII, XI, X, II, Fibrin), Stabilisierung des Ruhepotentials (Erregbarkeit von Neuronen, neuromuskulären Endplatten)
 Interzellulär: Calcium ist Teil der "Kittmasse" in tight junctions, welche Zellen zusammenhält / abdichtet
Interzellulär: Calcium ist Teil der "Kittmasse" in tight junctions, welche Zellen zusammenhält / abdichtet
 Intrazellulär: Signalstoff (second messenger, Muskelkontraktion: elektro-mechanische Koppelung)
Intrazellulär: Signalstoff (second messenger, Muskelkontraktion: elektro-mechanische Koppelung)
Calcium ist mit über 1g/kg in
Milch und Milchprodukten, Makrelen, Sardinen, Soja- und Weizenprodukten
enthalten. Ungenügende Aufnahme von Calcium infolge falscher Ernährung,
Verdauungs- und Resorptionsstörungen, schwerem Magnesium- oder Vit.
D-Mangel kann (bei extrazellulärem Mangel an Ca++) zu tetanischen
Krämpfen, Herzrhythmusstörungen und (bei Entspeicherung aus dem Knochen)
zu Osteoporose führen.
Der extrazelluläre Calciumspiegel wird über Parathormon, Calcitonin und Calcitriol reguliert.
 Die tägliche Ca++-Zufuhr mit der Nahrung
sollte 1,0-1,5 g betragen (1 mmol = 40 mg); Gute Calciumquellen sind
Milch und Milchprodukte, Sojabohnen, Spinat, Broccoli.
Die tägliche Ca++-Zufuhr mit der Nahrung
sollte 1,0-1,5 g betragen (1 mmol = 40 mg); Gute Calciumquellen sind
Milch und Milchprodukte, Sojabohnen, Spinat, Broccoli.
Unterversorgung kann die Entwicklung von
Osteoporose fördern. Referenzwert: 1 g Calc
ium / Tag.
Altersabhängigkeit: 0-6 Monate
200, 6-12 Monate 260 mg/d; 1-3 Jahre 700 mg/d; 4-8 Jahre 1000 mg/d;
9-18 Jahre 1300 mg/d; Erwachsene: 1000 mg/d; Frauen ab 51 und Männer ab
71 1200 mg/d.
 EU-RDA für Calcium: 800 mg
EU-RDA für Calcium: 800 mg
 Calcium (Blutplasma)
Calcium (Blutplasma)
2,2-2,65 mM
davon etwa
die Hälfte frei (ional), die andere Hälfte komplex (Phosphat, Oxalat
u.a.) bzw. an Plasmaprotein (vor allem Albumin) gebunden
 Zur Regulation der Calciumresorption s. dort
Zur Regulation der Calciumresorption s. dort
 Phosphat (Blutplasma)
0,8-1,6 mM (2,5-5,0 mg/dl)
Phosphat (Blutplasma)
0,8-1,6 mM (2,5-5,0 mg/dl)
 Die tägliche Phosphor-Aufnahme
einer erwachsenen Person sollte mindestens ~0,7 Gramm betragen. Gute
Phosphatquellen sind Milchprodukte, Bohnen, Walnüsse, Fleisch, Fisch,
Brot.
Die tägliche Phosphor-Aufnahme
einer erwachsenen Person sollte mindestens ~0,7 Gramm betragen. Gute
Phosphatquellen sind Milchprodukte, Bohnen, Walnüsse, Fleisch, Fisch,
Brot.
Ein typischer Wert wäre etwa 1,2
g/d.
 EU-RDA für Phosphor: 700 mg
EU-RDA für Phosphor: 700 mg
 (Atommasse 24): Der Körper einer erwachsenen Person enthält etwa 20 g
Magnesium - ~65% im Knochen, 27% im Skelettmuskel, 7% in anderen
Zellen, 1% im Extrazellulärraum.
(Atommasse 24): Der Körper einer erwachsenen Person enthält etwa 20 g
Magnesium - ~65% im Knochen, 27% im Skelettmuskel, 7% in anderen
Zellen, 1% im Extrazellulärraum.
Magnesiumionen beteiligen sich an hunderten Enzymreaktionen (ATP- und
Nukleinsäure-bindende Enzyme u.a.).
 Fast alle Enzyme, die mit
Nukleotiden (DNA, RNA) interagieren, benötigen Magnesiumionen als
Kofaktor (z.B. DNA-Helikase, RNA-Polymerase).
Fast alle Enzyme, die mit
Nukleotiden (DNA, RNA) interagieren, benötigen Magnesiumionen als
Kofaktor (z.B. DNA-Helikase, RNA-Polymerase).

 Mg++-Ionen
stabilisieren das Ruhepotential an Muskel- und Nervenzellen (u.a. im
Vegetativum).
Mg++-Ionen
stabilisieren das Ruhepotential an Muskel- und Nervenzellen (u.a. im
Vegetativum).
Magnesiummangel kann die Ursache neurologischer Symptome
wie Kopfschmerzen, Nervosität, Reizbarkeit, Müdigkeit und Schwächegefühl sein und auch Muskelkrämpfe und Herzrhythmusstörungen hervorrufen.
 Magnesium
muss stetig mit der Nahrung
zugeführt werden,
denn es geht laufend mit dem Harn verloren (~5% der glomerulär
filtrierten Menge - 95% werden tubulär rückresorbiert).
Magnesium
muss stetig mit der Nahrung
zugeführt werden,
denn es geht laufend mit dem Harn verloren (~5% der glomerulär
filtrierten Menge - 95% werden tubulär rückresorbiert).
Der tägliche Bedarf wird für Männer mit ~420 mg/d
und bei Frauen ~320 mg/d angegeben - etwa ein Drittel der mit der
Nahrung zugeführten Menge wird tatsächlich resorbiert. Mit dem Schweiß
verliert man ca. 1,3 mg/Liter, mit dem Harn 100-400 mg/Tag.
Gute Magnesiumquellen sind Fleisch, Fisch, Nüsse, Vollkornprodukte, Leber.
 EU-RDA für Magnesium: 375 mg
EU-RDA für Magnesium: 375 mg
 Magnesium (Blutserum)
0,7-1,2 mM (1,8-2,6 mg/dl)
Magnesium (Blutserum)
0,7-1,2 mM (1,8-2,6 mg/dl)
 Näheres zur Physiologie des
Näheres zur Physiologie des Calc
iums, Phosphats und Magnesiums siehe u.a. dort
 Spurenelemente
Spurenelemente

Biologisch bedeutsame Spurenelemente
H He
Li Be B C N O F Ne
Na Mg Al Si P S Cl Ar
K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr
Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe
Als Spurenelemente gelten all jene, die zu weniger als 0,01% zur Körpermasse beitragen (d.h. <7g bei 70 kg Körpergewicht; Beispiel Eisen: Körperspeicher normalerweise 3-5 g).
Die Resorption von Spurenelementen beträgt meist nur einen bestimmten Prozentsatz der mit der Nahrung angebotenen Menge und
hängt von der Verfügbarkeit an den Mucosazellen ab.
Unter Bioverfügbarkeit versteht
man im Allgemeinen denjenigen Anteil des Spurenelements, der nach
seiner Resorption tatsächlich im Stoffwechsel physiologisch aktiv wird.
Die Bioverfügbarkeit hängt von zahlreichen Faktoren ab: Wachstum,
Alter, Belastungen (körperliche Arbeit, Schwangerschaft, Laktation),
Anwesenheit anderer Elemente, Medikamente u.a.
Die hier erwähnten Spurenelemente haben eine gesicherte Stellung als
physiologisch notwendige Nahrungskomponenten. Zahlreiche weitere (Aluminium, Arsen, Bor,
Brom, Kadmium, Blei, Germanium, Lithium, Nickel, Rubidium, Silizium,
Zinn, Vanadium) werden als essentiell diskutiert, ihre physiologische Bedeutung ist aber unklar.
Eisen (Fe++ / Fe+++)
Eisen - Fe++ / Fe+++ - dient dem Sauerstofftransport und ist Kofaktor zahlreicher Redoxsysteme. Der Bedarf
für die tägliche Zufuhr mit der Nahrung beträgt 10-15 mg, der Resorptionsgrad ist abhängig von Darreichungsform: Eisen ist zu
10-40% aus organischer Bindung (Hämeisen) nutzbar, nicht so gut (wenige
%) aus pflanzlichen Quellen - abhängig auch von Begleitfaktoren.

 Abbildung: Eisenstoffwechsel an der Darmschleimhautzelle
Abbildung: Eisenstoffwechsel an der Darmschleimhautzelle
Nach Evstatiev R & Gasche C, Iron sensing and signalling. Gut 2012;61: 933-52
Eisen
wird apikal in zweiwertiger Form resorbiert, in der
Darmschleimhautzelle zwischengespeichert (labiler Pool) und basolateral
exportiert. Hier wird es durch Hephaestin zu dreiwertigem Eisen
oxidiert und über Transferrin durch den Extrazellulärraum transportiert
DcytB, duodenales Cytochrom B beschleunigt die Reduktion von Eisen

DMT-1,
divalent metal transporter befördert zweiwertiges Eisen in Darmzellen

HCP-1,
haem carrier protein 1 ist ein Häm-Rezeptor an der luminalen Oberfläche der Enterozyten, über den Hämeisen aufgenommen werden kann

HO-1, Hämoxygenase ist ein mikrosomales Enzym, das Eisen oxydiert

ISC,
iron-sulfur cluster, Eisen-Schwefel-Komplexe, die enzymatisch aktiv sind

Tf,
Transferrin

Ein Großteil der Eisenreserven des Körpers befindet sich im roten Blutfarbstoff der Erythrozyten (Hämoglobin).
Der tägliche Eisenverlust beträgt 1-2 mg oder mehr, hauptsächlich durch Blutungen (Menstruation, Verletzungen, abgestoßene Darmmukosa
u.a.) bedingt.
 Der Körper einer erwachsenen Person sollte 3-5 g Eisen enthalten.
Eisenmangel ist weltweit stark verbreitet und betrifft vermutlich
insgesamt etwa 2 Milliarden Menschen.
Der Körper einer erwachsenen Person sollte 3-5 g Eisen enthalten.
Eisenmangel ist weltweit stark verbreitet und betrifft vermutlich
insgesamt etwa 2 Milliarden Menschen.

Täglich müssen ≥1-2 mg Eisen resorbiert werden. Dazu ist die Zufuhr von
10-30 mg/d Nahrungseisen erforderlich (
Referenzwerte: Männer 10 mg/d, Frauen 15 mg/d). Eisen muss in zweiwertiger Form
angeboten werden,
um resorbiert werden zu können. Gut (10-20%) resorbierbar ist Eisen in
organischer Bindung (Hämeisen in Blut, Fleisch), weniger gut (zu 1-7%)
aus pflanzlichen Quellen. In höherer Konzentration, insbesondere in Zusammenwirken mit Vit. C, kann Eisen prooxidativ wirken.
 EU-RDA für Eisen: 14 mg
EU-RDA für Eisen: 14 mg

 Die Resorption verbessert sich bei
gleichzeitiger Anwesenheit von Vitamin C, Zitronensäure, Eiweiß.
Die Resorption verbessert sich bei
gleichzeitiger Anwesenheit von Vitamin C, Zitronensäure, Eiweiß.
 Viele
pflanzliche Stoffe hemmen sie, z.B. Oxalsäure (Spinat, Rhabarber,
Schokolade) und Gerbstoffe / Tannine (Rotwein, schwarzer Tee).
Viele
pflanzliche Stoffe hemmen sie, z.B. Oxalsäure (Spinat, Rhabarber,
Schokolade) und Gerbstoffe / Tannine (Rotwein, schwarzer Tee).
 Regulation der Eisenresorption s. dort
Regulation der Eisenresorption s. dort
 Eisen (Serum / Plasma)
Eisen (Serum / Plasma)
Männer 7-30 µM (39-168 µg/dl), Frauen 6-26 µM (34-145 µg/dl), Kinder 4-28 µM (22-156 µg/dl)
Gesteigert während der Schwangerschaft

Ausscheidung mit dem Harm: <1,8 µM/d (<100 µg/d)
 Zur Interaktiom von Darm (Resorption), Leber (Speicherung), Knochenmark (Erythropoese), Milz (Ery-Abbau) und Nieren (Erythropoetin) s. auch dort
Zur Interaktiom von Darm (Resorption), Leber (Speicherung), Knochenmark (Erythropoese), Milz (Ery-Abbau) und Nieren (Erythropoetin) s. auch dort
Zink (Zn++)
Eine erwachsene Person hat 1,5-2,5 g Zink in ihrem Körper, ziemlich gleichmäßig verteilt (kein spezifischer
Zinkspeicher). Zink wird hauptsächlich im Jejunum resorbiert (passive
Diffusion und aktiver transmembranaler Transport), die Aufnahme wird

 durch mehrere kleine organische Verbindungen wie z.B. Citrat gefördert,
durch mehrere kleine organische Verbindungen wie z.B. Citrat gefördert,
 andere hemmen sie (z.B. Phytinsäure: schlechte Zinkversorgung bei
(lakto)vegetarischer Kost).
andere hemmen sie (z.B. Phytinsäure: schlechte Zinkversorgung bei
(lakto)vegetarischer Kost).
Über 300 Enzyme sind zinkabhängig, sie werden
durch das Zinkatom stabilisiert: Oxidoreduktasen, Transferasen,
Hydrolasen, Lyasen, Isomerasen und Ligasen. Zink ist u.a. bedeutsam für Insulinspeicherung
in Beta-Zellen, beteiligt sich am Kollagenstoffwechsel, findet sich in
Polymerasen, interagiert mit zahlreichen Hormonen und Neurotransmittern
(Synthese, Speicherung, Sekretion, Rezeptorwirkung) und ist Bestandteil
von Transkriptionsfaktoren (Zinkfingerprotein).
Im Blut befindet sich nur ~0,5% des Körperbestandes (hauptsächlich in der Carboanhydrase der Erythrozyten).
Zinkmangel führt zu Störungen der Wundheilung, im Verdauungssystem
(Appetitverlust,
Durchfall), Integument (Dermatitis, Haarausfall) und Nervensystem
(Konzentrationsstörungen, Geruchs- und Geschmacksstörungen, Ataxie,
depressive Verstimmungen). Solche Symptome können bei einseitiger
Ernährung / ungenügender alimentärer Versorgung mit Zink auftreten
(vegane Kost, hoher Phytatgehalt).
 Der Tagesbedarf
an Zink liegt bei 7-10 mg
Der Tagesbedarf
an Zink liegt bei 7-10 mg (
Referenzwerte: Männer 10 mg/d, Frauen 7 mg/d)
. Gute Quellen sind Fleisch, Milch und Vollkornbrot.
 EU-RDA für Zink: 10 mg
EU-RDA für Zink: 10 mg
 Zink (Serum, Plasma)
Zink (Serum, Plasma)
70-150 µg/dl (11-23 µM)
57% an Albumin, 40% an α2-Makroglobulin, 3% an freie Aminosäuren gebunden
Ausgeschieden wird Zink zu ~90% über den Stuhl und zu ~10% über den Harn.
Jod (J / J-)
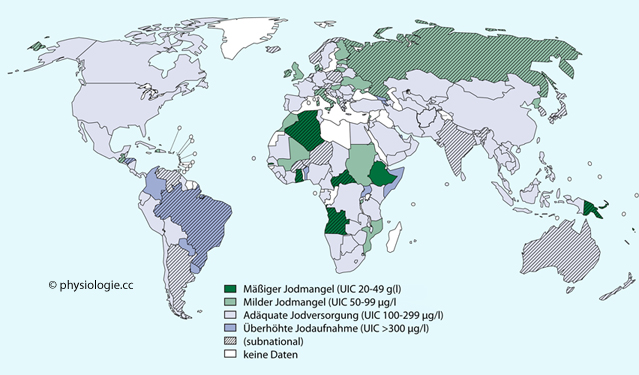
 Abbildung: Weltkarte der Jodidversorgung
Nach
Zimmermann MB, Boelaert K: Iodine deficiency and thyroid disorders. The
Lancet Diabetes & Endocrinology 2008; 372: 1250-62
Abbildung: Weltkarte der Jodidversorgung
Nach
Zimmermann MB, Boelaert K: Iodine deficiency and thyroid disorders. The
Lancet Diabetes & Endocrinology 2008; 372: 1250-62
Als Maß für die tägliche Jodidaufnahme wird (aus praktisch-messtechnischen Gründen) die Jodidkonzentration im Urin (UIC: urinary iodine concentration) herangezogen.
Laut WHO sollte die renale Jodidausscheidung etwa 150 µg/d betragen -
entsprechend einer Jodidkonzentration im Harn von ≥100 µg/l.
Jodmangel
tritt in Gebieten auf, die nur wenig Jod in der Nahrungskette aufweisen
und/oder in denen keine ausreichenden prophylaktischen Massnahmen
(Jodierung von Kochsalz) getroffen werden

Es ist Bestandteil der Schilddrüsenhormone; Jodmangel bedingt Struma  (Jodmangelkropf: das Schilddrüsengewebe ist durch TSH maximal angeregt und hypertrophiert) und Schilddrüsenunterfunktion (Hypothermie, Antriebslosigkeit etc).
(Jodmangelkropf: das Schilddrüsengewebe ist durch TSH maximal angeregt und hypertrophiert) und Schilddrüsenunterfunktion (Hypothermie, Antriebslosigkeit etc).
Jodmangel kommt geographisch gehäuft in Gegenden vor, die durch die
Ausspülung von Jod "freigewaschen" sind (Alpen, Anden u.a.) -
vorausgesetzt, die Betroffenen ernähren sich weitgehend von lokal
erzeugter Kost und verzichten auf Jodprophylaxe (jodiertes Kochsalz).
Allerdings ist die geographisch vorgegebene Situation durch
unterschiedliche gesundheitspolitische Maßnahmen verschiedener Staaten
z.T. extrem modifiziert, s.  Abbildung.
Abbildung.
In Meerwasser
findet sich Jodid in einer Konzentration von ~0,6 mg/l (Geruch!). Überdosierung mit Meersalz kann das
Schilddrüsensystem stark anregen, vor allem bei Menschen, die ohnehin
zu Hyperthyreose
neigen.
 Jod
Jod
Serum (proteingebunden): 40-80 µg/l (0,31-0,63 µM)

Ausscheidung mit dem Harn: 50-70 µg/d (Deutschland)
Die WHO fordert eine Ausscheidung von mindestens 100 µg/l oder 150 µg/Tag
(bei Schwangeren ≥220 µg/d, Stillenden ≥290 µg/d)
Fluoride  festigen Zähne und Knochen, indem sie in deren Matrix als Fluorapatit (statt Hydroxyapatit) eingelagert werden, Demineralisierung reduzieren und die Mineralisierung anregen.
Sie regen weiters die Osteoblastentätigkeit an.
festigen Zähne und Knochen, indem sie in deren Matrix als Fluorapatit (statt Hydroxyapatit) eingelagert werden, Demineralisierung reduzieren und die Mineralisierung anregen.
Sie regen weiters die Osteoblastentätigkeit an.
 ~1 mg/d
~1 mg/d (Säuglinge und Kinder ≥0,25 mg/d)
, bei hohem Fluorgehalt im Trinkwasser entsprechend weniger -
enthalten u.a. in Fisch, Milch. Geringe Fluoridzufuhr bei Kindern führt zu erhöhter Kariesanfälligkeit.
 EU-RDA für Fluorid: 3,5 mg
EU-RDA für Fluorid: 3,5 mg
Fluoridhaltiges
Mundwasser (Natrium- oder Zinnfluorid) ist zur Verhinderung von Karies
vor allem dann erfolgreich, wenn man ihm Zeit für die Diffusion in
Zahnschmelz (und Dentin) gibt (je länger die Mundspülung, desto besser
der Effekt).
 Fluorid (Serum / Plasma)
Fluorid (Serum / Plasma)
<50 µg/l (<2,6 µM)
toxisch ab 2 mg/l (105 µM)
 (mehrere Oxidationsstufen möglich, z.B. Se2-) liegt in der Nahrung vor
allem an Aminosäuren gebunden vor (Methionin, Cystein) und wird vor
allem im Dünndarm resorbiert. Es ist Bestandteil sogenannter Selenoproteine, z.B. der zytosolischen Glutathionperoxidase (GSH-Px), deren Hauptwirkung der Abbau von H2O2
ist (ein antioxidativer Effekt im Blutplasma ist hingegen
unwahrscheinlich). Zellmembranen können durch das Selenoprotein
Phospholipid-Hydroperoxid-GSH-Px geschützt werden (Selen als Radikalfänger: synergistische Wirkung mit Vitamin E). Selen ist u.a. auch an der
Aktivierung von Thyroxin (T4) zu Trijodthyronin (T3) beteiligt (Deiodasen sind Selenoproteine).
(mehrere Oxidationsstufen möglich, z.B. Se2-) liegt in der Nahrung vor
allem an Aminosäuren gebunden vor (Methionin, Cystein) und wird vor
allem im Dünndarm resorbiert. Es ist Bestandteil sogenannter Selenoproteine, z.B. der zytosolischen Glutathionperoxidase (GSH-Px), deren Hauptwirkung der Abbau von H2O2
ist (ein antioxidativer Effekt im Blutplasma ist hingegen
unwahrscheinlich). Zellmembranen können durch das Selenoprotein
Phospholipid-Hydroperoxid-GSH-Px geschützt werden (Selen als Radikalfänger: synergistische Wirkung mit Vitamin E). Selen ist u.a. auch an der
Aktivierung von Thyroxin (T4) zu Trijodthyronin (T3) beteiligt (Deiodasen sind Selenoproteine).
Selen
findet sich in Fisch, Fleisch und Eiern (Veganer, Achtung); der
Selengehalt von Ackerböden ist geographisch äußert unterschiedlich
(Keshan-Krankheit
nach nordostchinesischer Provinz benannt: Kardiomyopathie durch
Selenmangel). Teilweise werden Agrarprodukte systematisch kombiniert,
um Mangelerkrankungen vorzubeugen.
 Der tägliche Selen-Bedarf
beträgt 60-70 µg/d
Der tägliche Selen-Bedarf
beträgt 60-70 µg/d (
Referenzwerte: Männer 70 µg/d, Frauen 60 µg/d,
Säuglinge 10-15, Kinder 15-60 µg/d, mit dem Alter ansteigend). Höhere Dosen wirken potentiell toxisch,
die tolerierbare Obergrenze liegt wahrscheinlich bei ~400 µg/d.
 EU-RDA für Selen: 55 µg
EU-RDA für Selen: 55 µg
Der Körper einer erwachsenen Person enthält vermutlich 13-20 mg
Selen - vor allem in Nieren, Leber, Pankreas, Herz und
Skelettmuskulatur (Konzentrationswerte in dieser Reihenfolge, noch
höher als in den Nieren in Epi- und Hypophyse sowie Hoden - vermutlich
wegen der hohen Methionin-Einbaurate).
Selenmangel äußert sich am
raschesten in der Abnahme der Aktivität der zytosolischen
Glutathionperoxidase.
 Selen
Selen
Serum / Plasma
0,7-1,3 µM (55-103 µg/l)
niedrigere Werte bei Kindern (altersabhängig)
Vollblut
0,75-1,57 µM (59-124 µg/l)
Harn
0,06-0,38 µM (5-30 µg/l)
Der Körper einer erwachsenen Person enthält 10-20 mg Chrom.

Der Bedarf liegt unter 20 µg/d, die
tägliche Aufnahme von Chrom sollte wahrscheinlich 25-35 µg nicht
überschreiten (USA).
Referenzwerte: 30-100 µg/d.
 EU-RDA für Chrom: 40 µg
EU-RDA für Chrom: 40 µg
 Chrom
Chrom
Serum / Plasma: <0,4 µg/l
Vollblut: <0,7 µg/l
Harn: <1,5 µg/l
Kobalt ist in Fleisch, Leber, Nüssen u.a. zu finden; es ist Bestandteil des Vitamin B12
(Cobalamin) sowie mehrerer Enzyme (Cytochromoxidase, Superoxiddismutase
u.a.). Es wird über Nahrung und Getränke, auch über inhalierte Luft
aufgenommen. Im Körper liegt es (Bestand rund 1 mg) zu über 80% in Form von Vit. B12 vor, vor allem in Leber und Nieren.
 Der Bedarf wird auf 0,1 µg/d geschätzt und üblicherweise mit der Zufuhr von Vit.B12 gedeckt.
Der Bedarf wird auf 0,1 µg/d geschätzt und üblicherweise mit der Zufuhr von Vit.B12 gedeckt.
Kobaltmangel ist beim Menschen nicht bekannt, Vergiftungen
können z.B. bei der Herstellung von Farben, Futtermitteln,
Arzneimitteln, Katalysatoren oder in der Glasindustrie vorkommen.
 Kobalt
Kobalt
Serum: 0,3-3 µg/l
Vollblut: 0,5-3,9 µg/l
Harn: <1 µg/l
Abnahmen, Probenaufbereitung und Analysen müssen mit
spurenelementfreien oder beschichteten Röhrchen / Kanülen / Gefäßen /
Reagentien / Geräten vorgenommen werden, um Kontaminationen zu
vermeiden.
Kupfer
ist Bestandteil mehrerer Enzyme (Oxidoreduktasen), z.B.
 Coeruloplasmin (Ferroxidase I, oxidiert Fe2+ zu Fe3+),
Coeruloplasmin (Ferroxidase I, oxidiert Fe2+ zu Fe3+),
 Cytochromoxidase (bewirkt oxidative Phosphorylierung),
Cytochromoxidase (bewirkt oxidative Phosphorylierung),
 Superoxiddismutase (Radikalschutz),
Superoxiddismutase (Radikalschutz),
 Lysyloxidase (vernetzt Kollagen und Elastin),
Lysyloxidase (vernetzt Kollagen und Elastin),
 Tyrosinase (bewirkt Pigmentierung),
Tyrosinase (bewirkt Pigmentierung),
 Cholesterolhydrolasen (Cholesterinabbau)
Cholesterolhydrolasen (Cholesterinabbau)
und wird insbesondere in den
Mitochondrien benötigt. Weiters ist es an der Eisenresorption
beteiligt (Hephästinaktivität).
 Tagesbedarf: 1-2 mg
(Fleisch, Fisch, Innereien, Getreide, Nüsse). Kupfermangel bewirkt vor allem Anämie. Referenzwerte
Tagesbedarf: 1-2 mg
(Fleisch, Fisch, Innereien, Getreide, Nüsse). Kupfermangel bewirkt vor allem Anämie. Referenzwerte: 1,0-1,5 mg/d. Kupfermangel ist extrem selten (Leukopenie, Anämie).
 EU-RDA für Kupfer: 1 mg
EU-RDA für Kupfer: 1 mg
 Kupfer (Serum / Plasma)
Kupfer (Serum / Plasma)
Männer 11-22 µM (70-140 µg/dl), Frauen 13-24 µM (86-150 µg/dl)
Ausscheidung mit dem Harn: 0,15-0,95 µM/d
Kupfer wird über die Galle in den Darm befördert (geregelter Prozess) und mit den Fäzes ausgeschieden.
Kupfermangel kann
mitverantwortlich sein für die Entstehung von Anämien (wahrscheinlich
über Coeruloplasmin und Eisenaufnahme in Transferrin, vielleicht auch
über erhöhten Erythrozytenabbau durch sinkenden Gehalt an
Superoxiddismutase), Herzproblemen, Hypothermie, neuraler Degeneration, Störungen im Bindegewebe.
Kupfermangel kommt selten vor; er ist nachweisbar über Cu-Bestimmungen
in Lebergewebe, Serum und Harn. Die Ursachen können vielfältig sein
(geringe Zufuhr, gestörte Resorption, erhöhter Bedarf u.a.).
Mangan
ist ein Bestandteil mehrerer Enzyme, Mangelsymptome sind unbekannt. Es
wird über Nahrungsmittel (Vollkorn, Nüsse, Hülsenfrüchte, Tee) und
Getränke über den Dünndarm aufgenommen und in Leber, Nieren, Pankreas,
Knochenmark gespeichert (vor allem in den Mitochondrien; Körperbestand 10-20 mg). Mangan wird zu 95% über die Galle ausgeschieden.
Mangan unterstützt mehrere Körperfunktionen (Spermatogenese, Blutgerinnung, ZNS-Entwicklung) und ist Bestandteil oder Aktivator von Enzymen wie Pyruvatcarboxylase (Gluconeogenese), Mevalonatkinase (Cholesterinsynthese), Superoxiddismutase (Radikalschutz). Manganmangel ist beim Menschen nicht bekannt.
 <1 mg/d. Empfohlene Zufuhr 2-5 mg/d.
<1 mg/d. Empfohlene Zufuhr 2-5 mg/d.
 EU-RDA für Mangan: 2 mg
EU-RDA für Mangan: 2 mg
 Mangan (Serum)
Mangan (Serum)
Serum 0,3-1,1 µg/l (5-20 nM)
Vollblut 6-11 µg/l (110-200 nM)
Harn 0,1-0,5 µg/l (2-27 nM)
Molybdän wird im Dünndarm resorbiert (Hülsenfrüchte, Gemüse, Getreide,
Innereien, Milchprodukte), im Blut an α-Globulin und Erytrthrozyten
angelagert und hauptsächlich in Knochen (60%) und Leber (20%)
gespeichert (Körperbestand 8-10 mg). Die Ausscheidung erfolgt in erster
Linie über den Harn.
Mangelerscheinungen treten bei
oraler Ernährung nicht auf, eventuell bei ausschließlich parenteraler
Ernährung. Überschüssiges Molybdän wird rasch ausgeschieden, es kann Hyperurikämie auslösen (Gichtgefahr).

Der Tagesbedarf liegt bei 25 µg, die empfohlene Zufuhr 50-100 µg/d (nicht über 150 µg/d).
 EU-RDA für Molybdän: 50 µg
EU-RDA für Molybdän: 50 µg
 Molybdän
Molybdän
Serum <0,6 µg/l (<60 nM)
Harn 10-16 µg/l (100-165 nM)
 Vitamine
Vitamine
Vitamine sind organische
Verbindungen, die keine Energie liefern, im Stoffwechsel
Schlüsselfunktionen ausüben und vom Körper selbst nicht gebildet
werden. Sie werden in kleinen Mengen in der Nahrung benötigt, ein
Mangel führt zu oft unspezifischen Symptomen.
In Mitteleuropa bietet die Nahrung in aller Regel ausreichende Vitaminversorgung. Ausnahmen sind gegeben bei
 erhöhtem physiologischem Bedarf (Schwangere, Säuglinge)
erhöhtem physiologischem Bedarf (Schwangere, Säuglinge)
 ungenügender Zufuhr wegen Reduktionskost, veganer / vegetarischer Ernährungsweise
ungenügender Zufuhr wegen Reduktionskost, veganer / vegetarischer Ernährungsweise
 Resorptionsstörungen, z.B. genetisch bedingten Defekten an Enzymen oder Transportsystemen
Resorptionsstörungen, z.B. genetisch bedingten Defekten an Enzymen oder Transportsystemen
Der Bedarf an Vitaminen ist
individuell unterschiedlich und richtet sich u.a. nach genetischer Ausstattung, Alter,
Lebensgewohnheiten u.a.
 Bei Vitamin-Unterversorgung
können sich Probleme entwickeln, umso rascher, je kürzer die
Aufenthaltsdauer im Körper ist und je geringer die physiologischen
Speicher gefüllt sind. Mangelernährung führt zum Fehlen mehrerer
Nahrungskomponenten, "reine", nur ein Vitamin betreffende Symptome
finden sich sehr selten.
Nimmt man Nahrung bis zur Sättigung auf,
liefert diese so gut wie immer ausreichend Vitamine - soferne sie nicht
allzu einseitig ist ("Wunderkuren"). Supplementation mit Vitaminpräparaten ist fast immer überflüssig.
Vegetarische (kein Fleisch oder Fisch) und insbesondere vegane Kost (keinerlei Produkte tierischen Ursprungs) muss
hingegen sorgfältig kombiniert werden, um Mangelzustände zu vermeiden.
Bei Vitamin-Unterversorgung
können sich Probleme entwickeln, umso rascher, je kürzer die
Aufenthaltsdauer im Körper ist und je geringer die physiologischen
Speicher gefüllt sind. Mangelernährung führt zum Fehlen mehrerer
Nahrungskomponenten, "reine", nur ein Vitamin betreffende Symptome
finden sich sehr selten.
Nimmt man Nahrung bis zur Sättigung auf,
liefert diese so gut wie immer ausreichend Vitamine - soferne sie nicht
allzu einseitig ist ("Wunderkuren"). Supplementation mit Vitaminpräparaten ist fast immer überflüssig.
Vegetarische (kein Fleisch oder Fisch) und insbesondere vegane Kost (keinerlei Produkte tierischen Ursprungs) muss
hingegen sorgfältig kombiniert werden, um Mangelzustände zu vermeiden.
 Übermäßige Vitaminzufuhr
ist in entwickelten Ländern gang und gäbe und kann z.T. gravierende
Nebenwirkungen zeitigen. Daher hat man Obergrenzen der empfohlenen
Zufuhr definiert (UL: Tolerable upper intake level).
Übermäßige Vitaminzufuhr
ist in entwickelten Ländern gang und gäbe und kann z.T. gravierende
Nebenwirkungen zeitigen. Daher hat man Obergrenzen der empfohlenen
Zufuhr definiert (UL: Tolerable upper intake level).
Aus
praktischen Gründen (Absorption im Darm) unterscheidet man
 fettlösliche
(A, D, E, K) - ihre Aufnahme bedingt funktionierende Fettresorption
(Pankreasfunktion, Gallesekretion, Transport über Chylomikronen). Sie
werden im Magen durch den niedrigen pH-Wert bzw. Proteolyse von
Proteinen, an die sie angelagert sein können, abgekoppelt. Im
proximalen Dünndarm werden sie nach dem Muster der Fettresorption
(Emulsion, Mizellenbildung) von der Schleimhaut (apikal) via Diffusion
oder Transporter aufgenommen und (basolateral) in Chylomikronen oder
VLDL-Partikel verpackt an das Interstitium weitergegeben. Die Lymphe
abtransportiert sie ab, die Leber nimmt sie via Endozytose auf;
fettlösliche
(A, D, E, K) - ihre Aufnahme bedingt funktionierende Fettresorption
(Pankreasfunktion, Gallesekretion, Transport über Chylomikronen). Sie
werden im Magen durch den niedrigen pH-Wert bzw. Proteolyse von
Proteinen, an die sie angelagert sein können, abgekoppelt. Im
proximalen Dünndarm werden sie nach dem Muster der Fettresorption
(Emulsion, Mizellenbildung) von der Schleimhaut (apikal) via Diffusion
oder Transporter aufgenommen und (basolateral) in Chylomikronen oder
VLDL-Partikel verpackt an das Interstitium weitergegeben. Die Lymphe
abtransportiert sie ab, die Leber nimmt sie via Endozytose auf;
 wasserlösliche Vitamine (B-Komplex, Vit. C u.a.).
wasserlösliche Vitamine (B-Komplex, Vit. C u.a.).

Über
Chylomikronen,
VLDL,
IDL und
LDL s. auch
dort
Die Versorgung lässt sich bei den fettlöslichen Vitaminen über ihren
Plasmaspiegel abschätzen, bei den wasserlöslichen in vielen Fällen über
die Ausscheidung mit dem Harn; für einige Vitamine gibt es funktionelle
Kriterien (z.B. Knochendichte für Vit.D, Transketolase-Test für Vit. B1
etc.) von verschieden guter Spezifität.
Fettlösliche Vitamine werden
(unter Beteiligung der Gallensäuren, wie bei allen intestinal
resorbierten Lipiden) im proximalen Dünndarm aufgenommen und - in
Chylomikronen verpackt - mit
der Lymphe weitertransportiert; schließlich erreichen sie (mit
Chylomikronenresten) Leber - die sie speichern kann (lange Verweildauer
im Organismus) - und andere Organe.
 Bei fettlöslichen Vitaminen (vor allem A, D) besteht die Gefahr einer Überdosierung.
Bei fettlöslichen Vitaminen (vor allem A, D) besteht die Gefahr einer Überdosierung.
FETTLÖSLICHE VITAMINE
Die im Folgenden angegebenen Werte für den Vitamingehalt in
Nahrungsmitteln sind jeweils gerundet und orientieren sich weitgehend an Angaben
in Biesalski / Schrezenmeir / Weber / Weiß, Vitamine (Thieme 1997, ISBN
3131184019). EU-RDA-Werte repräsentieren aktuelle Empfehlungen zur Vitaminzufuhr (RDA = recommended daily allowance)
Die
Moleküle der Vitamine A, D, E und K haben lange nichtpolare (und daher
lipophile) Seitenketten, die ihnen ihre Fettlöslichkeit verleihen und
sie in Leber und Fettgewebe speicherbar machen. Die speziellen Seitenketten beeinflussen Wirkmuster und Speicherort des jeweiligen Vitamins. Für die Aufnahme der Vitamine aus dem Darm wirken die Mechanismen der Fettresorption
(Emulgierung mittels Gallensäuren etc). Anschließend werden sie in
Chylomikronen eingebaut und in dieser Form u.a. zur Leber
transportiert.
Vitamin A (Retinol / Retinal / Retinsäure)
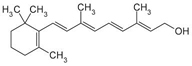
 Retinol
Retinol
Retinol (Vit. A1) und 3-Dehydroretinol (Vit. A2)
sind natürlich vorkommende Vorstufen für die Synthese des Vitamin A.
Photosynthetische Bakterien, Algen und höhere Pflanzen machen daraus
Carotinoide; ß-Carotin ist das wichtigste Protivamin A.

Gute Vitamin-A-Quellen:
ß-Carotine: Spinat, Karotten, dunkelgrünes Gemüse, gelb-orange Gemüsepflanzen
Retinol: Leber(tran), Milchprodukte, Eier
Carotinoide
und Vitamin A werden im Duodenum und oberen Jejunum resorbiert,
Gallensäuren und deren Salze erleichtern diesen Vorgang (fettlösliches Vitamin). Intestinale Mucosazellen
hydrolysieren resorbiertes Vit. A zu Retinol. Carotinoide oxidieren sie
zu Retinal (all-trans-Form); dieses wird anschließend zu Retinol
reduziert, zu Retinsäure oxidiert oder zu 11-cis-Retinal isomerisiert.
Retinol wird mit langkettigen Fettsäuren verestert, von der Lymphe via
Chylomikronen zur Leber gebracht und hier gespeichert. Zur
Verfügbarkeit im Körper wird Vit. A aus der Esterform abgespalten und
via Retinolbindendes Protein (RBP) - das sich seinerseits an Präalbumin
bindet - ohne renalen Filtrationsverlust in die Peripherie gebracht. Vitaminabhängige Zellen nehmen aus diesem Komplex Vit.A über RBP-Rezeptoren auf.
 Retinol (Serum / Plasma)
1-2,8 µM
Retinol (Serum / Plasma)
1-2,8 µM
Stoffe mit Vitamin A-Wirksamkeit
sind Retinol (Retinylester), Retinal und Retinsäure (retina = Netzhaut). Retinsäure-bedingte Genregulation erfolgt
über nukleäre Rezeptoren (RAR: retinoic acid receptors).
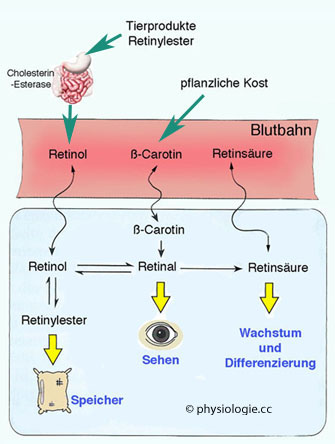
 Abbildung:
Abbildung: Das Vitamin A-System
Modifiziert nach Horn, Biochemie des Menschen (5. Aufl.) Thieme 2012
>90% des Retinols im Blut ist an Retinol-bindendes Protein (RBP) gebunden. Die
verschiedenen Spielarten des Vitamins sind weitgehend ineinander
überführbar (Ausnahme: Retinsäure) und haben jeweils spezifische
Wirkungen

Retinol, Retinal und Retinsäure können im Körper (z.B. der Leber) ineinander
umgewandelt werden, nur die Oxidation Retinal → Retinsäure ist
irreversibel ( Abbildung). Im Blut transportiert wird Retinol an RBP (retinol binding protein)
gebunden (dieser Komplex wird in der Niere teilweise glomerulär
filtriert und über den Megalin-Rezeptor tubulär rückresorbiert). Mehr
als
die Hälfte des im Körper gespeicherten Retinlyesters befindet sich in
den Stellatumzellen (Stern-, Ito-Zellen) der Leber.
Abbildung). Im Blut transportiert wird Retinol an RBP (retinol binding protein)
gebunden (dieser Komplex wird in der Niere teilweise glomerulär
filtriert und über den Megalin-Rezeptor tubulär rückresorbiert). Mehr
als
die Hälfte des im Körper gespeicherten Retinlyesters befindet sich in
den Stellatumzellen (Stern-, Ito-Zellen) der Leber.
 Über Retinal und den Sehvorgang (Sehpurpur) s. dort
Über Retinal und den Sehvorgang (Sehpurpur) s. dort
 Retinal - die Aldehydform des Retinols ("Vitamin-A-Aldehyd") - ist am Sehvorgang beteiligt: es wird als Bestandteil des Rhodopsins - an das Membranprotein Opsin
gekoppelt - in der Netzhaut benötigt (Retinalmangel bedingt Nachtblindheit).
Retinal - die Aldehydform des Retinols ("Vitamin-A-Aldehyd") - ist am Sehvorgang beteiligt: es wird als Bestandteil des Rhodopsins - an das Membranprotein Opsin
gekoppelt - in der Netzhaut benötigt (Retinalmangel bedingt Nachtblindheit).
Licht verwandelt die bei Dunkelheit vorliegende Form
11-cis-Retinal zu all-trans-Retinal, worauf das ans Opsin angedockte Transduzin
(ein G-Protein) dissoziiert und die α-Untereinheit eine
Phosphodiesterase aktiviert, welche cGMP zu GMP abbaut. Das c-GMP hält
im Dunkelzustand einen Na-Ca-Kanal offen, was die Zelle depolarisiert
und die Transmitterproduktion der Sinneszelle aufrechterhält.
Belichtung unterbricht diesen Mechanismus, die Kationenkanäle
schließen, es wird weniger Transmitter freigesetzt, und diese Änderung
wirkt als Signal an den angekoppelten Nervenzellen in der Netzhaut.
 Retinsäure (retinoic acid) entsteht durch Oxidation von Retinal (irreversibler Schritt). Sie ist an der Morphogenese von
Organsystemen des Feten beteiligt und reguliert Wachstum und Differenzierung
epithelialer Gewebe (Haut, Respirationssystem, Darmschleimhaut), aber
auch blutbildender Zellen.
Retinsäure (retinoic acid) entsteht durch Oxidation von Retinal (irreversibler Schritt). Sie ist an der Morphogenese von
Organsystemen des Feten beteiligt und reguliert Wachstum und Differenzierung
epithelialer Gewebe (Haut, Respirationssystem, Darmschleimhaut), aber
auch blutbildender Zellen.
Vitaminmangel verursacht trockene Haut und
Bindehaut (Xerophthalmie); Retinsäure wirkt
vorbeugend gegen Hauttumoren. Retinsäure wird in der Leber glukuroniert und über Galle und Niere ausgeschieden.
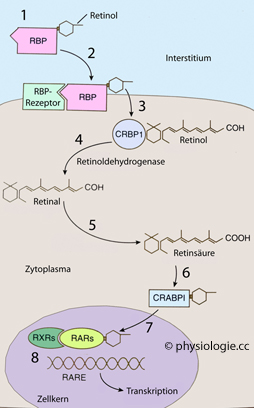
 Abbildung: Vitamin A in der Zelle
Abbildung: Vitamin A in der Zelle
Nach einer Vorlage in Carlson BM, Human Embryology and Developmental Biology, 7th ed. 2024 (Elsevier)
1: Retinol bindet im Interstitium an retinolbindendes Protein (RBP)
2: Dieser Komplex bindet an einen RBP-Rezeptor in der Zellmembran
3: In der Zelle löst sich Retinol vom Komplex und bindet an ein intrazelluläres retinolbindendes Protein (CRBP1, cellular retinol-binding protein 1)
4: Retinol wird durch Einwirken von Retinolgehydrogenase zur Aldehydform Retinal
5: Retinal wird durch Einwirken von Retinaldehydrogenase zu Retinsäure
6: Retinsäure bindet an CRABP1 (cellular retinoic acid-binding protein 1)
7: Im Zellkern bindet Retinsäure an einen Komplex aus zwei nukleären Retinsäure-Rezeptoren, z.B. RXR (retinoid X receptor) und RAR (retinoic acid receptor)
8: Dieser Komplex bindet wiederum an einen hormonempfindlichen Bereich der DNA (RARE, retinoic acid response element)...
9: ...wodurch der Transkriptionsvorgang gestartet wird

 Die wichtigste Transportform im Körper ist Retinol (Vitamin A1, die Alkoholform), aus ihr können alle anderen Formen gebildet werden. Die Speicherform ist Retinylester, vorwiegend in
dieser Form wird Vit.A auch im Darm rersorbiert. Die Regulation des
Vitaminspiegels im Blut erfolgt auf Basis der Umwandlung von ß-Carotin
in Retinal; bei erhöhtem Vitaminbedarf wird Carotin vermehrt in
Retinal umgewandelt (Dioxygenase).
Die wichtigste Transportform im Körper ist Retinol (Vitamin A1, die Alkoholform), aus ihr können alle anderen Formen gebildet werden. Die Speicherform ist Retinylester, vorwiegend in
dieser Form wird Vit.A auch im Darm rersorbiert. Die Regulation des
Vitaminspiegels im Blut erfolgt auf Basis der Umwandlung von ß-Carotin
in Retinal; bei erhöhtem Vitaminbedarf wird Carotin vermehrt in
Retinal umgewandelt (Dioxygenase).
Vitamin A entsteht in tierischem Stoffwechsel - Leber, Fisch,
Vollmilch; in Nahrungsmitteln hauptsächlich Retinylester. Im Darm setzt
eine pankreatische Esterase daraus Retinol frei, dieses
wird über einen Carrier resorbiert. Eisbärenleber enthält große Mengen an Vit.A; Schwangere
sollten nicht zu viel Leber zu sich nehmen, da eine Intoxikation des
Feten möglich ist (Haut- und Schleimhautveränderungen).
Pflanzen enthalten Provitamine (Carotine), vor allem gelbes Gemüse und Früchte (ß-Carotin). Auch reichliche Zufuhr von ß-Carotin führt nicht zu Hypervitaminose.
Der
tägliche Bedarf an Vit.A (Retinylester)
beträgt ~1 mg (Frauen in gebärfähigem Alter, Schwangere und Stillende
bis 1,8 mg/d, Säuglinge 0,6 mg/d - etwa diese Menge wird mit der
Muttermilch produziert -, Kinder bis 10 Jahre 0,8 mg/d). Die Obergrenze
(UL) beträgt 3 mg/d. Referenzwerte: Männer 1,0, Frauen 0,8 mg Retinoläquivalent / Tag.
Weiters
wird eine tägliche Aufnahme von 2-4 mg ß-Karotin empfohlen, möglicherweise ist wegen dessen krebsverhindernder Wirkung eine wesentlich
höhere Versorgung (15 mg/d) optimal (keine Nebenwirkungen).
 EU-RDA für Vitamin A: 800 µg Retinol
EU-RDA für Vitamin A: 800 µg Retinol
Vitamin-A-reiche Nahrungsmittel
1 IE entspricht 0,3 mg Retinol
|
|
Vit-A-Gehalt (IE/100 g)
|
Fischleberöl
|
75.000
|
| Rohe Rinderleber |
20.000 - 50.000 |
| Butter |
2.000 - 3.500 |
| Käse |
500 - 1.000
|
Gekochte Eier
|
150 - 500
|
Pasteurisierte Milch
|
100 - 300
|
Dosenhering
|
200
|
Der Tagesbedarf
an Vit. A (0,9-1,0 mg) ist z.B. enthalten in 10 g Leber, 100 g Leberwurst, 150 g
Butter, 200 g Thunfisch oder Camembert, 300 g Emmentaler oder Mozzarella, 3 Liter Vollmilch.
Vitamin-A-Mangel findet sich vor allem in Entwicklungsländern; Nachtblindheit (Stäbchen stärker betroffen) und sogar Erblindung können die Folge sein, ferner Infektionsneigung und Krebsgefahr (Dedifferenzierung von Epithelzellen).
Vitamin D (Vitamin-D-Hormon, Calciferol, Calcitriol)
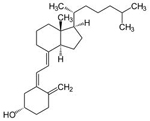
 Cholecalciferol
Cholecalciferol
D-Vitamine
können aus endogenen Vorstufen synthetisiert werden und stellen
insoferne streng genommen keine Vitamine dar. So entsteht unter
UV-Bestrahlung der Haut Cholecalciferol (Vit. D3) aus der Vorstufe 7-Dehydrocholesterin (dem wichtigsten Provitamin D);
Ergocalciferol entsteht aus Ergosterin. Die im Körper biologisch aktive Form des Vitamin D3 ist 1,25-Dihydroxycholecalciferol (1,25[OH]2D3) - die Leber hydroxyliert an der C25-Position, die Niere an der C1-Position ( Abbildung).
Abbildung).

Gute Vitamin-D-Quellen:
Ergocalciferol (Vit. D2): Leber, Eier, Fettfische, getrocknete Pilze
Cholecalciferol (D3): Wird auch in der Haut unter UV-Bestrahlung gebildet
Vitamin D
(Calciferol)
 wirkt (wie Vitamin A) über nukleäre Rezeptoren auf die Transkription einer großen Zahl von Genen. Es hat
dementsprechend zahlreiche Funktionen (teils erwünschte, eventuell
teils unerwünschte Wirkungen). Es fördert die Aufnahme und Verwertung
von Calcium und Phosphor sowie die
Erhaltung der Knochen- und Muskelsubstanz. Weiters unterstützt es
Kreislauffunktion, Immunabwehr und Zellstoffwechsel.
wirkt (wie Vitamin A) über nukleäre Rezeptoren auf die Transkription einer großen Zahl von Genen. Es hat
dementsprechend zahlreiche Funktionen (teils erwünschte, eventuell
teils unerwünschte Wirkungen). Es fördert die Aufnahme und Verwertung
von Calcium und Phosphor sowie die
Erhaltung der Knochen- und Muskelsubstanz. Weiters unterstützt es
Kreislauffunktion, Immunabwehr und Zellstoffwechsel.
Sowohl eine
geringe (Mangelsymptomatik) als auch eine überhöhte Zufuhr
(Krebsinduktion?) dieses Vitamins wirkt sich nachteilig auf die
Gesundheit aus; dies ist ein kontroversiell diskutiertes Gebiet.

 Abbildung: UV-B und endogene Vitamin-D-Synthese, exogene Zufuhr, Aktivierung durch Leber und Niere
Modifiziert nach Doorenbos
CRC, van den Born J, Navis G, de Borst MH. Possible renoprotection by
vitamin D in chronic renal disease: beyond mineral metabolism. Nature
Rev Nephrol 2009; 5: 691-700
Abbildung: UV-B und endogene Vitamin-D-Synthese, exogene Zufuhr, Aktivierung durch Leber und Niere
Modifiziert nach Doorenbos
CRC, van den Born J, Navis G, de Borst MH. Possible renoprotection by
vitamin D in chronic renal disease: beyond mineral metabolism. Nature
Rev Nephrol 2009; 5: 691-700
Vitamin D3
entsteht in der Haut unter Einwirkung von UV-B-Licht (etwa 280-320 nm) aus
7-Dehydrocholesterin und liegt im Blut an DBP (Vit.D-bindendes Protein)
gebunden vor.
Die Leber konvertiert zu 25(OH), die Niere zu 1,25(OH)2-Vitamin D3 (Calcitriol) - die biologisch aktive Form. Die den letzteren Schritt beschleunigende 1α-Hydroxylase
wird durch mehrere Faktoren reguliert, wie Parathormon und Calcitonin.
Das Vitamin kann durch Hinzufügen einer weiteren Hydroxylgruppe an C24 inaktiviert werden, diese Form wird ausgeschieden
 Mindestens 80% des im Körper befindlichen Vitamin D entsteht durch Lichteinwirkung:
Mindestens 80% des im Körper befindlichen Vitamin D entsteht durch Lichteinwirkung:

Die
Haut
bildet unter Einwirkung von UVB aus der Vorstufe 7-Dehydrocholesterin
bis zu 1000 IU/min Provitamin D
3 (umso effizienter, je weniger Melanin
sie enthält), das spontan zu Vit. D
3 (Cholecalciferol) isomerisiert;

D
3-Vitamin wird über das
Vitamin D-bindende Protein (DBP) im Blut transportiert;

die
Leber bildet daraus 25(OH)Vit.D (25-Hydroxycholecalciferol,
Calcidiol), und

die
Niere (1α-Hydroxylase) das biologisch aktive
1,25-(OH
2)-D
3 (1,25-Dihydroxycholecalciferol,
Calcitriol). Dieser letzte Schritt wird (mittels Enzyminduktion) durch
Parathormon und
Calcitonin gefördert, weiters durch Östrogene und erniedrigten
Calciumspiegel im Blut.
Die Regulierung des 1,25-(OH2)-D3-Serumspiegels
erfolgt vorwiegend durch die renale 1α-Hydroxylase, da (das
biologisch aktive) Calcitriol eine kurze Halbwertszeit (wenige Stunden)
hat.
Calcidiol hingegen hat eine Halbwertszeit von ~2 Wochen: Der Vitamin-D-Status korreliert mit dem 25(OH)Vit.D-Serumspiegel:
Beurteilung des Vitamin-D-Status
Nach Biesalski / Bischoff / Pirlich / Weimann: Ernährungsmedizin, 5. Aufl. 2018
|
25(OH)D3-Serumspiegel
|
Status
|
| >75 nM/l (>30 ng/ml) |
ausreichend
|
>50 nM/l (>20 ng/ml)
|
wahrscheinlich ausreichend
|
30-50 nM/l (12-20 ng/ml)
|
unzureichend
|
12-30 nM/l (5-12 ng/ml)
|
Mangel
|
<12 nM/l (<5 ng/ml)
|
schwerer Mangel
|
 Entscheidend ist die Effizienz der
intrazellulären Wirkung. Diese hängt von der Menge verfügbarer Rezeptoren ab, und die Zahl der Rezeptoren ist regulierbar. Ein niedriger Serumwert lässt sich also durch upregulation auf Rezeptorebene kompensieren und muss sich nicht zwingend als Vit-D-Mangel manifestieren.
Die "klassische" Wirkung des Vitamins ist die Regulierung von Calciumhaushalt und Knochenfunktion. Schwerer Vitamin-D-Mangel (s. Tabelle) hat
Entscheidend ist die Effizienz der
intrazellulären Wirkung. Diese hängt von der Menge verfügbarer Rezeptoren ab, und die Zahl der Rezeptoren ist regulierbar. Ein niedriger Serumwert lässt sich also durch upregulation auf Rezeptorebene kompensieren und muss sich nicht zwingend als Vit-D-Mangel manifestieren.
Die "klassische" Wirkung des Vitamins ist die Regulierung von Calciumhaushalt und Knochenfunktion. Schwerer Vitamin-D-Mangel (s. Tabelle) hat
 bei Kindern Rachitis (Deformierungen vor allem im Bereich des Thorax - “Hühnerbrust” -,
des Beckens (Verengungen) und der Extremitäten (O-Beine),
bei Kindern Rachitis (Deformierungen vor allem im Bereich des Thorax - “Hühnerbrust” -,
des Beckens (Verengungen) und der Extremitäten (O-Beine),
 bei Erwachsenen Osteomalazie (Erweichung der Knochenmasse, erhöhte
Anfälligkeit für Knochenbrüche) zur Folge.
bei Erwachsenen Osteomalazie (Erweichung der Knochenmasse, erhöhte
Anfälligkeit für Knochenbrüche) zur Folge.
Vitamin D hat offenbar auch ("nicht-klassische") Effekte auf
Immunsystem, Kreislauf und Zellstoffwechsel.
 Bis zu 20% des Vitamin D im Körper wird über die Nahrung
aufgenommen. Referenzwerte
Bis zu 20% des Vitamin D im Körper wird über die Nahrung
aufgenommen. Referenzwerte: 20 µg Calciferole / Tag
(1µg=40 IU). Aufnahme Vit-D-reicher Nahrung (fetter Fisch, Pilze, Eier, Avocado,
Kuhmilch) sowie
Supplementierung (400 IU/d oder höher) ist in höheren geographischen
Breiten über das ganze Jahr zu empfehlen. Intoxikation (Serum-25(OH)-Vit.D-Spiegel über 150 ng/ml) ist bei dieser Dosierung
nicht zu erwarten.
Für Kinder bis zu einem Jahr wird eine tägliche Zufuhr von 400 IU (10
µg/d) empfohlen, sonst 600 IU/d (15 µg/d), bei Senioren über 75 Jahren
800 IU/d (20 µg/d).
Die Meinungen zur optimalen Vitaminzufuhr (Cholecalciferol) sind in der scientific community unterschiedlich; die neue EU-Richtlinie empfiehlt einen relativ niedrigen Wert:
 EU-RDA für Vitamin D: 5 µg Cholecalciferol
EU-RDA für Vitamin D: 5 µg Cholecalciferol
Vitamin-D-reiche Nahrungsmittel
|
|
Vit-D-Gehalt (µg/100g)
|
Aal
|
90
|
Hering
|
30
|
andere Fischsorten
|
<30
|
Fleisch
|
<10
|
Käse, Milchprodukte
|
<1
|
15 µg Vit.D sind z.B. enthalten in ~20 g Aal oder 50 g Hering.
Andere (auch "Vit-D-reiche") Nahrungsmittel können bei üblicher Zufuhr
den Bedarf kaum decken.
Vitamin-D-Mangel betrifft etwa
jeden zweiten Menschen - insbesondere in der sonnenarmen Periode von
Oktober bis März
(gilt etwa ab dem 40. Breitengrad). Dies führt u.a. zu Muskelschwäche,
diffusen Knochen- und Muskelschmerzen, erhöhter Erkrankungshäufigkeit.
Mangelbedingte Sterblichkeit kann durch Vit-D-Supplementierung gesenkt
werden.
Vitamin E (α-Tocopherol u.a.)
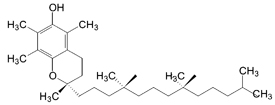
 α-Tocopherol
α-Tocopherol
Die lange Seitenkette des Moleküls dient der Verankerung in der Zellmembran.
Der Begriff "Vitamin E" ist eine Sammelbezeichnung für natürlich vorkommende pflanzliche Moleküle (methylierte Phenole: Tokopherole und Tokotrienole)
mit Vitamin E-Wirkung. Als fettlösliches Vitamin wird Vit. E unter
Wirkung von Gallensäuren gut resorbiert. Der Körper speichert es in
Fettdepots (Adipozyten, Leberzellen) sowie in Membranstrukturen. Im
Kreislauf wird es via VLDL und Chylomikronen transportiert.

Gute Vitamin-E-Quellen: Pflanzen- bzw. Samenöle (insbesondere mit hohem Anteil an ungesättigten Fettsäuren), Gemüse, Nüsse, grünes Blattgemüse
Das wichtigste Vitamin E ist α-Tocopherol - dessen Aktivität dient als Standard, und es hat im Blut ein eigenes α-Tocopherol-Transferprotein (α-TTP),
das von Leber- und Gehirnzellen gebildet wird und dessen Fehlen zu
neurologischen Störungen führt. Die Leber empfängt resorbiertes
Tocopherol über Chylomikronen bzw. Remnants und ladet es auf VLDL. In
der Peripherie wird das Vitamin über Lipidrezeptoren aufgenommen. Vit.E wird in Fett- und
Muskelgewebe gespeichert, ist aber in Mangelzeiten nur begrenzt
mobilisierbar.
 α-Tocopherol (Serum)
12-46 µM (γ-Tocopherol etwa ein Zehntel davon)
α-Tocopherol (Serum)
12-46 µM (γ-Tocopherol etwa ein Zehntel davon)
Relativ: 4-7 µM / mM Cholesterin oder 0,8 mg/g Gesamtlipid
Halbwertszeit im Plasma 5-7 Tage
Tocopherol wirkt antioxidativ, zusammen mit den Vitaminen A und C sowie
selen- und kupferabhängigen Enzymen als Schutzsystem, das
reaktionsfreudige Substanzen (Radikale) bindet (“Radikalfänger”) und
unschädlich macht - vor allem in Membranen, in denen sich das
fettlösliche Molekül anreichert. Die physiologische Bedeutung
(nichtantioxidative Funktionen?) ist nach wie vor unklar (neuromuskuläre
Signalübertragung?), präventive Effekte sind beim Menschen nicht
bewiesen.

 Vitamin E wirkt antioxidativ
Vitamin E wirkt antioxidativ

Vitamin E schützt mehrfach gesättigte Fettsäuren in Zellmembranen

Vitamin E bewahrt Lipoproteine niedriger Dichte (LDL) vor Oxidation

: Männer 14, Frauen 12 mg Tocopheroläquivalent / Tag
. Der Bedarf hängt von der
Zufuhr an Polyen-Fettsäuren ab - je Gramm Dien-Fettsäure(äquivalent)
sollten 0,5 mg RRR-α-Tocopherol aufgenommen werden (RRR:
R-Konfiguration an den drei Chiralitätszentren des Moleküls). Gute
Quellen sind
Oliven,
Sonnenblumenkerne, Weizenkeime, Mais, Sojapflanzen, Reis, Gerste,
Hafer.
 EU-RDA für Vitamin E: 12 mg Tocopherol
EU-RDA für Vitamin E: 12 mg Tocopherol
Vitamin-E-Mangelversorgung kann durch Fettresorptionsstörungen bedingt
sein.
Vitamin K (Phyllochinon u.a.)
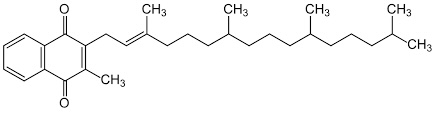
 Phyllochinon (Vit. K1)
Phyllochinon (Vit. K1)
In der Natur kommen Moleküle mit Vit-K-Wirkung in Pflanzen (Vit. K1, Phyllochinone - phyllos (gr) = Blatt) und Bakterien vor (Vit. K2, methylierte Quinone - Menachinone). Das synthetisch hergestellte Menadion (Vit. K3) wird von hepatischen Mikrosomen zu Vit. K2
verwandelt. In der Nahrung vorhandenes und von Darmbakterien
produziertes Vit. K wird im oberen Dünndarm zu 15-65% resorbiert und
via Chylomikronen zur Leber gebracht. Die Speicherkapazität des
Organismus (Leber, Milz) für Vit. K ist gering, Mangelerscheinungen
können innerhalb weniger Tage auftreten..

Gute Vitamin-K-Quellen:
Vit. K1: Grünblättriges Gemüse, Sauerkraut, Eigelb, Käse, Leber
Bakterien im Dickdarm synthetisieren Vit. K2
Vitamin K (benannt nach seiner Rolle in der Gerinnung: dänisch koagulation)
tritt in Unterformen auf: Vit. K1 = Phyllochinon, Vit. K2 = Menachinon, Vit. K3 = Menadion, Vit. K4 = Menadiolester.
Die Leber benötigt Vit. K zur Carboxylierung spezifischer Glutaminsäurereste - es ist ein Coenzym einer im endoplasmatischen Retikulum bzw. extrazellulär
wirksamen γ-Carboxylase ( s. dort). Diese modifiziert Zielproteine (Gerinnungsfaktoren II, VII, IX, X, Protein C und S) zu Ca++-Chelatoren - mittels des Ca++ binden die Faktoren an membranständige Phospholipide aktivierter Zellen.
s. dort). Diese modifiziert Zielproteine (Gerinnungsfaktoren II, VII, IX, X, Protein C und S) zu Ca++-Chelatoren - mittels des Ca++ binden die Faktoren an membranständige Phospholipide aktivierter Zellen.
Dies ist auch für den Knochenstoffwechsel bedeutsam; in Osteoblasten wird das Knochenprotein Osteocalcin carboxyliert, es bindet an Ca++-Ionen bzw. Apatit, was zwar keinen Einfluss auf die Knochendichte hat, aber die Knochenqualität verbessert (verringerte Brüchigkeit).

 Die Hydrochinonform von Vit. K ist ein Cofaktor der γ-Carboxylase
Die Hydrochinonform von Vit. K ist ein Cofaktor der γ-Carboxylase
 γ-Carboxylase aktiviert die Gerinnungsfaktoren II, VII, IX und X
γ-Carboxylase aktiviert die Gerinnungsfaktoren II, VII, IX und X
 Dadurch binden diese Faktoren Ca++ und Phospholipide von Thrombozyten und Gefäßwandzellen
Dadurch binden diese Faktoren Ca++ und Phospholipide von Thrombozyten und Gefäßwandzellen
Der tägliche Bedarf an Vit. K wird auf 65-70 µg geschätzt (Referenzwerte: Männer 70, Frauen 60 µg Phyllochinone / Tag)
. Das Vitamin
liegt in zwei verschiedenen Formen (je nach Seitenkette) vor:
Pflanzlichen Ursprungs ist das Phyllochinon (Vit. K1); einige Bakterien bilden Menachinon
(Vit. K2). Ob Bakterien zur Vit-K-Versorgung wesentlich beitragen, ist umstritten. Gute Quellen sind Zerealien, Spinat, Grünkohl und andere Gemüse, Fleisch, Innereien.
 EU-RDA für Vitamin K: 75 µg Phyllochinon
EU-RDA für Vitamin K: 75 µg Phyllochinon
 Über die Rolle des Vit. K für die Gerinnungsfaktoren II, VII, IX und X ("Prothrombinkomplex") und die klinische Bedeutung von Vitamin-K-Antagonisten zur Abschwächung der Gerinnungsaktivität (Verlängerung der Gerinnungszeit) s. dort
Über die Rolle des Vit. K für die Gerinnungsfaktoren II, VII, IX und X ("Prothrombinkomplex") und die klinische Bedeutung von Vitamin-K-Antagonisten zur Abschwächung der Gerinnungsaktivität (Verlängerung der Gerinnungszeit) s. dort
Vitamin K-reiche Nahrungsmittel
Nach Biesalski / Bischoff / Pirlich / Weimann: Ernährungsmedizin, 5. Aufl. 2018 (Thieme)
|
Fette & Öle
|
Vit-K-Gehalt
(µg/100g)
| Gemüse & Pilze
|
Vit-K-Gehalt
(µg/100g) |
Butter
|
60
| Blumenkohl
|
300
|
Maiskeimöl
|
50
| Brokkoli
|
130
|
Sonnenblumenöl
|
500
| grüne Erbsen
|
<40
|
Fleisch
|
| Hagebutten
|
≤100
|
Huhn
|
300
| Kohl (grün)
|
125
|
Hühnerleber
|
590
| Kopfsalat
|
200
|
Hammelfleisch
(ohne Fett)
|
≤200
| Rosenkohl
|
570
|
Kalbsleber
|
150
| Rotkohl
|
≤300
|
Rindfleisch
(ohne Fett)
|
210
| Sauerkraut
|
1540
|
Rinderleber
|
300
| Sojabohnen
|
190
|
Getreide
|
| Sojamehl
|
200
|
Hafer (entspelzt)
|
50
| Spinat
|
350
|
Weizenkeime
|
350
|
Zwiebel
|
>300
|
Weizenkleie
|
80
|
|
|
Der Vitamin-K-Tagesbedarf
(65-70 µg) ist z.B. enthalten in 20 g Weizenkeimen, 25 g Kohlsprossen,
50 g Kalbsleber, 100 g Butter, 120 g Kartoffeln, 130 g Spargeln, 150 g
Rinderleber oder Weizen-Vollkorn, 220 g Topfen (Speisequark), 400 g
Schweinefleisch.
Bei Behandlung mit Kumarinderivaten zur Gerinnungshemmung (Marcoumar®) treten Symptome eines Vitamin-K-Mangels auf.
 Vitamin K (Serum)
130-1190 ng/l (0,28-2,64 nM)
Vitamin K (Serum)
130-1190 ng/l (0,28-2,64 nM)

WASSERLÖSLICHE VITAMINE


Abbildung: Einige theoretische Speicherzeiten für Vitamine im Körper (Zeit bis Erschöpfung der Reserven bei fehlender Zufuhr)
Vitamin
B1 ist das am raschesten aufgebrauchte wasserlösliche Vitamin (~10 Tage Reserve), der
Vorrat an Vit. B12 (Leber) sollte für mehrere Jahre halten

Wasserlösliche Vitamine (B-Komplex, C, Folsäure, Biotin, Pantothensäure) haben einige weitgehend gemeinsame Eigenschaften:
 In pflanzlicher Kost enthalten (Ausnahme: B12)
In pflanzlicher Kost enthalten (Ausnahme: B12)
 Sie werden kaum gespeichert, Zufuhr in kurzen Intervallen nötig (Ausnahme: B12)
Sie werden kaum gespeichert, Zufuhr in kurzen Intervallen nötig (Ausnahme: B12)
 Sie wirken als Enzym-Bestandteile (s. Tabelle)
Sie wirken als Enzym-Bestandteile (s. Tabelle)

Enzyme, für deren Aktivität Vitamine erforderlich sind
Nach Panini SR, Medical Biochemistry, 2nd ed. 2021 (Thieme) |
Vitamin
|
Cofaktor / Komponente, assoziierte Enzyme, Funktionen
|
B1 (Thiamin)
|
Thiamin ist ein Cofaktor für
Pyruvatdehydrogenase (Bildung von Coenzym A)
α-Ketoglutarat-Dehydrogenase (Bildung von Succinyl-CoA)
BCKDC (branched chain α-keto acid dehydrogenase complex) (Abbau von Valin, Leuzin, Isoleuzin)
Transketolase (Transfer von 2C-Fragmenten im Pentosephosphatweg)
|
Pantothensäure
(B5)
|
Pantothensäure ist eine Komponente von
Coenzym A (Aktivierung von Molekülen, Transfer von Fettsäuregruppen)
Fettsäuresynthase (Bildung von Fettsäuren)
|
B6 (Pyridoxin)
|
Pyridoxalphosphat ist ein Cofaktor für
Transaminasen (Aminogruppentransfer zwischen Amino- und Ketosäuren)
Decarboxylasen (essentiell für Synthese von Neurotransmittern)
Glycogenphosphorylase (Glycogenolyse)
δ-Aminolävulinatsynthase (geschwindigkeitsbestimmender Schritt der Häm- / Porphyrinsynthese)
|
B12 (Cobalamin)
|
Cobalamine sind Cofaktoren für
Methylmalonyl-CoA-Synthase (Abbau ungeradzahliger Fettsäuren)
Methioninsynthase (Übertragung einer Methylgruppe auf Tetrahydrofolat)
|
Biotin
|
Biotin ist ein Cofaktor für
Pyruvatcarboxylase (irreversible Bildung von Oxalacetat aus Pyruvat)
Acetyl-CoA-Carboxylase (irreversible Bildung von Malonyl-CoA aus Acetyl-CoA)
|
Folsäure
|
Derivate der Tetrahydrofolsäure (THF) sind 1C-Donatoren. Homocystein wird zu Methionin
|
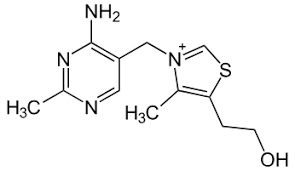
 Thiamin
Thiamin
Vitamin B1
(Thiamin, Aneurin, Beri-Beri-Schutzstoff) kann pflanzlichen oder
bakteriellen Ursprungs sein und kommt frei, an Protein gebunden oder
als Phosphatester vor. Der Darm resorbiert das Vitamin rasch und
phosphoryliert es teilweise zu Thiaminpyrophosphat (TPP), die
wichtigste Coenzymform. Das restliche Thiamin gelangt zur Leber und
wird dort kurzzeitig gespeichert.

Gute Vitamin-B1-Quellen: Samen, Nüsse, Weizenkeime, Hülsenfrüchte
Vitamin B1
(Thiamin  ) ist vor allem im Kohlenhydratstoffwechsel (oxidative Decarboxylierung von α-Ketosäuren) wichtig (
) ist vor allem im Kohlenhydratstoffwechsel (oxidative Decarboxylierung von α-Ketosäuren) wichtig ( s. Tabelle).
s. Tabelle).
Der Körper enthält etwa 20-30 mg Thiamin, bei einer durchschnittlichen täglichen Aufnahme von 1,2 mg
ein
kurzfristiger Speicher (dieses Vitamin geht bei mangelnder Zufuhr am
schnellsten verloren, seine biologische Halbwertszeit beträgt knapp 2
Wochen - der niedrigste Wert aller Vitamine).
Thiamin wird im Jejunum durch aktiven Transport aufgenommen,
mittels Thiaminkinase und ATP zu Thiaminpyrosphosphat (TPP) aktiviert
(in Darm und Leber) und dem Organismus in dieser Form zur Verfügung
gestellt. TPP ist Coenzym bei Reaktionen, die Zielmoleküle oxidieren
und gleichzeitig decarboxylieren (dabei entsteht CO2). TPP-abhängige Enzyme sind die Pyruvat-Dehydrogenase, α-Ketoglutarat-Dehydrogenase und Transketolase (Pentosephosphatzyklus).
Neben Folsäure ist Thiamin dasjenige Vitamin, dessen Bedarfsdeckung in
hoch entwickelten Industrienationen häufig unzureichend ist.
Gute Thiaminquellen
sind Getreideprodukte und Schweinefleisch (bei entsprechend vitaminreicher Mast), Fisch, Innereien.

 Die aktive Form von Vit.B1 ist Thiamin-Pyrophosphat (TPP)
Die aktive Form von Vit.B1 ist Thiamin-Pyrophosphat (TPP)
 Es dient als Cofaktor für Enzyme, die CO2 von ß-Ketosäuren entfernen (oxidative Decarboxylierung)
Es dient als Cofaktor für Enzyme, die CO2 von ß-Ketosäuren entfernen (oxidative Decarboxylierung)
 Es überträgt C-Fragmente
Es überträgt C-Fragmente
Als Thiamin-Tagesbedarf
gilt für Männer 1,2, für Frauen 1,0 mg/d. Sein Wert hängt von
zahlreichen Faktoren ab - Gravidität und Laktation, schwere
Muskelarbeit, Fieber, Alkoholkonsum gehören zu Stressfaktoren, die den
Vitaminbedarf erhöhen bzw. einen Mangelzustand bewirken können.
Bezogen auf die Energiezufuhr sollten mindestens 0,33 mg pro 1000
Cal (4,2 MJ) aufgenommen werden. Bei einem Tagesumsatz von 2000 Cal ergibt sich
damit ein Bedarf von mindestens ~0,7 mg/d, bei 3000 Cal von ≥1 mg/d.
Diese Werte werden bei üblichen Ernährungsgewohnheiten oft nicht erreicht.
 EU-RDA für Vitamin B1: 1,1 mg Thiamin
EU-RDA für Vitamin B1: 1,1 mg Thiamin
Vitamin B1-reiche Nahrungsmittel
Nach Biesalski / Bischoff / Pirlich / Weimann: Ernährungsmedizin, 5. Aufl. 2018 (Thieme) |
|
Thiamin-
gehalt (mg/100g)
|
Thiamin-
gehalt (mg/100g)
|
|
Thiamin-
gehalt (mg/100g) |
Thiamin-
gehalt
(mg/100g)
|
Spargel
|
0,2
|
0,8
| Rindfleisch
|
0,6
|
0,5
|
Schweine-
fleisch
|
0,7-0,9
|
0,5
| Huhn
|
0,1
|
0,1
|
Spinat
|
0,2
|
0,4
| Getreide
|
0,5-2,0
|
0,1-0,5
|
Leber
|
0,3
|
0,2
| Vollkorn
|
0,3-1,5
|
0,1-0,3
|
Bohnen
|
0,6
|
0,2
| Vollkornbrot
|
0,3
|
0,1
|
Milch
(-produkte)
|
0,3-0,5
|
≤0,1
|
Walnüsse
|
0,5
|
0,1
|
Der Vitamin-B1-Tagesbedarf ist z.B. enthalten in 120 g Schweinefleisch (vitamingemästete
Tiere), 240 g Haferflocken oder Vollkornmehl, 360 g Ente, Leber oder
Niere, 600 g Kalbfleisch, Lachs, Zander, Gemüse oder Hülsenfrüchte,
1200 g Rindfleisch oder Kartoffeln.
Etwa 30 mg Thiamin sind (bei physiologischem Status) im
Körper einer erwachsenen Person gespeichert: ~40% in der Muskulatur,
der Rest zum Großteil in den Eingeweiden. 75% des im Blut vorhandenen
VitB1 befindet sich in den Erythrozyten (das ist nur ca. 1% des Gesamtkörperthiamins).
Der Thiaminstatus lässt sich am besten über die Aktivität der Erythrozyten-Transketolase abschätzen (ETKA-Test),
weil die roten Blutkörperchen von einem Thiaminmangel als erste
betroffen sind. (Das Testergebnis ist von mehreren Begleitfaktoren
beeinflusst, wie diverse Pharmaka, Eisenmangel, Alkoholkonsum).
Kriterium ist das Verhältnis von stimulierter zu basaler ETKA, es
sollte nicht über 1,2 betragen.
Thiaminmangel kommt durch
einseitige und
unausgewogene Ernährung zustande und besteht häufig bei Alkoholkranken
(Folge: Polyneuropathien, Wernicke-Enzepalopathie).
Dabei sind vor allem glukoseabhängige Organe betroffen (Gehirn,
peripheres Nervensystem; Erythrozyten, weil sie vom Pentosephosphatweg
abhängig sind).
Die
klassische Mangelerkrankung Beriberi ("große Schwäche") - mit neurologischen und psychischen Störungen - tritt bei ausschließlicher Ernährung mit poliertem
(maschinell geschältem) Reis oder weißem Mehl auf.
 Transketolaseaktivität
Vollblut: 9-12 µmol/h/ml
Transketolaseaktivität
Vollblut: 9-12 µmol/h/ml
Erythrozyten: 0,75-1,3 U/g Hämoglobin
Vitamin B2 (Riboflavin)
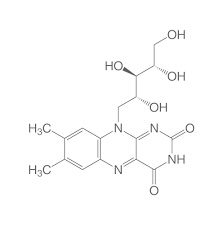
 Riboflavin
Riboflavin
Biologisch
weit verbreitet ist auch dieses Vitamin, das als Coenzym zahlreicher
elektronenübertragender Enzyme in der Form von
Flavin-Adenin-Dinukleotid (FAD) und Flavin-Mononukleotid (FMN) von
Pflanzen und Mikroorganismen gebildet wird und meist an Protein
gebunden vorliegt. Aus dieser Bindung wird es zunächst im Magen gelöst
(niedriger pH), durch Phosphatasen in Riboflavin umgewandelt, im
Dünndarm mittels Na+-abhängigem Transport resorbiert und
dabei phosphoryliert. Ein Teil des Vitamins rezirkuliert im
enterohepatischen Kreislauf; gelangt es in die Peripherie, wird es von
Zellen (wor allem in Leber, Niere, Herz, Dünndarm) aufgenommen und zu
FAD / FMN umgewandelt. Hier erleichtert es Redoxvorgänge (oxidative
Phosphorylierung, Synthese von Fettsäuren u.a.) und ist Bestandteil
mehrerer Enzyme. Ausgeschieden wird das Vitamin über die Niere.

Gute Vitamin-B2-Quellen: Milch, Innereien, Eier, Nüsse, Samen, Fisch, Pilze
Vitamin B2 (Riboflavin) - Coenzym der Flavoproteine, die als Oxidoreduktasen fungieren -
ist besonders für den Energie- und Eiweißstoffwechsel bedeutsam. Erniedrigte Aktivität der erythrozytären Glutathionreduktase ist ein primäres Zeichen eines Riboflavinmangels (Erythrozyten-Enzymtest!). In der Niere wird Riboflavin tubulär sezerniert.
Die Quelle für die Aufnahme im Darm sind vor allem Flavoproteine,
sie
werden zu Riboflavin gespalten und dieses (vor allem aktiv) resorbiert
- und in den Mucosazellen entsteht daraus Flavin-Adenin-Dinukleotid
(FAD) und Flavinmononukleotid (FMN). Im Blut wird das (wiederum
abgespaltene) Riboflavin an Albumin gebunden transportiert, da es sonst
schlecht löslich ist. FAD-abhängig sind mehrere Enzyme, z.B. im Citratzyklus die Succinat-Dehydrogenase.
Riboflavin hat zahlreiche Aufgaben, dementsprechend breit ist die
Symptomatik eines Mangelzustandes: Haut- und Schleimhautläsionen
(Rhagaden an den Mundwinkeln, Glossitis), Kornea-Vaskularisierung,
Katarakt, Glaskörpertrübungen.

 FMN (Flavin-Mononukleotid) und FAD (Flavin-Adenin-Dinukleotid) sind
Coenzyme von Oxidoreduktasen, sie übertragen Elektronen
FMN (Flavin-Mononukleotid) und FAD (Flavin-Adenin-Dinukleotid) sind
Coenzyme von Oxidoreduktasen, sie übertragen Elektronen
Der Tagesbedarf an Riboflavin
beträgt 0,6 mg/1000 Cal, oder mindestens 1,2 mg/d bei erwachsenen
Personen. Empfohlen sind für Männer 1,4 und für Frauen 1,1 mg Vit.B2
pro Tag. Der Vitaminbedarf steigt von 0,3 mg/d bei Säuglingen bis ca.
1,5 (Frauen) bzw. 1,7 mg/d (Männer), Stillende benötigen 2,3 mg/d. Das
Vitamin findet sich reichlich in Hefe, Leber, Milch, Milchprodukten.
 EU-RDA für Vitamin B2: 1,4 mg Riboflavin
EU-RDA für Vitamin B2: 1,4 mg Riboflavin
Vitamin B2-reiche Nahrungsmittel
Nach Biesalski / Bischoff / Pirlich / Weimann: Ernährungsmedizin, 5. Aufl. 2018 (Thieme)
|
|
Riboflavin-
gehalt (mg/100g)
|
|
Riboflaving-
ehalt (mg/100g)
|
Hefe
|
5,4
| Huhn
|
0,2
|
Leber
|
3,5
| Spinat, Avocado
|
0,15
|
Käse
|
0,2-0,5
| Obst
|
<0,1
|
Eier, Schweinefleisch
|
0,3
| Getreide
|
0,2
|
Fisch
|
0,2-0,3
| Brot
|
<0,1
|
Spargel, Broccoli
|
0,2
| Walnüsse
|
0,1
|
Milch(-produkte)
|
0,15-0,2
|
Schokolade
|
0,4
|
Der Vitamin-B2-Tagesbedarf
(1,5 mg) ist z.B. enthalten in 50 g Leber oder Niere, 150 g Herz oder
Keimen, 200 g Camembert oder Roquefort-Käse, 300 g Schnittkäse, 700 g
Fleisch, 750 g Fisch oder Vollmilch.
 Riboflavin
Riboflavin
Serum / Plasma: 40-240 µg/l
Urin: >200 µg/d (>80 µg/g Kreatinin) (nahrungsbedingte Einflüsse)
Klassische Ariboflavinose ist gekennzeichnet durch Cheilose
(Mundwinkelragaden), Stomatitis (Mundfäule) und Dermatitis ("Ekzeme").
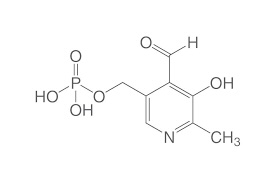
 Pyridoxalphosphat (PLP, PALP, P5P)
Pyridoxalphosphat (PLP, PALP, P5P)
Pyridoxin, Pyridoxal und Pyridoxamin - diese drei Derivate des Pyridins werden unter dem Begriff Vitamin B6
zusammengefasst und liegen vorwiegend als Phosphate vor - sind Produkte
zahlreicher Pflanzen und Mikroorganismen. Alkalische Phosphatasen im
Darm spalten das Phosphat ab, das Vitamin wird resorbiert und dann
wieder ATP-abhängig phosphoryliert. Pyridoxalphosphat ist die bedeutendste Form des Vit. B6, mit dem Harn wird das Vitamin vor allem als 4-Pyridoxalsäure ausgeschieden. Vit. B6
ist ein Cofaktor für zahlreiche Enzyme (Transaminierungen,
Decarboxylierungen, Aminosäuremetabolismus, Lipidstoffwechsel,
Serotoninsynthese u.a.). Unter anderem ist es für die Synthese von GABA sehr wichtig (Verlust der inhibitorischen Wirkung dieses Neurotransmitters kann schwere Krämpfe zur Folge haben).

Gute Vitamin-B6-Quellen: Hefe, Leber, Weizenkeime, Hafer, Nüsse, Bohnen, Avocados, Bananen
Vitamin B6
ist ein Sammelbegriff (alkoholische
Form: Pyridoxin; Aldehyd: Pyridoxal; Amin: Pyridoxamin; biologisch
aktiv ist der in der Leber entstehende Phosphorsäureester
Pyridoxalphosphat) und ist das bedeutendste Coenzym des
Proteinstoffwechsels. Vitamin-B6-abhängig sind (unter vielen) z.B.
 die Alanin-Aminotransferase (ALT - früher: GPT) und die Aspartat-Aminotransferase (AST - früher: GOP), beide sind im Aminosäurestoffwechsel tätig (Transaminierungen, d.h. Umbau von Amino- zu Ketosäure)
die Alanin-Aminotransferase (ALT - früher: GPT) und die Aspartat-Aminotransferase (AST - früher: GOP), beide sind im Aminosäurestoffwechsel tätig (Transaminierungen, d.h. Umbau von Amino- zu Ketosäure)
 die für die Hämoglobinsynthese benötigte δ-Aminolävulinsäure-Synthetase
die für die Hämoglobinsynthese benötigte δ-Aminolävulinsäure-Synthetase
 die Glykogen-Phosphorylase, welche Glykogen abbaut
die Glykogen-Phosphorylase, welche Glykogen abbaut
 die Glutamat-Decarboxylase für die Synthese von GABA und die Tyrosin-Decarboxylase für die Bildung von Tyramin (Abbauprodukt des Tyrosins, wird mit dem Stuhl ausgeschieden)
die Glutamat-Decarboxylase für die Synthese von GABA und die Tyrosin-Decarboxylase für die Bildung von Tyramin (Abbauprodukt des Tyrosins, wird mit dem Stuhl ausgeschieden)
Die
Resorption erfolgt passiv von Duodenum bis Ileum. Die meist
unphosphorylierten B6-Vitamine werden von der Leber phosphoryliert;
eine Oxidase erzeugt schließlich Pyridoxalphosphat (PALP). Das Vitamin kommt so gut wie überall vor; wichtige
Quellen sind Fleisch, Innereien und
einige Getreide- und Gemüsearten.
 Der
Bedarf an Vit. B6 beträgt für Männer 1,5 und für Frauen 1,2 mg pro Tag. Er steigt mit dem Proteinumsatz und ist von Gesundheitszustand und
Ernährungsweise abhängig.
Der
Bedarf an Vit. B6 beträgt für Männer 1,5 und für Frauen 1,2 mg pro Tag. Er steigt mit dem Proteinumsatz und ist von Gesundheitszustand und
Ernährungsweise abhängig.
 EU-RDA für Vitamin B6: 1,4 mg Pyrodoxin / Pyridoxal / Pyridoxamin
EU-RDA für Vitamin B6: 1,4 mg Pyrodoxin / Pyridoxal / Pyridoxamin
Vitamin B6-reiche Nahrungsmittel
Nach Biesalski / Bischoff / Pirlich / Weimann: Ernährungsmedizin, 5. Aufl. 2018
|
|
Vitamin-B6-Gehalt (mg/100g)
|
Leber
|
0,9
|
Walnüsse
|
0,8
|
Fisch
|
0,3 - 0,8
|
Huhn
|
0,3 - 0,6
|
Schweinefleisch
|
0,3 - 0,5
|
Bohnen
|
0,1 - 0,6
|
| Reis |
0,1 - 0,5 |
Avocado, Erdnüsse
|
0,4
|
Spinat, Kartoffeln, Zerealien
|
0,3
|
Der Vitamin-B6-Tagesbedarf
ist in etwa enthalten in 60 g Keimen, 175 g Sojabohnen, 200 g
Rinderleber oder Hafervollkorn, 300 g Linsen, 400 g Rindfleisch,
Schweinefleisch oder Fisch, 450 g Vollkornmehl, 500 g Lammfleisch, 1000
g Gemüse
 Vit. B6 (PALP)
Vit. B6 (PALP)
Plasma: 5-30 µg/l (20-121 mM) - Mangel unter 2,5 g/l - Mangel unter 2,5 µg/l
Ausscheidung mit dem Harn: 500-800 µg/24 h (200-300 µg/g Kreatinin)

Aktivitätskoeffizient ASAT (Aspartat-Aminotransferase) in Erys: bis 1,5
Aktivitätskoeffizient ALAT (Alanin-Aminotransferase) in Erys: bis 1,2
Folsäure  (Vitamin B9)
(Vitamin B9)
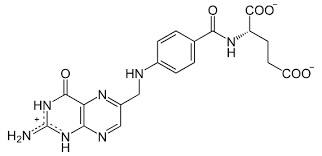
 Tetrahydrofolsäure
Tetrahydrofolsäure
Folsäure (Pteroylpolyglutamat) wird von vielen Mikroorganismen (z.B. der Darmflora), höheren Pflanzen und auch Tierarten synthetisiert.
Der Name leitet sich davon ab, dass sie in grünen Blättern (folia) zu finden ist.
Dieses Derivat des Pteridins (bestehend aus einem Pyrazin- und einem
Pyrimidinring) liegt in der Natur mit Glutamatmolekülen konjugiert vor.
Die Darmmucosa formt das Vitaminmolekül im Rahmen der Resorption zu
Methyltetrahydrofolsäure um, die in den Kreislauf abgegeben wird.
Daraus entsteht unter Mitwirkung von Vit. B12 Tetrahydrofolsäure ( Abbildung);
dieses Coenzym ist die biologisch aktive Form des Vitamins und
beteiligt sich an zahlreichen metabolischen Reaktionen, insbesondere im Nukleinsäure-Stoffwechsel (DNA-Synthese).
Abbildung);
dieses Coenzym ist die biologisch aktive Form des Vitamins und
beteiligt sich an zahlreichen metabolischen Reaktionen, insbesondere im Nukleinsäure-Stoffwechsel (DNA-Synthese).

Gute Folsäure-Quellen: Hefe, Leber, Spinat
Die Leber eines Erwachsenen ist in der Lage, 12-15 mg
Folsäure zu speichern; dieser Vorrat reicht für ≥3 Monate. Im Extrazellulärraum liegt Folsäure an Plasmaprotein gebunden vor.
Folsäure liegt in unterschiedlichen Oxidationszuständen vor. Biologisch
aktiv ist die (enzymatisch) vollständig reduzierte 5,6,7,8-Tetrahydrofolsäure
(THF),
diese entsteht vor allem in den Mitochondrien. THF ist für die
DNA-Synthese unabdingbar (Co-Faktor für die Bildung von Purinen und
Pyrimidinen) und auch für Reaktionen im Rahmen des
Aminosäuremetabolismus wesentlich.
Die häufig im
Körper vorzufindende methylierte Form (Methyl-THF) muss zu THF
ungewandelt werden, was durch (das durch Demethylierung aus Methionin entstehende) Homozystein erfolgt (zytoplasmatische "Regenerierung", Vitamin B12 ist dabei ein Kofaktor und B12-Mangel kann zu THF-Mangel führen).
 THF kann dann C1-Einheiten auf ihre Zielmoleküle übertragen. Folsäure erleichtert den Transfer von Methyl-, Formyl- und Hydroxymethylgruppen von einem Molekül auf ein anderes. Rasch wachsende Gewebe benötigen THF wegen ihrer Rolle für die DNA-Synthese ganz besonders.
THF kann dann C1-Einheiten auf ihre Zielmoleküle übertragen. Folsäure erleichtert den Transfer von Methyl-, Formyl- und Hydroxymethylgruppen von einem Molekül auf ein anderes. Rasch wachsende Gewebe benötigen THF wegen ihrer Rolle für die DNA-Synthese ganz besonders.
 Der tägliche Bedarf an Folsäure (Folsäureäquivalente: FÄ) beträgt beim Erwachsenen 300-400 µg
(bei Schwangeren bis 600 µg). Die
enterische Resorptionskapazität ist weit höher (bis zu 15 mg/d), mit vollwertiger Nahrung werden leicht 2 mg/d aufgenommen. Der
küchentechnische Verlust durch Erhitzen, Sauerstoffeinfluss und
Verwerfen des Kochwassers beträgt bis zu 90%. Reich an Folsäure sind u.a. frisches grünes Gemüse, Weizenkeime, Sojabohnen, Hefe, Eidotter, einige Früchte -
und Leber.
Der tägliche Bedarf an Folsäure (Folsäureäquivalente: FÄ) beträgt beim Erwachsenen 300-400 µg
(bei Schwangeren bis 600 µg). Die
enterische Resorptionskapazität ist weit höher (bis zu 15 mg/d), mit vollwertiger Nahrung werden leicht 2 mg/d aufgenommen. Der
küchentechnische Verlust durch Erhitzen, Sauerstoffeinfluss und
Verwerfen des Kochwassers beträgt bis zu 90%. Reich an Folsäure sind u.a. frisches grünes Gemüse, Weizenkeime, Sojabohnen, Hefe, Eidotter, einige Früchte -
und Leber.
 EU-RDA für Vitamin B9: 200 µg Folsäure
EU-RDA für Vitamin B9: 200 µg Folsäure
Folsäurereiche Nahrungsmittel
Nach Biesalski / Bischoff / Pirlich / Weimann: Ernährungsmedizin, 5. Aufl. 2018
|
|
Folsäuregehalt
(µg FÄ/100g)
|
Weizenkeime
|
271
|
| Weizenkleie |
159 |
Spinat
|
134
|
| Eidotter |
127 |
Endivie
|
116
|
Leber (Rind, Schwein)
|
108
|
Kohlsprossen (Brokkoli)
|
103
|
Nüsse, Mehl
|
40-55
|
 Folsäure (Serum)
1,5-17 µg/l (anzustreben >2,5 µg/l)
Folsäure (Serum)
1,5-17 µg/l (anzustreben >2,5 µg/l)
Unterversorgung
macht sich vor allem in der DNA-Synthese bemerkbar (so werden weniger
Erythrozyten hergestellt - megaloblastäre Anämie, fetale
Neuralrohrdefekte in der Schwangerschaft) und kommt vor infolge
 ungenügender Zufuhr (Fehlernährung,
Zubereitungsverluste, Alkoholiker)
ungenügender Zufuhr (Fehlernährung,
Zubereitungsverluste, Alkoholiker)
 erhöhtem Bedarf (pubertärer
Wachstumsschub, Schwangerschaft, Laktation, Infekte)
erhöhtem Bedarf (pubertärer
Wachstumsschub, Schwangerschaft, Laktation, Infekte)
 Interferenz mit Pharmaka (z.B. oralen Kontrazeptiva).
Interferenz mit Pharmaka (z.B. oralen Kontrazeptiva).
 Cobalamin
Cobalamin
Cobalamine - Vertreter der sogenannten Vitamin-B12-Gruppe - sind modifizierte Porphyrine. Sie repräsentieren die am komplexesten aufgebauten Vitamine und werden in der Natur von Mikroorganismen synthetisiert. Der führende Vertreter dieser Molekülgruppe ist das Adenosylcobolamin (Coenzym B12). Das Molekül hat Cobalt als Zentralatom, das reaktive Zentrum kann eine Hydroxylgruppe (-OH), Methylgruppe (-CH3) oder Cyanogruppe (-CN) enthalten. Vitamin-B12-Coenzyme
wirken als Isomerasen und Methyltransferasen, sind an der
Proteinsynthese und DNA-Synthese beteiligt und für das Wachstum rasch
proliferierender Zellen unentbehrlich (Epithelien, Knochenmark).
Über Resorption und Transport s. unten und  dort
dort
 Gute Vitamin-B12-Quellen: Leber, Nieren, Eier, Milch, Käse, Fleisch
Gute Vitamin-B12-Quellen: Leber, Nieren, Eier, Milch, Käse, Fleisch
Durchschnittliche mitteleuropäische Kost enthält 5-25 µg Bit. B12 pro Tag. Der tägliche Bedarfswert liegt bei 2-3 µg; die Resorption erfordert mehrere Hilfsfaktoren:
 Im Speichel vorhandenes Haptocorrin (ein Transcobalamin: TC I) schützt mit der Nahrung aufgenommenes Vitamin B12
vor dem sauren Magensaft (das Vitamin ist säureempfindlich).
Im Speichel vorhandenes Haptocorrin (ein Transcobalamin: TC I) schützt mit der Nahrung aufgenommenes Vitamin B12
vor dem sauren Magensaft (das Vitamin ist säureempfindlich).
 Im
Duodenum entkoppelt es von Haptocorrin und bindet stattdessen an das gastrische Glykoprotein Intrinsic Factor (IF), der IF-B12-Komplex ist resistent gegenüber Proteasen im Dünndarm.
Im
Duodenum entkoppelt es von Haptocorrin und bindet stattdessen an das gastrische Glykoprotein Intrinsic Factor (IF), der IF-B12-Komplex ist resistent gegenüber Proteasen im Dünndarm.
 Im unteren Ileum (wo auch Folat zur Aufnahme gelangt) wird dieser Komplex über eigene Rezeptorkomplexe aufgenommen und das Vitamin mittels rezeptorvermittelter Endozytose resorbiert (Cubilin in der Darmschleimhaut bindet an den Intrinsic factor-Cobalamin-Komplex und ermöglicht so seine Aufnahme).
Im unteren Ileum (wo auch Folat zur Aufnahme gelangt) wird dieser Komplex über eigene Rezeptorkomplexe aufgenommen und das Vitamin mittels rezeptorvermittelter Endozytose resorbiert (Cubilin in der Darmschleimhaut bindet an den Intrinsic factor-Cobalamin-Komplex und ermöglicht so seine Aufnahme).
 Der Intrinsic Factor wird lysosomal abgebaut und Vit.B12 an Transcobalamin II (TC II) gebunden; in dieser Form zirkuliert es im Blut.
Der Intrinsic Factor wird lysosomal abgebaut und Vit.B12 an Transcobalamin II (TC II) gebunden; in dieser Form zirkuliert es im Blut.
In der Leber findet sich ein hepatischer Vitaminspeicher von 3-4 (bis zu 10) mg (Tagesbedarf 3 µg).
Dementsprechend macht sich eine chronische Unterversorgung mit
Cobalamin (z.B. nach totaler Gastrektomie) oft erst nach mehreren
Jahren bemerkbar (vorausgesetzt, die hepatischen Vitaminspeicher waren
nicht schon vorher entleert).
3 bis 8 µg/d gelangen mit der Galle in den Darm, davon rezirkuliert knapp die Hälfte über den enterohepatischen Kreislauf.
Vitamin B12 wird von Mikroorganismen (auch im Dickdarm) gebildet. Vitamin B12-Mangel beruht meist auf einer Störung im komplexen Mechanismus der B12-Aufnahme in den Körper (z.B. wegen der Anwesenheit von Antikörpern gegen intrinsic factor), nur selten auf mangelndem diätetischen Angebot.
Sowohl Vitamin B12 als auch Folsäure werden zur Purin- und Pyrimidinsynthese (hauptsächlich Thymidylat) und damit zum Aufbau von DNA benötigt. Intrazellulär liegt Vitamin B12 in Form zweier aktiver Coenzyme vor: Methylcobalamin (unterstützt Methioninsynthetase, wichtig für die DNA-Synthese) und Desoxyadenoslycobalamin (ein Cofaktor der mitochondrialen Mutase, wichtig für den Kohlenhydrat- und Lipidstoffwechsel).
In der Niere filtriertes Vitamin wird über den tubulären Megalinrezeptor (der Transcobalamin II bindet) zurückgewonnen.
Vitamin B12 beteiligt sich als Coenzym an zwei wichtigen Reaktionen:
 Bildung von Succinyl-CoA in den Mitochondrien
(Methylmalonyl-CoA-Mutase) - Abbau von ungeradzahligen Fettsäuren und
einigen Aminosäuren im Citratzyklus
Bildung von Succinyl-CoA in den Mitochondrien
(Methylmalonyl-CoA-Mutase) - Abbau von ungeradzahligen Fettsäuren und
einigen Aminosäuren im Citratzyklus
 Zytoplasmatischer Folsäure-, Methionin- und Homocysteinstoffwechsel
(Homocystein-Methyltransferase bzw. Methionin-Synthase) - Methylierung und Proteinsynthese.
Zytoplasmatischer Folsäure-, Methionin- und Homocysteinstoffwechsel
(Homocystein-Methyltransferase bzw. Methionin-Synthase) - Methylierung und Proteinsynthese.
 Der Tagesbedarf beträgt 2-3 µg.
Die Ernährung liefert meist mehr als der
physiologische Bedarf erfordert; enterohepatische Wiederverwertung und
ein großer Körperspeicher erlauben es, Versorgungslücken für Monate bis Jahre zu überbrücken.
Der Tagesbedarf beträgt 2-3 µg.
Die Ernährung liefert meist mehr als der
physiologische Bedarf erfordert; enterohepatische Wiederverwertung und
ein großer Körperspeicher erlauben es, Versorgungslücken für Monate bis Jahre zu überbrücken.
 EU-RDA für Vitamin B12: 2,5 µg Cobalamin
EU-RDA für Vitamin B12: 2,5 µg Cobalamin
 Vit B12 stammt auch von Mikroorganismen im Darm, die mit verzehrtem Gemüse in den Körper gelangen. Die Produktion durch Darmbakterien ist
aber nicht ausreichend, strikt vegane Kost führt manchmal zu Mangelerscheinungen.
Vit B12 stammt auch von Mikroorganismen im Darm, die mit verzehrtem Gemüse in den Körper gelangen. Die Produktion durch Darmbakterien ist
aber nicht ausreichend, strikt vegane Kost führt manchmal zu Mangelerscheinungen.
Vitamin B12-reiche Nahrungsmittel
|
|
Vitamin-B12-Gehalt
(µg/100g)
|
Rinderleber
|
70
|
Rindernieren
|
31
|
Hefe
|
20
|
Leberwurst
|
16
|
Kalbsherz
|
11
|
Eier
|
2,5
|
Käse
|
1,6 - 2,5
|
Milch
|
1,5
|
Der Vitamin-B12-Tagesbedarf
(mit 3 µg angenommen) ist z.B. enthalten in 4 g Rinderleber, 30 g Makrele, 90 g
geräuchertem Lachs, 100 g Kabeljaufilet, 120 g Hühnerei, 130 g
gekochtem Lachs, 150 g Hartkäse (vollfett), 170 g frischem Rindfleisch, ~220 g Scholle oder Kabeljau.
 Vitamin B12 (Serum)
160-1000 ng/l (~110-740 pM)
Halbwertszeit im Plasma ~5 Tage, in der Leber >1 Jahr
Vitamin B12 (Serum)
160-1000 ng/l (~110-740 pM)
Halbwertszeit im Plasma ~5 Tage, in der Leber >1 Jahr
Vitamin B12-Mangel
Mangel tritt meist infolge von Resorptionsstörungen auf:
 Mangel an intrinsic factor: Atrophische Gastritis, Magenoperationen
Mangel an intrinsic factor: Atrophische Gastritis, Magenoperationen
 Erschwerte Resorption: Erkrankungen des Ileums, z.B. Mb. Crohn
Erschwerte Resorption: Erkrankungen des Ileums, z.B. Mb. Crohn
Selten kann chronische
Mangelversorgung (strikte Veganer) die Ursache sein. Auch Vitaminverbrauch durch Parasiten (Fischbandwurm) kommt infrage.
Die Symptome treten mit großer Verzögerung auf und sind gekennzeichnet
durch hämatologische (megaloblastäre, "perniziöse" Anämie) und
neurologische Veränderungen (funikuläre Myelose). Vitamin B12-Mangel kann bleibende Schäden am Zentralnervensystem verursachen. Ältere Menschen haben
oft niedrige Vitamin-B12-Blutwerte, und B12-Mangel kann zu Demenz oder psychiatrischen Problemen führen, ohne dass eine Anämie vorhanden sein muss.
Vitamin C (Ascorbinsäure)

Gute Vitamin-C-Quellen: Zitrusgewächse, Hagebutten, Kiwi, Preiselbeeren, Tomaten, Kohl, Paprika, Früchte, Gemüse
Etwa 80% des in der Nahrung vorhandenen Vitamin
C werden vom Körper aufgenommen; dieser Anteil sinkt mit
steigender Dosis, z.B. auf 50% bei 1,5 g/d und auf nur 16% bei 12 g/d. Im
Blut liegt es zu ~75% frei gelöst, zu ~25% an Plasmaprotein gebunden vor.
 Vit.C
wirkt als Redoxsystem im allgemeinen antioxidativ, wirkt also reduzierend, hält z.B. Eisen im zweiwertigen Zustand
Vit.C
wirkt als Redoxsystem im allgemeinen antioxidativ, wirkt also reduzierend, hält z.B. Eisen im zweiwertigen Zustand
 Vit.C
ist Cofaktor zahlreicher Enzyme, die für posttranslationale Modifikation und Hydroxylierung von
Prokollagen bei der Kollagensynthese benötigt werden (Prolin durch Prolylhydroxylase, Lysin durch Lysylhydroxylasen)
Vit.C
ist Cofaktor zahlreicher Enzyme, die für posttranslationale Modifikation und Hydroxylierung von
Prokollagen bei der Kollagensynthese benötigt werden (Prolin durch Prolylhydroxylase, Lysin durch Lysylhydroxylasen)
 Vit.C regeneriert verbrauchtes Vit.E und arbeitet mit Glutathion
bei Oxidationsreaktionen zusammen, es schützt vor Schäden durch freie Radikale
Vit.C regeneriert verbrauchtes Vit.E und arbeitet mit Glutathion
bei Oxidationsreaktionen zusammen, es schützt vor Schäden durch freie Radikale
 Vit.C wird für die Noradrenalinsynthese (als Cofaktor für die Dopaminhydroxylase und Elektronendonator), die Eisenresorption im Darm (Reduktion von dreiwertigem Eisen zu Fe2+, Verbesserung der Resorption phytathaltiger Nahrungsstoffe), als Cofaktor der 7α-Hydroxylase in der Leber (Synthese von Gallensäuren) und für die
Infekabwehr (Schutz der Phagozytenmembran) benötigt.
Vit.C wird für die Noradrenalinsynthese (als Cofaktor für die Dopaminhydroxylase und Elektronendonator), die Eisenresorption im Darm (Reduktion von dreiwertigem Eisen zu Fe2+, Verbesserung der Resorption phytathaltiger Nahrungsstoffe), als Cofaktor der 7α-Hydroxylase in der Leber (Synthese von Gallensäuren) und für die
Infekabwehr (Schutz der Phagozytenmembran) benötigt.
Die Ausscheidung über die Nieren erfolgt z.T. direkt, z.T. über Oxalat
(35-50% der täglich 30-40 mg ausgeschiedenen Oxalats stammen aus dem
Abbau von Ascorbinsäure).
 Der
tägliche Vit-C-Bedarf beträgt für Männer 110 und für Frauen 95 mg
(Raucher ~150 mg/d). Hypervitaminose ist nicht bekannt, das Vitamin wird über
die Nieren und (bei Dosen ab ~3 g/d, also dem 40-fachen des Bedarfs)
auch über den Darm ausgeschieden. Vitamin C in höherer Dosierung wirkt
allerdings prooxidativ, z.B. auch in Kombination mit Eisen, dessen
Resorption durch Vit. C begünstigt wird.
Der
tägliche Vit-C-Bedarf beträgt für Männer 110 und für Frauen 95 mg
(Raucher ~150 mg/d). Hypervitaminose ist nicht bekannt, das Vitamin wird über
die Nieren und (bei Dosen ab ~3 g/d, also dem 40-fachen des Bedarfs)
auch über den Darm ausgeschieden. Vitamin C in höherer Dosierung wirkt
allerdings prooxidativ, z.B. auch in Kombination mit Eisen, dessen
Resorption durch Vit. C begünstigt wird.
 EU-RDA für Vitamin C: 80 mg Ascorbinsäure
EU-RDA für Vitamin C: 80 mg Ascorbinsäure
Vitamin C-reiche Nahrungsmittel
Nach Biesalski / Bischoff / Pirlich / Weimann: Ernährungsmedizin, 5. Aufl. 2018
|
|
Vit.-C-Gehalt
(mg/100g)
|
Acerola (Ahornkische) (roh)
|
1500
|
Hagebutten (roh)
|
1250
|
Sanddornsaft
|
266
|
| schwarze Johannisbeeren |
189
|
Paprika (roh)
|
140
|
Der Vitamin-C-Tagesbedarf
(75 mg) ist z.B. enthalten in 50 g Paprika, 60 g Kohlsprossen
(Brokkoli, Rosenkohl), 80 g Grünkohl oder Fenchel, 120 g Zitrusfrüchten,
150 g Spinat, 200 g Lauch oder Chinakohl, 500 g Kartoffeln, 600 g
Äpfeln, Pfirsichen, Kirschen oder Marillen (Aprikosen)
 Vitamin C (Ascorbinsäure + Dehydroascorbinsäure)
Vitamin C (Ascorbinsäure + Dehydroascorbinsäure)
Blutplasma: 4-15 mg/l (23-85 µM) - Mangel unter 2 mg/l
Leukozyten: 1,1-3,0 fM / Leukozyt (20-53 µg/10
8 Leukozyten) - Mangel unter 0,57 fM/Leuko
Ausscheidung mir dem Harn: 8-27 mg/24 h
 Leichter Vit. C-Mangel (chronisch
einseitige Ernährung) bewirkt Müdigkeit, Schwäche und
Infektanfälligkeit;
Leichter Vit. C-Mangel (chronisch
einseitige Ernährung) bewirkt Müdigkeit, Schwäche und
Infektanfälligkeit;
 schwerer, lang anhaltender Mangel (2-4 Monate) Skorbut
(scurvy) (Kollagensynthese!) - gekennzeichnet durch Zahnfleischbluten, mangelhafte
Wundheilung, Probleme an Haut, Knochen, Bewegungsapparat, neurologische
Symptome.
schwerer, lang anhaltender Mangel (2-4 Monate) Skorbut
(scurvy) (Kollagensynthese!) - gekennzeichnet durch Zahnfleischbluten, mangelhafte
Wundheilung, Probleme an Haut, Knochen, Bewegungsapparat, neurologische
Symptome.
Biotin (Vitamin H, Vitamin B7)
 Biotin
Biotin
Das aus zahlreichen mikrobiellen und pflanzlichen Quellen stammende bizyklische Biotin liegt
in der Nahrung hauptsächlich
proteingebunden vor. Im Darm spaltet das Verdauungsenzym Biotinidase
(im Sekret des Pankreas und des Dünndarms vorhanden) freies Biotin ab,
das vor allem im Jejunum resorbiert und vor allem von Leber, Muskeln
und Nieren aufgenommen wird. Hier beteiligt es sich an zahlreichen
metabolischen Vorgängen, u.a. der Synthese von Aminosäuren, Fettsäuren
und Glucose. Ausgeschieden wird das Vitamin über die Nieren und mit dem
Stuhl.

Gute Biotin-Quellen: Hefe, Leber, Eigelb, Tomaten, Sojabohnen, Reis, Weizenkleie
Die Resorption des Vitamins kann durch Anwesenheit eines Eiklar-Proteins
(Avidin) behindert werden, vorausgesetzt, man nimmt große Mengen roher
Eier zu sich.
Biotin
wird enzymatisch an einige Carboxylasen angelagert und macht diese
funktionstüchtig (ohne angelagertes Biotin nennt man sie Apocarboxylasen). Biotin ist bedeutsam für Funktionen in Zellplasma (Enzymaktivitäten für
Protein-, Kohlenhydrat- und Fettstoffwechsel) und Zellkern
(Modifikation von Histonen).
 Der tägliche Bedarf liegt bei 30-60 µg/d. Darmbakterien können sich an der
Zufuhr beteiligen, ernährungsbedingte Mangelzustände sind selten. Das
Vitamin hat eine hohe therapeutische
Breite, man kennt keine Hypervitaminose.
Der tägliche Bedarf liegt bei 30-60 µg/d. Darmbakterien können sich an der
Zufuhr beteiligen, ernährungsbedingte Mangelzustände sind selten. Das
Vitamin hat eine hohe therapeutische
Breite, man kennt keine Hypervitaminose.
 EU-RDA für Vitamin B7: 50 µg Biotin
EU-RDA für Vitamin B7: 50 µg Biotin
Biotinreiche Nahrungsmittel
|
|
Biotingehalt
(µg/100g)
|
Leber
|
100
|
Sojabohnen
|
60
|
Walnüsse, Erdnüsse
|
35
|
Hühnerei (roh)
|
20
|
 Biotin (Serum, Vollblut)
200-500 ng/l (0,82-2,05 nM)
Biotin (Serum, Vollblut)
200-500 ng/l (0,82-2,05 nM)
Zu den Biotinmangel-Symptomen gehören Hautentzündungen, Haarausfall und neurologische Störungen.
Niacin (Nicotinsäure, Vitamin B3)
Niacin
wird von Mikroben, Pflanzen und vielen Säugetieren aus der Aminosäure
Tryptophan synthetisiert und kommt in so gut wie allen pflanzlichen und
tierischen Nahrungsmitteln vor. Beim Menschen ist dieser Mechanismus
unzureichend - daher ist Niacin ein Vitamin -, nur etwa 2% des mit der
Nahrung zugeführten Tryptophans wird in Niacin umgewandelt (60 mg Tryptophan können 1 mg
Nicotinamidäquivalente generieren). Die Leber bildet aus dem Vitamin die Coenzymformen NAD+ / NADP+ - diese wirken in zahlreichen Oxidoreductasen (Citratzyklus, oxidative Phosphorylierung, Fettsäuresynthese u.a.).

Gute Niacin-Quellen: Fleisch, Hefeprodukte, Nüsse, Hülsenfrüchte, Fisch, Gemüse
Für Redoxreaktionen ist dieses Vitamin - bestehend aus den beiden Stoffen Nicotinsäure und Nicotinamid - eines der wichtigsten Coenzyme u.a. für Oxidoreduktasen, Dehydrogenasen / Decarboxylasen, posttranslationale Modifizierung DNA-gebundener Proteine. NADH wirkt als Elektronenüberträger (vom Citratzyklus auf den Komplex I der Elektronentransportkette), NADPH wirkt als Reduktionsmittel bei der Lipidsynthese und schützt vor der Wirkung von Radikalen, indem es Glutathion im reduzierten Zustand erhält.
Auch als Pellagra preventing factor bekannt - Pellagra ist in Europa sehr selten -, beteiligt sich
Niacin am Protein-,
Kohlenhydrat- und Fettstoffwechsel sowie an der Energiebereitstellung
im Citratzyklus. Es hat antioxidative Wirkung und soll für die
Regenerationsfähigkeit mehrerer Gewebe bedeutsam sein.

 Aktives Vit. B3 tritt auf als NAD+ (Nikotinamid-Adenin-Dinukleotid) und NADP+ (-Phosphat)
Aktives Vit. B3 tritt auf als NAD+ (Nikotinamid-Adenin-Dinukleotid) und NADP+ (-Phosphat)
 Reduktion ergibt NADH und HADPH, beide dienen als Elektronenüberträger
Reduktion ergibt NADH und HADPH, beide dienen als Elektronenüberträger
Der tägliche
Niacinbedarf liegt für Männer bei 15 und für Frauen bei 12 mg Niacinäquivalent pro Tag,
ein Teil des Bedarfs kann aus dem
Tryptophanmetabolismus gedeckt werden. Wie bei Thiamin, ist auch der
Niacinbedarf an die Energiezufuhr geknüpft zu beurteilen. Dosierungen
über 500 mg/d Niacin können
Hypervitaminosesymptome bedingen.
 EU-RDA für Vitamin B3: 16 mg Niacin
EU-RDA für Vitamin B3: 16 mg Niacin
Niacinreiche Nahrungsmittel
|
|
Niacingehalt (mg/100g)
|
Niacinnährstoffdichte (mg/1000 Cal)
|
Rinderleber
|
15
|
107
|
Schweineleber
|
15
|
94
|
Kaninchenfleisch
|
8
|
56
|
Erbsen
|
1,7
|
49
|
Grünkohl
|
1,4
|
47
|
Kalbfleisch
|
6
|
38
|
Chicoree
|
0,5
|
38
|
| Lachs |
7 |
34 |
Hühnerfleisch
|
8
|
33
|
Kopfsalat
|
0,4
|
30
|
Der Niacin-Tagesbedarf
(15 mg) ist z.B. enthalten in 100 g Kalbsleber, 200 g Rindfleisch, 250
g Weizenvollkorn, 300 g Schweinefleisch oder Fisch, 750 g Erbsen, 950 g
Kohlrabi, 1250 g Kartoffeln.
Niacin kann durch Biosynthese aus der essentiellen Aminosäure Tryptophan gewonnen werden.
 Niacin
Ausscheidung von N1-Methyl-Nicotinamid mit dem Harn: 2,4-6,4 mg/24 h (1,6-4,3 mg/g Kreatinin)
Niacin
Ausscheidung von N1-Methyl-Nicotinamid mit dem Harn: 2,4-6,4 mg/24 h (1,6-4,3 mg/g Kreatinin)
Pellagra ist charakterisierrt durch Dermatitis (pelle agra = raue Haut), Diarrhoe, Demenz. Unbehandelt kann schwerer Niacinmangel zum Tod führen.

Gute Pantothensäure-Quellen: Hefe, Getreide, Hering, Pilze, Eigelb, Leber
ist ein Bestandteil des Coenzyms A (Citratzyklus, Aktivierung von Carboxylsäuren) und des Fettsäure-Synthase-Komplexes.
Sie ist für Stoffwechsel, Wachstum und Differenzierung unverzichtbar.
Pantothensäure wird von Bakterien der Darmflora aus Alanin und
Pantoinsäure hergestellt und kommt in der Nahrung praktisch überall vor
(πάντοθεν = überall). Im Dünndarrm resorbiert, wird Pantothensäure im Blut an Protein gebunden transportiert.
 Der tägliche Bedarf beträgt ~6 mg (Säuglinge 2-3, Kinder 4-6 mg/d). Die therapeutische Breite ist hoch: Erst langfristige Zufuhr
von >10 g/d (mehr als das Tausendfache des Bedarfs!) führen zu Störungen an Gefäßen und Darm.
Der tägliche Bedarf beträgt ~6 mg (Säuglinge 2-3, Kinder 4-6 mg/d). Die therapeutische Breite ist hoch: Erst langfristige Zufuhr
von >10 g/d (mehr als das Tausendfache des Bedarfs!) führen zu Störungen an Gefäßen und Darm.
 EU-RDA für Vitamin B5: 6 mg Pantothensäure
EU-RDA für Vitamin B5: 6 mg Pantothensäure
Pantothensäurereiche Nahrungsmittel
|
|
Pantothensäuregehalt (mg/100g)
|
Leber (Rind, Schwein)
|
6 - 8
|
Nieren (Rind, Schwein)
|
3 - 4
|
| Eigelb |
3,5 |
| Hirn (Rind, Schwein) |
2,5
|
Eier
|
1,3
|
Hering
|
1,0
|
Der Pantothensäure-Tagesbedarf
(6 mg) ist z.B. enthalten in 100 g Leber, 400 g Wassermelonen, 450 g
Vollkornmehl, 600 g Hering, 800 g Schweinefleisch, 1000 g Lachs.
 Pantothensäure
Pantothensäure
Ausscheidung mit dem Harn: Um 4,8 mg/24 h (3,7 mg/g Kreatinin) - Werte unter 1 mg/24 h deuten auf Mangel hin
Vollblut: 1,1-2,0 mg/l (5,0-8,8 µM)
Serum: 0,2-1,1 mg/l
Pantothen-Unterversorgung ist in Europa kaum bekannt; Mangel führt zu Müdigkeit und Schwächegefühl, Schmerzen,
Dermatitis u.a. (burning feet syndrome wurde im 2. Weltkrieg beobachtet).
 Weitere Vitamine werden in
unseren Breiten fast immer in ausreichender Menge zugeführt, so dass
Mangelerscheinungen unter physiologischen Umständen äußerst selten sind.
Weitere Vitamine werden in
unseren Breiten fast immer in ausreichender Menge zugeführt, so dass
Mangelerscheinungen unter physiologischen Umständen äußerst selten sind.


 Natrium (im Körper insgesamt
~100 g; Tagesbedarf 1-3 g oder 2-7 g Kochsalz) ist das Leitkation des Extrazellulärraums (~140 mM: Osmo-, Volumenregulation). Es liegt etwa zur Hälfte als freies Ion (davon 2/3 Kochsalz, 1/3 Bicarbonat), zur Hälfte gebunden vor (Knochen). Die Niere passt die Ausscheidung der Zufuhr an (Aldosteron, natriuretische Peptide). Isotone Kochsalzlösung enthält 9 g NaCl /l. Kalium (~150 g, oder ~50 mM/kg KG, Tagesbedarf ~4 g) befindet sich zu 98% intrazellulär (~150 mM) und
beteiligt sich an Membranpotential, Aktionspotential, Zellwachstum,
Hormonfreisetzung (z.B. Insulin), Blutdruck (antihypertensiv),
Säure-Basen- Gleichgewicht (renale Säureausscheidung). Kalium findet sich in praktisch allen Nahrungsmitteln Natrium (im Körper insgesamt
~100 g; Tagesbedarf 1-3 g oder 2-7 g Kochsalz) ist das Leitkation des Extrazellulärraums (~140 mM: Osmo-, Volumenregulation). Es liegt etwa zur Hälfte als freies Ion (davon 2/3 Kochsalz, 1/3 Bicarbonat), zur Hälfte gebunden vor (Knochen). Die Niere passt die Ausscheidung der Zufuhr an (Aldosteron, natriuretische Peptide). Isotone Kochsalzlösung enthält 9 g NaCl /l. Kalium (~150 g, oder ~50 mM/kg KG, Tagesbedarf ~4 g) befindet sich zu 98% intrazellulär (~150 mM) und
beteiligt sich an Membranpotential, Aktionspotential, Zellwachstum,
Hormonfreisetzung (z.B. Insulin), Blutdruck (antihypertensiv),
Säure-Basen- Gleichgewicht (renale Säureausscheidung). Kalium findet sich in praktisch allen Nahrungsmitteln
 Calcium trägt mit
~1,2 kg zu 1-2% zum Körpergewicht bei (>99% in Knochen und Zähnen), die tägliche Zufuhr sollte ≥1 g betragen (>1g/kg finden
sich in Milch / Milchprodukten). Ca++-Ionen
sind ein Cofaktor für die Blutgerinnung, stabilisieren das
Ruhepotential, sind ein intrazellulärer Signalstoff. Falsche Ernährung, Verdauungsstörungen,
mangelnde Belastung der Knochen, Vit. D-Mangel kann zu Osteoporose
führen. Der extrazelluläre Ca++-Spiegel wird über Parathormon, Calcitonin und Calcitriol reguliert; im Blutplasma beträgt er
~2,5 mM, zur Hälfte frei, zur Hälfte komplex (Phosphat, Oxalat) und an Plasmaprotein (Albumin) gebunden. Magnesium (Tagesbedarf
~0,4 g; im Körper
~20 g, davon 65% im Knochen, 27% im Skelettmuskel) wird von den meisten nukleotidwirksamen Enzymen benötigt und stabilisiert das Ruhepotential an Muskel- und Nervenzellen. Schweiß enthält 1,3 mg/l, mit dem Harn verliert man 100-400 mg/d. Magnesiummangel kann Muskelkrämpfe, Herzrhythmusstörungen, neurologische Störungen bewirken Calcium trägt mit
~1,2 kg zu 1-2% zum Körpergewicht bei (>99% in Knochen und Zähnen), die tägliche Zufuhr sollte ≥1 g betragen (>1g/kg finden
sich in Milch / Milchprodukten). Ca++-Ionen
sind ein Cofaktor für die Blutgerinnung, stabilisieren das
Ruhepotential, sind ein intrazellulärer Signalstoff. Falsche Ernährung, Verdauungsstörungen,
mangelnde Belastung der Knochen, Vit. D-Mangel kann zu Osteoporose
führen. Der extrazelluläre Ca++-Spiegel wird über Parathormon, Calcitonin und Calcitriol reguliert; im Blutplasma beträgt er
~2,5 mM, zur Hälfte frei, zur Hälfte komplex (Phosphat, Oxalat) und an Plasmaprotein (Albumin) gebunden. Magnesium (Tagesbedarf
~0,4 g; im Körper
~20 g, davon 65% im Knochen, 27% im Skelettmuskel) wird von den meisten nukleotidwirksamen Enzymen benötigt und stabilisiert das Ruhepotential an Muskel- und Nervenzellen. Schweiß enthält 1,3 mg/l, mit dem Harn verliert man 100-400 mg/d. Magnesiummangel kann Muskelkrämpfe, Herzrhythmusstörungen, neurologische Störungen bewirken
 Phosphor
ist das mengenmäßig am stärksten mit der Umwelt ausgetauschte Mineral
(1-2 g/d); der Körper enthält
~700 g, etwa 85% davon in Knochen und Zähnen. Der Phosphatspiegel im Blutplasma beträgt 0,8-1,6 mM. Im
Organismus fast ausschließlich als Phosphat, wird Phosphor vor allem
für den Knochen und als Bestandteil von Nukleotiden benötigt (DNA, RNA, ATP) Phosphor
ist das mengenmäßig am stärksten mit der Umwelt ausgetauschte Mineral
(1-2 g/d); der Körper enthält
~700 g, etwa 85% davon in Knochen und Zähnen. Der Phosphatspiegel im Blutplasma beträgt 0,8-1,6 mM. Im
Organismus fast ausschließlich als Phosphat, wird Phosphor vor allem
für den Knochen und als Bestandteil von Nukleotiden benötigt (DNA, RNA, ATP)
 Spurenelemente tragen zu weniger als 0,01% zur Körpermasse bei. Die Bioverfügbarkeit (der im Stoffwechsel physiologisch aktive Anteil eines Spurenelements) hängt von Wachstum, Alter, Belastung, Schwangerschaft, Laktation u.a. ab. Eisen (3-5 g im Körper) dient
dem Sauerstofftransport (Hämoglobin) und ist Cofaktor von Redoxsystemen (Bedarf
10-15 mg in der Nahrung, zu 10-40% aus Fleisch / Blut nutzbar, zu
wenigen % aus pflanzlichen Quellen; täglicher Verlust ≥1-2 mg). Fe++ wird resorbiert, an der basolateralen Enterozytenmembran durch Hephaestin zu Fe+++ oxidiert, über Transferrin transportiert. Zink
(im Körper
~2 g; Tagesbedarf 7-10 mg) wird von >300 Enzymen benötigt (Kollagenstoffwechsel, Polymerasen); für
Insulinspeicherung in ß-Zellen;
Synthese, Speicherung, Sekretion, Rezeptorwirkung von Signalstoffen;
Transkription (Zinkfingerproteine). Jod (Tagesbedarf 0,2 mg) ist Bestandteil der Schilddrüsenhormone; Jodmangel bedingt Schilddrüsenunterfunktion. Fluor (Bedarf ~1 mg/d) wird in Zähne und Knochen eingelagert, geringe Fluoridzufuhr bei Kindern führt zu erhöhter Kariesanfälligkeit. Selen (60-70 µg/d)
ist ein Radikalfänger (synergistische Wirkung mit Vitamin E) und ist an
der Aktivierung von T4 zu T3 beteiligt (Dejodasen sind Selenoproteine). Kupfer (Speicher 50-120 mg, Tagesbedarf 1-2 mg) ist Bestandteil mehrerer Enzyme (Mitochondrien) und an der Eisenresorption beteiligt (Hephästinaktivität) Spurenelemente tragen zu weniger als 0,01% zur Körpermasse bei. Die Bioverfügbarkeit (der im Stoffwechsel physiologisch aktive Anteil eines Spurenelements) hängt von Wachstum, Alter, Belastung, Schwangerschaft, Laktation u.a. ab. Eisen (3-5 g im Körper) dient
dem Sauerstofftransport (Hämoglobin) und ist Cofaktor von Redoxsystemen (Bedarf
10-15 mg in der Nahrung, zu 10-40% aus Fleisch / Blut nutzbar, zu
wenigen % aus pflanzlichen Quellen; täglicher Verlust ≥1-2 mg). Fe++ wird resorbiert, an der basolateralen Enterozytenmembran durch Hephaestin zu Fe+++ oxidiert, über Transferrin transportiert. Zink
(im Körper
~2 g; Tagesbedarf 7-10 mg) wird von >300 Enzymen benötigt (Kollagenstoffwechsel, Polymerasen); für
Insulinspeicherung in ß-Zellen;
Synthese, Speicherung, Sekretion, Rezeptorwirkung von Signalstoffen;
Transkription (Zinkfingerproteine). Jod (Tagesbedarf 0,2 mg) ist Bestandteil der Schilddrüsenhormone; Jodmangel bedingt Schilddrüsenunterfunktion. Fluor (Bedarf ~1 mg/d) wird in Zähne und Knochen eingelagert, geringe Fluoridzufuhr bei Kindern führt zu erhöhter Kariesanfälligkeit. Selen (60-70 µg/d)
ist ein Radikalfänger (synergistische Wirkung mit Vitamin E) und ist an
der Aktivierung von T4 zu T3 beteiligt (Dejodasen sind Selenoproteine). Kupfer (Speicher 50-120 mg, Tagesbedarf 1-2 mg) ist Bestandteil mehrerer Enzyme (Mitochondrien) und an der Eisenresorption beteiligt (Hephästinaktivität)
 Vitamine können vom Körper selbst nicht gebildet werden und üben im Stoffwechsel Schlüsselfunktionen aus. Mangel kann bei Unterernährung (Hunger, Reduktionskost, vegane Ernährung),
erhöhtem physiologischem Bedarf (Schwangere, Säuglinge) oder
Resorptionsstörungen auftreten. Der Bedarf ist individuell
unterschiedlich (genetische Ausstattung, Alter, Lebensgewohnheiten).
Supplementation mit Vitaminpräparaten ist meist überflüssig; bei fettlöslichen Vitaminen (vor allem A, D) besteht die Gefahr einer Überdosierung (Obergrenzen: Tolerable upper intake level). Entsprechend der Absorption im Darm (Pankreas, Galle, Transport) unterscheidet
man fettlösliche (A,D,E,K) und wasserlösliche Vitamine (B-Komplex, Vit.
C, Niazin, Pantothenat). Der Vitaminstatus lässt sich bei fettlöslichen Vitaminen über ihren
Plasmaspiegel abschätzen, bei wasserlöslichen in vielen Fällen über die
Ausscheidung mit dem Harn; für einige gibt es funktionelle Kriterien
(Vit.D: Knochendichte, Vit.B1: Transketolase-Test) Vitamine können vom Körper selbst nicht gebildet werden und üben im Stoffwechsel Schlüsselfunktionen aus. Mangel kann bei Unterernährung (Hunger, Reduktionskost, vegane Ernährung),
erhöhtem physiologischem Bedarf (Schwangere, Säuglinge) oder
Resorptionsstörungen auftreten. Der Bedarf ist individuell
unterschiedlich (genetische Ausstattung, Alter, Lebensgewohnheiten).
Supplementation mit Vitaminpräparaten ist meist überflüssig; bei fettlöslichen Vitaminen (vor allem A, D) besteht die Gefahr einer Überdosierung (Obergrenzen: Tolerable upper intake level). Entsprechend der Absorption im Darm (Pankreas, Galle, Transport) unterscheidet
man fettlösliche (A,D,E,K) und wasserlösliche Vitamine (B-Komplex, Vit.
C, Niazin, Pantothenat). Der Vitaminstatus lässt sich bei fettlöslichen Vitaminen über ihren
Plasmaspiegel abschätzen, bei wasserlöslichen in vielen Fällen über die
Ausscheidung mit dem Harn; für einige gibt es funktionelle Kriterien
(Vit.D: Knochendichte, Vit.B1: Transketolase-Test)
 Vitamin A (Retinol / Retinal / Retinsäure) wird in der Leber gespeichert (Ito-Zellen), im Blut sind >90% des Retinols an Retinol-bindendes Protein gebunden. Pflanzen enthalten Provitamine (Carotine); aus Retinol können alle anderen Formen gebildet werden (Tagesbedarf ~1 mg). Retinal
ist Bestandteil des Rhodopsins (Retinalmangel bedingt Nachtblindheit: retina = Netzhaut),
Oxidation macht es (irreversibel) zu Retinsäure (fetale Morphogenese,
Wachstum und Differenzierung epithelialer Gewebe und blutbildender
Zellen) Vitamin A (Retinol / Retinal / Retinsäure) wird in der Leber gespeichert (Ito-Zellen), im Blut sind >90% des Retinols an Retinol-bindendes Protein gebunden. Pflanzen enthalten Provitamine (Carotine); aus Retinol können alle anderen Formen gebildet werden (Tagesbedarf ~1 mg). Retinal
ist Bestandteil des Rhodopsins (Retinalmangel bedingt Nachtblindheit: retina = Netzhaut),
Oxidation macht es (irreversibel) zu Retinsäure (fetale Morphogenese,
Wachstum und Differenzierung epithelialer Gewebe und blutbildender
Zellen)
 Vitamin D (Vit-D-Hormon, Calciferol, Calcitriol) fördert
die Aufnahme und Verwertung von Calcium und Phosphor sowie die
Erhaltung der Knochen- und Muskelsubstanz, unterstützt Kreislauf,
Immunabwehr und Stoffwechsel (Tagesbedarf 15 µg).
Vit.D3 entsteht in der Haut durch UV-B-Licht aus 7-Dehydrocholesterin;
die Leber konvertiert es zu 25(OH), die Niere zu 1,25(OH)2-Vit.D3
(Calcitriol), die biologisch aktive Form. ≥80% des im Körper
befindlichen Vit.D entsteht üblicherweise durch Lichteinwirkung. Die Wirkung hängt
von der Menge verfügbarer Rezeptoren ab (regulierbar), der Serumwert
alleine ist nur begrenzt aussagekräftig Vitamin D (Vit-D-Hormon, Calciferol, Calcitriol) fördert
die Aufnahme und Verwertung von Calcium und Phosphor sowie die
Erhaltung der Knochen- und Muskelsubstanz, unterstützt Kreislauf,
Immunabwehr und Stoffwechsel (Tagesbedarf 15 µg).
Vit.D3 entsteht in der Haut durch UV-B-Licht aus 7-Dehydrocholesterin;
die Leber konvertiert es zu 25(OH), die Niere zu 1,25(OH)2-Vit.D3
(Calcitriol), die biologisch aktive Form. ≥80% des im Körper
befindlichen Vit.D entsteht üblicherweise durch Lichteinwirkung. Die Wirkung hängt
von der Menge verfügbarer Rezeptoren ab (regulierbar), der Serumwert
alleine ist nur begrenzt aussagekräftig
 Vitamin E (α-Tokopherol) wirkt
antioxidativ (wie Vit.A, Vit. C) und wird in Fett- und Muskelgewebe gespeichert, sein Fehlen führt zu neurologischen Störungen (Tagesbedarf 12-20 mg α-Tokopherol). Vitamin K (Tagesbedarf 65-70 µg) existiert
als Vit.K1 (Phyllochinon), Vit.K2 (Menachinon), Vit.K3 (Menadion),
Vit.K4 (Menadiolester). Die Leber benötigt Vit.K zur Modifizierung von
Zielproteinen wie Gerinnungsfaktoren (II, VII, IX, X, Protein C und S)
zu Ca++-Chelatoren - bedeutsam auch für den Knochen (Carboxylierung von Osteocalcin in Osteoblasten verbessert die Knochenqualität) Vitamin E (α-Tokopherol) wirkt
antioxidativ (wie Vit.A, Vit. C) und wird in Fett- und Muskelgewebe gespeichert, sein Fehlen führt zu neurologischen Störungen (Tagesbedarf 12-20 mg α-Tokopherol). Vitamin K (Tagesbedarf 65-70 µg) existiert
als Vit.K1 (Phyllochinon), Vit.K2 (Menachinon), Vit.K3 (Menadion),
Vit.K4 (Menadiolester). Die Leber benötigt Vit.K zur Modifizierung von
Zielproteinen wie Gerinnungsfaktoren (II, VII, IX, X, Protein C und S)
zu Ca++-Chelatoren - bedeutsam auch für den Knochen (Carboxylierung von Osteocalcin in Osteoblasten verbessert die Knochenqualität)
 Vitamin B1 (Thiamin; Tagesbedarf
~1 mg)
wird im Kohlenhydratstoffwechsel benötigt (oxidative Decarboxylierung
von α-Ketosäuren). Die Körperspeicher sind gering (20-30 mg) und rasch
erschöpft (biologische Halbwertszeit knapp 2 Wochen).
Der Thiaminstatus lässt sich über die Aktivität der
Erythrozyten-Transketolase abschätzen (ETKA-Test): Das Verhältnis von
stimulierter zu basaler ETKA sollte ≤1,2 sein. Vitamin B2
(Riboflavin; Tagesbedarf ≥1,2 mg) dient dem Energie- und
Eiweißstoffwechsel; im Darm entsteht daraus FAD und Flavinmononukleotid (FMN). FAD-abhängig sind mehrere Enzyme,
z.B. im Citratzyklus. Vitamin B6
(Pyridoxin, Pyridoxal, Pyridoxamin; biologisch aktiv:
Pyridoxalphosphat) ist das bedeutendste Coenzym des
Proteinstoffwechsels (Enzyme wie ALAT und ASAT, Hämoglobinsynthese,
Glykogenabbau, GABA-Synthese u.a.). Der Tagesbedarf (Männer 1,5, Frauen 1,2 mg/d) steigt mit dem Proteinumsatz. Vitamin B12 (Cobalamine; Tagesbedarf 2-3 µg, die Leber speichert bis zu 10 mg; auch die Darmflora bildert Vit.B12)
koppelt im Speichel an Haptocorrin (schützt vor Magensaft), im Duodenum
an Intrinsic Factor (schützt vor Proteasen) und wird im unteren Ileum
resorbiert (rezeptorvermittelte Endozytose mittels Cubilin). An
Transcobalamin II gebunden gelangt es durch den Kreislauf. Vit.B12 wird
(wie Folsäure) für Purin- und Pyrimidinsynthese (DNA) benötigt, für Methylierung und Proteinsynthese,
Fettsäureabbau u.a. Chronischer Vit.B12-Mangel führt zu megaloblastärer
Anämie und neurologischen Veränderungen (funikuläre Myelose). Folsäure (Tagesbedarf 0,3-0,6 mg; 12-15 mg in Leber gespeichert) ist für die DNA-Synthese bedeutsam Vitamin B1 (Thiamin; Tagesbedarf
~1 mg)
wird im Kohlenhydratstoffwechsel benötigt (oxidative Decarboxylierung
von α-Ketosäuren). Die Körperspeicher sind gering (20-30 mg) und rasch
erschöpft (biologische Halbwertszeit knapp 2 Wochen).
Der Thiaminstatus lässt sich über die Aktivität der
Erythrozyten-Transketolase abschätzen (ETKA-Test): Das Verhältnis von
stimulierter zu basaler ETKA sollte ≤1,2 sein. Vitamin B2
(Riboflavin; Tagesbedarf ≥1,2 mg) dient dem Energie- und
Eiweißstoffwechsel; im Darm entsteht daraus FAD und Flavinmononukleotid (FMN). FAD-abhängig sind mehrere Enzyme,
z.B. im Citratzyklus. Vitamin B6
(Pyridoxin, Pyridoxal, Pyridoxamin; biologisch aktiv:
Pyridoxalphosphat) ist das bedeutendste Coenzym des
Proteinstoffwechsels (Enzyme wie ALAT und ASAT, Hämoglobinsynthese,
Glykogenabbau, GABA-Synthese u.a.). Der Tagesbedarf (Männer 1,5, Frauen 1,2 mg/d) steigt mit dem Proteinumsatz. Vitamin B12 (Cobalamine; Tagesbedarf 2-3 µg, die Leber speichert bis zu 10 mg; auch die Darmflora bildert Vit.B12)
koppelt im Speichel an Haptocorrin (schützt vor Magensaft), im Duodenum
an Intrinsic Factor (schützt vor Proteasen) und wird im unteren Ileum
resorbiert (rezeptorvermittelte Endozytose mittels Cubilin). An
Transcobalamin II gebunden gelangt es durch den Kreislauf. Vit.B12 wird
(wie Folsäure) für Purin- und Pyrimidinsynthese (DNA) benötigt, für Methylierung und Proteinsynthese,
Fettsäureabbau u.a. Chronischer Vit.B12-Mangel führt zu megaloblastärer
Anämie und neurologischen Veränderungen (funikuläre Myelose). Folsäure (Tagesbedarf 0,3-0,6 mg; 12-15 mg in Leber gespeichert) ist für die DNA-Synthese bedeutsam
 Vitamin C (Ascorbinsäure, Tagesbedarf
~0,1 g) wirkt meist antioxidativ (Redoxsystem, regeneriert auch verbrauchtes Vit.E) und
ist Cofaktor zahlreicher Enzyme (z.B. Kollagensynthese), hilft bei der
Synthese von Noradrenalin, Eisenresorption, Infekabwehr. Biotin (Tagesbedarf 30-60 µg) ist
bedeutsam für Enzymaktivitäten im Protein-, Kohlenhydrat- und
Fettstoffwechsel und im Zellkern (Modifikation von Histonen). Niazin (Nikotinsäure und Nikotinamid - Tagesbedarf 12-15 mg) ist ein Elektronenüberträger: NAD+ bzw. NADP+
für Oxidoreduktasen, Dehydrogenasen / Decarboxylasen,
posttranslationale Modifizierung DNA-gebundener Proteine, beteiligt
sich am Protein-, Kohlenhydrat- und Fettstoffwechsel und an der
Energiebereitstellung im Citratzyklus. 60 mg Tryptophan können 1 mg Nikotinamidäquivalente generieren. Pantothensäure (Tagesbedarf ~6 mg) ist Bestandteil des Coenzyms A (Citratzyklus) und der Fettsäure-Synthase und kommt in der Nahrung praktisch überall vor Vitamin C (Ascorbinsäure, Tagesbedarf
~0,1 g) wirkt meist antioxidativ (Redoxsystem, regeneriert auch verbrauchtes Vit.E) und
ist Cofaktor zahlreicher Enzyme (z.B. Kollagensynthese), hilft bei der
Synthese von Noradrenalin, Eisenresorption, Infekabwehr. Biotin (Tagesbedarf 30-60 µg) ist
bedeutsam für Enzymaktivitäten im Protein-, Kohlenhydrat- und
Fettstoffwechsel und im Zellkern (Modifikation von Histonen). Niazin (Nikotinsäure und Nikotinamid - Tagesbedarf 12-15 mg) ist ein Elektronenüberträger: NAD+ bzw. NADP+
für Oxidoreduktasen, Dehydrogenasen / Decarboxylasen,
posttranslationale Modifizierung DNA-gebundener Proteine, beteiligt
sich am Protein-, Kohlenhydrat- und Fettstoffwechsel und an der
Energiebereitstellung im Citratzyklus. 60 mg Tryptophan können 1 mg Nikotinamidäquivalente generieren. Pantothensäure (Tagesbedarf ~6 mg) ist Bestandteil des Coenzyms A (Citratzyklus) und der Fettsäure-Synthase und kommt in der Nahrung praktisch überall vor
|

 Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.
Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.




 Bedarf an
Mineralstoffen, Spurenelementen, Vitaminen
Bedarf an
Mineralstoffen, Spurenelementen, Vitaminen
 Askorbinsäure: Verhindert Skorbut
Askorbinsäure: Verhindert Skorbut Spurenelemente
Spurenelemente
 Vitamine
Vitamine

 Abbildung: Täglicher Bedarf einer erwachsenen Person an Mineralstoffen, Spurenelementen und Vitaminen
Abbildung: Täglicher Bedarf einer erwachsenen Person an Mineralstoffen, Spurenelementen und Vitaminen
 Zur Definition von RDA-Werten s. auch dort
Zur Definition von RDA-Werten s. auch dort
 Abbildung: Prozentueller Anteil der Elemente am Körpergewicht
Abbildung: Prozentueller Anteil der Elemente am Körpergewicht
 5 g Kochsalz bedeuten 2,3 g Natrium.
5 g Kochsalz bedeuten 2,3 g Natrium.  Eine "physiologische (isotone) Kochsalzlösung" (Grundlage für Infusionslösungen) ist 0,9%-ig, d.h. 1 Liter enthält 9 g NaCl.
Eine "physiologische (isotone) Kochsalzlösung" (Grundlage für Infusionslösungen) ist 0,9%-ig, d.h. 1 Liter enthält 9 g NaCl. Einerseits sollten mindestens einige mg/kg Körpergewicht täglich
zugeführt
werden, um das extrazelluläre Volumen stabil zu halten - chronische
Unterversorgung mit Kochsalz führt (auch bei maximaler
Aldosteronwirkung) zu Hypotonizität, Hypovolämie und Hypotonie,
schließlich zu Kreislaufversagen
Einerseits sollten mindestens einige mg/kg Körpergewicht täglich
zugeführt
werden, um das extrazelluläre Volumen stabil zu halten - chronische
Unterversorgung mit Kochsalz führt (auch bei maximaler
Aldosteronwirkung) zu Hypotonizität, Hypovolämie und Hypotonie,
schließlich zu Kreislaufversagen Andererseits können größere Mengen die Osmo- und Volumenregulation überfordern, da der Körper nicht auf die Ausscheidung von hochkonzentriertem Salz angepasst ist. Zwar kann die Niere die Ausscheidung der Zufuhr anpassen (je mehr
Kochsalz zugeführt wird, desto geringer ist die
Aldosteronbildung, und es wird mehr Natrium
ausgeschieden), aber dies funktioniert nur in einem relativ begrenzten Osmolaritätsbereich.
Andererseits können größere Mengen die Osmo- und Volumenregulation überfordern, da der Körper nicht auf die Ausscheidung von hochkonzentriertem Salz angepasst ist. Zwar kann die Niere die Ausscheidung der Zufuhr anpassen (je mehr
Kochsalz zugeführt wird, desto geringer ist die
Aldosteronbildung, und es wird mehr Natrium
ausgeschieden), aber dies funktioniert nur in einem relativ begrenzten Osmolaritätsbereich. Der tägliche Bedarf an Natrium
wird mit 1 bis 3 Gramm (entspricht ~2-7 g Kochsalz) angegeben; nach
der Empfehlung der Deutschen Gesellschaft für Ernährung sollten
erwachsene Personen nicht mehr als 6 g Kochsalz täglich konsumieren (Referenzwert: 1,5 g Natrium / Tag).
Der tägliche Bedarf an Natrium
wird mit 1 bis 3 Gramm (entspricht ~2-7 g Kochsalz) angegeben; nach
der Empfehlung der Deutschen Gesellschaft für Ernährung sollten
erwachsene Personen nicht mehr als 6 g Kochsalz täglich konsumieren (Referenzwert: 1,5 g Natrium / Tag). Die tägliche Aufnahme von Chlorid (Atommasse 35,5) ergibt sich im Wesentlichen aus der Kochsalzaufnahme (Empfehlung Erwachsene: 3,2 g Cl/d).
Die tägliche Aufnahme von Chlorid (Atommasse 35,5) ergibt sich im Wesentlichen aus der Kochsalzaufnahme (Empfehlung Erwachsene: 3,2 g Cl/d). 3 g NaCl / kg KG / Tag (also bei 70 kg Körpergewicht etwa 210 g/d) ist eine potenziell tödliche Dosis.
3 g NaCl / kg KG / Tag (also bei 70 kg Körpergewicht etwa 210 g/d) ist eine potenziell tödliche Dosis.
 Abbildung: Na-K-ATPase
Abbildung: Na-K-ATPase s. dort)
s. dort)
 Membranpotential und Erregung (Reizbeantwortung, Aktionspotentiale etc)
Membranpotential und Erregung (Reizbeantwortung, Aktionspotentiale etc) Zellwachstum (Kaliumtransport, Zellvolumen)
Zellwachstum (Kaliumtransport, Zellvolumen) Hormonfreisetzung (z.B. Insulin aus Pankreas)
Hormonfreisetzung (z.B. Insulin aus Pankreas) Blutdruck (schützt vor Hypertension)
Blutdruck (schützt vor Hypertension) Säure-Basen-Gleichgewicht (renale Säureausscheidung)
Säure-Basen-Gleichgewicht (renale Säureausscheidung) Der tägliche Bedarf an Kalium
liegt möglicherweise höher als die
übliche Aufnahme von 2,0-3,5 g/d (0,75-1,25 mM/kg/d) - empfohlen werden 4,7 g/d (120 mM/d). Referenzwert: 4 g Kalium täglich.
Der tägliche Bedarf an Kalium
liegt möglicherweise höher als die
übliche Aufnahme von 2,0-3,5 g/d (0,75-1,25 mM/kg/d) - empfohlen werden 4,7 g/d (120 mM/d). Referenzwert: 4 g Kalium täglich. Hülsenfrüchte (Linsen 800, Erbsen 900, weiße Bohnen 1300, Sojabohnen 1700)
Hülsenfrüchte (Linsen 800, Erbsen 900, weiße Bohnen 1300, Sojabohnen 1700) Nüsse (500-600)
Nüsse (500-600) Gemüse (z.B. Spargel 200, Kartoffeln 400, Spinat 600)
Gemüse (z.B. Spargel 200, Kartoffeln 400, Spinat 600) Vollmilchschokolade 400, Kakaopulver 1500
Vollmilchschokolade 400, Kakaopulver 1500 Getreidepridukte (Reis 150, div. Brotsorten 240-440, Kleie über 1000)
Getreidepridukte (Reis 150, div. Brotsorten 240-440, Kleie über 1000) manche Obstsorten (über 300: Bananen, Schwarze Johannisbeeren, Honigmelone)
manche Obstsorten (über 300: Bananen, Schwarze Johannisbeeren, Honigmelone) Fisch (220-440), Fleisch (250-420)
Fisch (220-440), Fleisch (250-420) Zur Regulation der intestinalen Kaliumresorption s. dort
Zur Regulation der intestinalen Kaliumresorption s. dort Zur Dynamik des Kaliums in der Niere s. dort
Zur Dynamik des Kaliums in der Niere s. dort Zur Physiologie des Natriums und Kaliums (Leitkation der intrazellulären Flüssigkeit: ~30 l bei ~70 kg KG) s. u.a. II.9, X.6, XII.8.
Zur Physiologie des Natriums und Kaliums (Leitkation der intrazellulären Flüssigkeit: ~30 l bei ~70 kg KG) s. u.a. II.9, X.6, XII.8. 
 Abbildung: Calciumbilanz einer erwachsenen Person
Abbildung: Calciumbilanz einer erwachsenen Person
 Bestandteil des Knochens. Die Einlagerung / Mobilisierung von Calciumionen in den / aus dem riesigen Knochenspeicher (etwa 1,2 kg oder 3.104 mmol) steht unter mehrfacher hormoneller Kontrolle, der Austausch mit dem Körper beträgt ungefähr 300 mg in 24 Stunden (
Bestandteil des Knochens. Die Einlagerung / Mobilisierung von Calciumionen in den / aus dem riesigen Knochenspeicher (etwa 1,2 kg oder 3.104 mmol) steht unter mehrfacher hormoneller Kontrolle, der Austausch mit dem Körper beträgt ungefähr 300 mg in 24 Stunden ( Abbildung).
Abbildung). Extrazellulär: Cofaktor für die Blutgerinnung (Faktoren XII, XI, X, II, Fibrin), Stabilisierung des Ruhepotentials (Erregbarkeit von Neuronen, neuromuskulären Endplatten)
Extrazellulär: Cofaktor für die Blutgerinnung (Faktoren XII, XI, X, II, Fibrin), Stabilisierung des Ruhepotentials (Erregbarkeit von Neuronen, neuromuskulären Endplatten) Interzellulär: Calcium ist Teil der "Kittmasse" in tight junctions, welche Zellen zusammenhält / abdichtet
Interzellulär: Calcium ist Teil der "Kittmasse" in tight junctions, welche Zellen zusammenhält / abdichtet Intrazellulär: Signalstoff (second messenger, Muskelkontraktion: elektro-mechanische Koppelung)
Intrazellulär: Signalstoff (second messenger, Muskelkontraktion: elektro-mechanische Koppelung) Die tägliche Ca++-Zufuhr mit der Nahrung
sollte 1,0-1,5 g betragen (1 mmol = 40 mg); Gute Calciumquellen sind
Milch und Milchprodukte, Sojabohnen, Spinat, Broccoli.
Die tägliche Ca++-Zufuhr mit der Nahrung
sollte 1,0-1,5 g betragen (1 mmol = 40 mg); Gute Calciumquellen sind
Milch und Milchprodukte, Sojabohnen, Spinat, Broccoli. Calcium (Blutplasma)
Calcium (Blutplasma) Zur Regulation der Calciumresorption s. dort
Zur Regulation der Calciumresorption s. dort (1-2 g/d); der Körper einer erwachsenen Person enthält rund 700 g Phosphor, etwa 85% davon in Knochen
und Zähnen.
(1-2 g/d); der Körper einer erwachsenen Person enthält rund 700 g Phosphor, etwa 85% davon in Knochen
und Zähnen.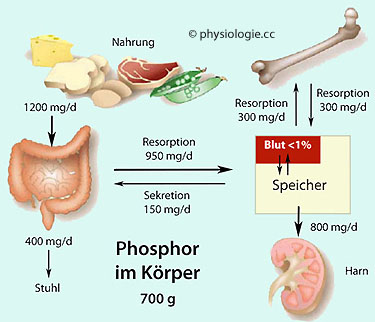
 Abbildung: Phosphorbilanz einer erwachsenen Person
Abbildung: Phosphorbilanz einer erwachsenen Person Die tägliche Phosphor-Aufnahme
einer erwachsenen Person sollte mindestens ~0,7 Gramm betragen. Gute
Phosphatquellen sind Milchprodukte, Bohnen, Walnüsse, Fleisch, Fisch,
Brot.
Die tägliche Phosphor-Aufnahme
einer erwachsenen Person sollte mindestens ~0,7 Gramm betragen. Gute
Phosphatquellen sind Milchprodukte, Bohnen, Walnüsse, Fleisch, Fisch,
Brot.  (Atommasse 24): Der Körper einer erwachsenen Person enthält etwa 20 g
Magnesium - ~65% im Knochen, 27% im Skelettmuskel, 7% in anderen
Zellen, 1% im Extrazellulärraum.
(Atommasse 24): Der Körper einer erwachsenen Person enthält etwa 20 g
Magnesium - ~65% im Knochen, 27% im Skelettmuskel, 7% in anderen
Zellen, 1% im Extrazellulärraum. Fast alle Enzyme, die mit
Nukleotiden (DNA, RNA) interagieren, benötigen Magnesiumionen als
Kofaktor (z.B. DNA-Helikase, RNA-Polymerase).
Fast alle Enzyme, die mit
Nukleotiden (DNA, RNA) interagieren, benötigen Magnesiumionen als
Kofaktor (z.B. DNA-Helikase, RNA-Polymerase). 
 Mg++-Ionen
stabilisieren das Ruhepotential an Muskel- und Nervenzellen (u.a. im
Vegetativum).
Mg++-Ionen
stabilisieren das Ruhepotential an Muskel- und Nervenzellen (u.a. im
Vegetativum).  Magnesium
muss stetig mit der Nahrung
zugeführt werden,
denn es geht laufend mit dem Harn verloren (~5% der glomerulär
filtrierten Menge - 95% werden tubulär rückresorbiert).
Magnesium
muss stetig mit der Nahrung
zugeführt werden,
denn es geht laufend mit dem Harn verloren (~5% der glomerulär
filtrierten Menge - 95% werden tubulär rückresorbiert). 
 Abbildung: Eisenstoffwechsel an der Darmschleimhautzelle
Abbildung: Eisenstoffwechsel an der Darmschleimhautzelle DMT-1, divalent metal transporter befördert zweiwertiges Eisen in Darmzellen
DMT-1, divalent metal transporter befördert zweiwertiges Eisen in Darmzellen  HCP-1, haem carrier protein 1 ist ein Häm-Rezeptor an der luminalen Oberfläche der Enterozyten, über den Hämeisen aufgenommen werden kann
HCP-1, haem carrier protein 1 ist ein Häm-Rezeptor an der luminalen Oberfläche der Enterozyten, über den Hämeisen aufgenommen werden kann  HO-1, Hämoxygenase ist ein mikrosomales Enzym, das Eisen oxydiert
HO-1, Hämoxygenase ist ein mikrosomales Enzym, das Eisen oxydiert  ISC, iron-sulfur cluster, Eisen-Schwefel-Komplexe, die enzymatisch aktiv sind
ISC, iron-sulfur cluster, Eisen-Schwefel-Komplexe, die enzymatisch aktiv sind  Tf, Transferrin
Tf, Transferrin
 Der Körper einer erwachsenen Person sollte 3-5 g Eisen enthalten.
Eisenmangel ist weltweit stark verbreitet und betrifft vermutlich
insgesamt etwa 2 Milliarden Menschen.
Der Körper einer erwachsenen Person sollte 3-5 g Eisen enthalten.
Eisenmangel ist weltweit stark verbreitet und betrifft vermutlich
insgesamt etwa 2 Milliarden Menschen. Täglich müssen ≥1-2 mg Eisen resorbiert werden. Dazu ist die Zufuhr von
10-30 mg/d Nahrungseisen erforderlich (Referenzwerte: Männer 10 mg/d, Frauen 15 mg/d). Eisen muss in zweiwertiger Form
angeboten werden,
um resorbiert werden zu können. Gut (10-20%) resorbierbar ist Eisen in
organischer Bindung (Hämeisen in Blut, Fleisch), weniger gut (zu 1-7%)
aus pflanzlichen Quellen. In höherer Konzentration, insbesondere in Zusammenwirken mit Vit. C, kann Eisen prooxidativ wirken.
Täglich müssen ≥1-2 mg Eisen resorbiert werden. Dazu ist die Zufuhr von
10-30 mg/d Nahrungseisen erforderlich (Referenzwerte: Männer 10 mg/d, Frauen 15 mg/d). Eisen muss in zweiwertiger Form
angeboten werden,
um resorbiert werden zu können. Gut (10-20%) resorbierbar ist Eisen in
organischer Bindung (Hämeisen in Blut, Fleisch), weniger gut (zu 1-7%)
aus pflanzlichen Quellen. In höherer Konzentration, insbesondere in Zusammenwirken mit Vit. C, kann Eisen prooxidativ wirken.
 Die Resorption verbessert sich bei
gleichzeitiger Anwesenheit von Vitamin C, Zitronensäure, Eiweiß.
Die Resorption verbessert sich bei
gleichzeitiger Anwesenheit von Vitamin C, Zitronensäure, Eiweiß.  Viele
pflanzliche Stoffe hemmen sie, z.B. Oxalsäure (Spinat, Rhabarber,
Schokolade) und Gerbstoffe / Tannine (Rotwein, schwarzer Tee).
Viele
pflanzliche Stoffe hemmen sie, z.B. Oxalsäure (Spinat, Rhabarber,
Schokolade) und Gerbstoffe / Tannine (Rotwein, schwarzer Tee).  Eisen (Serum / Plasma)
Eisen (Serum / Plasma) 
 Zur Interaktiom von Darm (Resorption), Leber (Speicherung), Knochenmark (Erythropoese), Milz (Ery-Abbau) und Nieren (Erythropoetin) s. auch dort
Zur Interaktiom von Darm (Resorption), Leber (Speicherung), Knochenmark (Erythropoese), Milz (Ery-Abbau) und Nieren (Erythropoetin) s. auch dort
 durch mehrere kleine organische Verbindungen wie z.B. Citrat gefördert,
durch mehrere kleine organische Verbindungen wie z.B. Citrat gefördert,
 andere hemmen sie (z.B. Phytinsäure: schlechte Zinkversorgung bei
(lakto)vegetarischer Kost).
andere hemmen sie (z.B. Phytinsäure: schlechte Zinkversorgung bei
(lakto)vegetarischer Kost).  Der Tagesbedarf
an Zink liegt bei 7-10 mg (Referenzwerte: Männer 10 mg/d, Frauen 7 mg/d). Gute Quellen sind Fleisch, Milch und Vollkornbrot.
Der Tagesbedarf
an Zink liegt bei 7-10 mg (Referenzwerte: Männer 10 mg/d, Frauen 7 mg/d). Gute Quellen sind Fleisch, Milch und Vollkornbrot.  Zink (Serum, Plasma)
Zink (Serum, Plasma) 
 Abbildung: Weltkarte der Jodidversorgung
Abbildung: Weltkarte der Jodidversorgung
 (Jodmangelkropf: das Schilddrüsengewebe ist durch TSH maximal angeregt und hypertrophiert) und Schilddrüsenunterfunktion (Hypothermie, Antriebslosigkeit etc).
(Jodmangelkropf: das Schilddrüsengewebe ist durch TSH maximal angeregt und hypertrophiert) und Schilddrüsenunterfunktion (Hypothermie, Antriebslosigkeit etc). Abbildung.
Abbildung.  Jod
Jod
 festigen Zähne und Knochen, indem sie in deren Matrix als Fluorapatit (statt Hydroxyapatit) eingelagert werden, Demineralisierung reduzieren und die Mineralisierung anregen.
Sie regen weiters die Osteoblastentätigkeit an.
festigen Zähne und Knochen, indem sie in deren Matrix als Fluorapatit (statt Hydroxyapatit) eingelagert werden, Demineralisierung reduzieren und die Mineralisierung anregen.
Sie regen weiters die Osteoblastentätigkeit an.  ~1 mg/d (Säuglinge und Kinder ≥0,25 mg/d), bei hohem Fluorgehalt im Trinkwasser entsprechend weniger - enthalten u.a. in Fisch, Milch. Geringe Fluoridzufuhr bei Kindern führt zu erhöhter Kariesanfälligkeit.
~1 mg/d (Säuglinge und Kinder ≥0,25 mg/d), bei hohem Fluorgehalt im Trinkwasser entsprechend weniger - enthalten u.a. in Fisch, Milch. Geringe Fluoridzufuhr bei Kindern führt zu erhöhter Kariesanfälligkeit. (mehrere Oxidationsstufen möglich, z.B. Se2-) liegt in der Nahrung vor
allem an Aminosäuren gebunden vor (Methionin, Cystein) und wird vor
allem im Dünndarm resorbiert. Es ist Bestandteil sogenannter Selenoproteine, z.B. der zytosolischen Glutathionperoxidase (GSH-Px), deren Hauptwirkung der Abbau von H2O2
ist (ein antioxidativer Effekt im Blutplasma ist hingegen
unwahrscheinlich). Zellmembranen können durch das Selenoprotein
Phospholipid-Hydroperoxid-GSH-Px geschützt werden (Selen als Radikalfänger: synergistische Wirkung mit Vitamin E). Selen ist u.a. auch an der
Aktivierung von Thyroxin (T4) zu Trijodthyronin (T3) beteiligt (Deiodasen sind Selenoproteine).
(mehrere Oxidationsstufen möglich, z.B. Se2-) liegt in der Nahrung vor
allem an Aminosäuren gebunden vor (Methionin, Cystein) und wird vor
allem im Dünndarm resorbiert. Es ist Bestandteil sogenannter Selenoproteine, z.B. der zytosolischen Glutathionperoxidase (GSH-Px), deren Hauptwirkung der Abbau von H2O2
ist (ein antioxidativer Effekt im Blutplasma ist hingegen
unwahrscheinlich). Zellmembranen können durch das Selenoprotein
Phospholipid-Hydroperoxid-GSH-Px geschützt werden (Selen als Radikalfänger: synergistische Wirkung mit Vitamin E). Selen ist u.a. auch an der
Aktivierung von Thyroxin (T4) zu Trijodthyronin (T3) beteiligt (Deiodasen sind Selenoproteine). Der tägliche Selen-Bedarf
beträgt 60-70 µg/d (Referenzwerte: Männer 70 µg/d, Frauen 60 µg/d, Säuglinge 10-15, Kinder 15-60 µg/d, mit dem Alter ansteigend). Höhere Dosen wirken potentiell toxisch,
die tolerierbare Obergrenze liegt wahrscheinlich bei ~400 µg/d.
Der tägliche Selen-Bedarf
beträgt 60-70 µg/d (Referenzwerte: Männer 70 µg/d, Frauen 60 µg/d, Säuglinge 10-15, Kinder 15-60 µg/d, mit dem Alter ansteigend). Höhere Dosen wirken potentiell toxisch,
die tolerierbare Obergrenze liegt wahrscheinlich bei ~400 µg/d. Selen
Selen Der Bedarf liegt unter 20 µg/d, die
tägliche Aufnahme von Chrom sollte wahrscheinlich 25-35 µg nicht
überschreiten (USA). Referenzwerte: 30-100 µg/d.
Der Bedarf liegt unter 20 µg/d, die
tägliche Aufnahme von Chrom sollte wahrscheinlich 25-35 µg nicht
überschreiten (USA). Referenzwerte: 30-100 µg/d. Der Bedarf wird auf 0,1 µg/d geschätzt und üblicherweise mit der Zufuhr von Vit.B12 gedeckt.
Der Bedarf wird auf 0,1 µg/d geschätzt und üblicherweise mit der Zufuhr von Vit.B12 gedeckt.  Kobalt
Kobalt Coeruloplasmin (Ferroxidase I, oxidiert Fe2+ zu Fe3+),
Coeruloplasmin (Ferroxidase I, oxidiert Fe2+ zu Fe3+),  Cytochromoxidase (bewirkt oxidative Phosphorylierung),
Cytochromoxidase (bewirkt oxidative Phosphorylierung),  Superoxiddismutase (Radikalschutz),
Superoxiddismutase (Radikalschutz), Lysyloxidase (vernetzt Kollagen und Elastin),
Lysyloxidase (vernetzt Kollagen und Elastin), Tyrosinase (bewirkt Pigmentierung),
Tyrosinase (bewirkt Pigmentierung), Cholesterolhydrolasen (Cholesterinabbau)
Cholesterolhydrolasen (Cholesterinabbau)  Tagesbedarf: 1-2 mg
(Fleisch, Fisch, Innereien, Getreide, Nüsse). Kupfermangel bewirkt vor allem Anämie. Referenzwerte: 1,0-1,5 mg/d. Kupfermangel ist extrem selten (Leukopenie, Anämie).
Tagesbedarf: 1-2 mg
(Fleisch, Fisch, Innereien, Getreide, Nüsse). Kupfermangel bewirkt vor allem Anämie. Referenzwerte: 1,0-1,5 mg/d. Kupfermangel ist extrem selten (Leukopenie, Anämie). Kupfer (Serum / Plasma)
Kupfer (Serum / Plasma) <1 mg/d. Empfohlene Zufuhr 2-5 mg/d.
<1 mg/d. Empfohlene Zufuhr 2-5 mg/d. Mangan (Serum)
Mangan (Serum)  Der Tagesbedarf liegt bei 25 µg, die empfohlene Zufuhr 50-100 µg/d (nicht über 150 µg/d).
Der Tagesbedarf liegt bei 25 µg, die empfohlene Zufuhr 50-100 µg/d (nicht über 150 µg/d). Vit. D
Vit. D  Vit. E
Vit. E  Vit. K
Vit. K  Vit. B1
Vit. B1  Bit. B2
Bit. B2  Bit. B6
Bit. B6  Folat
Folat  Vit. B12
Vit. B12  Vit. C
Vit. C  Biotin
Biotin  Niazin
Niazin  Pantothensäure
Pantothensäure erhöhtem physiologischem Bedarf (Schwangere, Säuglinge)
erhöhtem physiologischem Bedarf (Schwangere, Säuglinge) ungenügender Zufuhr wegen Reduktionskost, veganer / vegetarischer Ernährungsweise
ungenügender Zufuhr wegen Reduktionskost, veganer / vegetarischer Ernährungsweise Resorptionsstörungen, z.B. genetisch bedingten Defekten an Enzymen oder Transportsystemen
Resorptionsstörungen, z.B. genetisch bedingten Defekten an Enzymen oder Transportsystemen Bei Vitamin-Unterversorgung
können sich Probleme entwickeln, umso rascher, je kürzer die
Aufenthaltsdauer im Körper ist und je geringer die physiologischen
Speicher gefüllt sind. Mangelernährung führt zum Fehlen mehrerer
Nahrungskomponenten, "reine", nur ein Vitamin betreffende Symptome
finden sich sehr selten.
Bei Vitamin-Unterversorgung
können sich Probleme entwickeln, umso rascher, je kürzer die
Aufenthaltsdauer im Körper ist und je geringer die physiologischen
Speicher gefüllt sind. Mangelernährung führt zum Fehlen mehrerer
Nahrungskomponenten, "reine", nur ein Vitamin betreffende Symptome
finden sich sehr selten.  Übermäßige Vitaminzufuhr
ist in entwickelten Ländern gang und gäbe und kann z.T. gravierende
Nebenwirkungen zeitigen. Daher hat man Obergrenzen der empfohlenen
Zufuhr definiert (UL: Tolerable upper intake level).
Übermäßige Vitaminzufuhr
ist in entwickelten Ländern gang und gäbe und kann z.T. gravierende
Nebenwirkungen zeitigen. Daher hat man Obergrenzen der empfohlenen
Zufuhr definiert (UL: Tolerable upper intake level). fettlösliche
(A, D, E, K) - ihre Aufnahme bedingt funktionierende Fettresorption
(Pankreasfunktion, Gallesekretion, Transport über Chylomikronen). Sie
werden im Magen durch den niedrigen pH-Wert bzw. Proteolyse von
Proteinen, an die sie angelagert sein können, abgekoppelt. Im
proximalen Dünndarm werden sie nach dem Muster der Fettresorption
(Emulsion, Mizellenbildung) von der Schleimhaut (apikal) via Diffusion
oder Transporter aufgenommen und (basolateral) in Chylomikronen oder
VLDL-Partikel verpackt an das Interstitium weitergegeben. Die Lymphe
abtransportiert sie ab, die Leber nimmt sie via Endozytose auf;
fettlösliche
(A, D, E, K) - ihre Aufnahme bedingt funktionierende Fettresorption
(Pankreasfunktion, Gallesekretion, Transport über Chylomikronen). Sie
werden im Magen durch den niedrigen pH-Wert bzw. Proteolyse von
Proteinen, an die sie angelagert sein können, abgekoppelt. Im
proximalen Dünndarm werden sie nach dem Muster der Fettresorption
(Emulsion, Mizellenbildung) von der Schleimhaut (apikal) via Diffusion
oder Transporter aufgenommen und (basolateral) in Chylomikronen oder
VLDL-Partikel verpackt an das Interstitium weitergegeben. Die Lymphe
abtransportiert sie ab, die Leber nimmt sie via Endozytose auf; wasserlösliche Vitamine (B-Komplex, Vit. C u.a.).
wasserlösliche Vitamine (B-Komplex, Vit. C u.a.).
 Bei fettlöslichen Vitaminen (vor allem A, D) besteht die Gefahr einer Überdosierung.
Bei fettlöslichen Vitaminen (vor allem A, D) besteht die Gefahr einer Überdosierung. 
 Retinol
Retinol
 Retinol (Serum / Plasma)
Retinol (Serum / Plasma) 
 Abbildung: Das Vitamin A-System
Abbildung: Das Vitamin A-System
 Abbildung). Im Blut transportiert wird Retinol an RBP (retinol binding protein)
gebunden (dieser Komplex wird in der Niere teilweise glomerulär
filtriert und über den Megalin-Rezeptor tubulär rückresorbiert). Mehr
als
die Hälfte des im Körper gespeicherten Retinlyesters befindet sich in
den Stellatumzellen (Stern-, Ito-Zellen) der Leber.
Abbildung). Im Blut transportiert wird Retinol an RBP (retinol binding protein)
gebunden (dieser Komplex wird in der Niere teilweise glomerulär
filtriert und über den Megalin-Rezeptor tubulär rückresorbiert). Mehr
als
die Hälfte des im Körper gespeicherten Retinlyesters befindet sich in
den Stellatumzellen (Stern-, Ito-Zellen) der Leber. Retinal - die Aldehydform des Retinols ("Vitamin-A-Aldehyd") - ist am Sehvorgang beteiligt: es wird als Bestandteil des Rhodopsins - an das Membranprotein Opsin
gekoppelt - in der Netzhaut benötigt (Retinalmangel bedingt Nachtblindheit).
Retinal - die Aldehydform des Retinols ("Vitamin-A-Aldehyd") - ist am Sehvorgang beteiligt: es wird als Bestandteil des Rhodopsins - an das Membranprotein Opsin
gekoppelt - in der Netzhaut benötigt (Retinalmangel bedingt Nachtblindheit).  Retinsäure (retinoic acid) entsteht durch Oxidation von Retinal (irreversibler Schritt). Sie ist an der Morphogenese von
Organsystemen des Feten beteiligt und reguliert Wachstum und Differenzierung
epithelialer Gewebe (Haut, Respirationssystem, Darmschleimhaut), aber
auch blutbildender Zellen.
Retinsäure (retinoic acid) entsteht durch Oxidation von Retinal (irreversibler Schritt). Sie ist an der Morphogenese von
Organsystemen des Feten beteiligt und reguliert Wachstum und Differenzierung
epithelialer Gewebe (Haut, Respirationssystem, Darmschleimhaut), aber
auch blutbildender Zellen. 
 Abbildung: Vitamin A in der Zelle
Abbildung: Vitamin A in der Zelle
 Die wichtigste Transportform im Körper ist Retinol (Vitamin A1, die Alkoholform), aus ihr können alle anderen Formen gebildet werden. Die Speicherform ist Retinylester, vorwiegend in
dieser Form wird Vit.A auch im Darm rersorbiert. Die Regulation des
Vitaminspiegels im Blut erfolgt auf Basis der Umwandlung von ß-Carotin
in Retinal; bei erhöhtem Vitaminbedarf wird Carotin vermehrt in
Retinal umgewandelt (Dioxygenase).
Die wichtigste Transportform im Körper ist Retinol (Vitamin A1, die Alkoholform), aus ihr können alle anderen Formen gebildet werden. Die Speicherform ist Retinylester, vorwiegend in
dieser Form wird Vit.A auch im Darm rersorbiert. Die Regulation des
Vitaminspiegels im Blut erfolgt auf Basis der Umwandlung von ß-Carotin
in Retinal; bei erhöhtem Vitaminbedarf wird Carotin vermehrt in
Retinal umgewandelt (Dioxygenase).
 ß-Carotine wirken als Antioxidantien (Oxidationsschutz)
ß-Carotine wirken als Antioxidantien (Oxidationsschutz) Retinal wird zur Produktion von Rhodopsin benötigt (Bei Mangel Nachtblindheit)
Retinal wird zur Produktion von Rhodopsin benötigt (Bei Mangel Nachtblindheit) Retinsäure bindet (über nukleäre Rezeptoren) an DNA und steuert die Differenzierung von Epithelzellen
Retinsäure bindet (über nukleäre Rezeptoren) an DNA und steuert die Differenzierung von Epithelzellen

 Cholecalciferol
Cholecalciferol Abbildung).
Abbildung).
 Vitamin D (Serum)
Vitamin D (Serum) In unseren Breiten finden sich meist Serumwerte zwischen 8 (!) und 80 ng/ml
In unseren Breiten finden sich meist Serumwerte zwischen 8 (!) und 80 ng/ml

 wirkt (wie Vitamin A) über nukleäre Rezeptoren auf die Transkription einer großen Zahl von Genen. Es hat
dementsprechend zahlreiche Funktionen (teils erwünschte, eventuell
teils unerwünschte Wirkungen). Es fördert die Aufnahme und Verwertung
von Calcium und Phosphor sowie die
Erhaltung der Knochen- und Muskelsubstanz. Weiters unterstützt es
Kreislauffunktion, Immunabwehr und Zellstoffwechsel.
wirkt (wie Vitamin A) über nukleäre Rezeptoren auf die Transkription einer großen Zahl von Genen. Es hat
dementsprechend zahlreiche Funktionen (teils erwünschte, eventuell
teils unerwünschte Wirkungen). Es fördert die Aufnahme und Verwertung
von Calcium und Phosphor sowie die
Erhaltung der Knochen- und Muskelsubstanz. Weiters unterstützt es
Kreislauffunktion, Immunabwehr und Zellstoffwechsel. 
 Abbildung: UV-B und endogene Vitamin-D-Synthese, exogene Zufuhr, Aktivierung durch Leber und Niere
Abbildung: UV-B und endogene Vitamin-D-Synthese, exogene Zufuhr, Aktivierung durch Leber und Niere
 Die Haut
bildet unter Einwirkung von UVB aus der Vorstufe 7-Dehydrocholesterin
bis zu 1000 IU/min Provitamin D3 (umso effizienter, je weniger Melanin
sie enthält), das spontan zu Vit. D3 (Cholecalciferol) isomerisiert;
Die Haut
bildet unter Einwirkung von UVB aus der Vorstufe 7-Dehydrocholesterin
bis zu 1000 IU/min Provitamin D3 (umso effizienter, je weniger Melanin
sie enthält), das spontan zu Vit. D3 (Cholecalciferol) isomerisiert;  D3-Vitamin wird über das Vitamin D-bindende Protein (DBP) im Blut transportiert;
D3-Vitamin wird über das Vitamin D-bindende Protein (DBP) im Blut transportiert;  die Leber bildet daraus 25(OH)Vit.D (25-Hydroxycholecalciferol, Calcidiol), und
die Leber bildet daraus 25(OH)Vit.D (25-Hydroxycholecalciferol, Calcidiol), und  die Niere (1α-Hydroxylase) das biologisch aktive
1,25-(OH2)-D3 (1,25-Dihydroxycholecalciferol, Calcitriol). Dieser letzte Schritt wird (mittels Enzyminduktion) durch Parathormon und Calcitonin gefördert, weiters durch Östrogene und erniedrigten Calciumspiegel im Blut.
die Niere (1α-Hydroxylase) das biologisch aktive
1,25-(OH2)-D3 (1,25-Dihydroxycholecalciferol, Calcitriol). Dieser letzte Schritt wird (mittels Enzyminduktion) durch Parathormon und Calcitonin gefördert, weiters durch Östrogene und erniedrigten Calciumspiegel im Blut. Entscheidend ist die Effizienz der
intrazellulären Wirkung. Diese hängt von der Menge verfügbarer Rezeptoren ab, und die Zahl der Rezeptoren ist regulierbar. Ein niedriger Serumwert lässt sich also durch upregulation auf Rezeptorebene kompensieren und muss sich nicht zwingend als Vit-D-Mangel manifestieren.
Entscheidend ist die Effizienz der
intrazellulären Wirkung. Diese hängt von der Menge verfügbarer Rezeptoren ab, und die Zahl der Rezeptoren ist regulierbar. Ein niedriger Serumwert lässt sich also durch upregulation auf Rezeptorebene kompensieren und muss sich nicht zwingend als Vit-D-Mangel manifestieren. bei Kindern Rachitis (Deformierungen vor allem im Bereich des Thorax - “Hühnerbrust” -,
des Beckens (Verengungen) und der Extremitäten (O-Beine),
bei Kindern Rachitis (Deformierungen vor allem im Bereich des Thorax - “Hühnerbrust” -,
des Beckens (Verengungen) und der Extremitäten (O-Beine),  bei Erwachsenen Osteomalazie (Erweichung der Knochenmasse, erhöhte
Anfälligkeit für Knochenbrüche) zur Folge.
bei Erwachsenen Osteomalazie (Erweichung der Knochenmasse, erhöhte
Anfälligkeit für Knochenbrüche) zur Folge. Bis zu 20% des Vitamin D im Körper wird über die Nahrung
aufgenommen. Referenzwerte: 20 µg Calciferole / Tag (1µg=40 IU). Aufnahme Vit-D-reicher Nahrung (fetter Fisch, Pilze, Eier, Avocado,
Kuhmilch) sowie
Supplementierung (400 IU/d oder höher) ist in höheren geographischen
Breiten über das ganze Jahr zu empfehlen. Intoxikation (Serum-25(OH)-Vit.D-Spiegel über 150 ng/ml) ist bei dieser Dosierung
nicht zu erwarten.
Bis zu 20% des Vitamin D im Körper wird über die Nahrung
aufgenommen. Referenzwerte: 20 µg Calciferole / Tag (1µg=40 IU). Aufnahme Vit-D-reicher Nahrung (fetter Fisch, Pilze, Eier, Avocado,
Kuhmilch) sowie
Supplementierung (400 IU/d oder höher) ist in höheren geographischen
Breiten über das ganze Jahr zu empfehlen. Intoxikation (Serum-25(OH)-Vit.D-Spiegel über 150 ng/ml) ist bei dieser Dosierung
nicht zu erwarten.
 α-Tocopherol
α-Tocopherol
 α-Tocopherol (Serum)
α-Tocopherol (Serum) 
 Vitamin E wirkt antioxidativ
Vitamin E wirkt antioxidativ Vitamin E schützt mehrfach gesättigte Fettsäuren in Zellmembranen
Vitamin E schützt mehrfach gesättigte Fettsäuren in Zellmembranen Vitamin E bewahrt Lipoproteine niedriger Dichte (LDL) vor Oxidation
Vitamin E bewahrt Lipoproteine niedriger Dichte (LDL) vor Oxidation 

 Phyllochinon (Vit. K1)
Phyllochinon (Vit. K1)
 s. dort). Diese modifiziert Zielproteine (Gerinnungsfaktoren II, VII, IX, X, Protein C und S) zu Ca++-Chelatoren - mittels des Ca++ binden die Faktoren an membranständige Phospholipide aktivierter Zellen.
s. dort). Diese modifiziert Zielproteine (Gerinnungsfaktoren II, VII, IX, X, Protein C und S) zu Ca++-Chelatoren - mittels des Ca++ binden die Faktoren an membranständige Phospholipide aktivierter Zellen. 
 Die Hydrochinonform von Vit. K ist ein Cofaktor der γ-Carboxylase
Die Hydrochinonform von Vit. K ist ein Cofaktor der γ-Carboxylase γ-Carboxylase aktiviert die Gerinnungsfaktoren II, VII, IX und X
γ-Carboxylase aktiviert die Gerinnungsfaktoren II, VII, IX und X Dadurch binden diese Faktoren Ca++ und Phospholipide von Thrombozyten und Gefäßwandzellen
Dadurch binden diese Faktoren Ca++ und Phospholipide von Thrombozyten und Gefäßwandzellen
 Über die Rolle des Vit. K für die Gerinnungsfaktoren II, VII, IX und X ("Prothrombinkomplex") und die klinische Bedeutung von Vitamin-K-Antagonisten zur Abschwächung der Gerinnungsaktivität (Verlängerung der Gerinnungszeit) s. dort
Über die Rolle des Vit. K für die Gerinnungsfaktoren II, VII, IX und X ("Prothrombinkomplex") und die klinische Bedeutung von Vitamin-K-Antagonisten zur Abschwächung der Gerinnungsaktivität (Verlängerung der Gerinnungszeit) s. dort
 Abbildung: Einige theoretische Speicherzeiten für Vitamine im Körper (Zeit bis Erschöpfung der Reserven bei fehlender Zufuhr)
Abbildung: Einige theoretische Speicherzeiten für Vitamine im Körper (Zeit bis Erschöpfung der Reserven bei fehlender Zufuhr)
 In pflanzlicher Kost enthalten (Ausnahme: B12)
In pflanzlicher Kost enthalten (Ausnahme: B12) Sie werden kaum gespeichert, Zufuhr in kurzen Intervallen nötig (Ausnahme: B12)
Sie werden kaum gespeichert, Zufuhr in kurzen Intervallen nötig (Ausnahme: B12) Sie wirken als Enzym-Bestandteile (s. Tabelle)
Sie wirken als Enzym-Bestandteile (s. Tabelle)
 Thiamin
Thiamin
 ) ist vor allem im Kohlenhydratstoffwechsel (oxidative Decarboxylierung von α-Ketosäuren) wichtig (
) ist vor allem im Kohlenhydratstoffwechsel (oxidative Decarboxylierung von α-Ketosäuren) wichtig ( s. Tabelle).
s. Tabelle).

 Die aktive Form von Vit.B1 ist Thiamin-Pyrophosphat (TPP)
Die aktive Form von Vit.B1 ist Thiamin-Pyrophosphat (TPP) Es dient als Cofaktor für Enzyme, die CO2 von ß-Ketosäuren entfernen (oxidative Decarboxylierung)
Es dient als Cofaktor für Enzyme, die CO2 von ß-Ketosäuren entfernen (oxidative Decarboxylierung) Es überträgt C-Fragmente
Es überträgt C-Fragmente


 FMN (Flavin-Mononukleotid) und FAD (Flavin-Adenin-Dinukleotid) sind
Coenzyme von Oxidoreduktasen, sie übertragen Elektronen
FMN (Flavin-Mononukleotid) und FAD (Flavin-Adenin-Dinukleotid) sind
Coenzyme von Oxidoreduktasen, sie übertragen Elektronen
 Riboflavin
Riboflavin
 Pyridoxalphosphat (PLP, PALP, P5P)
Pyridoxalphosphat (PLP, PALP, P5P)
 die Alanin-Aminotransferase (ALT - früher: GPT) und die Aspartat-Aminotransferase (AST - früher: GOP), beide sind im Aminosäurestoffwechsel tätig (Transaminierungen, d.h. Umbau von Amino- zu Ketosäure)
die Alanin-Aminotransferase (ALT - früher: GPT) und die Aspartat-Aminotransferase (AST - früher: GOP), beide sind im Aminosäurestoffwechsel tätig (Transaminierungen, d.h. Umbau von Amino- zu Ketosäure) die für die Hämoglobinsynthese benötigte δ-Aminolävulinsäure-Synthetase
die für die Hämoglobinsynthese benötigte δ-Aminolävulinsäure-Synthetase die Glykogen-Phosphorylase, welche Glykogen abbaut
die Glykogen-Phosphorylase, welche Glykogen abbaut die Glutamat-Decarboxylase für die Synthese von GABA und die Tyrosin-Decarboxylase für die Bildung von Tyramin (Abbauprodukt des Tyrosins, wird mit dem Stuhl ausgeschieden)
die Glutamat-Decarboxylase für die Synthese von GABA und die Tyrosin-Decarboxylase für die Bildung von Tyramin (Abbauprodukt des Tyrosins, wird mit dem Stuhl ausgeschieden) Der
Bedarf an Vit. B6 beträgt für Männer 1,5 und für Frauen 1,2 mg pro Tag. Er steigt mit dem Proteinumsatz und ist von Gesundheitszustand und
Ernährungsweise abhängig.
Der
Bedarf an Vit. B6 beträgt für Männer 1,5 und für Frauen 1,2 mg pro Tag. Er steigt mit dem Proteinumsatz und ist von Gesundheitszustand und
Ernährungsweise abhängig.  Vit. B6 (PALP)
Vit. B6 (PALP)

 Tetrahydrofolsäure
Tetrahydrofolsäure Abbildung);
dieses Coenzym ist die biologisch aktive Form des Vitamins und
beteiligt sich an zahlreichen metabolischen Reaktionen, insbesondere im Nukleinsäure-Stoffwechsel (DNA-Synthese).
Abbildung);
dieses Coenzym ist die biologisch aktive Form des Vitamins und
beteiligt sich an zahlreichen metabolischen Reaktionen, insbesondere im Nukleinsäure-Stoffwechsel (DNA-Synthese).

 Der tägliche Bedarf an Folsäure (Folsäureäquivalente: FÄ) beträgt beim Erwachsenen 300-400 µg
(bei Schwangeren bis 600 µg). Die
enterische Resorptionskapazität ist weit höher (bis zu 15 mg/d), mit vollwertiger Nahrung werden leicht 2 mg/d aufgenommen. Der
küchentechnische Verlust durch Erhitzen, Sauerstoffeinfluss und
Verwerfen des Kochwassers beträgt bis zu 90%. Reich an Folsäure sind u.a. frisches grünes Gemüse, Weizenkeime, Sojabohnen, Hefe, Eidotter, einige Früchte -
und Leber.
Der tägliche Bedarf an Folsäure (Folsäureäquivalente: FÄ) beträgt beim Erwachsenen 300-400 µg
(bei Schwangeren bis 600 µg). Die
enterische Resorptionskapazität ist weit höher (bis zu 15 mg/d), mit vollwertiger Nahrung werden leicht 2 mg/d aufgenommen. Der
küchentechnische Verlust durch Erhitzen, Sauerstoffeinfluss und
Verwerfen des Kochwassers beträgt bis zu 90%. Reich an Folsäure sind u.a. frisches grünes Gemüse, Weizenkeime, Sojabohnen, Hefe, Eidotter, einige Früchte -
und Leber. ungenügender Zufuhr (Fehlernährung,
Zubereitungsverluste, Alkoholiker)
ungenügender Zufuhr (Fehlernährung,
Zubereitungsverluste, Alkoholiker) erhöhtem Bedarf (pubertärer
Wachstumsschub, Schwangerschaft, Laktation, Infekte)
erhöhtem Bedarf (pubertärer
Wachstumsschub, Schwangerschaft, Laktation, Infekte)  Interferenz mit Pharmaka (z.B. oralen Kontrazeptiva).
Interferenz mit Pharmaka (z.B. oralen Kontrazeptiva). 
 Cobalamin
Cobalamin dort
dort
 Im Speichel vorhandenes Haptocorrin (ein Transcobalamin: TC I) schützt mit der Nahrung aufgenommenes Vitamin B12
vor dem sauren Magensaft (das Vitamin ist säureempfindlich).
Im Speichel vorhandenes Haptocorrin (ein Transcobalamin: TC I) schützt mit der Nahrung aufgenommenes Vitamin B12
vor dem sauren Magensaft (das Vitamin ist säureempfindlich).  Im
Duodenum entkoppelt es von Haptocorrin und bindet stattdessen an das gastrische Glykoprotein Intrinsic Factor (IF), der IF-B12-Komplex ist resistent gegenüber Proteasen im Dünndarm.
Im
Duodenum entkoppelt es von Haptocorrin und bindet stattdessen an das gastrische Glykoprotein Intrinsic Factor (IF), der IF-B12-Komplex ist resistent gegenüber Proteasen im Dünndarm.  Im unteren Ileum (wo auch Folat zur Aufnahme gelangt) wird dieser Komplex über eigene Rezeptorkomplexe aufgenommen und das Vitamin mittels rezeptorvermittelter Endozytose resorbiert (Cubilin in der Darmschleimhaut bindet an den Intrinsic factor-Cobalamin-Komplex und ermöglicht so seine Aufnahme).
Im unteren Ileum (wo auch Folat zur Aufnahme gelangt) wird dieser Komplex über eigene Rezeptorkomplexe aufgenommen und das Vitamin mittels rezeptorvermittelter Endozytose resorbiert (Cubilin in der Darmschleimhaut bindet an den Intrinsic factor-Cobalamin-Komplex und ermöglicht so seine Aufnahme).  Der Intrinsic Factor wird lysosomal abgebaut und Vit.B12 an Transcobalamin II (TC II) gebunden; in dieser Form zirkuliert es im Blut.
Der Intrinsic Factor wird lysosomal abgebaut und Vit.B12 an Transcobalamin II (TC II) gebunden; in dieser Form zirkuliert es im Blut.  Bildung von Succinyl-CoA in den Mitochondrien
(Methylmalonyl-CoA-Mutase) - Abbau von ungeradzahligen Fettsäuren und
einigen Aminosäuren im Citratzyklus
Bildung von Succinyl-CoA in den Mitochondrien
(Methylmalonyl-CoA-Mutase) - Abbau von ungeradzahligen Fettsäuren und
einigen Aminosäuren im Citratzyklus Zytoplasmatischer Folsäure-, Methionin- und Homocysteinstoffwechsel
(Homocystein-Methyltransferase bzw. Methionin-Synthase) - Methylierung und Proteinsynthese.
Zytoplasmatischer Folsäure-, Methionin- und Homocysteinstoffwechsel
(Homocystein-Methyltransferase bzw. Methionin-Synthase) - Methylierung und Proteinsynthese.  Der Tagesbedarf beträgt 2-3 µg.
Die Ernährung liefert meist mehr als der
physiologische Bedarf erfordert; enterohepatische Wiederverwertung und
ein großer Körperspeicher erlauben es, Versorgungslücken für Monate bis Jahre zu überbrücken.
Der Tagesbedarf beträgt 2-3 µg.
Die Ernährung liefert meist mehr als der
physiologische Bedarf erfordert; enterohepatische Wiederverwertung und
ein großer Körperspeicher erlauben es, Versorgungslücken für Monate bis Jahre zu überbrücken.  Vit B12 stammt auch von Mikroorganismen im Darm, die mit verzehrtem Gemüse in den Körper gelangen. Die Produktion durch Darmbakterien ist
aber nicht ausreichend, strikt vegane Kost führt manchmal zu Mangelerscheinungen.
Vit B12 stammt auch von Mikroorganismen im Darm, die mit verzehrtem Gemüse in den Körper gelangen. Die Produktion durch Darmbakterien ist
aber nicht ausreichend, strikt vegane Kost führt manchmal zu Mangelerscheinungen. Vitamin B12 (Serum)
Vitamin B12 (Serum)  Mangel an intrinsic factor: Atrophische Gastritis, Magenoperationen
Mangel an intrinsic factor: Atrophische Gastritis, Magenoperationen Erschwerte Resorption: Erkrankungen des Ileums, z.B. Mb. Crohn
Erschwerte Resorption: Erkrankungen des Ileums, z.B. Mb. Crohn
 Ascorbinsäure
Ascorbinsäure 

 Vit.C
wirkt als Redoxsystem im allgemeinen antioxidativ, wirkt also reduzierend, hält z.B. Eisen im zweiwertigen Zustand
Vit.C
wirkt als Redoxsystem im allgemeinen antioxidativ, wirkt also reduzierend, hält z.B. Eisen im zweiwertigen Zustand Vit.C
ist Cofaktor zahlreicher Enzyme, die für posttranslationale Modifikation und Hydroxylierung von
Prokollagen bei der Kollagensynthese benötigt werden (Prolin durch Prolylhydroxylase, Lysin durch Lysylhydroxylasen)
Vit.C
ist Cofaktor zahlreicher Enzyme, die für posttranslationale Modifikation und Hydroxylierung von
Prokollagen bei der Kollagensynthese benötigt werden (Prolin durch Prolylhydroxylase, Lysin durch Lysylhydroxylasen) Vit.C regeneriert verbrauchtes Vit.E und arbeitet mit Glutathion
bei Oxidationsreaktionen zusammen, es schützt vor Schäden durch freie Radikale
Vit.C regeneriert verbrauchtes Vit.E und arbeitet mit Glutathion
bei Oxidationsreaktionen zusammen, es schützt vor Schäden durch freie Radikale Vit.C wird für die Noradrenalinsynthese (als Cofaktor für die Dopaminhydroxylase und Elektronendonator), die Eisenresorption im Darm (Reduktion von dreiwertigem Eisen zu Fe2+, Verbesserung der Resorption phytathaltiger Nahrungsstoffe), als Cofaktor der 7α-Hydroxylase in der Leber (Synthese von Gallensäuren) und für die
Infekabwehr (Schutz der Phagozytenmembran) benötigt.
Vit.C wird für die Noradrenalinsynthese (als Cofaktor für die Dopaminhydroxylase und Elektronendonator), die Eisenresorption im Darm (Reduktion von dreiwertigem Eisen zu Fe2+, Verbesserung der Resorption phytathaltiger Nahrungsstoffe), als Cofaktor der 7α-Hydroxylase in der Leber (Synthese von Gallensäuren) und für die
Infekabwehr (Schutz der Phagozytenmembran) benötigt. Der
tägliche Vit-C-Bedarf beträgt für Männer 110 und für Frauen 95 mg
(Raucher ~150 mg/d). Hypervitaminose ist nicht bekannt, das Vitamin wird über
die Nieren und (bei Dosen ab ~3 g/d, also dem 40-fachen des Bedarfs)
auch über den Darm ausgeschieden. Vitamin C in höherer Dosierung wirkt
allerdings prooxidativ, z.B. auch in Kombination mit Eisen, dessen
Resorption durch Vit. C begünstigt wird.
Der
tägliche Vit-C-Bedarf beträgt für Männer 110 und für Frauen 95 mg
(Raucher ~150 mg/d). Hypervitaminose ist nicht bekannt, das Vitamin wird über
die Nieren und (bei Dosen ab ~3 g/d, also dem 40-fachen des Bedarfs)
auch über den Darm ausgeschieden. Vitamin C in höherer Dosierung wirkt
allerdings prooxidativ, z.B. auch in Kombination mit Eisen, dessen
Resorption durch Vit. C begünstigt wird. Vitamin C (Ascorbinsäure + Dehydroascorbinsäure)
Vitamin C (Ascorbinsäure + Dehydroascorbinsäure)  Leichter Vit. C-Mangel (chronisch
einseitige Ernährung) bewirkt Müdigkeit, Schwäche und
Infektanfälligkeit;
Leichter Vit. C-Mangel (chronisch
einseitige Ernährung) bewirkt Müdigkeit, Schwäche und
Infektanfälligkeit;  schwerer, lang anhaltender Mangel (2-4 Monate) Skorbut
(scurvy) (Kollagensynthese!) - gekennzeichnet durch Zahnfleischbluten, mangelhafte
Wundheilung, Probleme an Haut, Knochen, Bewegungsapparat, neurologische
Symptome.
schwerer, lang anhaltender Mangel (2-4 Monate) Skorbut
(scurvy) (Kollagensynthese!) - gekennzeichnet durch Zahnfleischbluten, mangelhafte
Wundheilung, Probleme an Haut, Knochen, Bewegungsapparat, neurologische
Symptome.
 Biotin
Biotin
 Der tägliche Bedarf liegt bei 30-60 µg/d. Darmbakterien können sich an der
Zufuhr beteiligen, ernährungsbedingte Mangelzustände sind selten. Das
Vitamin hat eine hohe therapeutische
Breite, man kennt keine Hypervitaminose.
Der tägliche Bedarf liegt bei 30-60 µg/d. Darmbakterien können sich an der
Zufuhr beteiligen, ernährungsbedingte Mangelzustände sind selten. Das
Vitamin hat eine hohe therapeutische
Breite, man kennt keine Hypervitaminose. 


 Aktives Vit. B3 tritt auf als NAD+ (Nikotinamid-Adenin-Dinukleotid) und NADP+ (-Phosphat)
Aktives Vit. B3 tritt auf als NAD+ (Nikotinamid-Adenin-Dinukleotid) und NADP+ (-Phosphat) Reduktion ergibt NADH und HADPH, beide dienen als Elektronenüberträger
Reduktion ergibt NADH und HADPH, beide dienen als Elektronenüberträger
 Niacin
Niacin 
 Pantothensäure
Pantothensäure 

 Der tägliche Bedarf beträgt ~6 mg (Säuglinge 2-3, Kinder 4-6 mg/d). Die therapeutische Breite ist hoch: Erst langfristige Zufuhr
von >10 g/d (mehr als das Tausendfache des Bedarfs!) führen zu Störungen an Gefäßen und Darm.
Der tägliche Bedarf beträgt ~6 mg (Säuglinge 2-3, Kinder 4-6 mg/d). Die therapeutische Breite ist hoch: Erst langfristige Zufuhr
von >10 g/d (mehr als das Tausendfache des Bedarfs!) führen zu Störungen an Gefäßen und Darm.  Pantothensäure
Pantothensäure  Weitere Vitamine werden in
unseren Breiten fast immer in ausreichender Menge zugeführt, so dass
Mangelerscheinungen unter physiologischen Umständen äußerst selten sind.
Weitere Vitamine werden in
unseren Breiten fast immer in ausreichender Menge zugeführt, so dass
Mangelerscheinungen unter physiologischen Umständen äußerst selten sind.
 Natrium (im Körper insgesamt
~100 g; Tagesbedarf 1-3 g oder 2-7 g Kochsalz) ist das Leitkation des Extrazellulärraums (~140 mM: Osmo-, Volumenregulation). Es liegt etwa zur Hälfte als freies Ion (davon 2/3 Kochsalz, 1/3 Bicarbonat), zur Hälfte gebunden vor (Knochen). Die Niere passt die Ausscheidung der Zufuhr an (Aldosteron, natriuretische Peptide). Isotone Kochsalzlösung enthält 9 g NaCl /l. Kalium (~150 g, oder ~50 mM/kg KG, Tagesbedarf ~4 g) befindet sich zu 98% intrazellulär (~150 mM) und
beteiligt sich an Membranpotential, Aktionspotential, Zellwachstum,
Hormonfreisetzung (z.B. Insulin), Blutdruck (antihypertensiv),
Säure-Basen- Gleichgewicht (renale Säureausscheidung). Kalium findet sich in praktisch allen Nahrungsmitteln
Natrium (im Körper insgesamt
~100 g; Tagesbedarf 1-3 g oder 2-7 g Kochsalz) ist das Leitkation des Extrazellulärraums (~140 mM: Osmo-, Volumenregulation). Es liegt etwa zur Hälfte als freies Ion (davon 2/3 Kochsalz, 1/3 Bicarbonat), zur Hälfte gebunden vor (Knochen). Die Niere passt die Ausscheidung der Zufuhr an (Aldosteron, natriuretische Peptide). Isotone Kochsalzlösung enthält 9 g NaCl /l. Kalium (~150 g, oder ~50 mM/kg KG, Tagesbedarf ~4 g) befindet sich zu 98% intrazellulär (~150 mM) und
beteiligt sich an Membranpotential, Aktionspotential, Zellwachstum,
Hormonfreisetzung (z.B. Insulin), Blutdruck (antihypertensiv),
Säure-Basen- Gleichgewicht (renale Säureausscheidung). Kalium findet sich in praktisch allen Nahrungsmitteln Calcium trägt mit
~1,2 kg zu 1-2% zum Körpergewicht bei (>99% in Knochen und Zähnen), die tägliche Zufuhr sollte ≥1 g betragen (>1g/kg finden
sich in Milch / Milchprodukten). Ca++-Ionen
sind ein Cofaktor für die Blutgerinnung, stabilisieren das
Ruhepotential, sind ein intrazellulärer Signalstoff. Falsche Ernährung, Verdauungsstörungen,
mangelnde Belastung der Knochen, Vit. D-Mangel kann zu Osteoporose
führen. Der extrazelluläre Ca++-Spiegel wird über Parathormon, Calcitonin und Calcitriol reguliert; im Blutplasma beträgt er
~2,5 mM, zur Hälfte frei, zur Hälfte komplex (Phosphat, Oxalat) und an Plasmaprotein (Albumin) gebunden. Magnesium (Tagesbedarf
~0,4 g; im Körper
~20 g, davon 65% im Knochen, 27% im Skelettmuskel) wird von den meisten nukleotidwirksamen Enzymen benötigt und stabilisiert das Ruhepotential an Muskel- und Nervenzellen. Schweiß enthält 1,3 mg/l, mit dem Harn verliert man 100-400 mg/d. Magnesiummangel kann Muskelkrämpfe, Herzrhythmusstörungen, neurologische Störungen bewirken
Calcium trägt mit
~1,2 kg zu 1-2% zum Körpergewicht bei (>99% in Knochen und Zähnen), die tägliche Zufuhr sollte ≥1 g betragen (>1g/kg finden
sich in Milch / Milchprodukten). Ca++-Ionen
sind ein Cofaktor für die Blutgerinnung, stabilisieren das
Ruhepotential, sind ein intrazellulärer Signalstoff. Falsche Ernährung, Verdauungsstörungen,
mangelnde Belastung der Knochen, Vit. D-Mangel kann zu Osteoporose
führen. Der extrazelluläre Ca++-Spiegel wird über Parathormon, Calcitonin und Calcitriol reguliert; im Blutplasma beträgt er
~2,5 mM, zur Hälfte frei, zur Hälfte komplex (Phosphat, Oxalat) und an Plasmaprotein (Albumin) gebunden. Magnesium (Tagesbedarf
~0,4 g; im Körper
~20 g, davon 65% im Knochen, 27% im Skelettmuskel) wird von den meisten nukleotidwirksamen Enzymen benötigt und stabilisiert das Ruhepotential an Muskel- und Nervenzellen. Schweiß enthält 1,3 mg/l, mit dem Harn verliert man 100-400 mg/d. Magnesiummangel kann Muskelkrämpfe, Herzrhythmusstörungen, neurologische Störungen bewirken Phosphor
ist das mengenmäßig am stärksten mit der Umwelt ausgetauschte Mineral
(1-2 g/d); der Körper enthält
~700 g, etwa 85% davon in Knochen und Zähnen. Der Phosphatspiegel im Blutplasma beträgt 0,8-1,6 mM. Im
Organismus fast ausschließlich als Phosphat, wird Phosphor vor allem
für den Knochen und als Bestandteil von Nukleotiden benötigt (DNA, RNA, ATP)
Phosphor
ist das mengenmäßig am stärksten mit der Umwelt ausgetauschte Mineral
(1-2 g/d); der Körper enthält
~700 g, etwa 85% davon in Knochen und Zähnen. Der Phosphatspiegel im Blutplasma beträgt 0,8-1,6 mM. Im
Organismus fast ausschließlich als Phosphat, wird Phosphor vor allem
für den Knochen und als Bestandteil von Nukleotiden benötigt (DNA, RNA, ATP)  Spurenelemente tragen zu weniger als 0,01% zur Körpermasse bei. Die Bioverfügbarkeit (der im Stoffwechsel physiologisch aktive Anteil eines Spurenelements) hängt von Wachstum, Alter, Belastung, Schwangerschaft, Laktation u.a. ab. Eisen (3-5 g im Körper) dient
dem Sauerstofftransport (Hämoglobin) und ist Cofaktor von Redoxsystemen (Bedarf
10-15 mg in der Nahrung, zu 10-40% aus Fleisch / Blut nutzbar, zu
wenigen % aus pflanzlichen Quellen; täglicher Verlust ≥1-2 mg). Fe++ wird resorbiert, an der basolateralen Enterozytenmembran durch Hephaestin zu Fe+++ oxidiert, über Transferrin transportiert. Zink
(im Körper
~2 g; Tagesbedarf 7-10 mg) wird von >300 Enzymen benötigt (Kollagenstoffwechsel, Polymerasen); für
Insulinspeicherung in ß-Zellen;
Synthese, Speicherung, Sekretion, Rezeptorwirkung von Signalstoffen;
Transkription (Zinkfingerproteine). Jod (Tagesbedarf 0,2 mg) ist Bestandteil der Schilddrüsenhormone; Jodmangel bedingt Schilddrüsenunterfunktion. Fluor (Bedarf ~1 mg/d) wird in Zähne und Knochen eingelagert, geringe Fluoridzufuhr bei Kindern führt zu erhöhter Kariesanfälligkeit. Selen (60-70 µg/d)
ist ein Radikalfänger (synergistische Wirkung mit Vitamin E) und ist an
der Aktivierung von T4 zu T3 beteiligt (Dejodasen sind Selenoproteine). Kupfer (Speicher 50-120 mg, Tagesbedarf 1-2 mg) ist Bestandteil mehrerer Enzyme (Mitochondrien) und an der Eisenresorption beteiligt (Hephästinaktivität)
Spurenelemente tragen zu weniger als 0,01% zur Körpermasse bei. Die Bioverfügbarkeit (der im Stoffwechsel physiologisch aktive Anteil eines Spurenelements) hängt von Wachstum, Alter, Belastung, Schwangerschaft, Laktation u.a. ab. Eisen (3-5 g im Körper) dient
dem Sauerstofftransport (Hämoglobin) und ist Cofaktor von Redoxsystemen (Bedarf
10-15 mg in der Nahrung, zu 10-40% aus Fleisch / Blut nutzbar, zu
wenigen % aus pflanzlichen Quellen; täglicher Verlust ≥1-2 mg). Fe++ wird resorbiert, an der basolateralen Enterozytenmembran durch Hephaestin zu Fe+++ oxidiert, über Transferrin transportiert. Zink
(im Körper
~2 g; Tagesbedarf 7-10 mg) wird von >300 Enzymen benötigt (Kollagenstoffwechsel, Polymerasen); für
Insulinspeicherung in ß-Zellen;
Synthese, Speicherung, Sekretion, Rezeptorwirkung von Signalstoffen;
Transkription (Zinkfingerproteine). Jod (Tagesbedarf 0,2 mg) ist Bestandteil der Schilddrüsenhormone; Jodmangel bedingt Schilddrüsenunterfunktion. Fluor (Bedarf ~1 mg/d) wird in Zähne und Knochen eingelagert, geringe Fluoridzufuhr bei Kindern führt zu erhöhter Kariesanfälligkeit. Selen (60-70 µg/d)
ist ein Radikalfänger (synergistische Wirkung mit Vitamin E) und ist an
der Aktivierung von T4 zu T3 beteiligt (Dejodasen sind Selenoproteine). Kupfer (Speicher 50-120 mg, Tagesbedarf 1-2 mg) ist Bestandteil mehrerer Enzyme (Mitochondrien) und an der Eisenresorption beteiligt (Hephästinaktivität)  Vitamine können vom Körper selbst nicht gebildet werden und üben im Stoffwechsel Schlüsselfunktionen aus. Mangel kann bei Unterernährung (Hunger, Reduktionskost, vegane Ernährung),
erhöhtem physiologischem Bedarf (Schwangere, Säuglinge) oder
Resorptionsstörungen auftreten. Der Bedarf ist individuell
unterschiedlich (genetische Ausstattung, Alter, Lebensgewohnheiten).
Supplementation mit Vitaminpräparaten ist meist überflüssig; bei fettlöslichen Vitaminen (vor allem A, D) besteht die Gefahr einer Überdosierung (Obergrenzen: Tolerable upper intake level). Entsprechend der Absorption im Darm (Pankreas, Galle, Transport) unterscheidet
man fettlösliche (A,D,E,K) und wasserlösliche Vitamine (B-Komplex, Vit.
C, Niazin, Pantothenat). Der Vitaminstatus lässt sich bei fettlöslichen Vitaminen über ihren
Plasmaspiegel abschätzen, bei wasserlöslichen in vielen Fällen über die
Ausscheidung mit dem Harn; für einige gibt es funktionelle Kriterien
(Vit.D: Knochendichte, Vit.B1: Transketolase-Test)
Vitamine können vom Körper selbst nicht gebildet werden und üben im Stoffwechsel Schlüsselfunktionen aus. Mangel kann bei Unterernährung (Hunger, Reduktionskost, vegane Ernährung),
erhöhtem physiologischem Bedarf (Schwangere, Säuglinge) oder
Resorptionsstörungen auftreten. Der Bedarf ist individuell
unterschiedlich (genetische Ausstattung, Alter, Lebensgewohnheiten).
Supplementation mit Vitaminpräparaten ist meist überflüssig; bei fettlöslichen Vitaminen (vor allem A, D) besteht die Gefahr einer Überdosierung (Obergrenzen: Tolerable upper intake level). Entsprechend der Absorption im Darm (Pankreas, Galle, Transport) unterscheidet
man fettlösliche (A,D,E,K) und wasserlösliche Vitamine (B-Komplex, Vit.
C, Niazin, Pantothenat). Der Vitaminstatus lässt sich bei fettlöslichen Vitaminen über ihren
Plasmaspiegel abschätzen, bei wasserlöslichen in vielen Fällen über die
Ausscheidung mit dem Harn; für einige gibt es funktionelle Kriterien
(Vit.D: Knochendichte, Vit.B1: Transketolase-Test)  Vitamin A (Retinol / Retinal / Retinsäure) wird in der Leber gespeichert (Ito-Zellen), im Blut sind >90% des Retinols an Retinol-bindendes Protein gebunden. Pflanzen enthalten Provitamine (Carotine); aus Retinol können alle anderen Formen gebildet werden (Tagesbedarf ~1 mg). Retinal
ist Bestandteil des Rhodopsins (Retinalmangel bedingt Nachtblindheit: retina = Netzhaut),
Oxidation macht es (irreversibel) zu Retinsäure (fetale Morphogenese,
Wachstum und Differenzierung epithelialer Gewebe und blutbildender
Zellen)
Vitamin A (Retinol / Retinal / Retinsäure) wird in der Leber gespeichert (Ito-Zellen), im Blut sind >90% des Retinols an Retinol-bindendes Protein gebunden. Pflanzen enthalten Provitamine (Carotine); aus Retinol können alle anderen Formen gebildet werden (Tagesbedarf ~1 mg). Retinal
ist Bestandteil des Rhodopsins (Retinalmangel bedingt Nachtblindheit: retina = Netzhaut),
Oxidation macht es (irreversibel) zu Retinsäure (fetale Morphogenese,
Wachstum und Differenzierung epithelialer Gewebe und blutbildender
Zellen)  Vitamin D (Vit-D-Hormon, Calciferol, Calcitriol) fördert
die Aufnahme und Verwertung von Calcium und Phosphor sowie die
Erhaltung der Knochen- und Muskelsubstanz, unterstützt Kreislauf,
Immunabwehr und Stoffwechsel (Tagesbedarf 15 µg).
Vit.D3 entsteht in der Haut durch UV-B-Licht aus 7-Dehydrocholesterin;
die Leber konvertiert es zu 25(OH), die Niere zu 1,25(OH)2-Vit.D3
(Calcitriol), die biologisch aktive Form. ≥80% des im Körper
befindlichen Vit.D entsteht üblicherweise durch Lichteinwirkung. Die Wirkung hängt
von der Menge verfügbarer Rezeptoren ab (regulierbar), der Serumwert
alleine ist nur begrenzt aussagekräftig
Vitamin D (Vit-D-Hormon, Calciferol, Calcitriol) fördert
die Aufnahme und Verwertung von Calcium und Phosphor sowie die
Erhaltung der Knochen- und Muskelsubstanz, unterstützt Kreislauf,
Immunabwehr und Stoffwechsel (Tagesbedarf 15 µg).
Vit.D3 entsteht in der Haut durch UV-B-Licht aus 7-Dehydrocholesterin;
die Leber konvertiert es zu 25(OH), die Niere zu 1,25(OH)2-Vit.D3
(Calcitriol), die biologisch aktive Form. ≥80% des im Körper
befindlichen Vit.D entsteht üblicherweise durch Lichteinwirkung. Die Wirkung hängt
von der Menge verfügbarer Rezeptoren ab (regulierbar), der Serumwert
alleine ist nur begrenzt aussagekräftig Vitamin E (α-Tokopherol) wirkt
antioxidativ (wie Vit.A, Vit. C) und wird in Fett- und Muskelgewebe gespeichert, sein Fehlen führt zu neurologischen Störungen (Tagesbedarf 12-20 mg α-Tokopherol). Vitamin K (Tagesbedarf 65-70 µg) existiert
als Vit.K1 (Phyllochinon), Vit.K2 (Menachinon), Vit.K3 (Menadion),
Vit.K4 (Menadiolester). Die Leber benötigt Vit.K zur Modifizierung von
Zielproteinen wie Gerinnungsfaktoren (II, VII, IX, X, Protein C und S)
zu Ca++-Chelatoren - bedeutsam auch für den Knochen (Carboxylierung von Osteocalcin in Osteoblasten verbessert die Knochenqualität)
Vitamin E (α-Tokopherol) wirkt
antioxidativ (wie Vit.A, Vit. C) und wird in Fett- und Muskelgewebe gespeichert, sein Fehlen führt zu neurologischen Störungen (Tagesbedarf 12-20 mg α-Tokopherol). Vitamin K (Tagesbedarf 65-70 µg) existiert
als Vit.K1 (Phyllochinon), Vit.K2 (Menachinon), Vit.K3 (Menadion),
Vit.K4 (Menadiolester). Die Leber benötigt Vit.K zur Modifizierung von
Zielproteinen wie Gerinnungsfaktoren (II, VII, IX, X, Protein C und S)
zu Ca++-Chelatoren - bedeutsam auch für den Knochen (Carboxylierung von Osteocalcin in Osteoblasten verbessert die Knochenqualität)  Vitamin B1 (Thiamin; Tagesbedarf
~1 mg)
wird im Kohlenhydratstoffwechsel benötigt (oxidative Decarboxylierung
von α-Ketosäuren). Die Körperspeicher sind gering (20-30 mg) und rasch
erschöpft (biologische Halbwertszeit knapp 2 Wochen).
Der Thiaminstatus lässt sich über die Aktivität der
Erythrozyten-Transketolase abschätzen (ETKA-Test): Das Verhältnis von
stimulierter zu basaler ETKA sollte ≤1,2 sein. Vitamin B2
(Riboflavin; Tagesbedarf ≥1,2 mg) dient dem Energie- und
Eiweißstoffwechsel; im Darm entsteht daraus FAD und Flavinmononukleotid (FMN). FAD-abhängig sind mehrere Enzyme,
z.B. im Citratzyklus. Vitamin B6
(Pyridoxin, Pyridoxal, Pyridoxamin; biologisch aktiv:
Pyridoxalphosphat) ist das bedeutendste Coenzym des
Proteinstoffwechsels (Enzyme wie ALAT und ASAT, Hämoglobinsynthese,
Glykogenabbau, GABA-Synthese u.a.). Der Tagesbedarf (Männer 1,5, Frauen 1,2 mg/d) steigt mit dem Proteinumsatz. Vitamin B12 (Cobalamine; Tagesbedarf 2-3 µg, die Leber speichert bis zu 10 mg; auch die Darmflora bildert Vit.B12)
koppelt im Speichel an Haptocorrin (schützt vor Magensaft), im Duodenum
an Intrinsic Factor (schützt vor Proteasen) und wird im unteren Ileum
resorbiert (rezeptorvermittelte Endozytose mittels Cubilin). An
Transcobalamin II gebunden gelangt es durch den Kreislauf. Vit.B12 wird
(wie Folsäure) für Purin- und Pyrimidinsynthese (DNA) benötigt, für Methylierung und Proteinsynthese,
Fettsäureabbau u.a. Chronischer Vit.B12-Mangel führt zu megaloblastärer
Anämie und neurologischen Veränderungen (funikuläre Myelose). Folsäure (Tagesbedarf 0,3-0,6 mg; 12-15 mg in Leber gespeichert) ist für die DNA-Synthese bedeutsam
Vitamin B1 (Thiamin; Tagesbedarf
~1 mg)
wird im Kohlenhydratstoffwechsel benötigt (oxidative Decarboxylierung
von α-Ketosäuren). Die Körperspeicher sind gering (20-30 mg) und rasch
erschöpft (biologische Halbwertszeit knapp 2 Wochen).
Der Thiaminstatus lässt sich über die Aktivität der
Erythrozyten-Transketolase abschätzen (ETKA-Test): Das Verhältnis von
stimulierter zu basaler ETKA sollte ≤1,2 sein. Vitamin B2
(Riboflavin; Tagesbedarf ≥1,2 mg) dient dem Energie- und
Eiweißstoffwechsel; im Darm entsteht daraus FAD und Flavinmononukleotid (FMN). FAD-abhängig sind mehrere Enzyme,
z.B. im Citratzyklus. Vitamin B6
(Pyridoxin, Pyridoxal, Pyridoxamin; biologisch aktiv:
Pyridoxalphosphat) ist das bedeutendste Coenzym des
Proteinstoffwechsels (Enzyme wie ALAT und ASAT, Hämoglobinsynthese,
Glykogenabbau, GABA-Synthese u.a.). Der Tagesbedarf (Männer 1,5, Frauen 1,2 mg/d) steigt mit dem Proteinumsatz. Vitamin B12 (Cobalamine; Tagesbedarf 2-3 µg, die Leber speichert bis zu 10 mg; auch die Darmflora bildert Vit.B12)
koppelt im Speichel an Haptocorrin (schützt vor Magensaft), im Duodenum
an Intrinsic Factor (schützt vor Proteasen) und wird im unteren Ileum
resorbiert (rezeptorvermittelte Endozytose mittels Cubilin). An
Transcobalamin II gebunden gelangt es durch den Kreislauf. Vit.B12 wird
(wie Folsäure) für Purin- und Pyrimidinsynthese (DNA) benötigt, für Methylierung und Proteinsynthese,
Fettsäureabbau u.a. Chronischer Vit.B12-Mangel führt zu megaloblastärer
Anämie und neurologischen Veränderungen (funikuläre Myelose). Folsäure (Tagesbedarf 0,3-0,6 mg; 12-15 mg in Leber gespeichert) ist für die DNA-Synthese bedeutsam Vitamin C (Ascorbinsäure, Tagesbedarf
~0,1 g) wirkt meist antioxidativ (Redoxsystem, regeneriert auch verbrauchtes Vit.E) und
ist Cofaktor zahlreicher Enzyme (z.B. Kollagensynthese), hilft bei der
Synthese von Noradrenalin, Eisenresorption, Infekabwehr. Biotin (Tagesbedarf 30-60 µg) ist
bedeutsam für Enzymaktivitäten im Protein-, Kohlenhydrat- und
Fettstoffwechsel und im Zellkern (Modifikation von Histonen). Niazin (Nikotinsäure und Nikotinamid - Tagesbedarf 12-15 mg) ist ein Elektronenüberträger: NAD+ bzw. NADP+
für Oxidoreduktasen, Dehydrogenasen / Decarboxylasen,
posttranslationale Modifizierung DNA-gebundener Proteine, beteiligt
sich am Protein-, Kohlenhydrat- und Fettstoffwechsel und an der
Energiebereitstellung im Citratzyklus. 60 mg Tryptophan können 1 mg Nikotinamidäquivalente generieren. Pantothensäure (Tagesbedarf ~6 mg) ist Bestandteil des Coenzyms A (Citratzyklus) und der Fettsäure-Synthase und kommt in der Nahrung praktisch überall vor
Vitamin C (Ascorbinsäure, Tagesbedarf
~0,1 g) wirkt meist antioxidativ (Redoxsystem, regeneriert auch verbrauchtes Vit.E) und
ist Cofaktor zahlreicher Enzyme (z.B. Kollagensynthese), hilft bei der
Synthese von Noradrenalin, Eisenresorption, Infekabwehr. Biotin (Tagesbedarf 30-60 µg) ist
bedeutsam für Enzymaktivitäten im Protein-, Kohlenhydrat- und
Fettstoffwechsel und im Zellkern (Modifikation von Histonen). Niazin (Nikotinsäure und Nikotinamid - Tagesbedarf 12-15 mg) ist ein Elektronenüberträger: NAD+ bzw. NADP+
für Oxidoreduktasen, Dehydrogenasen / Decarboxylasen,
posttranslationale Modifizierung DNA-gebundener Proteine, beteiligt
sich am Protein-, Kohlenhydrat- und Fettstoffwechsel und an der
Energiebereitstellung im Citratzyklus. 60 mg Tryptophan können 1 mg Nikotinamidäquivalente generieren. Pantothensäure (Tagesbedarf ~6 mg) ist Bestandteil des Coenzyms A (Citratzyklus) und der Fettsäure-Synthase und kommt in der Nahrung praktisch überall vor