

Eine Reise durch die Physiologie - Wie der Körper des Menschen funktioniert

Blutdruck, Wasserhaushalt, Säure-Basen-Status

 Elektrolyte
Elektrolyte
© H. Hinghofer-Szalkay
 Chlorid: χλωρóς = hellgrün (Farbe des Chlorgases)
Chlorid: χλωρóς = hellgrün (Farbe des Chlorgases)
Hodgkin-Huxley-Gleichungen zum Membranpotential: Alan L. Hodgkin, Andrew F. Huxley
Kalium: القلية "al-qalya", Pflanzenasche
Mineral: aes minerale = Grubenerz (mina = Mine)
Natrium: ناترون "natrun“, Natron
Kalium ist das "Leitkation" des intrazellulären Raums (~150 mM/l, extrazellulär 4-5 mM/l). Seine Tendenz, aus der Zelle zu diffundieren, lädt diese elektrisch auf (Ruhepotential, weitgehend identisch mit dem Kalium-Gleichgewichtspotential).
Natrium hingegen ist das Leitkation des extrazellulären
Raums (140-145 mM/l, intrazellulär meist um die 10 mM/l). Damit ist es
- zusammen mit Begleitanionen, wie Chlorid - hauptverantwortlich für
Osmolalität und Volumen des Extrazellulärraums.
Der Hauptmotor der Ungleichverteilung zwischen Intra- und Extrazellulärraum ist die Natrium-Kalium-Pumpe.
Diese steht unter regulativen Einflüssen, wie auch andere
Transportermoleküle und Permeasen; so nimmt unter Aldosteronwirkung der
Einbau von Natriumkanälen (ENaC) in die Nierentubuli - und die
Natrium-Rückresorption - zu.
Über die Referenzbereiche hinaus veränderte Natrium- und Kaliumwerte im Blutplasma signalisieren Elektrolytstoffwechselstörungen.
Diese treten auf, wenn Zu- und Abfluss der Alkalimetalle nicht ausbalanciert sind. Die Nieren sind der primäre Ort der
Regulation; Aldosteron - eines der wenigen wirklich lebenswichtigen Hormone - ist der führende endokrine Player im Salzhaushalt. Erhöhter extrazellulärer Kaliumspiegel (Hyperkaliämie)
regt hormonelle Antworten an (Insulin, Adrenalin, Aldosteron -
Steigerung der Na-K-Pumpaktivität), die den Transport von Kalium in die
Zellen verstärkt und damit den Kaliumspiegel korrigiert.
Abweichungen der Elektrolytwerte können typische Veränderungen im Kammerteil des EKG erzeugen.
|
Natrium / Chlorid  Kalium
Kalium  Elektrolyte und EKG
Elektrolyte und EKG
 Praktische Aspekte
Praktische Aspekte  Core messages
Core messages
Mineralstoffe
 sind im Körper unverzichtbar. Zu ihnen
gehören Natrium
sind im Körper unverzichtbar. Zu ihnen
gehören Natrium  (sodium), Chlor
(sodium), Chlor  , Kalium
, Kalium  (potassium), Calcium, Magnesium, Phosphor und
Schwefel. Ihre
tägliche Zufuhrmenge liegt beim Erwachsenen im Gramm-Bereich (>0,1 g/d).
(potassium), Calcium, Magnesium, Phosphor und
Schwefel. Ihre
tägliche Zufuhrmenge liegt beim Erwachsenen im Gramm-Bereich (>0,1 g/d).

Ursache für die unterschiedliche Konzentration von Natrium- und Kalium-Ionen im Körper (extra- vs. intrazellulär) ist in erster Linie die Na+-K+-ATPase. Sie ist der einzige aktive
Transporteur für Natrium (aus der Zelle) und der wichtigste für Kalium
(in die Zelle). Natrium ist das Leitkation der extrazellulären, Kalium das der intrazellulären Flüssigkeiten.

Zur
Funktionsweise der Na/K-ATPase s.
dort
Natrium und Chlorid: Die Regulation von Kochsalz
1 mol Kochsalz (NaCl) sind 58,5 g (Atomgewicht Na: 23, Cl 35,5). 1 g Kochsalz besteht aus 0,393 (23/58,5) g Natrium und 0,607 (35,5/58.5) g Chlor (Gewichtsverhältnis etwa 2:3). Der Körper enthält ~58 mM/kg KG Natrium und ~33 mM/kg KG Chlorid. Die Aufnahme von Natrium erfolgt über die Nahrung, die Ausscheidung überwiegend über den Harn.
 Freies Na+ (bei 70 kg Körpermasse etwa 2 Mol oder ~46 g) findet sich im Körper zum Großteil als NaCl, zu einem kleineren als Bicarbonat (NaHCO3) und in anderen Natriumsalzen. Na+ ist osmotisch aktiv und mit der Osmoregulation direkt verknüpft. Natrium ist u.a. auch für die Auslösung der meisten Aktionspotentiale
ausschlaggebend.
Freies Na+ (bei 70 kg Körpermasse etwa 2 Mol oder ~46 g) findet sich im Körper zum Großteil als NaCl, zu einem kleineren als Bicarbonat (NaHCO3) und in anderen Natriumsalzen. Na+ ist osmotisch aktiv und mit der Osmoregulation direkt verknüpft. Natrium ist u.a. auch für die Auslösung der meisten Aktionspotentiale
ausschlaggebend.
 Etwa die gleiche Menge gebundenes, vor allem im Knochen gespeichertes Natrium ist nicht direkt in die Osmoregulation eingebunden.
Etwa die gleiche Menge gebundenes, vor allem im Knochen gespeichertes Natrium ist nicht direkt in die Osmoregulation eingebunden.
Natriumionen sind an Nervenleitung, Muskelfunktion (Aktionspotentiale), Sekretionsvorgängen und Flüssigkeitsbilanz beteiligt. Natrium ist weiters involviert in die Resorption von Nährstoffen aus dem Darm und in der Niere: Glucose, Galactose (über SGLT1) und Aminosäuren
werden über die apikale Membran der Enterozyten via Cotransport
(Symport) in die Zellen aufgenommen. Das gilt auch für die tubuläre
Rückresorption der genannten Stoffe in den Nieren (s. dort).
Die physiologische Bandbreite der täglichen Natriumzufuhr ist relativ gering:
 Einerseits führt chronische
Unterversorgung mit Kochsalz (auch bei maximaler
Aldosteronwirkung) zu Hypotonizität, Hypovolämie und Hypotonie,
schließlich zu Kreislaufversagen
Einerseits führt chronische
Unterversorgung mit Kochsalz (auch bei maximaler
Aldosteronwirkung) zu Hypotonizität, Hypovolämie und Hypotonie,
schließlich zu Kreislaufversagen
 Andererseits
können größere Mengen die Osmo- und Volumenregulation überfordern, da
der Körper nicht auf die Ausscheidung von hochkonzentriertem Salz
angepasst ist. Zwar kann die Niere die Ausscheidung der Zufuhr anpassen
(je mehr Kochsalz zugeführt wird, desto geringer ist die
Aldosteronbildung, und es wird mehr Natrium ausgeschieden), aber dies
funktioniert nur in einem relativ begrenzten Osmolaritätsbereich.
Andererseits
können größere Mengen die Osmo- und Volumenregulation überfordern, da
der Körper nicht auf die Ausscheidung von hochkonzentriertem Salz
angepasst ist. Zwar kann die Niere die Ausscheidung der Zufuhr anpassen
(je mehr Kochsalz zugeführt wird, desto geringer ist die
Aldosteronbildung, und es wird mehr Natrium ausgeschieden), aber dies
funktioniert nur in einem relativ begrenzten Osmolaritätsbereich.
 Die tägliche Natriumzufuhr sollte 1 g/d (0,5-1,5 Gramm) betragen; oft
werden diese Werte deutlich überschritten ("Nachsalzen").
Die tägliche Natriumzufuhr sollte 1 g/d (0,5-1,5 Gramm) betragen; oft
werden diese Werte deutlich überschritten ("Nachsalzen").

 Abbildung: Durchschnittliche Verteilungs- und Umsatzwerte von Natrium im Körper einer erwachsenen Person
Abbildung: Durchschnittliche Verteilungs- und Umsatzwerte von Natrium im Körper einer erwachsenen Person
Nach einer Vorlage in Boron / Boulpaep, Medical Physiology, 1st ed. Saunders 2003
Angenommen ist ein minimaler Schweißverlust (perspiratio insensibilis)
 Natrium
Plasma, Serum 135-145 mM
Schweiß: 5-35 mM
Natrium
Plasma, Serum 135-145 mM
Schweiß: 5-35 mM
 Ausscheidung mit dem Harn: 100-250 mmol/24 h
Ausscheidung mit dem Harn: 100-250 mmol/24 h
 Chlorid
Plasma, Serum 98-107 mM
Chlorid
Plasma, Serum 98-107 mM
 Ausscheidung mit dem Harn:
Erwachsene 40-250 mmol/24 h
Kinder 20-115 mmol/24 h
Ausscheidung mit dem Harn:
Erwachsene 40-250 mmol/24 h
Kinder 20-115 mmol/24 h
In den Zellen ist die Natriumkonzentration unterschiedlich, aber generell niedrig; ~10 mM/l Zytosol ist ein typischer Wert.
Es besteht ein Na-Konzentrationsgradient von etwa 14:1 in Richtung
Zellinneres. Dieser Gradient treibt die Depolarisierungsphase der
meisten erregbaren Zellen an ( Abbildung oben).
Abbildung oben).
Natriummangel (Hyponatriämie) kann durch Erbrechen, Durchfall oder
Verluste über die Nieren bedingt sein und äußert sich in Muskelschwäche
und herabgesetztem Blutdruck.
 Der Natriumspiegel (und die Natriumkonzentration in diversen Körperflüssigkeiten) wird über mehrere Methoden bestimmt: Flammenphotometrie als Referenzmethode (angeregte Natriumatome emittieren Licht von 589.3 nm Wellenlänge), potentiometrisch (ionenselektive Elektroden), oder enzymatisch (Spektrophotometrie).
Der Natriumspiegel (und die Natriumkonzentration in diversen Körperflüssigkeiten) wird über mehrere Methoden bestimmt: Flammenphotometrie als Referenzmethode (angeregte Natriumatome emittieren Licht von 589.3 nm Wellenlänge), potentiometrisch (ionenselektive Elektroden), oder enzymatisch (Spektrophotometrie).
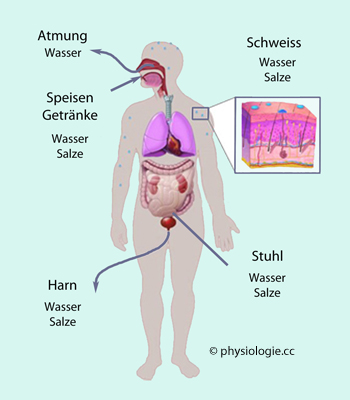

Abbildung: Einstellung der Natrium (Salz)- und Wasserbilanz
Nach Ruginsk SG et al, Gaseous modulators in the
control of the hypothalamic neurohypophyseal system. Physiology 2015;
30: 127‐38
Das
Bild zeigt Orte der Aufnahme und Ausscheidung von Wasser und
Elektrolyten. Die Zufuhr erfolgt hauptsächlich über den Darm
(metabolisches Oxidationswasser ~300 ml/d), die Ausscheidung hauptsächlich über die Nieren (Exspirationsluft ~350 ml/d, Schweiß - der auch etwas Natrium enthält - je nach thermoregulatorischen Anforderungen)

 Kochsalz kann bei intensivem Schwitzen in erheblichen Mengen
verlorengehen. So bedeutet z.B. die Sekretion von 5 l Schweiß einen
Verlust von ~300 mM Natrium und ~220 mM Chlorid, das bedeutet fast 15
Gramm Kochsalz. Im Extrazellulärraum bindet diese Menge Salz ein
Volumen von mehr als 1,5 Liter Wasser (Schweiß ist hypoton).
Kochsalz kann bei intensivem Schwitzen in erheblichen Mengen
verlorengehen. So bedeutet z.B. die Sekretion von 5 l Schweiß einen
Verlust von ~300 mM Natrium und ~220 mM Chlorid, das bedeutet fast 15
Gramm Kochsalz. Im Extrazellulärraum bindet diese Menge Salz ein
Volumen von mehr als 1,5 Liter Wasser (Schweiß ist hypoton).
Der effizienteste Weg, eine Dehydrierung durch z.B. Hitzeeinwirkung
oder körperliche Arbeit auszugleichen, ist die Aufnahme von Wasser und
einer entsprechenden Menge Salz (Rehydrierungsgetränk; gesalzene Suppe
bei Diarrhoe etc). Die aufgenommene Menge Kochsalz steuert über die Osmoregulation
automatisch die Bindung eines entsprechenden Flüssigkeitsvolumens, das
im Wesentlichen im Extrazellulärraum verbleibt, soferne nicht die Volumenregulation Überschussflüssigkeit wieder aus dem Körper entfernt.
Die Dynamik des NaCl-Austausches im Körper ist in der Abbildung links
oben gezeigt. Während die tägliche Aufnahme mit der Nahrung in der
Größenordnung von 120 mM Natrium (entsprechend knapp 2,8 g Na oder 7
Gramm Kochsalz) liegt, tauscht die Niere in 24 Stunden die unglaubliche
Menge von fast 1,5 kg Kochsalz aus (im gezeigten Beispiel werden 99,6%
der glomerulär filtrierten Menge rückresorbiert, nur 0,4%
ausgeschieden).
Die Regulierung des Natriumhaushalts erfolgt
 vegetativ (der Sympathikus
fördert Kochsalzkonservierung im Körper) und
vegetativ (der Sympathikus
fördert Kochsalzkonservierung im Körper) und
 hormonell (Aldosteron, natriuretische Peptide, Adrenomedullin).
hormonell (Aldosteron, natriuretische Peptide, Adrenomedullin).
Das meiste Natrium wird im Dünndarm ("externes", mit der Nahrung zugeführtes Na+) und in der Niere aufgenommen ("internes", nach der glomerulären Filtration aus dem Tubulus re-absorbiertes Na+). Der proximale Tubulus nimmt den Großteil des filtrierten Natriums auf. Daran sind mehrere Transporter beteiligt; der wichtigste ist der Na+-H+-Austauscher NHE3 (sodium and hydrogen exchanger 3),
der an der apikalen Membran Natrium aufnimmt und Wasserstoffionen
ausscheidet. NHE3 bewirkt insgesamt (direkt, und indirekt über die
Bildung eines Chlorid-Gradienten) ~70% der Natriumresorption und ~90%
der Bicarbonatresorption des proximalen Tubulus. Damit ist dieser
Transporter am Zurückgewinnen von Natrium, an der Einstellung des Blutdrucks und an der pH-Regulation beteiligt.
 "Physiologische (isotone) Kochsalzlösung" (Grundlage für Infusionslösungen) ist 0,9%-ig, d.h. 1 Liter enthält 9 g NaCl.
"Physiologische (isotone) Kochsalzlösung" (Grundlage für Infusionslösungen) ist 0,9%-ig, d.h. 1 Liter enthält 9 g NaCl.
Der
Ursprung der meisten Elemente liegt in kosmischen Kernfusionsvorgängen,
die sehr hohe Dichte- und Temperaturwerte voraussetzen. So entsteht Kalium in massiven Sternen (≥1010 kg/m3) aus Sauerstoff bei Temperaturen von über einer Milliarde Grad (1.5×109
K / 130 keV). Dann wird es zusammen mit anderen,
ebenfalls durch Kernfusion entstandenen Elementen in das angrenzende
Universum verteilt (Supernova-Explosionen). Aus solchem "Sternenstaub" können Planeten
entstehen und (zumindest im Falle der Erde) als chemische Grundlage für lebende
Systeme dienen. Dabei kommt es zur "Sortierung" verschiedener Ionen entsprechend ihrer Funktionen in der Zelle.


Abbildung: Kaliumbestände und -umsatz im Körper einer erwachsenen Person
Nach einer Vorlage in Boron / Boulpaep, Medical Physiology, 1st ed. Saunders 2003

Membrantransportsysteme unterscheiden zwischen verschiedenen Ionen (Na, K, Ca...)
und ermöglichen selektiven, gerichteten Transport - und damit Anreicherung in
Kompartimenten, im Fall des Kaliums im Intrazellulärraum.
Kalium kommt in der Geosphäre seltener vor als Natrium; im Meerwasser
beträgt seine Konzentration 0,4 g/l, d.h. fast 30mal weniger als
Natrium.
Die Kaliumzufuhr mit der Ernährung ist dennoch meist
ausreichend, die Niere scheidet sogar überschüssiges Kalium aus; Grund
ist die Tatsache, dass Kalium generell in organischem Material (als "Leitkation" des Intrazellulärraums) vorliegt.

Zur
Bestimmung des intrazellulären Flüssigkeitsvolumens s.
dort
Kaliumpool und Kalium-Umsatz:
Der Großteil (98%) des Körperkaliums
befindet sich in den Zellen (beim Erwachsenen 3000-4000 mmol),
extrazellulär
finden sich nur 2% (~65 mmol,  Abbildung). Die tägliche Aufnahme mit
der Nahrung beträgt ~120 mmol (im steady state
verlassen 10% davon den
Körper über den Stuhl, 90% über den Harn). Das bedeutet, dass pro Tag
3-4% des im Körper vorhandenen Kaliums ausgeschieden werden (und
dieselbe Menge mit der Nahrung resorbiert wird).
Abbildung). Die tägliche Aufnahme mit
der Nahrung beträgt ~120 mmol (im steady state
verlassen 10% davon den
Körper über den Stuhl, 90% über den Harn). Das bedeutet, dass pro Tag
3-4% des im Körper vorhandenen Kaliums ausgeschieden werden (und
dieselbe Menge mit der Nahrung resorbiert wird).
Funktionen: Kalium ist mit ~150 mM in der intrazellulären Flüssigkeit das
Leitkation in den Zellen.
Es baut das Ruhepotential auf und beteiligt sich allgemein an
elektrophysiologischen Vorgängen sowie am Säure-Basen-Gleichgewicht.
Bei ausgeglichener Kost nimmt man pro 1000
Kalorien zwischen 0,8 und 1,5 Gramm Kalium zu sich. Die wichtigsten
Kaliumquellen in unserer Kost sind Kartoffeln, Obst, Gemüse, Fleisch.
Zum tatsächlichen täglichen Kaliumbedarf des Organismus gibt es keine
verlässlichen Ansatzpunkte (1,9-5,6 g/d?).
 Kalium
Kalium
Plasma 3,5-4,5 mM, Serum 3,5-5,1 mM
Neugeborene 3,7-5,9 mM, Kleinkinder 4,1-5,3 mM

Ausscheidung mit dem Harn 35-100 mmol/24 h
Die Kaliumkonzentration in der Zelle ist hoch (≥120 mM/l), bedingt durch die Tätigkeit der Na-K-Pumpe.
Kaliummangel entsteht durch
verstärkte Verluste über die Nieren (harntreibende Mittel, verstärkte
Aldosteronwirkung), Erbrechen oder Durchfall; Folgen sind
Muskelschwäche oder Herzrhythmusstörungen.
 Der Kaliumspiegel im Blutserum (und die Kaliumkonzentration in anderen
Körperflüssigkeiten, insbesondere Urin) wird - wie bei Natrium - über
mehrere Methoden bestimmt: Flammenphotometrie als Referenzmethode (Emissionswellenlänge 766.5 nm), potentiometrisch (ionenselektive Elektroden - Valinomycin als Elektrophor), oder enzymatisch (Spektrophotometrie).
Der Kaliumspiegel im Blutserum (und die Kaliumkonzentration in anderen
Körperflüssigkeiten, insbesondere Urin) wird - wie bei Natrium - über
mehrere Methoden bestimmt: Flammenphotometrie als Referenzmethode (Emissionswellenlänge 766.5 nm), potentiometrisch (ionenselektive Elektroden - Valinomycin als Elektrophor), oder enzymatisch (Spektrophotometrie).
 Über die Art und Weise, wie
die Niere angesichts unterschiedlicher diätetischer Versorgung mit
Kalium umgeht, s. dort
Über die Art und Weise, wie
die Niere angesichts unterschiedlicher diätetischer Versorgung mit
Kalium umgeht, s. dort


Abbildung: Hyperkaliämie bewirkt Kaliumverlagerung in die Muskulatur
Nach einer Vorlage in Boron / Boulpaep, Medical Physiology, 1st ed. Saunders 2003
Plötzliche Hyperkaliämie
(im Bild rechts angedeutet) regt ß-Zellen im Pankreas zur Ausschüttung von Insulin, und Zellen der
Nebenniere zur Produktion von Adrenalin und Aldosteron an. Insulin, Adrenalin und Aldosteron verlagern Kalium in Muskelzellen, indem sie die
Na/K-Pumpe anregen, was
Kalium in den Intrazellulärraum verlagert und den Serum-Kaliumspiegel
weniger stark ansteigen lässt (dämpfender Effekt auf den
Kalium-Plasmaspiegel).
Schadhafte Regelmechanismen (z.B. Diabetes mellitus,
Hypertension mit kompromittiertem Reninsystem) oder Medikamente wie
beta-Blocker schwächen die zelluläre Kalium-Pufferung und können eine
Neigung zu Hyperkaliämie bedingen, was im Extremfall zu Herzstillstand führen kann

Die wichtigsten hormonellen Faktoren zur Regulierung des Kaliumhaushalts sind Insulin, Katecholamine und Aldosteron. Erhöhung des Plasma-Kaliumspiegels triggert die Sekretion von Insulin, Adrenalin und Aldosteron ( Abbildung):
Abbildung):
 Insulin (aus Betazellen der Bauchspeicheldrüse) steigert die Glucose- und Kaliumaufnahme in die Zelle (→ Kaliumspiegel sinkt) und wirkt kaliumkonservierend. Glucocorticoide - die "Gegenspieler" des Insulins - regen die Kaliumausscheidung meist an; sie tun das durch Erhöhung der glomerulären Filtration und damit Steigerung der distalen Durchflussrate im Nephron (
Insulin (aus Betazellen der Bauchspeicheldrüse) steigert die Glucose- und Kaliumaufnahme in die Zelle (→ Kaliumspiegel sinkt) und wirkt kaliumkonservierend. Glucocorticoide - die "Gegenspieler" des Insulins - regen die Kaliumausscheidung meist an; sie tun das durch Erhöhung der glomerulären Filtration und damit Steigerung der distalen Durchflussrate im Nephron ( vgl. dort).
vgl. dort).
 Adrenalin (aus dem Nebennierenmark) bewirkt zunächst Kaliumausstrom aus den Zellen (α-Rezeptoren in der Leber öffnen calciumabhängige Kaliumkanäle → Kaliumspiegel steigt) und dann Kaliumaufnahme in die Zellen (ß-Rezeptoren im Muskelgewebe regen die Na/K-Pumpe an → Kaliumspiegel sinkt),
dies ist der länger anhaltende Effekt. Durch die vermehrte Aufnahme von
Kalium in die Körperzellen einerseits, Inhibition der Kaliumsekretion
in distalen Nephronabschnitten andererseits senkt Adrenalin die Kaliumausscheidung.
Adrenalin (aus dem Nebennierenmark) bewirkt zunächst Kaliumausstrom aus den Zellen (α-Rezeptoren in der Leber öffnen calciumabhängige Kaliumkanäle → Kaliumspiegel steigt) und dann Kaliumaufnahme in die Zellen (ß-Rezeptoren im Muskelgewebe regen die Na/K-Pumpe an → Kaliumspiegel sinkt),
dies ist der länger anhaltende Effekt. Durch die vermehrte Aufnahme von
Kalium in die Körperzellen einerseits, Inhibition der Kaliumsekretion
in distalen Nephronabschnitten andererseits senkt Adrenalin die Kaliumausscheidung.
 Aldosteron (aus der zona glomerulosa der Nebennierenrinde)
regt (innerhalb von Stunden) die basolaterale Na/K-ATPase an, wodurch
mehr Kalium in die spätdistalen Tubulus- und Sammelrohrepithelzellen
aufgenommen werden kann. Weiters steigert Aldosteron die Expression
apikaler Natriumkanäle (ENaCs) und fördert damit indirekt die Kaliumsekretion (
Aldosteron (aus der zona glomerulosa der Nebennierenrinde)
regt (innerhalb von Stunden) die basolaterale Na/K-ATPase an, wodurch
mehr Kalium in die spätdistalen Tubulus- und Sammelrohrepithelzellen
aufgenommen werden kann. Weiters steigert Aldosteron die Expression
apikaler Natriumkanäle (ENaCs) und fördert damit indirekt die Kaliumsekretion ( vgl. dort).
vgl. dort).
Insgesamt funktioniert die Gegenregulation bei Hyperkaliämie gestaffelt in zwei Stufen:
 Kurzzeitregulation (Kalium in die Zellen): Anregung der Na-K-Pumpe verlagert vermehrt Kalium aus dem
Extra- in den Intrazellulärraum
Kurzzeitregulation (Kalium in die Zellen): Anregung der Na-K-Pumpe verlagert vermehrt Kalium aus dem
Extra- in den Intrazellulärraum
 Längerfristige Regulation (Kalium in die Umwelt): Erhöhung der Kaliumausscheidung (Erfolgsorgan Niere
Längerfristige Regulation (Kalium in die Umwelt): Erhöhung der Kaliumausscheidung (Erfolgsorgan Niere  s. dort).
s. dort).
Der Plasma-Kaliumspiegel steigt auch bei starker körperlicher Arbeit, z.T. durch Beschädigung von Zellen (u.a. Erythrozyten) mit Kaliumaustritt.
 Veränderungen des pH-Wertes im extrazellulären Raum beeinflussen den Kaliumhaushalt: Azidämie
steigert (Hyperkaliämie), Alkaliämie senkt den Kaliumspiegel im
Blutplasma (Hypokaliämie). Das ist klinisch wichtig, weil Maßnahmen zur
Änderung des pH im Blut (externe Pufferung) automatisch den
Kalliumspiegel ändern. Wie funktioniert das?
Veränderungen des pH-Wertes im extrazellulären Raum beeinflussen den Kaliumhaushalt: Azidämie
steigert (Hyperkaliämie), Alkaliämie senkt den Kaliumspiegel im
Blutplasma (Hypokaliämie). Das ist klinisch wichtig, weil Maßnahmen zur
Änderung des pH im Blut (externe Pufferung) automatisch den
Kalliumspiegel ändern. Wie funktioniert das?
Wasserstoffionen dringen bei Azidose vermehrt durch die Zellmembran und
senken den intrazellulären pH (die "externe" Azidose säuert auch den
Intrazellulärraum an). Dies hemmt Kaliumtransporter (Na/K-Pumpe, NKCC2) in der Zellmembran. Azidose senkt daher die Aufnahme von Kalium in die Zelle und führt zu einer Umverlagerung von Kalium aus dem Intra- in den Extrazellulärraum, was Hyperkaliämie bewirken kann (umgekehrt senkt Alkalose den Kaliumspiegel).
 Abbildung dazu s. dort
Abbildung dazu s. dort
 Behandlung einer Azidose (Infusion von Pufferbasen) kann eine gleichzeitig bestehende Hyperkaliämie zum Verschwinden bringen.
Behandlung einer Azidose (Infusion von Pufferbasen) kann eine gleichzeitig bestehende Hyperkaliämie zum Verschwinden bringen.

Azidose senkt, Alkalose erhöht die Kaliumausscheidung - vorwiegend über die nephron-distale Kaliumsekretion. Vermutlich ist die Urasche eine pH-abhängige Wirkung auf apikale K+-Kanäle sowie die basolaterale Na/K-Pumpe.

Über
Ca++ und
Mg++ siehe
dort
Elektrolyte und EKG
Elektrolytstörungen (K+, Ca++) machen sich im EKG bemerkbar ( Abbildung):
Abbildung):

 Abbildung: EKG-Veränderungen bei erniedrigtem (oben) und erhöhtem Kaliumspiegel (unten)
Abbildung: EKG-Veränderungen bei erniedrigtem (oben) und erhöhtem Kaliumspiegel (unten)
Nach einer Vorlage in Rolf Heinecker, EKG in Praxis und Klinik, 12. Aufl, Thieme Verlag
Kaliumwerte in mM.
Absinken des Kaliumspiegels (oben) führt zu Abflachung oder Negativierung der T-Welle, eine U-Welle kann auftreten, vor allem bei extremer Hypokaliämie.
Bei gesteigertem Kaliumspiegel (unten) flacht die P-Welle ab, der QRS-Komplex wird weiter, die T-Welle wird höher und spitzt sich zu

 Hypokaliämie bedingt
Senkungen der ST-Strecke, Abflachung der T- und Auftreten einer U-Welle;
Hypokaliämie bedingt
Senkungen der ST-Strecke, Abflachung der T- und Auftreten einer U-Welle;
 Hyperkaliämie spitze ("zeltförmige") T-Wellen und (ab ~8 mM
Serumkalium) schwere Veränderungen vor allem im Kammerteil. Starke Hyperkaliämie kann zu akutem
Herz-Kreislaufversagen führen und lebensgefährlich sein;
Hyperkaliämie spitze ("zeltförmige") T-Wellen und (ab ~8 mM
Serumkalium) schwere Veränderungen vor allem im Kammerteil. Starke Hyperkaliämie kann zu akutem
Herz-Kreislaufversagen führen und lebensgefährlich sein;
 Hypocalcämie verursacht eine Verlängerung der QT-Strecke,
Hypocalcämie verursacht eine Verlängerung der QT-Strecke,
 Hypercalcämie hingegen eine Verkürzung der QT-Strecke.
Hypercalcämie hingegen eine Verkürzung der QT-Strecke.
Störungen des
Wasser- und Elektrolythaushalts werden durch Faktoren verursacht,
welche die Aufnahme, Ausscheidung und Verteilung von Wasser und
Elektrolyten beeinflussen. Störungen der Regulation von Wasser,
Natrium, Kalium und pH treten meist kombiniert auf.
Lost at sea: Die
Natriumkonzentration von Meerwasser
beträgt ~11 g/l (Blutplasma 3,5 g/l). Die Niere ist nicht in der Lage,
derart konzentriertes Kochsalz auszuscheiden, ohne dass es zu
einem zusätzlichen Verlust an Wasser kommt (Harnstoff muss
ausgeschieden werden). Die Aufnahme von Meerwasser
alleine (ohne Süßwasser) führt zu hypertoner Dehydration und nach
einiger Zeit zu Kreislaufversagen.
Akuter Natriummangel tritt bei intensivem Verlust von
Körperflüssigkeiten auf (Verbrennungen, intensives Erbrechen, starker
Durchfall). Die Folge ist insbesondere Kreislaufschwäche; Ersatz durch
Kochsalzinfusion ist erforderlich.
 Azidose führt zum Austritt von Kaliumionen aus den Zellen und
Hyperkaliämie, und Hyperkaliämie treibt Wasserstoffionen aus den
Zellen, was Azidose zur Folge hat. Bei Alkalose ist es umgekehrt. Über den
zugrunde liegenden Mechanismus
Azidose führt zum Austritt von Kaliumionen aus den Zellen und
Hyperkaliämie, und Hyperkaliämie treibt Wasserstoffionen aus den
Zellen, was Azidose zur Folge hat. Bei Alkalose ist es umgekehrt. Über den
zugrunde liegenden Mechanismus  s. dort.
s. dort.
Praktische Bedeutung: Behandelt man eine Azidose,
wird dadurch eine allfällig gleichzeitig vorhandene Hyperkaliämie
automatisch gelindert. Behandlung einer normokaliämischen Alkalose
hingegen kann zu Hyperkaliämie führen.
Hypokaliämie erhöht die Säureausscheidung in der Niere und bewirkt
metabolische Alkalose. Umgekehrt kann Hyperkaliämie zu metabolischer
Azidose führen, vielleicht aufgrund verringerter Ammoniumausscheidung.
 Ursache für eine Hyperkaliämie
kann u.a. extreme Muskelbelastung, Insulinmangel, verminderte
Ausscheidung in der Niere, hohe Katecholaminwirkung
(α-Adreno-Agonisten) oder Zerstörung von Zellen (z.B. bei
Verbrennungen, Hämolyse) sein.
Ursache für eine Hyperkaliämie
kann u.a. extreme Muskelbelastung, Insulinmangel, verminderte
Ausscheidung in der Niere, hohe Katecholaminwirkung
(α-Adreno-Agonisten) oder Zerstörung von Zellen (z.B. bei
Verbrennungen, Hämolyse) sein.
Hypokaliämie kann verursacht sein z.B. durch Hyperaldosteronismus (erhöhte
Kaliumausscheidung in der Niere), Durchfall (gesteigerter Verlust mit
dem Stuhl), Insulin-Überdosierung (übertriebene Kaliumaufnahme in
insulinabhängige Zellen), nicht-kaliumschonende Diuretika, oder auch
Bulimie. Chronischer Kaliummangel führt zu degenerativen Erscheinungen
an Herz- und Skelettmuskel.


 Natrium in der extrazellulären Flüssigkeit (~140 mM/l) bestimmt dessen Volumen. Der Körper einer erwachsenen Person enthält
~100 g Na, etwa die Hälfte davon ist im Knochen gespeichert (osmoregulatorisch inaktiv). Natrium beteiligt sich an Nervenleitung, Muskelfunktion (Aktionspotentiale), Sekretionsvorgängen und Flüssigkeitsbilanz. Die tägliche Natriumzufuhr sollte
~1 g/d betragen,
um das extrazelluläre Volumen stabil zu halten (chronischer Salzmangel
führt trotz maximaler Aldosteronwirkung zu Hypovolämie und
Kreislaufversagen). Andererseits können größere Mengen die
Osmo- und Volumenregulation überfordern. Pro Liter Schweiß verliert man ~3 g Kochsalz; Hyponatriämie
senkt den Blutdruck und bewirkt Muskelschwäche. Die Regulierung des
Natriumhaushalts erfolgt nervös (Sympathikusaktivität hält NaCl im Körper)
und hormonell (Aldosteron hält Natrium im Körper, natriuretische Peptide scheiden Natrium aus). Physiologische Kochsalzlösung ist isoton (9 g NaCl/l; 0,9%-ig) Natrium in der extrazellulären Flüssigkeit (~140 mM/l) bestimmt dessen Volumen. Der Körper einer erwachsenen Person enthält
~100 g Na, etwa die Hälfte davon ist im Knochen gespeichert (osmoregulatorisch inaktiv). Natrium beteiligt sich an Nervenleitung, Muskelfunktion (Aktionspotentiale), Sekretionsvorgängen und Flüssigkeitsbilanz. Die tägliche Natriumzufuhr sollte
~1 g/d betragen,
um das extrazelluläre Volumen stabil zu halten (chronischer Salzmangel
führt trotz maximaler Aldosteronwirkung zu Hypovolämie und
Kreislaufversagen). Andererseits können größere Mengen die
Osmo- und Volumenregulation überfordern. Pro Liter Schweiß verliert man ~3 g Kochsalz; Hyponatriämie
senkt den Blutdruck und bewirkt Muskelschwäche. Die Regulierung des
Natriumhaushalts erfolgt nervös (Sympathikusaktivität hält NaCl im Körper)
und hormonell (Aldosteron hält Natrium im Körper, natriuretische Peptide scheiden Natrium aus). Physiologische Kochsalzlösung ist isoton (9 g NaCl/l; 0,9%-ig)
 Die alimentäre Zufuhr von Kalium (mit ~150 mM Leitkation des Intrazellulärraums) ist meist ausreichend (die Nieren scheiden überschüssiges Kalium aus). Die Zellen einer erwachsenen Person enthalten zusammen
~150 g Kalium, täglich werden
~5 g aufgenommen.
Kalium wird von der Na/K-ATPase intrazellulär angereichert, baut das
Ruhepotential auf (Auswärtsdiffusion) und beteiligt sich am
Säure-Basen-Gleichgewicht (Azidose senkt die Aufnahme von Kalium in die Zelle → Umverlagerung in den Extrazellulärraum; umgekehrt senkt Alkalose den Kaliumspiegel). Behandlung einer Azidose kann eine gleichzeitig bestehende Hyperkaliämie zum Verschwinden bringen (weniger H+ → mehr K+ in der Zelle). Hyperkaliämie (z.B.infolge intensiver Muskelbelastung) regt das Pankreas zu Insulinsekretion an (zelluläre K+-Aufnahme↑→ Kaliumspiegel sinkt), die
Nebennierenrinde zur Aldosteronsynthese
(Aldosteron fördert die Kaliumsekretion → Kaliumspiegel sinkt), das
Nebennierenmark zu Adrenalinsekretion (muskuläre ß-Rezeptoren regen die
Na/K-ATPase an → Kaliumspiegel sinkt anhaltend) Die alimentäre Zufuhr von Kalium (mit ~150 mM Leitkation des Intrazellulärraums) ist meist ausreichend (die Nieren scheiden überschüssiges Kalium aus). Die Zellen einer erwachsenen Person enthalten zusammen
~150 g Kalium, täglich werden
~5 g aufgenommen.
Kalium wird von der Na/K-ATPase intrazellulär angereichert, baut das
Ruhepotential auf (Auswärtsdiffusion) und beteiligt sich am
Säure-Basen-Gleichgewicht (Azidose senkt die Aufnahme von Kalium in die Zelle → Umverlagerung in den Extrazellulärraum; umgekehrt senkt Alkalose den Kaliumspiegel). Behandlung einer Azidose kann eine gleichzeitig bestehende Hyperkaliämie zum Verschwinden bringen (weniger H+ → mehr K+ in der Zelle). Hyperkaliämie (z.B.infolge intensiver Muskelbelastung) regt das Pankreas zu Insulinsekretion an (zelluläre K+-Aufnahme↑→ Kaliumspiegel sinkt), die
Nebennierenrinde zur Aldosteronsynthese
(Aldosteron fördert die Kaliumsekretion → Kaliumspiegel sinkt), das
Nebennierenmark zu Adrenalinsekretion (muskuläre ß-Rezeptoren regen die
Na/K-ATPase an → Kaliumspiegel sinkt anhaltend)
 Elektrolytstörungen beeinflussen das EKG: Hypokaliämie → Senkung der ST-Strecke, Abflachung der T- und Auftreten einer U-Welle; Hyperkaliämie → zeltförmige T-Wellen, ab ~8 mM Veränderungen im Kammerteil (evt. Herz-Kreislauf- Versagen); Hypocalcämie → Verlängerung der QT-Strecke; Hypercalcämie → Verkürzung der QT-Strecke Elektrolytstörungen beeinflussen das EKG: Hypokaliämie → Senkung der ST-Strecke, Abflachung der T- und Auftreten einer U-Welle; Hyperkaliämie → zeltförmige T-Wellen, ab ~8 mM Veränderungen im Kammerteil (evt. Herz-Kreislauf- Versagen); Hypocalcämie → Verlängerung der QT-Strecke; Hypercalcämie → Verkürzung der QT-Strecke
|

 Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.
Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.





 Elektrolyte
Elektrolyte
 Chlorid: χλωρóς = hellgrün (Farbe des Chlorgases)
Chlorid: χλωρóς = hellgrün (Farbe des Chlorgases) Kalium
Kalium  Elektrolyte und EKG
Elektrolyte und EKG
 Core messages
Core messages sind im Körper unverzichtbar. Zu ihnen
gehören Natrium
sind im Körper unverzichtbar. Zu ihnen
gehören Natrium  (sodium), Chlor
(sodium), Chlor  , Kalium
, Kalium  (potassium), Calcium, Magnesium, Phosphor und
Schwefel. Ihre
tägliche Zufuhrmenge liegt beim Erwachsenen im Gramm-Bereich (>0,1 g/d).
(potassium), Calcium, Magnesium, Phosphor und
Schwefel. Ihre
tägliche Zufuhrmenge liegt beim Erwachsenen im Gramm-Bereich (>0,1 g/d). 
 Abbildung: Beteiligung der Natrium- und Kaliumströme am Aktionspotential
Abbildung: Beteiligung der Natrium- und Kaliumströme am Aktionspotential 1952)
1952)
 vgl. Niere
und Salz-Wasser-Haushalt) bestimmt das
extrazelluläre Volumen. Natrium ist das "Leitkation" der
extrazellulären Flüssigkeiten (~140 mM/l),
deren
Osmolalität es zum Großteil trägt.
vgl. Niere
und Salz-Wasser-Haushalt) bestimmt das
extrazelluläre Volumen. Natrium ist das "Leitkation" der
extrazellulären Flüssigkeiten (~140 mM/l),
deren
Osmolalität es zum Großteil trägt.  Freies Na+ (bei 70 kg Körpermasse etwa 2 Mol oder ~46 g) findet sich im Körper zum Großteil als NaCl, zu einem kleineren als Bicarbonat (NaHCO3) und in anderen Natriumsalzen. Na+ ist osmotisch aktiv und mit der Osmoregulation direkt verknüpft. Natrium ist u.a. auch für die Auslösung der meisten Aktionspotentiale
ausschlaggebend.
Freies Na+ (bei 70 kg Körpermasse etwa 2 Mol oder ~46 g) findet sich im Körper zum Großteil als NaCl, zu einem kleineren als Bicarbonat (NaHCO3) und in anderen Natriumsalzen. Na+ ist osmotisch aktiv und mit der Osmoregulation direkt verknüpft. Natrium ist u.a. auch für die Auslösung der meisten Aktionspotentiale
ausschlaggebend.  Etwa die gleiche Menge gebundenes, vor allem im Knochen gespeichertes Natrium ist nicht direkt in die Osmoregulation eingebunden.
Etwa die gleiche Menge gebundenes, vor allem im Knochen gespeichertes Natrium ist nicht direkt in die Osmoregulation eingebunden.  Einerseits führt chronische
Unterversorgung mit Kochsalz (auch bei maximaler
Aldosteronwirkung) zu Hypotonizität, Hypovolämie und Hypotonie,
schließlich zu Kreislaufversagen
Einerseits führt chronische
Unterversorgung mit Kochsalz (auch bei maximaler
Aldosteronwirkung) zu Hypotonizität, Hypovolämie und Hypotonie,
schließlich zu Kreislaufversagen Andererseits
können größere Mengen die Osmo- und Volumenregulation überfordern, da
der Körper nicht auf die Ausscheidung von hochkonzentriertem Salz
angepasst ist. Zwar kann die Niere die Ausscheidung der Zufuhr anpassen
(je mehr Kochsalz zugeführt wird, desto geringer ist die
Aldosteronbildung, und es wird mehr Natrium ausgeschieden), aber dies
funktioniert nur in einem relativ begrenzten Osmolaritätsbereich.
Andererseits
können größere Mengen die Osmo- und Volumenregulation überfordern, da
der Körper nicht auf die Ausscheidung von hochkonzentriertem Salz
angepasst ist. Zwar kann die Niere die Ausscheidung der Zufuhr anpassen
(je mehr Kochsalz zugeführt wird, desto geringer ist die
Aldosteronbildung, und es wird mehr Natrium ausgeschieden), aber dies
funktioniert nur in einem relativ begrenzten Osmolaritätsbereich. Die tägliche Natriumzufuhr sollte 1 g/d (0,5-1,5 Gramm) betragen; oft
werden diese Werte deutlich überschritten ("Nachsalzen").
Die tägliche Natriumzufuhr sollte 1 g/d (0,5-1,5 Gramm) betragen; oft
werden diese Werte deutlich überschritten ("Nachsalzen"). 
 Abbildung: Durchschnittliche Verteilungs- und Umsatzwerte von Natrium im Körper einer erwachsenen Person
Abbildung: Durchschnittliche Verteilungs- und Umsatzwerte von Natrium im Körper einer erwachsenen Person Natrium
Natrium
 Chlorid
Chlorid
 Abbildung oben).
Abbildung oben). Der Natriumspiegel (und die Natriumkonzentration in diversen Körperflüssigkeiten) wird über mehrere Methoden bestimmt: Flammenphotometrie als Referenzmethode (angeregte Natriumatome emittieren Licht von 589.3 nm Wellenlänge), potentiometrisch (ionenselektive Elektroden), oder enzymatisch (Spektrophotometrie).
Der Natriumspiegel (und die Natriumkonzentration in diversen Körperflüssigkeiten) wird über mehrere Methoden bestimmt: Flammenphotometrie als Referenzmethode (angeregte Natriumatome emittieren Licht von 589.3 nm Wellenlänge), potentiometrisch (ionenselektive Elektroden), oder enzymatisch (Spektrophotometrie). 
 Abbildung: Einstellung der Natrium (Salz)- und Wasserbilanz
Abbildung: Einstellung der Natrium (Salz)- und Wasserbilanz
 Kochsalz kann bei intensivem Schwitzen in erheblichen Mengen
verlorengehen. So bedeutet z.B. die Sekretion von 5 l Schweiß einen
Verlust von ~300 mM Natrium und ~220 mM Chlorid, das bedeutet fast 15
Gramm Kochsalz. Im Extrazellulärraum bindet diese Menge Salz ein
Volumen von mehr als 1,5 Liter Wasser (Schweiß ist hypoton).
Kochsalz kann bei intensivem Schwitzen in erheblichen Mengen
verlorengehen. So bedeutet z.B. die Sekretion von 5 l Schweiß einen
Verlust von ~300 mM Natrium und ~220 mM Chlorid, das bedeutet fast 15
Gramm Kochsalz. Im Extrazellulärraum bindet diese Menge Salz ein
Volumen von mehr als 1,5 Liter Wasser (Schweiß ist hypoton).  vegetativ (der Sympathikus
fördert Kochsalzkonservierung im Körper) und
vegetativ (der Sympathikus
fördert Kochsalzkonservierung im Körper) und hormonell (Aldosteron, natriuretische Peptide, Adrenomedullin).
hormonell (Aldosteron, natriuretische Peptide, Adrenomedullin).  "Physiologische (isotone) Kochsalzlösung" (Grundlage für Infusionslösungen) ist 0,9%-ig, d.h. 1 Liter enthält 9 g NaCl.
"Physiologische (isotone) Kochsalzlösung" (Grundlage für Infusionslösungen) ist 0,9%-ig, d.h. 1 Liter enthält 9 g NaCl.
 Abbildung: Kaliumbestände und -umsatz im Körper einer erwachsenen Person
Abbildung: Kaliumbestände und -umsatz im Körper einer erwachsenen Person
 Abbildung). Die tägliche Aufnahme mit
der Nahrung beträgt ~120 mmol (im steady state
verlassen 10% davon den
Körper über den Stuhl, 90% über den Harn). Das bedeutet, dass pro Tag
3-4% des im Körper vorhandenen Kaliums ausgeschieden werden (und
dieselbe Menge mit der Nahrung resorbiert wird).
Abbildung). Die tägliche Aufnahme mit
der Nahrung beträgt ~120 mmol (im steady state
verlassen 10% davon den
Körper über den Stuhl, 90% über den Harn). Das bedeutet, dass pro Tag
3-4% des im Körper vorhandenen Kaliums ausgeschieden werden (und
dieselbe Menge mit der Nahrung resorbiert wird). Kalium
Kalium
 Der Kaliumspiegel im Blutserum (und die Kaliumkonzentration in anderen
Körperflüssigkeiten, insbesondere Urin) wird - wie bei Natrium - über
mehrere Methoden bestimmt: Flammenphotometrie als Referenzmethode (Emissionswellenlänge 766.5 nm), potentiometrisch (ionenselektive Elektroden - Valinomycin als Elektrophor), oder enzymatisch (Spektrophotometrie).
Der Kaliumspiegel im Blutserum (und die Kaliumkonzentration in anderen
Körperflüssigkeiten, insbesondere Urin) wird - wie bei Natrium - über
mehrere Methoden bestimmt: Flammenphotometrie als Referenzmethode (Emissionswellenlänge 766.5 nm), potentiometrisch (ionenselektive Elektroden - Valinomycin als Elektrophor), oder enzymatisch (Spektrophotometrie).  Über die Art und Weise, wie
die Niere angesichts unterschiedlicher diätetischer Versorgung mit
Kalium umgeht, s. dort
Über die Art und Weise, wie
die Niere angesichts unterschiedlicher diätetischer Versorgung mit
Kalium umgeht, s. dort
 Abbildung: Hyperkaliämie bewirkt Kaliumverlagerung in die Muskulatur
Abbildung: Hyperkaliämie bewirkt Kaliumverlagerung in die Muskulatur
 Abbildung):
Abbildung): Insulin (aus Betazellen der Bauchspeicheldrüse) steigert die Glucose- und Kaliumaufnahme in die Zelle (→ Kaliumspiegel sinkt) und wirkt kaliumkonservierend. Glucocorticoide - die "Gegenspieler" des Insulins - regen die Kaliumausscheidung meist an; sie tun das durch Erhöhung der glomerulären Filtration und damit Steigerung der distalen Durchflussrate im Nephron (
Insulin (aus Betazellen der Bauchspeicheldrüse) steigert die Glucose- und Kaliumaufnahme in die Zelle (→ Kaliumspiegel sinkt) und wirkt kaliumkonservierend. Glucocorticoide - die "Gegenspieler" des Insulins - regen die Kaliumausscheidung meist an; sie tun das durch Erhöhung der glomerulären Filtration und damit Steigerung der distalen Durchflussrate im Nephron ( vgl. dort).
vgl. dort). Adrenalin (aus dem Nebennierenmark) bewirkt zunächst Kaliumausstrom aus den Zellen (α-Rezeptoren in der Leber öffnen calciumabhängige Kaliumkanäle → Kaliumspiegel steigt) und dann Kaliumaufnahme in die Zellen (ß-Rezeptoren im Muskelgewebe regen die Na/K-Pumpe an → Kaliumspiegel sinkt),
dies ist der länger anhaltende Effekt. Durch die vermehrte Aufnahme von
Kalium in die Körperzellen einerseits, Inhibition der Kaliumsekretion
in distalen Nephronabschnitten andererseits senkt Adrenalin die Kaliumausscheidung.
Adrenalin (aus dem Nebennierenmark) bewirkt zunächst Kaliumausstrom aus den Zellen (α-Rezeptoren in der Leber öffnen calciumabhängige Kaliumkanäle → Kaliumspiegel steigt) und dann Kaliumaufnahme in die Zellen (ß-Rezeptoren im Muskelgewebe regen die Na/K-Pumpe an → Kaliumspiegel sinkt),
dies ist der länger anhaltende Effekt. Durch die vermehrte Aufnahme von
Kalium in die Körperzellen einerseits, Inhibition der Kaliumsekretion
in distalen Nephronabschnitten andererseits senkt Adrenalin die Kaliumausscheidung. Aldosteron (aus der zona glomerulosa der Nebennierenrinde)
regt (innerhalb von Stunden) die basolaterale Na/K-ATPase an, wodurch
mehr Kalium in die spätdistalen Tubulus- und Sammelrohrepithelzellen
aufgenommen werden kann. Weiters steigert Aldosteron die Expression
apikaler Natriumkanäle (ENaCs) und fördert damit indirekt die Kaliumsekretion (
Aldosteron (aus der zona glomerulosa der Nebennierenrinde)
regt (innerhalb von Stunden) die basolaterale Na/K-ATPase an, wodurch
mehr Kalium in die spätdistalen Tubulus- und Sammelrohrepithelzellen
aufgenommen werden kann. Weiters steigert Aldosteron die Expression
apikaler Natriumkanäle (ENaCs) und fördert damit indirekt die Kaliumsekretion ( vgl. dort).
vgl. dort). Kurzzeitregulation (Kalium in die Zellen): Anregung der Na-K-Pumpe verlagert vermehrt Kalium aus dem
Extra- in den Intrazellulärraum
Kurzzeitregulation (Kalium in die Zellen): Anregung der Na-K-Pumpe verlagert vermehrt Kalium aus dem
Extra- in den Intrazellulärraum  Längerfristige Regulation (Kalium in die Umwelt): Erhöhung der Kaliumausscheidung (Erfolgsorgan Niere
Längerfristige Regulation (Kalium in die Umwelt): Erhöhung der Kaliumausscheidung (Erfolgsorgan Niere  s. dort).
s. dort). Veränderungen des pH-Wertes im extrazellulären Raum beeinflussen den Kaliumhaushalt: Azidämie
steigert (Hyperkaliämie), Alkaliämie senkt den Kaliumspiegel im
Blutplasma (Hypokaliämie). Das ist klinisch wichtig, weil Maßnahmen zur
Änderung des pH im Blut (externe Pufferung) automatisch den
Kalliumspiegel ändern. Wie funktioniert das?
Veränderungen des pH-Wertes im extrazellulären Raum beeinflussen den Kaliumhaushalt: Azidämie
steigert (Hyperkaliämie), Alkaliämie senkt den Kaliumspiegel im
Blutplasma (Hypokaliämie). Das ist klinisch wichtig, weil Maßnahmen zur
Änderung des pH im Blut (externe Pufferung) automatisch den
Kalliumspiegel ändern. Wie funktioniert das?
 Behandlung einer Azidose (Infusion von Pufferbasen) kann eine gleichzeitig bestehende Hyperkaliämie zum Verschwinden bringen.
Behandlung einer Azidose (Infusion von Pufferbasen) kann eine gleichzeitig bestehende Hyperkaliämie zum Verschwinden bringen.

 Abbildung: EKG-Veränderungen bei erniedrigtem (oben) und erhöhtem Kaliumspiegel (unten)
Abbildung: EKG-Veränderungen bei erniedrigtem (oben) und erhöhtem Kaliumspiegel (unten)
 Hypokaliämie bedingt
Senkungen der ST-Strecke, Abflachung der T- und Auftreten einer U-Welle;
Hypokaliämie bedingt
Senkungen der ST-Strecke, Abflachung der T- und Auftreten einer U-Welle; Hyperkaliämie spitze ("zeltförmige") T-Wellen und (ab ~8 mM
Serumkalium) schwere Veränderungen vor allem im Kammerteil. Starke Hyperkaliämie kann zu akutem
Herz-Kreislaufversagen führen und lebensgefährlich sein;
Hyperkaliämie spitze ("zeltförmige") T-Wellen und (ab ~8 mM
Serumkalium) schwere Veränderungen vor allem im Kammerteil. Starke Hyperkaliämie kann zu akutem
Herz-Kreislaufversagen führen und lebensgefährlich sein; Hypocalcämie verursacht eine Verlängerung der QT-Strecke,
Hypocalcämie verursacht eine Verlängerung der QT-Strecke, Hypercalcämie hingegen eine Verkürzung der QT-Strecke.
Hypercalcämie hingegen eine Verkürzung der QT-Strecke. Azidose führt zum Austritt von Kaliumionen aus den Zellen und
Hyperkaliämie, und Hyperkaliämie treibt Wasserstoffionen aus den
Zellen, was Azidose zur Folge hat. Bei Alkalose ist es umgekehrt. Über den
zugrunde liegenden Mechanismus
Azidose führt zum Austritt von Kaliumionen aus den Zellen und
Hyperkaliämie, und Hyperkaliämie treibt Wasserstoffionen aus den
Zellen, was Azidose zur Folge hat. Bei Alkalose ist es umgekehrt. Über den
zugrunde liegenden Mechanismus  s. dort.
s. dort.  Ursache für eine Hyperkaliämie
kann u.a. extreme Muskelbelastung, Insulinmangel, verminderte
Ausscheidung in der Niere, hohe Katecholaminwirkung
(α-Adreno-Agonisten) oder Zerstörung von Zellen (z.B. bei
Verbrennungen, Hämolyse) sein.
Ursache für eine Hyperkaliämie
kann u.a. extreme Muskelbelastung, Insulinmangel, verminderte
Ausscheidung in der Niere, hohe Katecholaminwirkung
(α-Adreno-Agonisten) oder Zerstörung von Zellen (z.B. bei
Verbrennungen, Hämolyse) sein. 
 Natrium in der extrazellulären Flüssigkeit (~140 mM/l) bestimmt dessen Volumen. Der Körper einer erwachsenen Person enthält
~100 g Na, etwa die Hälfte davon ist im Knochen gespeichert (osmoregulatorisch inaktiv). Natrium beteiligt sich an Nervenleitung, Muskelfunktion (Aktionspotentiale), Sekretionsvorgängen und Flüssigkeitsbilanz. Die tägliche Natriumzufuhr sollte
~1 g/d betragen,
um das extrazelluläre Volumen stabil zu halten (chronischer Salzmangel
führt trotz maximaler Aldosteronwirkung zu Hypovolämie und
Kreislaufversagen). Andererseits können größere Mengen die
Osmo- und Volumenregulation überfordern. Pro Liter Schweiß verliert man ~3 g Kochsalz; Hyponatriämie
senkt den Blutdruck und bewirkt Muskelschwäche. Die Regulierung des
Natriumhaushalts erfolgt nervös (Sympathikusaktivität hält NaCl im Körper)
und hormonell (Aldosteron hält Natrium im Körper, natriuretische Peptide scheiden Natrium aus). Physiologische Kochsalzlösung ist isoton (9 g NaCl/l; 0,9%-ig)
Natrium in der extrazellulären Flüssigkeit (~140 mM/l) bestimmt dessen Volumen. Der Körper einer erwachsenen Person enthält
~100 g Na, etwa die Hälfte davon ist im Knochen gespeichert (osmoregulatorisch inaktiv). Natrium beteiligt sich an Nervenleitung, Muskelfunktion (Aktionspotentiale), Sekretionsvorgängen und Flüssigkeitsbilanz. Die tägliche Natriumzufuhr sollte
~1 g/d betragen,
um das extrazelluläre Volumen stabil zu halten (chronischer Salzmangel
führt trotz maximaler Aldosteronwirkung zu Hypovolämie und
Kreislaufversagen). Andererseits können größere Mengen die
Osmo- und Volumenregulation überfordern. Pro Liter Schweiß verliert man ~3 g Kochsalz; Hyponatriämie
senkt den Blutdruck und bewirkt Muskelschwäche. Die Regulierung des
Natriumhaushalts erfolgt nervös (Sympathikusaktivität hält NaCl im Körper)
und hormonell (Aldosteron hält Natrium im Körper, natriuretische Peptide scheiden Natrium aus). Physiologische Kochsalzlösung ist isoton (9 g NaCl/l; 0,9%-ig) Die alimentäre Zufuhr von Kalium (mit ~150 mM Leitkation des Intrazellulärraums) ist meist ausreichend (die Nieren scheiden überschüssiges Kalium aus). Die Zellen einer erwachsenen Person enthalten zusammen
~150 g Kalium, täglich werden
~5 g aufgenommen.
Kalium wird von der Na/K-ATPase intrazellulär angereichert, baut das
Ruhepotential auf (Auswärtsdiffusion) und beteiligt sich am
Säure-Basen-Gleichgewicht (Azidose senkt die Aufnahme von Kalium in die Zelle → Umverlagerung in den Extrazellulärraum; umgekehrt senkt Alkalose den Kaliumspiegel). Behandlung einer Azidose kann eine gleichzeitig bestehende Hyperkaliämie zum Verschwinden bringen (weniger H+ → mehr K+ in der Zelle). Hyperkaliämie (z.B.infolge intensiver Muskelbelastung) regt das Pankreas zu Insulinsekretion an (zelluläre K+-Aufnahme↑→ Kaliumspiegel sinkt), die
Nebennierenrinde zur Aldosteronsynthese
(Aldosteron fördert die Kaliumsekretion → Kaliumspiegel sinkt), das
Nebennierenmark zu Adrenalinsekretion (muskuläre ß-Rezeptoren regen die
Na/K-ATPase an → Kaliumspiegel sinkt anhaltend)
Die alimentäre Zufuhr von Kalium (mit ~150 mM Leitkation des Intrazellulärraums) ist meist ausreichend (die Nieren scheiden überschüssiges Kalium aus). Die Zellen einer erwachsenen Person enthalten zusammen
~150 g Kalium, täglich werden
~5 g aufgenommen.
Kalium wird von der Na/K-ATPase intrazellulär angereichert, baut das
Ruhepotential auf (Auswärtsdiffusion) und beteiligt sich am
Säure-Basen-Gleichgewicht (Azidose senkt die Aufnahme von Kalium in die Zelle → Umverlagerung in den Extrazellulärraum; umgekehrt senkt Alkalose den Kaliumspiegel). Behandlung einer Azidose kann eine gleichzeitig bestehende Hyperkaliämie zum Verschwinden bringen (weniger H+ → mehr K+ in der Zelle). Hyperkaliämie (z.B.infolge intensiver Muskelbelastung) regt das Pankreas zu Insulinsekretion an (zelluläre K+-Aufnahme↑→ Kaliumspiegel sinkt), die
Nebennierenrinde zur Aldosteronsynthese
(Aldosteron fördert die Kaliumsekretion → Kaliumspiegel sinkt), das
Nebennierenmark zu Adrenalinsekretion (muskuläre ß-Rezeptoren regen die
Na/K-ATPase an → Kaliumspiegel sinkt anhaltend) Elektrolytstörungen beeinflussen das EKG: Hypokaliämie → Senkung der ST-Strecke, Abflachung der T- und Auftreten einer U-Welle; Hyperkaliämie → zeltförmige T-Wellen, ab ~8 mM Veränderungen im Kammerteil (evt. Herz-Kreislauf- Versagen); Hypocalcämie → Verlängerung der QT-Strecke; Hypercalcämie → Verkürzung der QT-Strecke
Elektrolytstörungen beeinflussen das EKG: Hypokaliämie → Senkung der ST-Strecke, Abflachung der T- und Auftreten einer U-Welle; Hyperkaliämie → zeltförmige T-Wellen, ab ~8 mM Veränderungen im Kammerteil (evt. Herz-Kreislauf- Versagen); Hypocalcämie → Verlängerung der QT-Strecke; Hypercalcämie → Verkürzung der QT-Strecke