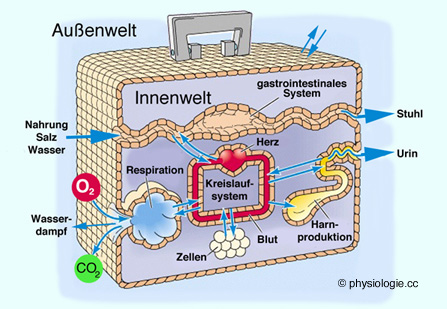
 Abbildung: Kompartimente und Systeme
Nach einer Vorlage bei Sinauer Associates (2001)
Abbildung: Kompartimente und Systeme
Nach einer Vorlage bei Sinauer Associates (2001)
Der
Organismus, unterwegs in seiner Umwelt: Er nimmt aus ihr Nahrung,
Elektrolyte, Wasser auf und gibt Urin, Wasserdampf und Stuhl an sie ab.
Der Blutkreislauf verteilt die Stoffe zwischen den verschiedenen
Kompartimenten des Körpers (konvektiver Transport)
 Kompartimente existieren auch in der Zelle:
Kompartimente existieren auch in der Zelle:
 Teils decken sie sich mit dem Volumen von Zellorganellen
(z.B. Zellkern, Mitochondrien, Inhalt von Golgi-Apparat, Vesikeln,
endoplasmatischem Retikulum u.a.), die durch Membranen sichtbar von
ihrer Umgebung separiert sind, welche für viele Moleküle eine
Diffusionsbarriere darstellen,
Teils decken sie sich mit dem Volumen von Zellorganellen
(z.B. Zellkern, Mitochondrien, Inhalt von Golgi-Apparat, Vesikeln,
endoplasmatischem Retikulum u.a.), die durch Membranen sichtbar von
ihrer Umgebung separiert sind, welche für viele Moleküle eine
Diffusionsbarriere darstellen,
 teils ergeben sie sich mittels molekularer Interaktionen und Strukturen durch "Gerüstmoleküle" (scaffold proteins), z.B. die Abgrenzung von zytoplasmatischen "Calciumwolken", die im Rahmen von Erregungsvorgängen vorübergehend frei- und wirksam werden.
teils ergeben sie sich mittels molekularer Interaktionen und Strukturen durch "Gerüstmoleküle" (scaffold proteins), z.B. die Abgrenzung von zytoplasmatischen "Calciumwolken", die im Rahmen von Erregungsvorgängen vorübergehend frei- und wirksam werden.

Zu
Verteilungsräumen (Flüssigkaitskompartimenten) im Körper s. auch
dort

 Abbildung: Zusammensetzung von Körperflüssigkeiten im Vergleich
Abbildung: Zusammensetzung von Körperflüssigkeiten im Vergleich
Nach einer Vorlage bei Thibodeau / Patton, Anatomy & Physiology (6th ed), Mosby Elsevier 2007
Blutplasma und interstitielle Flüssigkeit
sind beides extrazelluläre Flüssigkeiten und unterscheiden sich in
ihrer Zusammensetzung nur geringgradig - hohe Konzentration an Kochsalz
(Na+ / Cl-), Bikarbonatkonzentration (HCO3-) ~25
mM. Deutlich differieren sie in der Eiweißkonzentration (höher im
Blutplasma), aber auch in der Konzentration an organischen Säuren (org.
ac, höher im Interstitium). Insgesamt weist das Plasma eine etwas
höhere Gesamtkonzentration an gelösten Teilchen auf.
Die
intrazelluläre Flüssigkeit weist eine im Vergleich zu den
extrazellulären Flüssigkeiten wesentlich höhere Konzentration an
Kaliumionen (K+) und auch Magnesiumionen (Mg++)
auf - ein Ergebnis der Aktivität der Transporter in der Zellmembran
(vor allem der Na/K-ATPase). Vergleichsweise sehr hoch ist weiters die
Konzentration an Phosphaten (PO4-), Proteinen (beide wirken u.a. als Puffer) sowie der Sulfatspiegel (SO4-)
 Flüssigkeitsvolumina im Körper (Blutvolumen, Liquormenge, intra- und extrazelluläre Volumina,...) werden von physiologischen
Regelmechanismen in engen Bereichen gehalten,
was für die normale Funktionalität wichtig ist (z.B. Blutdruck, Kreislaufstabilität, Perfusion
von Organen etc). Dazu gehört die Aufnahme und Ausscheidung von Wasser
und Elektrolyten (Volumenregulation). Treibende Kraft für die
Aufrechterhaltung physiologischer Ionenkonzentrationen im Extra- und
Intrazellulärraum ist die Aktivität der zahlreichen verschiedenen
Transportsysteme in der Zellmembran, z.B. Na/K-Pumpe, Natriumkanäle,
Kaliumkanäle, Symporter, Antiporter.
Flüssigkeitsvolumina im Körper (Blutvolumen, Liquormenge, intra- und extrazelluläre Volumina,...) werden von physiologischen
Regelmechanismen in engen Bereichen gehalten,
was für die normale Funktionalität wichtig ist (z.B. Blutdruck, Kreislaufstabilität, Perfusion
von Organen etc). Dazu gehört die Aufnahme und Ausscheidung von Wasser
und Elektrolyten (Volumenregulation). Treibende Kraft für die
Aufrechterhaltung physiologischer Ionenkonzentrationen im Extra- und
Intrazellulärraum ist die Aktivität der zahlreichen verschiedenen
Transportsysteme in der Zellmembran, z.B. Na/K-Pumpe, Natriumkanäle,
Kaliumkanäle, Symporter, Antiporter.
Die Unterschiede in der Zusammensetzung der Körperflüssigkeiten präzisiert die folgende Tabelle:
Zusammensetzung von Körperflüssigkeiten
(gerundete Werte)
Modifiziert nach Boron / Boulpaep, Concise Medical Physiology. Elsevier 2021
|
|
Blutplasma
|
proteinfrei
|
Interstitium
|
Zelle
|
Na+ (mM)
|
142
|
153
|
145
|
~15
|
| K+ (mM) |
4,4
|
4,7
|
4,5
|
120
|
| Ca++ (mM) |
1,2 (ionisiert)
2,4 (gesamt)
|
1,3 (ionisiert) |
1,2 (ionisiert) |
0,0001 (ionisiert) |
| Mg++ (mM) |
0,6 (ionisiert)
0,9 (gesamt) |
0,6 (ionisiert) |
0,55 (ionisiert) |
1 (ionisiert)
|
| Cl- (mM) |
102
|
110
|
116
|
20
|
| HCO3- (mM) |
22 (arteriell)
24 (venös) |
24
|
25
|
16
|
| H2PO4- / HPO4-- (mM) |
0,7 (ionisiert)
1,4 (gesamt) |
0,75 (ionisiert) |
0,8 (ionisiert) |
0,7 (frei gelöst) |
Proteine
|
70 g/l
1 mM
|
-
|
~10 g/l
|
~300 g/l
|
Glucose
(mM)
|
5,5
|
5,9
|
5,9
|
sehr gering
|
pH
|
7,4
|
7,4
|
7,4
|
~7,2 |
Osmolalität
(mOsm / kg H2O)
|
291
|
290
|
290
|
290
|
Die Volumenwerte sind u.a. geschlechtsspezifisch:
Verteilung des Körperwassers
(gerundete Werte)
Nach Boron / Boulpaep, Concise Medical Physiology. Elsevier 2021
|
|
Männer
|
Volumen (l)
|
Frauen
|
Volumen (l)
|
Körperwasser (TBW) gesamt
|
60% KG
|
42
|
50% KG
|
35
|
Intrazelluläre Flüssigkeit
|
60% TBW
|
25
|
60% TBW |
21
|
Extrazelluläre Flüssigkeit (ECF)
|
40% TBW |
17
|
40% TBW |
14
|
Interstitielle Flüssigkeit
|
75% ECF
|
13
|
75% ECF |
10
|
Blutplasma
|
20% ECF |
3
|
20% ECF |
3
|
Transzelluläre Flüssigkeit
|
5% ECF |
1
|
5% ECF |
1
|
Blutvolumen
|
PV/(1-Ht)
|
6
|
PV/(1-Ht) |
5
|
KG = Körpergewicht,
PV = Plasmavolumen, Ht = Hämatokrit
Elektroneutralität:
In jeder Körperflüssigkeit ist die Zahl positiver und negativer
Ladungen gleich groß. Die wichtigsten positiven (kationischen) Ladungen
werden bereitgestellt durch (Na+) (vorwiegend extrazellulär) und K+ (vorwiegend intrazellulär), die wichtigsten negativen (anionischen) durch Chlorid, Bicarbonat, Proteine, Phosphat.
Die
Nieren sind unverzichtbar für die Ausscheidung von Wasser, Salzen und einigen
"harnpflichtigen" Stoffen; sie sind das exekutive Organ
für die Regulierung der Körperflüssigkeiten. Zu diesen zählt der Transportraum, der außerhalb der Zellen liegt (extrazelluläre Flüssigkeit), ein Teil davon ist das Blutplasma.
 Abbildung: Verteilung des Körperwassers bei einer 70kg schweren männlichen Referenzperson
Nach einer Vorlage in Boron W, Boulpaep E: Medical Physiology, 3rd ed., Elsevier 2016
Abbildung: Verteilung des Körperwassers bei einer 70kg schweren männlichen Referenzperson
Nach einer Vorlage in Boron W, Boulpaep E: Medical Physiology, 3rd ed., Elsevier 2016
Die
wichtigsten Kompartimente sind Blut (links), Interstitium
(extrazelluläre Geweberäume), transzelluläre Räume, sowie der intrazelluläre
Raum (rechts).
Von den ~13 l interstitieller Flüssigkeit sind ~8 l frei (direkt mit
Plasma oder Zellflüssigkeit austauschbar), 2 l im Knochen und 3 l in
festem Bindegewebe (z.B. Sehnen) fixiert (nur verzögert austauschbar).
Extrazelluläre Flüssigkeit ist reich an Kochsalz, intrazelluläre Flüssigkeit weist eine hohe Konzentration an Kalium auf

Ausreichendes Blutvolumen ist
eine Voraussetzung für
ein normales Funktionieren des Kreislaufs. Daher besteht ein enger
Zusammenhang zwischen Flüssigkeits- und Blutdruckregulation; die Niere ist direkt in die Aufrechterhaltung der Blutversorgung des ganzen Organismus involviert.
Der Körper besteht zu einem Großteil aus Wasser, das sich
unterschiedlich auf Subkompartimente verteilt: Rund 40% des
Körpergewichts sind intrazelluläres, rund 20% extrazelluläres Wasser
(bei hohem Fettanteil sind die Zahlen niedriger, bei niedrigem höher).
Die extrazelluläre Flüssigkeit ist als primärer Verteilungsraum für Substrate, Hormone, Stoffwechselprodukte, Medikamente etc. besonders signifikant:
Flüssigkeitskompartimente einer erwachsenen Person (70 kg)

Zahlen nach Lin / Smith / Pinnock, Fundamentals of Anaesthesia, 4th ed., Cambridge University Press 2016 |
Flüssigkeit
|
% des Körper-
gewichts
|
Volumen (l)
|
Interstitiell
|
15
|
10,5
|
Blutplasma
|
5
|
3,5
|
Transzellulär
|
1
|
0,7
|
Summe: Extrazellulär (gesamt)
|
21
|
14,
|
Dabei
besteht auch eine Altersabhängigkeit: Neugeborene bestehen zu 80% aus
Wasser, Babys mit 6 Monaten zu 70%, Einjährige zu 60% - das bleibt dann
ziemlich lang unverändert, erst bei älteren Personen nimmt der
Wasseranteil am Körpergewicht weiter ab, auf etwa 50%.
Gesamtkörperwasser
Die Bestimmung des Gesamtkörperwassers (TBW, total body water) erfolgt mit Tritiumoxid (T2O, 3H2O,
schwerem Wasser). Dieser Indikator verhält sich wie normales Wasser und
verteilt sich in der gesamten Körperflüssigkeit. Tritium (1 Proton, 2 Neutronen) ist
ein relativ stabiles Isotop des Wasserstoffs; es zerfällt mit einer
Halbwertszeit von ca. 12,3 Jahren zu Helium und emittiert dabei
Elektronen, ist also ein Betastrahler (radiometrische Bestimmung).
Indikatorverdünnungsprinzip: Eine Dosis T2O (wasserklare Flüssigkeit) mit bekanntem Volumen und bekannter Aktivität (Anfangsdosis) dient als Indikator und wird intravenös injiziert. Sie verteilt sich im Körper und wird gleichzeitig - wie Wasser allgemein - laufend filtriert und renal ausgeschieden.
Die bis zum Zeitpunkt der Äquilibrierung (dieser Zeitpunkt dient der TBW-Bestimmung) aus
dem Körper entfernte Menge des Indikators wird über die Radioaktivität
des in der entsprechenden Äquilibrierungszeit ausgeschiedenen Harns
abgeschätzt (die Ausscheidung mit dem Harn reduziert die im Verteilungsraum verbliebene Indikatormenge). Aus Volumen und Radioaktivität der Harnprobe wird die Menge enthaltenen T2O (in g) errechnet.
Extrazelluläre Flüssigkeit
Die Bestimmung des extrazellulären Flüssigkeitsvolumens (ECF, extracellular fluid volume) erfolgt mit einem Indikator, der nicht in andere Kompartimente übertritt, z.B. Inulin.
Inulin kann in Serumproben photometrisch bestimmt werden. Das
Indikatorverdünnungspronzip gilt hier sinngemäß in gleicher Weise.
Das jeweilige Verteilungsvolumen (V) wird dann berechnet nach der
Indikatormenge (M) im Körper (infundiert minus ausgeschieden) dividiert
durch die Konzentration (c) - jeweils nach vollständiger Durchmischung
im Kompartiment, also
V = M / c
In der extrazellulären Flüssigkeit
sind - zumindest für kurze Zeit - wesentlich stärkere Schwankungen der
Konzentrationswerte gelöster Stoffe tolerierbar als in der eng
regulierten intrazellulären Umgebung. Solche Abweichungen können durch
intensive Herausforderungen durch die Umwelt sowie durch Verletzungen
und Krankheiten auftreten. Die folgende Tabelle gibt entsprechende
mittlere Normalwerte, physiologische Schwankungsbreiten sowie
Grenzwerte an, die für kurze Zeit ohne letale Folgen bleiben können
(z.B. liegt der physiologische Referenzbereich für den
Blutzuckerspiegel etwa zwischen 70 und 115 mg/dl). Diese Bandbreiten
betragen meist zwischen 20 und 50% um den Mittelwert, geringer ist nur
diejenige für Kochsalz (7-10%).
Die kurzfristig
nicht-tödlichen Limits umfassen eine wesentlich größere Bandbreite -
hier zwischen 20 und 1500 mg/dl):
Extrazelluläre Flüssigkeit
Nach Guyton and Hall, Textbook of Medical Physiology, 15th ed. Elsevier 2026
|
Zustandsvariable
|
Normal-
Mittelwert
|
Normalbereich
|
Nichtletale Limits (für kurze Zeit, gerundet)
|
O2
|
40 mmHg
|
25-40
(~40%) |
10-1000
|
CO2
|
45 mmHg
|
41-51
(~20%) |
5-80
|
Na+
|
142 mM
|
135-145
(~7%) |
115-175
|
K+
|
4,2 mM
|
3,5-5,3
(~40%) |
1,5-9,0
|
Ca++
|
1,2 mM
|
1,0-1,4
(~30%) |
0,5-2,0
|
Cl-
|
106 mM
|
98-108
(~10%) |
70-130
|
Bicarbonat
|
24 mM
|
22-29
(~30%) |
8-45
|
Glucose
|
90 mg/dl
|
70-115
(~50%) |
20-1500
|
Temperatur
|
37°C
|
36,8-37,2
|
18-43
|
pH-Wert
[H+]
|
7,4
251 nM
|
7,3-7,5
200-316 (~46%) |
6,9-8,0
79-1000
|
Intrazelluläre Flüssigkeit
Das intrazelluläre Flüssigkeitsvolumen
(ICF, intracellular fluid volume) im Körper errechnet sich (näherungsweise, da unter Vernachlässigung des
transzellulären Volumens) als die Differenz [Gesamtkörperwasser] -
[extrazelluläres Flüssigkeitsvolumen].
 Rechenbeispiel: Es soll das intrazelluläre Flüssigkeitsvolumen einer Probandin ermittelt werden - aus folgenden Werten:
Rechenbeispiel: Es soll das intrazelluläre Flüssigkeitsvolumen einer Probandin ermittelt werden - aus folgenden Werten:
Infundiertes T2O: 2,5 g; ausgeschiedenes T2O: 0,4 g; T2O-Konzentration im Serum: 0,05 mg/ml
TBW: (2,5 - 0,4) / 0,05 = 42 Liter
Infundiertes Inulin: 1,6 g; ausgeschiedenes Inulin: 0,2 g; Inulinkonzentration im Serum: 0,1 mg/ml

ECF: (1,6 - 0,2) / 0,1 = 14 Liter
Resultat: Intrazelluläres Flüssigkeitsvolumen = 42 - 14 = 28 Liter
 Zur Zusammensetzung der intrazellulären Flüssigkeit s. oben
Zur Zusammensetzung der intrazellulären Flüssigkeit s. oben
Transzelluläre Flüssigkeiten
 Transzelluläre Flüssigkeiten sind extrazelluläre Flüssigkeiten, die sich in komplett von Epithel umkleideten Räumen (transzellulären Räumen) befinden.
Sie werden von unterschiedlichen Epithelien sezerniert, ihre
Zusammensatzung unterscheidet sich untereinander und auch von der des
Blutplasmas. Ihr Gesamtvolumen im Körper eines erwachsenen Menschen beträgt etwa 1 Liter.
Transzelluläre Flüssigkeiten sind extrazelluläre Flüssigkeiten, die sich in komplett von Epithel umkleideten Räumen (transzellulären Räumen) befinden.
Sie werden von unterschiedlichen Epithelien sezerniert, ihre
Zusammensatzung unterscheidet sich untereinander und auch von der des
Blutplasmas. Ihr Gesamtvolumen im Körper eines erwachsenen Menschen beträgt etwa 1 Liter.
Zu transzellulären Flüssigkeiten zählen
 Synovialflüssigkeit in
den Gelenksräumen (einige ml pro größerem Gelenk)
Synovialflüssigkeit in
den Gelenksräumen (einige ml pro größerem Gelenk)
 Hirn-Rückenmarks-Flüssigkeit (liquor cerebrospinalis, rund 150 ml, davon ca. 30 ml intraventrikulär)
Hirn-Rückenmarks-Flüssigkeit (liquor cerebrospinalis, rund 150 ml, davon ca. 30 ml intraventrikulär)
 Intraokuläre Flüssigkeit (0,25 ml Kammerwasser pro Auge)
Intraokuläre Flüssigkeit (0,25 ml Kammerwasser pro Auge)
 Pleuraflüssigkeit (10-20 ml, Proteinkonzentraion <15 g/l)
Pleuraflüssigkeit (10-20 ml, Proteinkonzentraion <15 g/l)
 Perikardialflüssigkeit (~20 ml)
Perikardialflüssigkeit (~20 ml)
 Peritonealflüssigkeit (10-20 ml, Ovulationsperiode bis 50 ml)
Peritonealflüssigkeit (10-20 ml, Ovulationsperiode bis 50 ml)
Flüssigkeit in der Harnblase oder im
Verdauungssystem zählt nicht dazu.
Natrium, extrazellulärer Raum, Kreislauf
 über verfügbares Blutvolumen und Kochsalzaufnahme; über den Hirnstamm
werden Blutgefäße (peripherer Widerstand) und Nieren (Salzausscheidung)
entsprechend gesteuert.
über verfügbares Blutvolumen und Kochsalzaufnahme; über den Hirnstamm
werden Blutgefäße (peripherer Widerstand) und Nieren (Salzausscheidung)
entsprechend gesteuert.
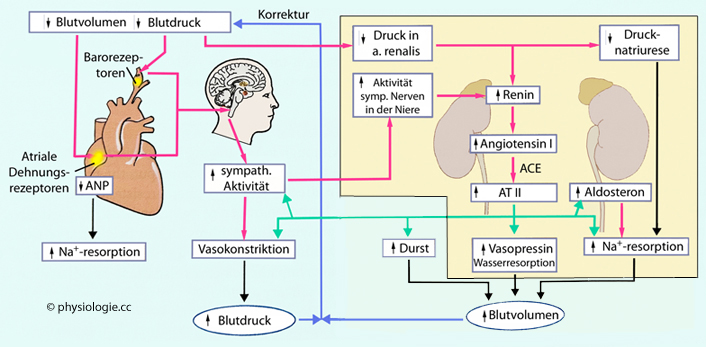
 Abbildung:
Regelkreis für Natriumhaushalt und Blutdruckregulation
Modifiziert
nach einer Vorlage bei Aaronson / Ward / Connolly, The Cardiovascular
System at a Glance, 5th ed. Wiley Blackwell 2020
Abbildung:
Regelkreis für Natriumhaushalt und Blutdruckregulation
Modifiziert
nach einer Vorlage bei Aaronson / Ward / Connolly, The Cardiovascular
System at a Glance, 5th ed. Wiley Blackwell 2020
Kreislauf und Nervensystem links, Nieren rechts. Rote Pfeile: Anregung, grüne Pfeile:
Angiotensinwirkungen, blaue Pfeile: Wiederherstellung normaler Volumen-
/ Blutdruckwerte.
Renale
Natriumresorption und damit Blutvolumenregulation werden durch eine
Rückkopplungsschleife stabilisiert, welche atriale Volumenrezeptoren im
Herzen, den nucleus tractus solitarii im Hirnstamm, den nucl.
paraventricularis im Hypothalamus und renale sympathische Nerven
umfasst. Die Aktivität renaler Sympathikusfasern wird von arteriellen
Barorezeptoren beeinflusst, die primär über Areale der
medulla oblongata wirken, sowie über die Osmolarität in Blut und Gehirn
(periphere Osmorezeptoren, Natriumsensoren im Hypothalamus).
Angiotensin (AT II) und
Aldosteron beeinflussen die entsprechende Aktivität im nucleus
paraventricularis des Hypothalamus, der spezialisierte Neuronen für die
Steuerung der Nieren oder von Arteriolen im gesamten Organismus
enthält. Dadurch können regulatorische Teilmechanismen gezielt
beeinflusst werden.
ACE = Angiotensin Converting Enzyme  ANP = atriale natriuretische Peptide
ANP = atriale natriuretische Peptide
 Adäquater
arterieller Blutdruck ist für die Nierenfunktion
entscheidend: Unter 10 kPa (75 mm Hg) sind Nierendurchblutung und
Harnbildung erschwert. Bei
mangelnder Blutversorgung aktiviert die Niere das Renin-Angiotensin-Aldosteron-System (
Adäquater
arterieller Blutdruck ist für die Nierenfunktion
entscheidend: Unter 10 kPa (75 mm Hg) sind Nierendurchblutung und
Harnbildung erschwert. Bei
mangelnder Blutversorgung aktiviert die Niere das Renin-Angiotensin-Aldosteron-System ( Abbildung).
Abbildung).
Aldosteron fördert die Rückgewinnung von Kochsalz (Abbildung) in Niere,
Schweiß- und Speicheldrüsen, Dünn- und Dickdarm, und fördert die
Ausscheidung von Kalium und H+. Es erhält das extrazelluläre
Volumen aufrecht. Daraus ergibt sich seine
positive Wirkung auf Blutvolumen und Kreislauf.
Vasopressin (ADH) wird bei Volumenmangel
(insbesondere bei akuter Hypovolämie) vermehrt sezerniert, es ist das
"Wassersparhormon" des Organismus und verstärkt die Rückresorption von
Wasser in den Nieren.
Volumenmangel stimuliert auch das Durstempfinden,
das sowohl über Druck- und Volumenfühler im Kreislauf, Osmorezeptoren
und hormonelle Einflüsse (z.B. Angiotensin II) im Gehirn ausgelöst wird
- Wasseraufnahme hilft, eine Dehydration wieder auszubalancieren.
Wohin gelangen infundierte Stoffe, und wie schnell?
Verteilung,
Anreicherung, Umbau und Ausscheidung eines Stoffes im Körper werden als
Kinetik  dieser Substanz bezeichnet. Diese hängt von Fettlöslichkeit,
Größe und Ladung des Moleküls, sowie dem Zustand der
Kapillarwände, des Interstitiums, der Zellmembranen, des Stoffwechsels
und der Ausscheidungswege ab.
dieser Substanz bezeichnet. Diese hängt von Fettlöslichkeit,
Größe und Ladung des Moleküls, sowie dem Zustand der
Kapillarwände, des Interstitiums, der Zellmembranen, des Stoffwechsels
und der Ausscheidungswege ab.
 Über Applikationswege s. dort
Über Applikationswege s. dort

 Abbildung: Physiologisches Kompartmentmodell zur Beschreibung des Austauschs von Substanzen im Körper
Abbildung: Physiologisches Kompartmentmodell zur Beschreibung des Austauschs von Substanzen im Körper
Nach einer Vorlage bei Enderle JD, Compartment
Modeling. Chapter 7 in: Enderle JD, Bronzino JD (eds): Introduction to
Biomedical Engineering (3rd ed), 2012, Academic Press
Die
Einteilung des Körpers in verschiedene Kompartimente / Verteilungsräume
erleichtert quantitative Formulierungen der Kinetik von Substanzen im
Organismus (Resorption, Verteilung, Abbau, Ausscheidung u.a.) und damit
eine exaktere Abschätzung von physiologisch, pharmakologisch,
toxikologisch relevanten Zeitverläufen (z.B. der Konzentration im Blut
oder anderer Größen).
Die Anzahl der berücksichtigten Verteilungsräume (z.B. Intra- und Extrazellulärraum, spezifische Gewebe / Organe) ist bestimmt durch die Anforderungen, die an das jeweilige Modell gestellt werden. Solchen Kompartimenten
werden aufgrund experimenteller Untersuchungen Kenngrößen zugewiesen
(Volumen, Austausch bestimmter Indikatoren u.a. - kinetische Zustandsgrößen). Das hier gezeigte
Kompartmentmodell unterscheidet Räume, die sich an der Anatomie
orientieren (Blut, Leber, Milz, Gastrointestinaltrakt, Nieren, Schilddrüse, Muskulatur).
Modelle sollen weder zu simpel noch zu komplex angesetzt sein, um Ergebnisse von befriedigender Genauigkeit zu liefern und für die
Praxis geeignet zu sein.
Ein gutes Modell kann
Eintritt, Verweildauer und Eliminierung bestimmter Stoffe (auch
Medikamente) in Verteilungsräumen des Organismus voraussagen
 Kompartimente: Der Organismus kann als ein System von Verteilungsräumen gesehen werden, in denen sich Stoffe vorzugsweise aufhalten - Beispiele sind der Intra- und der Extrazellulärraum, der Intra- und der Extravasalraum
usw.
Kompartimente: Der Organismus kann als ein System von Verteilungsräumen gesehen werden, in denen sich Stoffe vorzugsweise aufhalten - Beispiele sind der Intra- und der Extrazellulärraum, der Intra- und der Extravasalraum
usw.
Ein besonders wichtiger Verteilungsraum ist das Plasmavolumen,
d.h. der extrazelluläre Anteil des Blutvolumens - bei erwachsenen
Personen rund 3 Liter (abhängig von mehreren Größen, u.a. dem
Hämatokrit: bei 3 l Plasma und einem Hämatokrit - Volumenanteil von Blutkörperchen - von
0,4 ergibt sich 5 Liter Blutvolumen). Im Plasmavolumen lösen sich
primär die meisten Stoffe, welche die Blutbahn betreten, und das
Blutplasma ist die primäre Quelle von Flüssigkeit, die in das Gewebe filtriert (und den Zellen zur Verfügung gestellt) wird.
All diese Verteilungsräume haben definierte Aufgaben zu erfüllen
(z.B. das Blutvolumen als Basis-Zustandsgröße für die normale
Kreislauffunktion).
Ein “Indikator” (z.B. farbige oder radioaktive Substanz) wird
injiziert, seine Vermischung im Verteilungsraum abgewartet und seine
Konzentration bestimmt (je größer der Verteilungsraum, desto kleiner die
Konzentration des Stoffes).
Das Prinzip lautet: Konzentration des Indikatorstoffes (nach seiner
Verteilung) = Menge (M) des eingebrachten Indikators / Volumen (V), das
ermittelt werden soll: c = M / V. Das gesuchte Volumen errechnet sich als
Die Größe dieser physiologischen Verteilungsräume stellt eine wichtige
Information für den Arzt dar. Allerdings sind diese Volumina nicht
direkt meßbar, sondern nur indirekt bzw. durch komplizierte Verfahren.
Allgemein nennt man die Abschätzung eines solchen Verteilungsvolumens
eine Kompartmentanalyse: Das Volumen, in
dem sich ein Stoff verteilt, kann durch
Indikatorverdünnung gemessen
werden.
Meist nimmt man nach Injektion mehrfach
Blutproben, misst den Zeitverlauf des Konzentrationsabfalls und
extrapoliert den
Verteilungsraum zum Zeitpunkt der Injektion (Kompensation für
Ausscheidungsverlust). Kompartmentgrenzen werden von den sich
verteilenden Indikatorstoffen selten strikt eingehalten, was die
Berechnung von Verteilungsräumen erschwert. (Andererseits wäre ohne
solche "Undichtigkeiten" der Stoff unbegrenzt im Kompartment gefangen
und könnte nie ausgeschieden werden.)
Kennt man das
Volumen einer Körperflüssigkeit, so kann man aus der Konzentration
eines Stoffes dessen Menge im Kompartiment berechnen. Zum Beispiel:
 Wie viel Plasmaeiweiß befindet sich bei einer Eiweißkonzentration von 70
g/l in der Blutbahn, wenn das Plasmavolumen 3 Liter beträgt? (Antwort: 210 g)
Wie viel Plasmaeiweiß befindet sich bei einer Eiweißkonzentration von 70
g/l in der Blutbahn, wenn das Plasmavolumen 3 Liter beträgt? (Antwort: 210 g)
Kleine
Moleküle gelangen aus der Blutbahn rasch ins Interstitium. Große
Moleküle (Kolloide, Plasmaeiweiße) bleiben zunächst weitgehend im
Blutplasma - der Verlust von Albumin beträgt z.B. 5% der im Plasma
vorhandenen Menge pro Stunde.
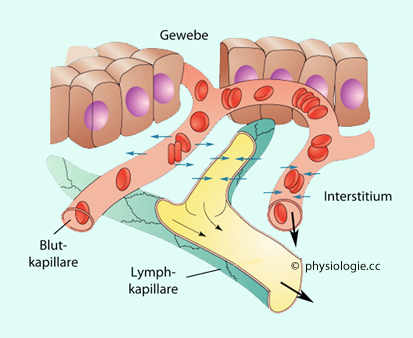
 Abbildung: Kompartimente - Zellen, Kapillaren, Interstitium
Nach einer Vorlage in Porth's Pathophysiology, 7th ed., 2005 Lippincott Williams & Wilkins
Abbildung: Kompartimente - Zellen, Kapillaren, Interstitium
Nach einer Vorlage in Porth's Pathophysiology, 7th ed., 2005 Lippincott Williams & Wilkins
Das
Kapillargebiet ist der Ort des Stoffaustauschs zwischen Transportsystem
(Blutkreislauf, Lymphsystem) und Zellen im Gewebe. Der extravasale
Stoffaustausch erfolgt über das Interstitium, das ist der Raum zwischen
Kapillaren einerseits, Gewebezellen andererseits
 Der Übertritt von Stoffen über Kompartimentgrenzen hinweg beruht auf
Der Übertritt von Stoffen über Kompartimentgrenzen hinweg beruht auf

Transport auf dem Blut- oder
Lymphweg
 Filtration
Filtration durch Kapillarwände (druckabhängig)
 Diffusion
Diffusion (konzentrationsabhängig; kann durch Permeasen unterstützt sein)

aktivem Transport (gegen ein Konzentrationsgefälle; energieverbrauchend)
 Osmose
Osmose (Wasser durchdringt semipermeable Grenzflächen, seinem Konzentrationsgradienten folgend)

anderen Mechanismen, z.B. Mitwandern gelöster Stoffe (
solvent drag, “Lösungsmittel-Sog”)
In der
Blutbahn verteilen sich infundierte Stoffe innerhalb von Minuten (Kreislauf als
Mischorgan; durchschnittliche Rezirkulation in ≤1 Minute). Die Aufnahme in das Interstitium und von hier in die Zellen
dauert Stunden bis Tage.


 Kompartimente sind funktionell definierte Verteilungsräume (z.B. Na+-Raum), sie können mit anatomisch definierten Räumen (z.B. Extrazellulärraum) mehr oder weniger exakt korrelieren. Extrazelluläre
Flüssigkeit ist reich an Kochsalz, intrazelluläre an Kalium.
Die extrazelluläre Flüssigkeit ist primärer Verteilungsraum für Substrate, Hormone, Stoffwechselprodukte, Medikamente. Von ~13 l
interstitieller Flüssigkeit sind ~8 l frei (direkt austauschbar), 2 l
im Knochen und 3 l in festem Bindegewebe "geparkt" und nur langsam austauschbar. Transzelluläre Flüssigkeiten befinden sich in epithelial umkleideten
Räumen, wie Liquor, Synovialflüssigkeit, Pleura-, Perikardial-, Peritonealflüssigkeit. Regelmechanismen stabilisieren die Volumina
von Blut (wichtig für Blutdruck, Perfusion u.a.), Liquor und anderen Flüssigkeiten, einschließlich die Aufnahme
(Darm) und Ausscheidung (Nieren) von Wasser und Elektrolyten (Volumenregulation) Kompartimente sind funktionell definierte Verteilungsräume (z.B. Na+-Raum), sie können mit anatomisch definierten Räumen (z.B. Extrazellulärraum) mehr oder weniger exakt korrelieren. Extrazelluläre
Flüssigkeit ist reich an Kochsalz, intrazelluläre an Kalium.
Die extrazelluläre Flüssigkeit ist primärer Verteilungsraum für Substrate, Hormone, Stoffwechselprodukte, Medikamente. Von ~13 l
interstitieller Flüssigkeit sind ~8 l frei (direkt austauschbar), 2 l
im Knochen und 3 l in festem Bindegewebe "geparkt" und nur langsam austauschbar. Transzelluläre Flüssigkeiten befinden sich in epithelial umkleideten
Räumen, wie Liquor, Synovialflüssigkeit, Pleura-, Perikardial-, Peritonealflüssigkeit. Regelmechanismen stabilisieren die Volumina
von Blut (wichtig für Blutdruck, Perfusion u.a.), Liquor und anderen Flüssigkeiten, einschließlich die Aufnahme
(Darm) und Ausscheidung (Nieren) von Wasser und Elektrolyten (Volumenregulation)
 Kompartimente gibt es auch in der Zelle: Teils decken sie sich mit dem Volumen von Zellorganellen, die durch Membranen umschlossen sind
(z.B. Zellkern, Mitochondrien), sie können sich auch vorübergehend
mittels molekularer Interaktionen und Strukturen ("Gerüstmoleküle")
ergeben, wie bei umschriebenen zytoplasmatischen Calciumwolken Kompartimente gibt es auch in der Zelle: Teils decken sie sich mit dem Volumen von Zellorganellen, die durch Membranen umschlossen sind
(z.B. Zellkern, Mitochondrien), sie können sich auch vorübergehend
mittels molekularer Interaktionen und Strukturen ("Gerüstmoleküle")
ergeben, wie bei umschriebenen zytoplasmatischen Calciumwolken
 Kinetik
betrifft Verteilung, Anreicherung, Umbau und Ausscheidung von Stoffen
im Körper. Sie hängt ab von Fettlöslichkeit, Größe und Ladung, Zustand
der Kapillarwände, des Interstitiums, der Zellmembranen, des
Stoffwechsels und der Ausscheidungswege. Verteilungsvolumina haben
definierte Aufgaben, z.B. ist das Blutvolumen eine basale Zustandsgröße
für die Kreislauffunktion (Vorlast für das Herz). Sie werden mittels Indikatorverdünnungsprinzip
bestimmt (Volumen = Menge / Konzentration). Meist werden nach Injektion
des Indikators mehrfach Blutproben genommen und aus dem Zeitverlauf des
Konzentrationsabfalls der Verteilungsraum extrapoliert (Zeitpunkt der
Injektion): Kleine Moleküle gelangen aus der Blutbahn rasch in das
Interstitium. Große Moleküle verbleiben zunächst im Blutplasma (Albuminverlust durch endotheliale Transzytose
~5%/h) Kinetik
betrifft Verteilung, Anreicherung, Umbau und Ausscheidung von Stoffen
im Körper. Sie hängt ab von Fettlöslichkeit, Größe und Ladung, Zustand
der Kapillarwände, des Interstitiums, der Zellmembranen, des
Stoffwechsels und der Ausscheidungswege. Verteilungsvolumina haben
definierte Aufgaben, z.B. ist das Blutvolumen eine basale Zustandsgröße
für die Kreislauffunktion (Vorlast für das Herz). Sie werden mittels Indikatorverdünnungsprinzip
bestimmt (Volumen = Menge / Konzentration). Meist werden nach Injektion
des Indikators mehrfach Blutproben genommen und aus dem Zeitverlauf des
Konzentrationsabfalls der Verteilungsraum extrapoliert (Zeitpunkt der
Injektion): Kleine Moleküle gelangen aus der Blutbahn rasch in das
Interstitium. Große Moleküle verbleiben zunächst im Blutplasma (Albuminverlust durch endotheliale Transzytose
~5%/h)
 Stoffe
übertreten Kompartimentgrenzen mittels Transport auf dem Blut- oder
Lymphweg, Filtration durch Kapillarwände, Diffusion, aktivem Transport,
Osmose oder andere Mechanismen (solvent drag). In der
Blutbahn verteilen sich infundierte Stoffe innerhalb von Minuten
(Kreislauf als Mischorgan; durchschnittliche Rezirkulationszeit ≤1
Minute) mittels konvektivem Transport. Die Aufnahme in das Interstitium (vorwiegend diffusiv) und von hier in die Zellen dauert Stunden bis Tage Stoffe
übertreten Kompartimentgrenzen mittels Transport auf dem Blut- oder
Lymphweg, Filtration durch Kapillarwände, Diffusion, aktivem Transport,
Osmose oder andere Mechanismen (solvent drag). In der
Blutbahn verteilen sich infundierte Stoffe innerhalb von Minuten
(Kreislauf als Mischorgan; durchschnittliche Rezirkulationszeit ≤1
Minute) mittels konvektivem Transport. Die Aufnahme in das Interstitium (vorwiegend diffusiv) und von hier in die Zellen dauert Stunden bis Tage
|

 Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.
Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.





 Verteilungsräume, Flüssigkeitshaushalt und Blutdruckregulation
Verteilungsräume, Flüssigkeitshaushalt und Blutdruckregulation
 Angiotensin: ανγειον = (Blut)Gefäß, tendere = (an)spannen
Angiotensin: ανγειον = (Blut)Gefäß, tendere = (an)spannen Gesamtkörperwasser
Gesamtkörperwasser  Extrazelluläre Flüssigkeit
Extrazelluläre Flüssigkeit  Intrazelluläre Flüssigkeit
Intrazelluläre Flüssigkeit  Transzelluläre Flüssigkeitsräume
Transzelluläre Flüssigkeitsräume  Natrium, extrazelluläres Volumen, Kreislauf
Natrium, extrazelluläres Volumen, Kreislauf  Verteilung infundierter / injizierter Substanzen
Verteilung infundierter / injizierter Substanzen
 Transzelluläre Flüssigkeit
Transzelluläre Flüssigkeit
 (compartments)
sind - morphologisch definierbare oder virtuelle - Volumina, in denen
sich körpereigene oder körperfremde Stoffe verteilen,
nachdem sie in
den Extrazellulärraum (in die Blutbahn) eingebracht wurden - durch
körpereigene Produktion (z.B. Kreatinin in der Muskulatur) oder von
außen (z.B. Injektion eines Pharmakons oder einer Indikatorsubstanz
(compartments)
sind - morphologisch definierbare oder virtuelle - Volumina, in denen
sich körpereigene oder körperfremde Stoffe verteilen,
nachdem sie in
den Extrazellulärraum (in die Blutbahn) eingebracht wurden - durch
körpereigene Produktion (z.B. Kreatinin in der Muskulatur) oder von
außen (z.B. Injektion eines Pharmakons oder einer Indikatorsubstanz  ).
).

 Teils decken sie sich mit dem Volumen von Zellorganellen
(z.B. Zellkern, Mitochondrien, Inhalt von Golgi-Apparat, Vesikeln,
endoplasmatischem Retikulum u.a.), die durch Membranen sichtbar von
ihrer Umgebung separiert sind, welche für viele Moleküle eine
Diffusionsbarriere darstellen,
Teils decken sie sich mit dem Volumen von Zellorganellen
(z.B. Zellkern, Mitochondrien, Inhalt von Golgi-Apparat, Vesikeln,
endoplasmatischem Retikulum u.a.), die durch Membranen sichtbar von
ihrer Umgebung separiert sind, welche für viele Moleküle eine
Diffusionsbarriere darstellen,  teils ergeben sie sich mittels molekularer Interaktionen und Strukturen durch "Gerüstmoleküle" (scaffold proteins), z.B. die Abgrenzung von zytoplasmatischen "Calciumwolken", die im Rahmen von Erregungsvorgängen vorübergehend frei- und wirksam werden.
teils ergeben sie sich mittels molekularer Interaktionen und Strukturen durch "Gerüstmoleküle" (scaffold proteins), z.B. die Abgrenzung von zytoplasmatischen "Calciumwolken", die im Rahmen von Erregungsvorgängen vorübergehend frei- und wirksam werden.
 Abbildung: Zusammensetzung von Körperflüssigkeiten im Vergleich
Abbildung: Zusammensetzung von Körperflüssigkeiten im Vergleich
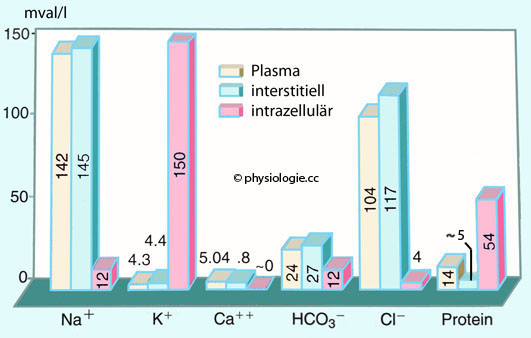
 Abbildung: Vergleich der wichtigsten Konzentrationswerte in Blutplasma, interstitieller und intrazellulärer Flüssigkeit
Abbildung: Vergleich der wichtigsten Konzentrationswerte in Blutplasma, interstitieller und intrazellulärer Flüssigkeit

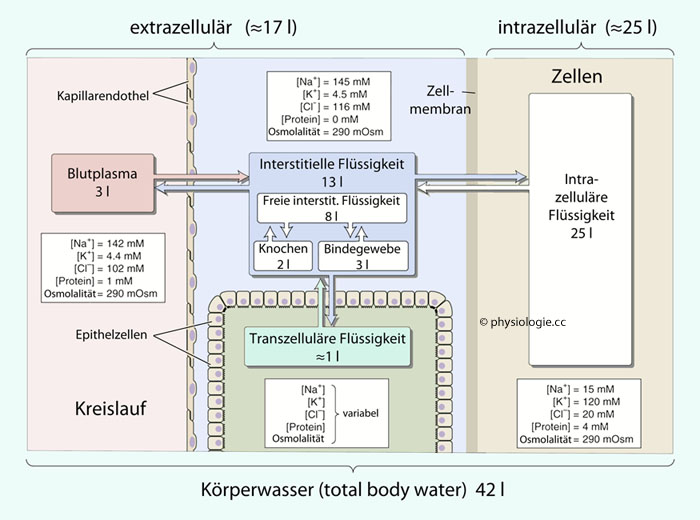
 Abbildung: Verteilung des Körperwassers bei einer 70kg schweren männlichen Referenzperson
Abbildung: Verteilung des Körperwassers bei einer 70kg schweren männlichen Referenzperson

 Rechenbeispiel: Es soll das intrazelluläre Flüssigkeitsvolumen einer Probandin ermittelt werden - aus folgenden Werten:
Rechenbeispiel: Es soll das intrazelluläre Flüssigkeitsvolumen einer Probandin ermittelt werden - aus folgenden Werten:
 Zur Zusammensetzung der intrazellulären Flüssigkeit s. oben
Zur Zusammensetzung der intrazellulären Flüssigkeit s. oben Transzelluläre Flüssigkeiten sind extrazelluläre Flüssigkeiten, die sich in komplett von Epithel umkleideten Räumen (transzellulären Räumen) befinden.
Sie werden von unterschiedlichen Epithelien sezerniert, ihre
Zusammensatzung unterscheidet sich untereinander und auch von der des
Blutplasmas. Ihr Gesamtvolumen im Körper eines erwachsenen Menschen beträgt etwa 1 Liter.
Transzelluläre Flüssigkeiten sind extrazelluläre Flüssigkeiten, die sich in komplett von Epithel umkleideten Räumen (transzellulären Räumen) befinden.
Sie werden von unterschiedlichen Epithelien sezerniert, ihre
Zusammensatzung unterscheidet sich untereinander und auch von der des
Blutplasmas. Ihr Gesamtvolumen im Körper eines erwachsenen Menschen beträgt etwa 1 Liter. Synovialflüssigkeit in
den Gelenksräumen (einige ml pro größerem Gelenk)
Synovialflüssigkeit in
den Gelenksräumen (einige ml pro größerem Gelenk) Hirn-Rückenmarks-Flüssigkeit (liquor cerebrospinalis, rund 150 ml, davon ca. 30 ml intraventrikulär)
Hirn-Rückenmarks-Flüssigkeit (liquor cerebrospinalis, rund 150 ml, davon ca. 30 ml intraventrikulär) Intraokuläre Flüssigkeit (0,25 ml Kammerwasser pro Auge)
Intraokuläre Flüssigkeit (0,25 ml Kammerwasser pro Auge) Pleuraflüssigkeit (10-20 ml, Proteinkonzentraion <15 g/l)
Pleuraflüssigkeit (10-20 ml, Proteinkonzentraion <15 g/l) Perikardialflüssigkeit (~20 ml)
Perikardialflüssigkeit (~20 ml) Peritonealflüssigkeit (10-20 ml, Ovulationsperiode bis 50 ml)
Peritonealflüssigkeit (10-20 ml, Ovulationsperiode bis 50 ml) über verfügbares Blutvolumen und Kochsalzaufnahme; über den Hirnstamm
werden Blutgefäße (peripherer Widerstand) und Nieren (Salzausscheidung)
entsprechend gesteuert.
über verfügbares Blutvolumen und Kochsalzaufnahme; über den Hirnstamm
werden Blutgefäße (peripherer Widerstand) und Nieren (Salzausscheidung)
entsprechend gesteuert.
 Abbildung:
Regelkreis für Natriumhaushalt und Blutdruckregulation
Abbildung:
Regelkreis für Natriumhaushalt und Blutdruckregulation ANP = atriale natriuretische Peptide
ANP = atriale natriuretische Peptide
 Abbildung).
Abbildung). dieser Substanz bezeichnet. Diese hängt von Fettlöslichkeit,
Größe und Ladung des Moleküls, sowie dem Zustand der
Kapillarwände, des Interstitiums, der Zellmembranen, des Stoffwechsels
und der Ausscheidungswege ab.
dieser Substanz bezeichnet. Diese hängt von Fettlöslichkeit,
Größe und Ladung des Moleküls, sowie dem Zustand der
Kapillarwände, des Interstitiums, der Zellmembranen, des Stoffwechsels
und der Ausscheidungswege ab. 
 Abbildung: Physiologisches Kompartmentmodell zur Beschreibung des Austauschs von Substanzen im Körper
Abbildung: Physiologisches Kompartmentmodell zur Beschreibung des Austauschs von Substanzen im Körper
 Wie viel Plasmaeiweiß befindet sich bei einer Eiweißkonzentration von 70
g/l in der Blutbahn, wenn das Plasmavolumen 3 Liter beträgt? (Antwort: 210 g)
Wie viel Plasmaeiweiß befindet sich bei einer Eiweißkonzentration von 70
g/l in der Blutbahn, wenn das Plasmavolumen 3 Liter beträgt? (Antwort: 210 g)
 Abbildung: Kompartimente - Zellen, Kapillaren, Interstitium
Abbildung: Kompartimente - Zellen, Kapillaren, Interstitium
 Transport auf dem Blut- oder Lymphweg
Transport auf dem Blut- oder Lymphweg Filtration durch Kapillarwände (druckabhängig)
Filtration durch Kapillarwände (druckabhängig) Diffusion (konzentrationsabhängig; kann durch Permeasen unterstützt sein)
Diffusion (konzentrationsabhängig; kann durch Permeasen unterstützt sein) aktivem Transport (gegen ein Konzentrationsgefälle; energieverbrauchend)
aktivem Transport (gegen ein Konzentrationsgefälle; energieverbrauchend) Osmose (Wasser durchdringt semipermeable Grenzflächen, seinem Konzentrationsgradienten folgend)
Osmose (Wasser durchdringt semipermeable Grenzflächen, seinem Konzentrationsgradienten folgend) anderen Mechanismen, z.B. Mitwandern gelöster Stoffe (solvent drag, “Lösungsmittel-Sog”)
anderen Mechanismen, z.B. Mitwandern gelöster Stoffe (solvent drag, “Lösungsmittel-Sog”)
 Kompartimente sind funktionell definierte Verteilungsräume (z.B. Na+-Raum), sie können mit anatomisch definierten Räumen (z.B. Extrazellulärraum) mehr oder weniger exakt korrelieren. Extrazelluläre
Flüssigkeit ist reich an Kochsalz, intrazelluläre an Kalium.
Die extrazelluläre Flüssigkeit ist primärer Verteilungsraum für Substrate, Hormone, Stoffwechselprodukte, Medikamente. Von ~13 l
interstitieller Flüssigkeit sind ~8 l frei (direkt austauschbar), 2 l
im Knochen und 3 l in festem Bindegewebe "geparkt" und nur langsam austauschbar. Transzelluläre Flüssigkeiten befinden sich in epithelial umkleideten
Räumen, wie Liquor, Synovialflüssigkeit, Pleura-, Perikardial-, Peritonealflüssigkeit. Regelmechanismen stabilisieren die Volumina
von Blut (wichtig für Blutdruck, Perfusion u.a.), Liquor und anderen Flüssigkeiten, einschließlich die Aufnahme
(Darm) und Ausscheidung (Nieren) von Wasser und Elektrolyten (Volumenregulation)
Kompartimente sind funktionell definierte Verteilungsräume (z.B. Na+-Raum), sie können mit anatomisch definierten Räumen (z.B. Extrazellulärraum) mehr oder weniger exakt korrelieren. Extrazelluläre
Flüssigkeit ist reich an Kochsalz, intrazelluläre an Kalium.
Die extrazelluläre Flüssigkeit ist primärer Verteilungsraum für Substrate, Hormone, Stoffwechselprodukte, Medikamente. Von ~13 l
interstitieller Flüssigkeit sind ~8 l frei (direkt austauschbar), 2 l
im Knochen und 3 l in festem Bindegewebe "geparkt" und nur langsam austauschbar. Transzelluläre Flüssigkeiten befinden sich in epithelial umkleideten
Räumen, wie Liquor, Synovialflüssigkeit, Pleura-, Perikardial-, Peritonealflüssigkeit. Regelmechanismen stabilisieren die Volumina
von Blut (wichtig für Blutdruck, Perfusion u.a.), Liquor und anderen Flüssigkeiten, einschließlich die Aufnahme
(Darm) und Ausscheidung (Nieren) von Wasser und Elektrolyten (Volumenregulation) Kompartimente gibt es auch in der Zelle: Teils decken sie sich mit dem Volumen von Zellorganellen, die durch Membranen umschlossen sind
(z.B. Zellkern, Mitochondrien), sie können sich auch vorübergehend
mittels molekularer Interaktionen und Strukturen ("Gerüstmoleküle")
ergeben, wie bei umschriebenen zytoplasmatischen Calciumwolken
Kompartimente gibt es auch in der Zelle: Teils decken sie sich mit dem Volumen von Zellorganellen, die durch Membranen umschlossen sind
(z.B. Zellkern, Mitochondrien), sie können sich auch vorübergehend
mittels molekularer Interaktionen und Strukturen ("Gerüstmoleküle")
ergeben, wie bei umschriebenen zytoplasmatischen Calciumwolken Kinetik
betrifft Verteilung, Anreicherung, Umbau und Ausscheidung von Stoffen
im Körper. Sie hängt ab von Fettlöslichkeit, Größe und Ladung, Zustand
der Kapillarwände, des Interstitiums, der Zellmembranen, des
Stoffwechsels und der Ausscheidungswege. Verteilungsvolumina haben
definierte Aufgaben, z.B. ist das Blutvolumen eine basale Zustandsgröße
für die Kreislauffunktion (Vorlast für das Herz). Sie werden mittels Indikatorverdünnungsprinzip
bestimmt (Volumen = Menge / Konzentration). Meist werden nach Injektion
des Indikators mehrfach Blutproben genommen und aus dem Zeitverlauf des
Konzentrationsabfalls der Verteilungsraum extrapoliert (Zeitpunkt der
Injektion): Kleine Moleküle gelangen aus der Blutbahn rasch in das
Interstitium. Große Moleküle verbleiben zunächst im Blutplasma (Albuminverlust durch endotheliale Transzytose
~5%/h)
Kinetik
betrifft Verteilung, Anreicherung, Umbau und Ausscheidung von Stoffen
im Körper. Sie hängt ab von Fettlöslichkeit, Größe und Ladung, Zustand
der Kapillarwände, des Interstitiums, der Zellmembranen, des
Stoffwechsels und der Ausscheidungswege. Verteilungsvolumina haben
definierte Aufgaben, z.B. ist das Blutvolumen eine basale Zustandsgröße
für die Kreislauffunktion (Vorlast für das Herz). Sie werden mittels Indikatorverdünnungsprinzip
bestimmt (Volumen = Menge / Konzentration). Meist werden nach Injektion
des Indikators mehrfach Blutproben genommen und aus dem Zeitverlauf des
Konzentrationsabfalls der Verteilungsraum extrapoliert (Zeitpunkt der
Injektion): Kleine Moleküle gelangen aus der Blutbahn rasch in das
Interstitium. Große Moleküle verbleiben zunächst im Blutplasma (Albuminverlust durch endotheliale Transzytose
~5%/h)  Stoffe
übertreten Kompartimentgrenzen mittels Transport auf dem Blut- oder
Lymphweg, Filtration durch Kapillarwände, Diffusion, aktivem Transport,
Osmose oder andere Mechanismen (solvent drag). In der
Blutbahn verteilen sich infundierte Stoffe innerhalb von Minuten
(Kreislauf als Mischorgan; durchschnittliche Rezirkulationszeit ≤1
Minute) mittels konvektivem Transport. Die Aufnahme in das Interstitium (vorwiegend diffusiv) und von hier in die Zellen dauert Stunden bis Tage
Stoffe
übertreten Kompartimentgrenzen mittels Transport auf dem Blut- oder
Lymphweg, Filtration durch Kapillarwände, Diffusion, aktivem Transport,
Osmose oder andere Mechanismen (solvent drag). In der
Blutbahn verteilen sich infundierte Stoffe innerhalb von Minuten
(Kreislauf als Mischorgan; durchschnittliche Rezirkulationszeit ≤1
Minute) mittels konvektivem Transport. Die Aufnahme in das Interstitium (vorwiegend diffusiv) und von hier in die Zellen dauert Stunden bis Tage