

Eine Reise durch die Physiologie - Wie der Körper des Menschen funktioniert

Somatosensorik
© H. Hinghofer-Szalkay

-Ästhesie: αἴσϑησις = Wahrnehmung, Empfindung
Braille-Schrift: Louis Braille
Dermatom: δέρμα = Haut‘, τομή tomḗ = (Ab-)Schnitt
Frey'sches Reizhaar: Maximilian v. Frey
Haptik: ἆφή = Berührung, ἁπτός = fühlbar
lemniskales System: lemniscus = Band, Schleife ("Schleifenbahn")
Lissauer-Trakt (tr. posterolateralis): Heinrich Lissauer
Meissner'sche Körperchen: Georg Meissner
Kinästhesie: κινειν = bewegen; αἴσθησις = Wahrnehmung
Krause'sche Endkolben: Wilhelm Krause
Merkel-Zellen: Friedrich Merkel
Ruffini-Körperchen: Angelo Ruffini
somatisch: σῶμα = Körper
Vater-Pacini-Körperchen: Abraham Vater, Filippo Pacini
Weber'scher Versuch: Ernst Weber
Physikalische Information (Druck, Berührung, Vibration, Kälte, Wärme) wird über Exterozeptoren (Haarfollikelrezeptoren, Merkelzellen, Ruffini-, Meissner-, Vater-Pacini-Körperchen) von der Haut (Oberflächensensibilität) und aus Muskeln (Muskelspindeln), Sehnen (Sehnenrezeptoren) und Bändern gesendet (Tiefensensibilität). Das ermöglicht die Analyse von Form, Gewicht, Volumen, Oberflächenbeschaffenheit berührter Gegenstände (Haptik) sowie Kraft, Lage und Bewegung im Bewegungsapparat (Kinästhesie).
Juckreiz löst Kratzbewegungen aus - im Gegensatz zu Schmerz, der Beugereflexe auslöst (und der mit dem Juckphänomen Auslöser wie Histamin, Rezeptoren wie TRP-Rezeptoren, Transmitter und C-Nervenfasern weitgehend überschneidend teilt).
Das Auflösungsvermögen (2-Punkte-Diskriminierung) richtet sich nach den
jeweiligen Ansprüchen an die Präzision der Informationsverarbeitung.
Afferenzen erfolgen über Aβ-, Aδ- und C-Fasern; das lemniskale System
leitet Impulse aus dem Gesichtsbereich über den N. trigeminus, vom Rest
der Körperoberfläche (Hinterkopf, Hals, Rumpf, Extremitäten) über
Leitungsbahnen im Rückenmark.
Neuronale Bearbeitung ("Umschaltungen")
erfolgt in Hirnstamm, Thalamus und hinterer Zentralwindung sowie
assoziierten Cortexarealen, wo aus Empfindungen Wahrnehmungen werden.
|
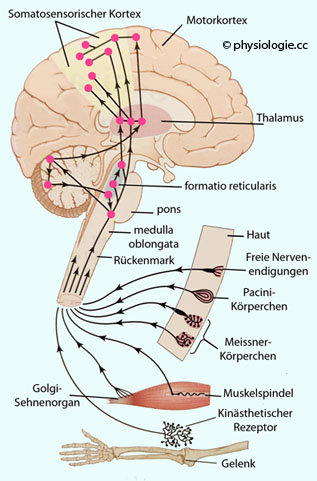
 Abbildung: Somatosensorische Achse des Nervernsystems
Abbildung: Somatosensorische Achse des Nervernsystems
Nach einer Vorlage bei Guyton and Hall, Textbook of Medical Physiology, 15th ed. Elsevier 2026
Sinnesrezeptoren
auf der Körperoberfläche (Haut) sowie in einigen tieferen Strukturen
(Muskelspindeln, Sehnenspindeln) generieren Informationen, die via
somatisch-afferente Nervenfasern an das ZNS vermittelt werden. Diese
Meldungen werden in Rückenmark, Hirnstamm, Klein- und Großhirn
verarbeitet, führen zu entsprechenden Wahrnehmungen und beeinflussen
Motorik, Verhalten, autonom-nervöse und hormonelle Reaktionen

Somatische
(körperliche) und viszerale (Eingeweide-) Sensibilität informieren das
ZNS fortlaufend über das "Hier und Jetzt" der körperlichen Zustände und
potentiellen Gefahren (Afferenzen). Dadurch versetzen sie den Körper in die Lage, jederzeit in angemessener Weise zu (re)agieren, wobei sich diese Efferenzen auf die Aktivität von Muskel- und Drüsenzellen auswirken.
 Sinnesmeldungen von der Körperoberfläche werden unter dem Begriff Oberflächensensibilität (kutane Sensibilität
- die Haut wird auch als das größte Sinnesorgan bezeichnet)
zusammengefasst, solche aus der Tiefe des Bewegungsapparates (Muskeln,
Sehnen, Gelenke etc) als Tiefensensibilität, beide zusammen als somatische Sensibilität oder Somatosensorik
Sinnesmeldungen von der Körperoberfläche werden unter dem Begriff Oberflächensensibilität (kutane Sensibilität
- die Haut wird auch als das größte Sinnesorgan bezeichnet)
zusammengefasst, solche aus der Tiefe des Bewegungsapparates (Muskeln,
Sehnen, Gelenke etc) als Tiefensensibilität, beide zusammen als somatische Sensibilität oder Somatosensorik .
.
 Über Tiefensensibilität (Propriozeption, Muskel- und Sehnenspindeln, Lagesinn, Kraftsinnn, Bewegungssinn) s. dort
Über Tiefensensibilität (Propriozeption, Muskel- und Sehnenspindeln, Lagesinn, Kraftsinnn, Bewegungssinn) s. dort
 Über viszerale Sensibilität / Interozeption s. dort und dort
Über viszerale Sensibilität / Interozeption s. dort und dort
Klassifizierung somatosensorischer Neuronen

Nach Liqun Luo, Principles of Neurobiology, 2nd ed. 2021
|
Empfindung
|
Reiztyp
|
Axonfaser
|
Periphere Endigung / Aktionspotentialmuster
|
Propriozeption
|
mechanisch
|
Aα, Aβ
|
Muskelspindeln
Sehnen
Gelenke
|
Berührung
|
mechanisch
|
Aβ |
Merkel-Zellen (SA)
|
| Aβ |
Meissner-Körperchen (RA)
|
| Aβ |
Pacini-Körperchen (RA)
|
Aβ, Aδ, C
|
Haarfollikel
|
Temperatur
Schmerz
Jucken
|
mechanisch
|
Aδ, C |
Freie Nervenendigungen in der Haut
|
Hitze
Kälte
chemisch
|
Aδ, C |
Freie Nervenendigungen in Haut und inneren Organen
|
Das Sinnesorgan des somatosensorischen
Systems ist die Haut und die Skelettmuskulatur (und damit das größte im
Körper). Es reagiert auf mechanische, chemische und Temperaturreize.
Aus diesen Stimuli leitet es Information über mechanische Reizung der
Haut (Druck, Berührung), Position und Bewegung der Körperteile
(Propriozeption), weiters über Temperatur (Thermosensitivität), Schmerz
(Nozizeption) sowie Juckreize (Prurizeption) ab. All diese Information
hängt mir Einflüssen aus der Umwelt zusammen (Exterozeption); Meldungen aus den Eingeweiden (viszerale Sensibilität, Interozeption) erfolgen über das autonome Nervensystem.
Der Zellkörper aller somatosensorischen Neurone liegt in einem Spinalganglion (dorsal root ganglion)
- davon verfügt der Mensch über 31 Paare (8 zervikale, 12 thorakale, je
5 lumbale und sakrale) - oder in einem der 2 Trigeminuskerne
(Gesichtsbereich). Die Neurone haben einen kurzen axonalen Fortsatz,
der sich dann aufteilt (Bifurkation) in ein peripheres Axon (sammelt Information von Haut und Muskeln) und ein zentrales Axon (sendet an Rückenmark bzw. Hirnstamm weiter -  Abbildung).
Abbildung).
Die an den
sensorischen Endigungen entstehenden reizproportionalen
Generatorpotentiale (Rezeptorpotentiale) werden in
Aktionspotentialfrequenzen übersetzt ("analog zu digital"). Die
räumlich-zeitlichen Muster der elektrischen Aktivität teilen dem ZNS
mit, welcher Art die sensorischen Reize sind, wo im Körper sie
entstehen und wie stark sie sind.

 Abbildung: Peripherie des somatosensorischen Systems
Abbildung: Peripherie des somatosensorischen Systems
Nach einer Vorlage in Liqun Luo, Principles of Neurobiology, 2nd ed. CRC Press 2021
Jeder Neuronentyp zeigt spezifische Endigungsmuster in der sensorischen
Peripherie und projiziert auf definierte laminae im Hinterhorn des
Rückenmarks. Die Leitungsgeschwindigkeiten reichen von ~100 m/s (sehr gut myelinisierte Aα-, rot - Muskelspindeln) bis zu ~1
m/s (kaum myelinisierte C-Fasern, hellgrün - dumpfer Schmerz).
Information von Merkel-Scheiben und Haarfollikeln wird über Aβ-Fasern geleitet, Temperaturempfindung und Schmerz
über Aδ-Fasern (blau, 1-5 m/s), Schmerz auch über C-Fasern (grün, 0,5-2
m/s). Aδ- und C-Fasern haben in der Peripherie freie Nervenendigungen.
Zahlreiche Fasern sind polymodal, sie dienen z.B. sowohl der Schmerz- als auch der Temperaturempfindung.
Afferenzen von Muskelspindeln (Aα) endigen im zentralen und ventralen
Spinalmark, von Haarfollikeln und Merkel-Scheiben in laminae III bis V,
von Thermosensoren in laminae I und V, und von Schmerzrezeptoren in
laminae I und II (vgl. weiter unten)

Die größte Zahl somatosensorischer Neurone entfällt auf mechanozeptive
- sowohl von der Körperoberfläche als aus der Muskulatur. Druck,
Berührung und Vibration (Mechanozeption) sprechen schon auf
geringgradige Kräfte an und werden als niedrigschwellige
Mechanorezeptoren (LTMR: low-threshold mechanoreceptors) bezeichnet. Mechanorezeptive Schmerzfasern hingegen sind HTMRs (high-threshold mechanoreceptors), sie reagieren erst auf höhere Verformungskräfte.
Somatosensorik wird über "pseudounipolare" sensorische Hinterhornzellen (dorsal root ganglion neurons) vermittelt,
deren periphere Endigungen die Haut (jeweils in einem Dermatom -  Abbildung oben),
Muskeln, Gelenkskapseln oder Eingeweide innervieren und über spezielle
Rezeptoren verfügen (Detektion mechanischer, thermischer, chemischer
Reize). Die zentralen Axonsegmente endigen im Rückenmark (Spinalnerven)
oder Hirnstamm (Hirnnerven). Der Körper des Neurons liegt jeweils in
einem Ganglion in der Nähe des ZNS.
Abbildung oben),
Muskeln, Gelenkskapseln oder Eingeweide innervieren und über spezielle
Rezeptoren verfügen (Detektion mechanischer, thermischer, chemischer
Reize). Die zentralen Axonsegmente endigen im Rückenmark (Spinalnerven)
oder Hirnstamm (Hirnnerven). Der Körper des Neurons liegt jeweils in
einem Ganglion in der Nähe des ZNS.
Die Mechano-, Thermo- und/oder Schmerzrezeption erfolgt über spezielle Ionenkanäle wie TRP-Kanäle an sensibel-afferenten Nervenzellen. Diese bestehen aus folgenden funktionellen Zonen:
 Rezeptive
Zone (verfügt über spezifische Rezeptoren und produziert
reizproportionale Rezeptorpotentiale, hat keine spannungsgesteuerten Na+- oder K+-Kanäle),
Rezeptive
Zone (verfügt über spezifische Rezeptoren und produziert
reizproportionale Rezeptorpotentiale, hat keine spannungsgesteuerten Na+- oder K+-Kanäle),
 Entstehungsort von Aktionspotentialen (spike generation site - mit spannungsgesteuerten Na+-Kanälen, üblicherweise unmittelbar vor der ersten Schwann-Zelle),
Entstehungsort von Aktionspotentialen (spike generation site - mit spannungsgesteuerten Na+-Kanälen, üblicherweise unmittelbar vor der ersten Schwann-Zelle),
 periphere Faser (leitet Aktionspotentiale zum ZNS),
periphere Faser (leitet Aktionspotentiale zum ZNS),
 Zellkörper (exprimiert u.a. Rezeptorproteine),
Zellkörper (exprimiert u.a. Rezeptorproteine),
 zentrale Faser in einem Spinal / Hirnnerv (mit
synaptischen Verschaltungen).
zentrale Faser in einem Spinal / Hirnnerv (mit
synaptischen Verschaltungen).
Mechanorezeptive Fasern beginnen in
kapselförmigen Hilfsapparaten (z.B. Tastkörperchen, Muskelspindel),
während Temperatur und Schmerz über freie Nervenendigungen vermittelt
werden.
Viszerale
Sensibilität vermittelt Information aus Eingeweiden wie Herz, Lunge,
gastrointestinalem System, Nieren und Urogenitalsystem. Zusammen
mit der Oberflächen- (Haut) und Tiefensensibilität (Muskeln, Sehnen, Gelenke) vermitteln diese Afferenzen laufend ein aktuelles Bild über Vorgänge in
der Umgebung (Exterozeption) und im Körper selbst (Interozeption),
wobei Vorgänge aus der somatischen Sensibilität z.T. bewusst werden,
solche aus den Eingeweiden in aller Regel unbewusst bleiben.
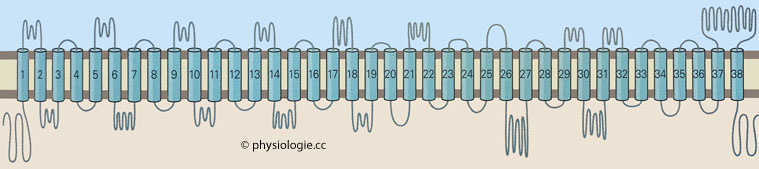
 Abbildung: Piezo-Protein
Abbildung: Piezo-Protein
Nach einer Vorlage in Kandel / Koester / Mack / Siegelbaum (eds), Principles of Neural Sciences, 6th ed. 2021 (McGraw Hill)
Das Protein besteht aus ~2500
Aminosäuren und hat zahlreiche transmembranale Sequenzen. Solchermaßen
fest in der Membran verankert, sind Piezo-Proteine die größten
Ionenkanäle, über die Säugetiere verfügen. Der Ionenkanal (durchgängig
für Kationen) ist aus drei gleichen Protein-Einheiten aufgebaut.
Zwei Isoformen fungieren als Mechanosensoren: Piezo1 (Abbildung)
vorwiegend in nicht-neuronalen Zellen (Epithelien, Blutgefäße,
Erythrozyten, Niere, Harnblase) und Piezo2 in rasch adaptierenden mechanosensiblen
Hinterhornzellen (z.B. versorgen solche Neurone glatte Muskulatur im
Lungengewebe, wo sie den Hering-Breuer-Reflex mediieren)
 Abbildung); TRP-Kanäle für Mechano-, Thermo- und Nozizeption. Im N. medianus finden sich z.B. 22 afferente und 8 efferente Fasertypen (zu Muskeln, Schweißdrüsen, Blutgefäßen).
Abbildung); TRP-Kanäle für Mechano-, Thermo- und Nozizeption. Im N. medianus finden sich z.B. 22 afferente und 8 efferente Fasertypen (zu Muskeln, Schweißdrüsen, Blutgefäßen).
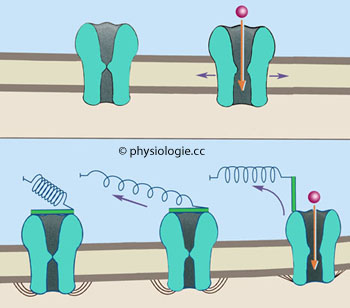
 Abbildung: Ionenkanäle in mechanorezeptiver Nervenzellmembran (schematisch)
Abbildung: Ionenkanäle in mechanorezeptiver Nervenzellmembran (schematisch)
Nach Lin SY, Corey DP. TRP channels in mechanosensation. Curr Opin Neurobiol 2005; 15: 350-7
Diese
Ionenkanäle werden durch mechanische Kräfte aktiviert, welche die
Zellmembran deformieren oder zerren.
Oben: Krafteinwirkung aus der
Lipidschichte (force from lipids)
Unten: Krafteinwirkung über (intra- oder extrazelluläre)
elastische Strukturproteine (force from filaments)
Mechanorezeptoren
reagieren auf physikalische Veränderungen wie Biegung und Streckung der
Haut (Vibration. Druck, Zerrung), Dehnung der Wand von Hohlräumen
(Vorhöfe, Ventrikel, Blutgefäße, Darm, Harnwege), Druck auf den
Halteapparat der Zähne, Dehnung von Muskel- und Sehnenspindeln, Gelenksrezeptoren.
Dabei spielen einerseits Deformationen der Lipidschichte
in der Membran (force from lipids)
eine Rolle, was über stärkere Wirkung hydrophober Gruppen auf den Rezeptor zu
Öffnung der Ionenkanäle führt. Das gilt beispielsweise bei Veränderung des Blutdrucks
(Gefäßwand) oder der osmotischen Konzentration (Zellschwellung), oder bei mechanischer Verankerung der Rezeptormoleküle mit der
Umgebung (force from filaments), welche die Kanäle "aufspreizen" ( Abbildung) - wie bei einigen Berührungsrezeptoren in der Haut oder Haarzellen im Innenohr.
Abbildung) - wie bei einigen Berührungsrezeptoren in der Haut oder Haarzellen im Innenohr.
Die somatische Sensibilität entwickelt sich in der
Embryonalperiode vor allen anderen Sinnessystemen. Er ermöglicht
nicht nur
die Detektion mechanischer, thermischer und Schmerzreize, sondern in
der Gesamtheit ein
"Körpergefühl", das dem Gehirn die Existenz des eigenen Körpers und
dessen Grenzen zur Umwelt zu signalisieren hilft.
Der Tastsinn (das
Tast-Sinnessystem) ist der am frühesten in Funktion tretende Sinn überhaupt:
Schon ab der 5. Schwangerschaftswoche lassen sich beim Embryo (zu dieser Zeit kaum länger als 1 cm) motorische Reaktionen
(Zurückweichen) auf mechanische Reizung im Gesichtsbereich nachweisen. Alle anderen
Sinne zeigen erst später Aktivitätszeichen.
Der rechte Parietallappen spielt die
führende Rolle im Rahmen der Sensibilität für, und Einordnung von
taktil-haptischen Informationen. Defekte in diesem Gehirnbereich können
zu ausgeprägten Störungen der Körperempfindung (z.B. Neglect-Syndrom)
führen.
Mechanosensibel sind (RA = rasch, SA = langsam adaptierend)
 Haarfollikelrezeptoren (hair follicle nerve receptors; RA- sowie SA-Rezeptoren) ermöglichen die Wahrnehmung von Bewegung und Abwinkelung von Haaren
Haarfollikelrezeptoren (hair follicle nerve receptors; RA- sowie SA-Rezeptoren) ermöglichen die Wahrnehmung von Bewegung und Abwinkelung von Haaren
 Merkelzellen
Merkelzellen  sind spezialisierte Epithelzellen, die sich zu Merkel-Scheiben (Merkel's disks) zusammentun
und noradrenerg (ß-Rezeptoren) auf die angeschlossenen sensorischen
Nervenfaserm wirken. Es handelt sich um SA1-Rezeptoren;
in der gesamten Haut insgesamt ~60 Millionen (in der Hand des Menschen machen sie ~25% der mechanosensorischen Innervation aus). SA bedeutet langsame
Adaptation, d.h. die Sensoren generieren bei konstantem Druck beständig
Aktionspotentiale ("Proportional"-Ansprechverhalten). Die betreffenden
rezeptiven Felder sind relativ
klein, die Auflösung ist hoch, es können feine Merkmale ertastet
werden. Merkel-Scheiben bezeichnet man auch als SAI-LTMR (slow-adapting type I low-threshold mechanoreceptors)
sind spezialisierte Epithelzellen, die sich zu Merkel-Scheiben (Merkel's disks) zusammentun
und noradrenerg (ß-Rezeptoren) auf die angeschlossenen sensorischen
Nervenfaserm wirken. Es handelt sich um SA1-Rezeptoren;
in der gesamten Haut insgesamt ~60 Millionen (in der Hand des Menschen machen sie ~25% der mechanosensorischen Innervation aus). SA bedeutet langsame
Adaptation, d.h. die Sensoren generieren bei konstantem Druck beständig
Aktionspotentiale ("Proportional"-Ansprechverhalten). Die betreffenden
rezeptiven Felder sind relativ
klein, die Auflösung ist hoch, es können feine Merkmale ertastet
werden. Merkel-Scheiben bezeichnet man auch als SAI-LTMR (slow-adapting type I low-threshold mechanoreceptors)
 Ruffini-Körperchen
Ruffini-Körperchen  (bulbous corpuscles, Ruffini endings; SA2-Rezeptoren) - auch SAII-LTMR (slow-adapting type II low-threshold mechanoreceptors)
- tragen zur kinästhetischen Kontrolle bei (Fingerposition und
-bewegung; in der Hand des Menschen machen sie ~20% der mechanosensorischen Innervation aus). Sie liegen tiefer als Merkelzellen und registrieren hier
Änderungen der mechnischen Spannung, unter der Gewebestrukturen stehen
- ähnlich den Golgi-Sehnenrezeptoren.
(bulbous corpuscles, Ruffini endings; SA2-Rezeptoren) - auch SAII-LTMR (slow-adapting type II low-threshold mechanoreceptors)
- tragen zur kinästhetischen Kontrolle bei (Fingerposition und
-bewegung; in der Hand des Menschen machen sie ~20% der mechanosensorischen Innervation aus). Sie liegen tiefer als Merkelzellen und registrieren hier
Änderungen der mechnischen Spannung, unter der Gewebestrukturen stehen
- ähnlich den Golgi-Sehnenrezeptoren.
 Meissner-Körperchen
Meissner-Körperchen  (Meissner's corpuscles; RA1-Rezeptoren, insgesamt etwa eine halbe Million) - auch RAI-LTMR (rapidly adapting type I low-threshold mechanoreceptors). In der Hand des Menschen machen sie ~40% der mechanosensorischen Innervation aus. Sie detektieren Bewegung der Haut, u.a. niedrigfrequente Vibration. RA bedeutet rasche Adaptation, d.h. die Sensoren feuern nur zu Beginn und nach Beendigung eines mechanischen Reizes ("Differenzial"-Ansprechverhalten)
(Meissner's corpuscles; RA1-Rezeptoren, insgesamt etwa eine halbe Million) - auch RAI-LTMR (rapidly adapting type I low-threshold mechanoreceptors). In der Hand des Menschen machen sie ~40% der mechanosensorischen Innervation aus. Sie detektieren Bewegung der Haut, u.a. niedrigfrequente Vibration. RA bedeutet rasche Adaptation, d.h. die Sensoren feuern nur zu Beginn und nach Beendigung eines mechanischen Reizes ("Differenzial"-Ansprechverhalten)
 Krause'sche-Endkolben
Krause'sche-Endkolben  (bulboid corpuscles, end-bulbs of Krause) innervieren Randzonen von Haut und Schleimhäuten, wie um die Lippen und äußeren Genitalien; vermutlich sind es RA-Rezeptoren.
(bulboid corpuscles, end-bulbs of Krause) innervieren Randzonen von Haut und Schleimhäuten, wie um die Lippen und äußeren Genitalien; vermutlich sind es RA-Rezeptoren.
 (Vater-) Pacini-Körperchen
(Vater-) Pacini-Körperchen  (Pacinian Corpuscle) - auch RAII-LTMR (rapidly adapting type II low-threshold mechanoreceptors)
- detektieren tiefen Druck. In der Hand des Menschen machen sie 10-15% der mechanosensorischen Innervation aus. Im Experiment reagieren sie empfindlich auf
Vibration - ein Reiztyp, der in der Natur so gut wie nicht vorkommt,
daher ist die Bezeichnung "Vibrationsrezeptor"
eigentlich irreführend. Plätzliche Lageveränderung eines Gegenstandes
wird von Pacini-Körperchen bereits detektiert, wenn sich die Position
um ca. 10 µm ändert. Das kann schon ausreichen, um beginnendes
"Rutschen" eines von Fingern gehaltenen Gegenstandes durch Erhöhung des
Griffdrucks rechtzeitig zu stoppen.
(Pacinian Corpuscle) - auch RAII-LTMR (rapidly adapting type II low-threshold mechanoreceptors)
- detektieren tiefen Druck. In der Hand des Menschen machen sie 10-15% der mechanosensorischen Innervation aus. Im Experiment reagieren sie empfindlich auf
Vibration - ein Reiztyp, der in der Natur so gut wie nicht vorkommt,
daher ist die Bezeichnung "Vibrationsrezeptor"
eigentlich irreführend. Plätzliche Lageveränderung eines Gegenstandes
wird von Pacini-Körperchen bereits detektiert, wenn sich die Position
um ca. 10 µm ändert. Das kann schon ausreichen, um beginnendes
"Rutschen" eines von Fingern gehaltenen Gegenstandes durch Erhöhung des
Griffdrucks rechtzeitig zu stoppen.
Die häufigsten taktilen Afferenzen zum ZNS bestehen aus RA1-Fasern (von Meissner'schen
Tastkörperchen). Pacini-Körperchen haben sehr große, Merkel- und
Meissner-Körperchen sehr kleine rezeptive Felder. Die Verteilung dieser Rezeptoren ist unterschiedlich: So finden sich
Meissner-Körperchen vorwiegend an besonders empfindlichen Stellen wie
Augenlidern, Handflächen und Fußsohlen, Genitalien, Brustwarzen;
Merkel-Scheiben kommen nur in tieferen Schichten der unbehaarten Haut
(glabrous skin) vor; Haarfollikelrezeptoren nur in behaarter Haut (hairy skin).
Rezeptoren in der Haut
Modifiziert nach Massey / Cunniffe / Noorani, Carpenter's Neurophysiology - A Conceptual Approach, 6th ed. CRC Press 2022 |
Bezeichnung
|
Adaptation
|
Faser
|
Reiz
|
Meissner
|
komplett
|
Aß
|
Scherkraft
|
Merkel
|
partiell
|
Aß
|
Kontakt
|
Pacini
|
komplett
|
Aß
|
tiefer Druck / Vibration
|
Ruffini
|
partiell
|
Aß
|
Spannung, Faltung
|
Krause
|
komplett
|
Aß
|
?
|
freie Endigung
|
keine
|
C
|
mechanisch, chemisch, Schmerz
|
warm
|
partiell
|
C
|
Wärme
|
kalt
|
partiell
|
Aδ, C
|
Kälte / Hize
|
Schmerz
|
?
|
Aδ, C |
Schmerz / mechanisch
|
Man schätzt, dass der menschliche Körper über mehrere hundert Millionen tastsensibler Rezeptoren verfügt (9.108?). Die Empfindlichkeit des
Tastsinns ist so hoch, dass man mit der Fingerspitze bereits einen
Gegenstand von 0,04 mm Durchmesser und 0,006 mm Höhe ertasten kann
(Braille-Punkte der Blindenschrift sind mehr als hundertmal größer:
Punkthöhe ≥0,4 mm).
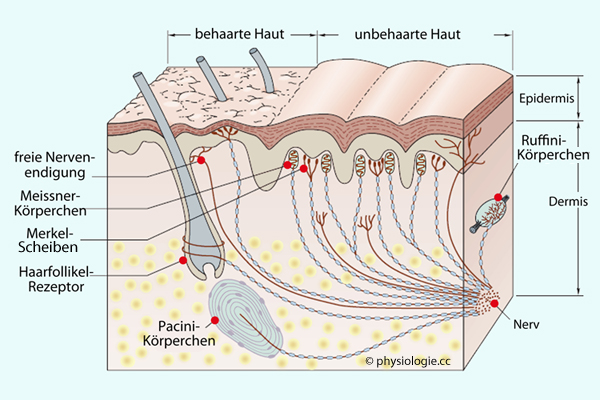
 Abbildung: Rezeptoren in der Haut
Nach einer Vorlage bei Kandel / Schwartz / Jessel: Principles of Neural Science, 4th ed. McGraw-Hill Professional 2000
Abbildung: Rezeptoren in der Haut
Nach einer Vorlage bei Kandel / Schwartz / Jessel: Principles of Neural Science, 4th ed. McGraw-Hill Professional 2000
Links: Behaarte Haut (hier übernehmen Haarfollikelrezeptoren die Rolle der Meissner-Körperchen als RA-Rezeptoren). Rechts: Unbehaarte Leistenhaut (Lippen, Handflächen, Fußsohlen).
Eingekapselte
Rezeptorstrukturen (in denen afferente Nervenfasern endigen) sind
Meissner-Körperchen, Merkel-Scheiben, Ruffini-Körperchen; sie finden
sich in unbehaarter Haut (Handflächen, Fußsohlen, Lippen, Augenlider,
Teile der Genitalien, Übergangsschleimhaut). Einige sind auch in
viszerale Strukturen, Gelenke, Ligamente und Bindegewebe eingebettet. Freie Nervenendigungen finden sich überall in der Haut (Haarfollikel verfügen über eigene Rezeptoren), weiters in Faszien sowie in Eingeweiden

Somatische Sensibilität umfasst
 Oberflächensensibilität
aus der Haut (
Oberflächensensibilität
aus der Haut ( Abbildung - Druck, Berührung, Vibration) - sie ermöglicht z.B. die
Ertastung auch kleinster Erhebungen an einer Oberfläche (wenige µm,
d.h. zwei Zehnerpotenzen weniger als gerade noch optisch wahrnehmbare
Strukturen) - und kann Schmerz vermitteln; und
Abbildung - Druck, Berührung, Vibration) - sie ermöglicht z.B. die
Ertastung auch kleinster Erhebungen an einer Oberfläche (wenige µm,
d.h. zwei Zehnerpotenzen weniger als gerade noch optisch wahrnehmbare
Strukturen) - und kann Schmerz vermitteln; und
 Tiefensensibilität in Muskeln, Sehnen, Gelenken und Bändern. Hier unterscheidet man Kraft-, Lage- (Stellungs-) und Bewegungssinn (Kinästhesie
Tiefensensibilität in Muskeln, Sehnen, Gelenken und Bändern. Hier unterscheidet man Kraft-, Lage- (Stellungs-) und Bewegungssinn (Kinästhesie  ).
).
 Kräfte werden vor allem über Sehnenspindeln detektiert, die auf Dehnung ansprechen und langsam adaptierten (SA-Rezeptoren: slowly adapting, Proportionaldetektion).
Kräfte werden vor allem über Sehnenspindeln detektiert, die auf Dehnung ansprechen und langsam adaptierten (SA-Rezeptoren: slowly adapting, Proportionaldetektion).
 Der Lage- bzw. Stellungssinn
informiert über die Winkelstellung der Gelenke und damit die Stellung
des Körpers in seiner Umgebung; er adaptiert kaum
(Proportionaldetektion). Gelenke
verfügen (wie die Haut) über mechanosensible Rezeptoren vom Typ
Ruffini, Vater-Pacini und Golgi; diese finden sich in Kapselgewebe,
Ligamenten, Menisci, Synovia, Fettgewebe und Periost. Knorpelgewebe ist
nicht innerviert, Hautrezeptoren spielen für den Stellungssinn so gut wie keine Rolle. Sollten in Gelenken Schmerzen auftreten, so entstehen diese durch Defekte (z.B. Einrisse) oder
Entzündungen (z.B. Osteoarthritis).
Der Lage- bzw. Stellungssinn
informiert über die Winkelstellung der Gelenke und damit die Stellung
des Körpers in seiner Umgebung; er adaptiert kaum
(Proportionaldetektion). Gelenke
verfügen (wie die Haut) über mechanosensible Rezeptoren vom Typ
Ruffini, Vater-Pacini und Golgi; diese finden sich in Kapselgewebe,
Ligamenten, Menisci, Synovia, Fettgewebe und Periost. Knorpelgewebe ist
nicht innerviert, Hautrezeptoren spielen für den Stellungssinn so gut wie keine Rolle. Sollten in Gelenken Schmerzen auftreten, so entstehen diese durch Defekte (z.B. Einrisse) oder
Entzündungen (z.B. Osteoarthritis).
Winkeländerungen der Gelenke werden in proximalen Gelenken präziser wahrgenommen (z.B. Schultergelenk: Wahrnehmungsschwelle 0,2° bei einer Geschwindigkeit von ≥0,3°/s) als in distalen
(z.B. Fingergelenk: 1,2° bei ≥10°/s) - Bewegungen in körpernahen
Gelenken wirken sich auf die Position (z.B. der Finger) stärker aus als
solche in körperfernen.
 Die Bewegungswahrnehmung erfolgt im Wesentlichen über Muskelspindel- und Sehnenspindelrezeptoren.
Die Bewegungswahrnehmung erfolgt im Wesentlichen über Muskelspindel- und Sehnenspindelrezeptoren.
Die sensorischen Fasern - Aβ, Aδ, C - sind meist
peptiderg (Substanz P, CGRP, Somatostatin, Neuropeptid Y, Galanin,
Enkephaline). Afferenzen
von der Tiefensensibilität im Rückenmark projizieren via
Hinterstrangbahn (funiculus posterior) und tractus spinothalamicus zum
Gehirn ( Abbildung unten: Rückenmarksquerschnitt).
Abbildung unten: Rückenmarksquerschnitt).
 Weiteres zu Tiefensensibilität, Muskel- und Sehnenspindeln s. dort
Weiteres zu Tiefensensibilität, Muskel- und Sehnenspindeln s. dort
Die komplexe Wahrnehmung der Natur berührter Gegenstände (Form,
Gewicht, Volumen, Oberflächenbeschaffenheit, Kanten usw.) wird als Haptik
 (haptische Wahrnehmung) bezeichnet.
(haptische Wahrnehmung) bezeichnet.
 Berührung ist nicht nur für Mechanorezeption, sondern auch für
die normale körperliche und seelische Entwicklung entscheidend (angenehme Berührungsreize führen zur Ausschüttung von Oxytocin).
Berührung ist nicht nur für Mechanorezeption, sondern auch für
die normale körperliche und seelische Entwicklung entscheidend (angenehme Berührungsreize führen zur Ausschüttung von Oxytocin).
Babys, die nicht berührt
(gestreichelt, umarmt) werden, entwickeln sich schlecht, bilden wenig
Wachstums- und viel Stresshormone; im Extremfall kann anhaltender völliger
haptischer Reizmangel sogar zum Tod führen.
Molekulare Grundlage der Mechanosensorik sind mechanosensitive Ionenkanäle (stretch-gated ion channels) in der Membran sensibler Axone. So verfügen sowohl Meissner- als auch Merkel-Rezeptoren (s. unten) über sogenannte Piezo2-Ionenkanäle (Piezo-type mechanosensitive ion channel component 2). Diese reagieren auf Scherkräfte durch mechanische Verankerung mit extrazellulären oder intrazellulären Faserstrukturen, oder auf tangentiale Streckung der Zellmembran, z.B. mit Öffnung und Einstrom von Na+ und/oder Ca++
reagieren. Dies führt zu reduziertem Generatorpotential und bei
Überschwelligkeit zur Auslösung von Aktionspotentialen. Möglicherweise
existieren auch Signalwege zu second-messenger-Mechanismen (IP3, DAG).
Die meisten Mechanosensoren der Oberflächensensibilität zeigen in ihrem Verhalten eine Mischung aus - unterschiedlich stark entwickeltem - Proportional- und Differential-Anteil (PD-Sensoren).
Taktile Information wird von 4 Arten von Mechanozeptoren vermittelt:
Rasch adaptierende (Meissner, Pacini) und langsam adaptierende (Merkel,
Pacini) ( Abbildung). Aktivitätsmuster der verschiedenen Afferenzen
von der Haut zum ZNS (Typ 1 von oberflächlich, Typ 2 von tiefer
gelegenen Mechanosensoren) lasssen sich mittels Mikroneurographie
separiert darstellen.
Abbildung). Aktivitätsmuster der verschiedenen Afferenzen
von der Haut zum ZNS (Typ 1 von oberflächlich, Typ 2 von tiefer
gelegenen Mechanosensoren) lasssen sich mittels Mikroneurographie
separiert darstellen.

Abbildung: Antwortverhalten von Mechanosensoren der Oberflächensensibilität
Modifiziert nach Johannson RS, Vallbo AB, Tactile sensory coding in the glabrous skin of the human hand. Trends Neurosci 1983; 6: 27-32
RA = Rapidly adapting, SA = Slowly adapting Rezeptoren. SA-Rezeptoren erkennen Fom und Konsistenz von Objekten, RA-Rezeptoren detektieren Bewegung und Vibration.
Oberflächliche Rezeptoren gehören zum Typ 1, tiefe zum Typ 2.
Meissner (RA1) und Merkel (SA1) -körperchen finden sich direkt unter
der Epidermis und haben kleine, ziemlich scharf begrenzte rezeptive
Felder. Ihre Afferenzen gehören zum Typ 1; sie innervieren jeweils 10-20 Körperchen.
Pacini (RA2) und Ruffini (SA2) -körperchen sind größer, liegen tiefer
in der Dermis (oder in der Subkutis) und haben größere, unscharf
begrenzte rezeptive Felder. Ihre Afferenzen gehören zum Typ 2; sie
innervieren jeweils ein Körperchen.

 Die epithelähnlichen Merkel-Tastzellen
bilden mit den Endigungen sensibler Neuriten (Aß,
also relativ rasch leitend) synaptische Komplexe, die man in behaarter
Haut an der Grenze zwischen Epidermis und Dermis rund um Haarwurzeln
(als "Haarscheiben" bzw. "Berührungskuppeln" ausgeformt), in
unbehaarter Haut in der Mitte von Papillenkämmen findet (
Die epithelähnlichen Merkel-Tastzellen
bilden mit den Endigungen sensibler Neuriten (Aß,
also relativ rasch leitend) synaptische Komplexe, die man in behaarter
Haut an der Grenze zwischen Epidermis und Dermis rund um Haarwurzeln
(als "Haarscheiben" bzw. "Berührungskuppeln" ausgeformt), in
unbehaarter Haut in der Mitte von Papillenkämmen findet ( Abbildung
oben).
Abbildung
oben).
In der Haut des Menschen finden sich etwa 70 Merkel-Zellen / cm2. Sie exprimieren Piezo2-Proteine (s. oben) und erhöhen ihr zytoplasmatisches [Ca++] bei Einwirkung von Druckkräften. Merkel-Zellen adaptieren kaum (SA: slowly adapting,
hoher Proportionalanteil), sie können bis zu einer halben Stunde nach
Beginn des mechanischen Reizes weiter feuern. Damit sind sie weitgehend
proportionalempfindlich und detektieren die Form (Ecken, Kanten, Krümmung..) und Konsistenz (weich, hart..) berührter Gegenstände über die Stärke einer Deformation der Haut.
Zugehörige afferente Neurone bezeichnet man als SA1-Fasern; die Neuronen innervieren jeweils alle Merkel-Zellen in 1-3 "Berührungskuppeln" (touch domes), insgesamt etwa 20 Merkel-Tastzellen pro Neuron. Pro cm2 Haut an den Fingerspitzen stammen rund 70 SA1-Fasern. An der Fingerspitze entspricht ein rezeptives Feld ca. 11 mm2 Haut; Gebiete mit niedrigerer Rezeptordichte weisen größere rezeptive Felder auf (geringeres Auflösungsvermögen). Die Zahl der Merkel-Zellen nimmt mit dem Alter deutlich ab.
 Auch Ruffini-Körperchen - in der inneren Handfläche ~20 / cm2 - adaptieren nur langsam und detektieren Dehnung der Haut (insbesondere
über Gelenken - damit tragen sie auch zur Tiefensensibilität bei),
wie sie z.B. bei Bewegung der Extremitäten auftritt. Man findet sie vor
allem über Finger- und Handwurzelgelenken, in der Nachbarschaft von
Fingernägeln, und entlang Hautfalten der Handflächen. Sie sind mit
bindegewebigen Fasern in ihrer Umgebung verankert. Sie werden vor allem
durch Dehnung der Haut in der Längsrichtung angeregt (
Auch Ruffini-Körperchen - in der inneren Handfläche ~20 / cm2 - adaptieren nur langsam und detektieren Dehnung der Haut (insbesondere
über Gelenken - damit tragen sie auch zur Tiefensensibilität bei),
wie sie z.B. bei Bewegung der Extremitäten auftritt. Man findet sie vor
allem über Finger- und Handwurzelgelenken, in der Nachbarschaft von
Fingernägeln, und entlang Hautfalten der Handflächen. Sie sind mit
bindegewebigen Fasern in ihrer Umgebung verankert. Sie werden vor allem
durch Dehnung der Haut in der Längsrichtung angeregt ( Abbildung
unten).
Abbildung
unten).
Ruffini-Körperchen sind niedrig
an der Zahl und haben große, unscharf begrenzte rezeptive Felder ( Abbildung).
Ruffini-Körperchen adaptieren ebenfalls nur langsam und geben bei
beständiger Reizung für längere Perioden Aktionspotentialsalven ab
(SA-System).
Abbildung).
Ruffini-Körperchen adaptieren ebenfalls nur langsam und geben bei
beständiger Reizung für längere Perioden Aktionspotentialsalven ab
(SA-System).
Während Merkel'sche Tastscheiben Druck senkrecht zur Hautoberfläche registrieren, sprechen Ruffini-Körperchen vorzugsweise auf horizontal auf das Hautgewebe einwirkende Druck- oder Dehnungsreize an.
Sie tragen zur haptischen Wahrnehmung (Stereognosie) bei - also zur
aktiven Wahrnehmung durch ("erforschendes") Berühren von Gegenständen
(Ertasten). Dabei kommt es auf die Perzeption des Musters von
Hautstreckung in der Hand an, insoferne spielt das SA2-System eher eine
propriozeptive als exterozeptive Rolle. Das gilt insbesondere für die
Detektion des Abwinkelns (Flexion) von Fingergelenken.
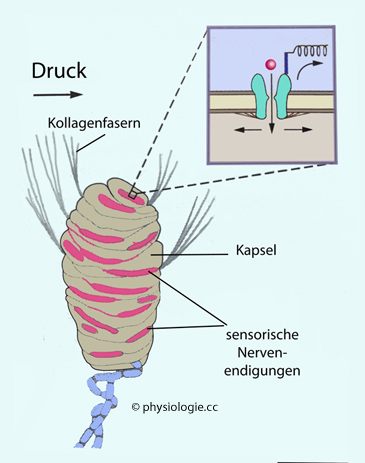
 Abbildung: Meissner'sches Tastkörperchen (RA1)
Abbildung: Meissner'sches Tastkörperchen (RA1)
Nach einer Vorlage in Kandel / Koester / Mack / Siegelbaum (eds), Principles of Neural Sciences, 6th ed. 2021 (McGraw Hill)
Druck oder Bewegung an der Haut überträgt sich
über Kollagenfasern auf die flüssigkeitsgefüllte Kapsel des
Tastkörperchens und öffnet mechanosensible Rezeptoren in der Membran
sensorischer Nervenendigungen (Inset), was Kationeneinstrom und
Depolarisierung verursacht.
Unten: Afferenter Nerv

 Meissner'sche Tastkörperchen (
Meissner'sche Tastkörperchen ( Abbildung; Durchmesser etwa 0,1 mm, Anzahl ~150 / cm2) bzw. Haarfollikelrezeptoren sind ausgeprägt differentialempfindlich: Bei konstantem Reiz nimmt ihre Entladungsfrequenz rasch ab. Haarfollikelrezeptoren
können Textur, Form und Festigkeit von Objekten signalisieren (sie
können rasch oder langsam adaptieren). Die
höchste Empfindlichkeit zeigen Meissner-Körperchen auf mechanische
Schwingungen mit einer Frequenz um ~50 Hz.
Abbildung; Durchmesser etwa 0,1 mm, Anzahl ~150 / cm2) bzw. Haarfollikelrezeptoren sind ausgeprägt differentialempfindlich: Bei konstantem Reiz nimmt ihre Entladungsfrequenz rasch ab. Haarfollikelrezeptoren
können Textur, Form und Festigkeit von Objekten signalisieren (sie
können rasch oder langsam adaptieren). Die
höchste Empfindlichkeit zeigen Meissner-Körperchen auf mechanische
Schwingungen mit einer Frequenz um ~50 Hz.
Diese langsam adaptierenden Rezeptoren sind für die Detektion rasch
veränderter Reizmuster (Berührung) ausgelegt und spielen mit ihrer
Spezialisierung auf relative Bewegungen von Gegenständen auf der Haut
u.a. für die Steuerung von Greifbewegungen eine
wichtige Rolle, die allerdings sowohl auf Signale aus dem RA- als auch
aus dem SA-System angewiesen ist. Jedes System hat dabei eine
spezifische Aufgabe; das RA1-System (Meissner-Körperchen) detektiert
das Tempo einer Greifbewegung und hört zu feuern auf, sobald der Griff
"steht"; und es hilft bei der Planung der zum Halten eines Gegenstandes
notwendigen Griffkraft.
Solche Rezeptoren nennt man RA (rapidly adapting), Haarfollikelrezeptoren auch RA-LTMRs (rapidly adapting low-threshold mechanoreceptors); zugehörige afferente Neurone bezeichnet man als RA-Fasern. Pro cm2 Haut an den Fingerspitzen stammen ca. 150 RA1-Fasern. Ein typisches RA1-Neuron innerviert 10-20 Meissner-Körperchen. Ein rezeptives Feld entspricht an der Fingerspitze ca. 25 mm2 Haut.
 Noch rascher adaptieren die (~2 mm langen und ~1 mm dicken) (Vater-) Pacini-Körperchen (PC für Pacinian Corpuscle). Sie sind bis zu 1 mal 2
mm groß, aus bis zu 70 zwiebelschalenartig angeordneten bindegewebigen
Schichten - mit einer viskösen Flüssigkeit dazwischen - aufgebaut, die
um eine zentrale Nervenfaser angeordnet sind. Auf der Fläche einer Hand finden sich
>600, ~40.000 in der gesamten Haut - rund 20 / cm2.
Noch rascher adaptieren die (~2 mm langen und ~1 mm dicken) (Vater-) Pacini-Körperchen (PC für Pacinian Corpuscle). Sie sind bis zu 1 mal 2
mm groß, aus bis zu 70 zwiebelschalenartig angeordneten bindegewebigen
Schichten - mit einer viskösen Flüssigkeit dazwischen - aufgebaut, die
um eine zentrale Nervenfaser angeordnet sind. Auf der Fläche einer Hand finden sich
>600, ~40.000 in der gesamten Haut - rund 20 / cm2.
Pacini-Körperchen sind die empfindlichsten Mechanodetektoren im
somatosensorischen System. Die
um das Axon zwiebelschalenartig angeordneten Lamellen geben bei
konstanter Druckbelastung rasch nach, dies erhöht die
Differentialempfindlichkeit des Sensors. Die rezeptiven Felder dieser Sensoren sind groß und unscharf begrenzt.
Druck auf ein Pacini-Körperchen reizt mechanosensitive
Ionenkanäle in der Membran des zentralen Axons (wenn
überschwellig, erfolgen Aktionspotentiale), aber nur für sehr kurze
Zeit: Schon nach wenigen Millisekunden läßt die Depolarisation nach (Adaptation) und
das Rezeptorpotential normalisiert sich.
Hat der Druckreiz angehalten und verschwindet dann, kommt
es wiederum zu einer kurzen Depolarisation (falls überschwellig,
wiederum von einer Erregung gefolgt). Die rasche Adaptation ist
mechanischen Eigenheiten des zwiebelschalenförmig angeordneten
Hilfsapparats (20 bis 70 bindegewebige Lagen) geschuldet; entfernt man
diesen, zeigt das verbliebene "nackte" Axon auf mechanische
Dauerreizung hin ein wesentlich schwächeres
Differential-Antwortverhalten seines Rezeptorpotentials. Die
Mechanosensibilität der Nervenendigung bleibt allerdings auch nach
Abtragen der Lamellen erhalten.
Afferenzen von Pacini-Körperchen fallen in die Kategorie RA2.
Pacini-Körperchen werden durch sich rasch änderndem Druck erregt. Experimentell nutzt man schwingende Körper als Reizquelle. Bei Reizfrequenzen >30Hz werden sie erregt (Frequenzbereich 60 bis 800
Hz, maximale Empfindlichkeit zwischen 200 und 300 Hz), können also Schwingungen aufnehmen (daher die eigentlich unsinnige Bezeichnung "Vibrationssinn").
Mechanorezeptoren: Eigenschaften
 
Modifiziert nach Fahlke / Linke / Raßler / Wiesner, Taschenatlas
Physiologie, 2. Aufl. 2015 (Urban & Fischer); und Kandel / Koester
/ Mack / Siegelbaum (eds), Principles of Neural Sciences, 6th ed. 2021
(McGraw Hill)
|
Rezeptortyp
|
Morphologie
|
Fasertyp
|
Adäquater Reiz
|
Adaptation
|
Empfindung
|
SA1
|
Merkel- Tastzellen
|
II
(Durchmesser 6-12 µm, Geschwindigkeit 35-70 m/s)
|
statische Hautdeformation
(0-100, optimal 5 Hz)
Reizschwelle 8 µm
|
langsam
|
Druck
|
SA2
|
Ruffini- Körperchen
|
Abscherung
Reizschwelle 40 µm
|
Scherkräfte
|
RA1
|
Meißner- Tastkörperchen
|
Vibration
(1-300, optimal 50 Hz)
Reizschwelle 2 µm
|
rasch |
Hautkontakt, niederfrequente Vibration
|
RA
|
Haarfollikel
|
Haar-
bewegungen
|
Hautkontakt, Berührung
|
RA2
|
Pacini- Körperchen
|
Vibration
(5-1000, optimal 200 Hz)
Reizschwelle 0,01 µm
|
sehr rasch
|
höherfrequente Vibration
|
|
freie Nerven- endigungen
|
Haut-
deformation
|
mittel
|
grober Hautkontakt
|
Thermo- rezeptoren
|
III, IV
|
15-35°C
|
kalt
|
IV
|
30-45°C
|
warm
|
Nozizeptoren
|
III
|
Gewebe- schädigung
|
nicht adaptierend
|
stechender Schmerz
|
IV
|
brennender Schmerz
|
Proprio- zeptoren
|
primäre Muskelspindeln
|
Ia
|
Muskellänge |
rasch
|
Vibration
|
sekundäre Muskelspindeln
|
II
|
langsam |
(Propriozeption)
|
Golgi- Sehnenorgane
|
Ib
|
Kraft an Sehne
|
Muskelkraft
|
Gelenk-
rezeptoren
|
II, III
|
Gelenk-
bewegung / Druck
|
Propriozeption
|
Die Afferenzen von den kutanen Mechanorezeptorarten (Meissner, Merkel, Pacini, Ruffini, Haarfollikel) laufen über Nervenfasern vom Typ Aß (Erlanger / Gasser) bzw. II (Lloyd / Hunt) (Tabelle), d.h. sie sind gut myelinisiert und leiten die Impulse rasch zum Zentralnervensystem.
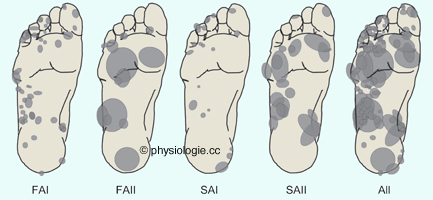
Obere Reihe: Rezeptive Felder von Mechanosensoren in den oberflächlichen (unmittelbar subepithelialen) Schichten der Dermis sind klein und eng begrenzt.
Untere Reihe: Rezeptive Felder tiefer in der Dermis gelegener
Mechanosensoren erstrecken sich über relativ große Hautbereiche. Für
SA2-Rezeptoreen (Ruffini) geben die Pfeile an, auf welche Richtung der
Hautdehnung die Rezeptoren bevorzugt ansprechen.
Je kleiner das rezeptive Feld, desto besser das Auflösungsvermögen

Die rezeptiven Felder der Meissner-Körperchen sind relativ klein, diejenigen von Pacini-Körperchen wesentlich größer ( Abbildung).
Abbildung).
 Umgekehrt reagieren Rezeptoren für Druckdetektion - Ruffini-Körperchen, Merkel-Tastscheiben
- stark proportionalempfindlich, d.h. sie adaptieren nur schwach (SA) und antworten ziemlich konstant auf die Stärke des mechanischen
Reizes.
Umgekehrt reagieren Rezeptoren für Druckdetektion - Ruffini-Körperchen, Merkel-Tastscheiben
- stark proportionalempfindlich, d.h. sie adaptieren nur schwach (SA) und antworten ziemlich konstant auf die Stärke des mechanischen
Reizes.
SA1 (Merkel'sche Tastscheiben) werden durch Druck senkrecht zur Hautoberfläche angeregt; SA2 (Ruffini-Körperchen) detektieren Druck / Dehnung horizontal im Gewebe.
 Über Schmerz s. dort, über Propriozeption s. dort
Über Schmerz s. dort, über Propriozeption s. dort
Pro cm2 Haut finden sich ~30 Druckrezeptoren und ~20
Tastpunkte. (Man schätzt, dass bei einem Händedruck mehr als tausend
Druckrezeptoren erregt werden.) Jede Hand enthält etwa 2500 Pacici-Körperchen (am dichtesten liegen diese in den Fingern).

Abbildung: Frequenzabhängige Empfindlichkeit stark adaptierender (RA)-Rezeptoren
Nach einer Vorlage bei chegg.com
Die
Empfindlichkeit rasch adaptierender Rezeptoren auf verschiedene
Anregefrequenzen ist unterschiedlich: Während
Vater-Pacini-Vibrationssensoren (rot) bei ~250 Schwingungen pro Sekunde am empfindlichsten sind, kann man Meissner'sche Tastkörperchen (blau) bei ~50 Hz am leichtesten aktivieren (vgl. Tabelle oben).
Die Frequenzabhängigkeit des menschlichen Vibrationssinns
(Wahrnehmungsschwelle) wird durch das gemeinsame Ansprechverhalten
dieser beiden Rezeptorpopulationen bestimmt

Dass RA-Rezeptoren unterschiedlich empfindlich auf Stärke (Eindringtiefe) und Frequenz mechanischer Reizung reagieren, zeigt die  Abbildung: Pacini-Vibrationssensoren maximal bei ~250, Meissner- Körperchen bei ~50 Hz. Diese Rezeptoren bestimmen gemeinsam Wahrnehmungsschwelle und Frequenzabhängigkeit des menschlichen Vibrationssinns.
Abbildung: Pacini-Vibrationssensoren maximal bei ~250, Meissner- Körperchen bei ~50 Hz. Diese Rezeptoren bestimmen gemeinsam Wahrnehmungsschwelle und Frequenzabhängigkeit des menschlichen Vibrationssinns.
Merkel-, Meissner-, Ruffini- und Pacini-Rezeptoren reagieren in unterschiedlicher Präzision
auf feine mechanische Reize, wie sie beim Ertasten von Konturen, z.B.
beim Erkennen von in Braille-Schrift gesetzten Buchstaben auftreten
(
gesetzten Buchstaben auftreten
( Abbildung):
Abbildung):
 Abbildung: Wie Tastrezeptoren auf Braille-Schrift reagieren
Modifiziert nach Phillips JR,
Johansson RS, Johnson KO: Representation of braille characters in human
nerve fibers. Exp Brain Res 1990; 81: 589-92
Abbildung: Wie Tastrezeptoren auf Braille-Schrift reagieren
Modifiziert nach Phillips JR,
Johansson RS, Johnson KO: Representation of braille characters in human
nerve fibers. Exp Brain Res 1990; 81: 589-92
Versuchsannahme
ist eine Ableitung von afferenten Nervenfasern, welche Information von
entlang der Fingerkuppe gelegenen Rezeptoren übermitteln. Die Muster in
den weißen Kästen ergeben sich aus Punkten, die einzelne Entladungen an
den Nervenfasern repräsentieren (Rezeptoraktivität).
Die Innervation von Merkel-Scheiben erfolgt über SA1-Fasern. Braille-Punkte sind ~1 mm voneinander entfernt (das ist mehr als der Durchmesser des einer SA1-Faser zugehörigen rezeptiven Feldes).
Je besser die resultierenden Muster den oben angedeuteten Noppen (Braille-Schrift) entsprechen, desto zuverlässiger (besser "lesbar") ist die im Gehirn empfangene Information

Rezeptoren auf der Fingerkuppe feuern beim Vorbeiziehen des Fingers über die Noppen der Blindenschrift (Rezeptoraktivität).
 Merkel-Scheiben
(SA1) haben relativ kleine rezeptive Felder und feuern, solange die Haut
durch den jeweiligen Reizpunkt verformt ist, das Erregungsmuster
spiegelt die Schrift präzise wider.
Merkel-Scheiben
(SA1) haben relativ kleine rezeptive Felder und feuern, solange die Haut
durch den jeweiligen Reizpunkt verformt ist, das Erregungsmuster
spiegelt die Schrift präzise wider.
 Meissner-Körperchen (RA1) adaptieren ähnlich langsam, haben aber größere rezeptive Felder, und die Abbildung der Noppen ist weniger genau.
Meissner-Körperchen (RA1) adaptieren ähnlich langsam, haben aber größere rezeptive Felder, und die Abbildung der Noppen ist weniger genau.
 Ruffini-Endigungen (SA2) reagieren auf Dehnung der Haut, adaptieren ebenfalls langsam, geben aber ein ziemlich verwaschenes Bild der Reizmuster.
Ruffini-Endigungen (SA2) reagieren auf Dehnung der Haut, adaptieren ebenfalls langsam, geben aber ein ziemlich verwaschenes Bild der Reizmuster.
 Pacini-Körperchen
(RA2) adaptieren sehr rasch und haben große rezeptive Felder, sie ermitteln
vor allem die Textur des Papiers, nicht so sehr die Position der Braille-Punkte.
Pacini-Körperchen
(RA2) adaptieren sehr rasch und haben große rezeptive Felder, sie ermitteln
vor allem die Textur des Papiers, nicht so sehr die Position der Braille-Punkte.
Das Ertasten von Oberflächendetails ist durch die kombinierte Funktion schnell adaptierender RA-Rezeptoren (Meissner-Körperchen) und langsam adaptierender SA-Rezeptoren (Merkel-Zellen) möglich
|
In Haut und Unterhaut (Oberflächensensibilität) werden
Druckreize als
Stärke einer gleichmäßig wirkenden Verformung erfasst (langsam
adaptierende Rezeptoren).
Der Tastsinn kann noch Schwingungen wahrnehmen, die nur ~0,02
Mikrometer Amplitude haben (ein Erythrozyt hat 7-8 Mikrometer
Durchmesser).
Berührung wird als Geschwindigkeit, mit der sich
Verformungsreize ändern, gemessen (rasch adaptierende Rezeptoren). Eine Geschwindigkeitsänderung
periodischer Verformungen mit Frequenzen bis 400 Hz erregt Rezeptoren
der Unterhaut und wird als Vibration wahrgenommen.
Wie präzise die Wahrnehmung berührter Gegenstände erfolgt, hängt von der Größe der rezeptiven Felder
der Haut ab. Diese überlappen sich in einem etwa hexagonalen Muster; je
kleiner der Durchmesser der Felder ist, desto genauer ist die
Identifikation bzw. Unterscheidung verschiedener Druckpunkte. Diese
Fähigkeit wird am einfachsten mittels Bestimmung des Mindestabstandes
zweier als getrennt wahrnehmbarer Reizpunkte (2-Punkt-Diskrimination)
erfasst ( Abbildung):
Abbildung):
 Abbildung: Rezeptive Felder und Zwei-Punkt-Diskriminationsvermögen der Haut
Nach einer Vorlage in in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Abbildung: Rezeptive Felder und Zwei-Punkt-Diskriminationsvermögen der Haut
Nach einer Vorlage in in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Links:
Mittlere Minimalabstände der 2-Punkt-Diskrimination an verschiedenen
Körperstellen (Beispiele: Zungenspitze ~1 mm, Fingerkuppe ~1 mm, Lippen
~5 mm, Unterarm 40 mm, vgl. Tabelle). Die Werte für definierte
Hautareale sind auf der linken und rechten Körperseite jeweils etwa
gleich groß.
Rechts oben: Bestimmung der Entfernung zweier gleichzeitig gereizter Druckpunkte mittels eines Ästhesiometers (cal(l)iper). Die Diskrimination ist an der Haut eines Fingers besser (geringere Distanz) als an der Haut des Unterarms.
Rechts unten:
Jeder Punkt auf der Haut ist mehrfach innerviert, die (etwa
kreisrunden) rezeptiven Felder (a, b, c) überschneiden sich. Die beiden
Druckpunkte können in geringem (grün), mittlerem (rot) und einem
Abstand wirken, der dem Durchmesser der Felder entspricht (blau). In
den drei Feldern ganz unten sind die Entladungsfrequenzen der
afferenten Neurone aus den rezeptiven Feldern a, b und c bei den
gezeigten Reizpunktabständen dargestellt.
 Ist der Reizabstand gering (grün), kommt aus Feld b (das beide Reize
empfängt) ein stärkeres Signal als aus den Feldern a und c. Dieses
Muster interpretiert das Gehirn als Reizung des rezeptiven Feldes b, es
wird nur ein Reizpunkt wahrgenommen.
Ist der Reizabstand gering (grün), kommt aus Feld b (das beide Reize
empfängt) ein stärkeres Signal als aus den Feldern a und c. Dieses
Muster interpretiert das Gehirn als Reizung des rezeptiven Feldes b, es
wird nur ein Reizpunkt wahrgenommen.
 Ist
der Reizabstand etwas größer (rot), kommt aus allen drei Feldern eine
etwa gleich starke Entladungsfrequenz des afferenten Neurons. Dieses
Muster interpretiert das Gehirn als gleich starke Reizung aller drei
rezeptiven Felder, es
wird ebenfalls nur ein (breiterer) Reizpunkt wahrgenommen.
Ist
der Reizabstand etwas größer (rot), kommt aus allen drei Feldern eine
etwa gleich starke Entladungsfrequenz des afferenten Neurons. Dieses
Muster interpretiert das Gehirn als gleich starke Reizung aller drei
rezeptiven Felder, es
wird ebenfalls nur ein (breiterer) Reizpunkt wahrgenommen.
 Ist
der Reizabstand so groß wie (oder größer als) der Durchmesser der
rezeptiven Felder (blau), kommt aus Feldern a und c (in deren Zentrum
die Reizpunkte liegen) ein stärkeres neuronales Signal als aus dem
mittigen Feld b. Diesen Kontrast interpretiert das Gehirn als Reizung
der rezeptiven Felder a und c, es werden (korrekterweise) zwei
Reizpunkte wahrgenommen.
Ist
der Reizabstand so groß wie (oder größer als) der Durchmesser der
rezeptiven Felder (blau), kommt aus Feldern a und c (in deren Zentrum
die Reizpunkte liegen) ein stärkeres neuronales Signal als aus dem
mittigen Feld b. Diesen Kontrast interpretiert das Gehirn als Reizung
der rezeptiven Felder a und c, es werden (korrekterweise) zwei
Reizpunkte wahrgenommen.
Fazit:
Der Abstand der beiden Reizpunkte muss mindestens dem (für die
betreffende Region typischen) Durchmesser der rezeptiven Felder
entsprechen, damit eine 2-Punkte-Diskrimination möglich ist. Je kleiner
die rezeptiven Felder, desto größer das Auflösungsvermögen, und desto
feiner die Wahrnehmung

Das Auflösungsvermögen der mechanischen Reizmuster wird über die Zweipunktschwelle
ermittelt (s.  Abbildung und Tabelle unten): Es ist dies der
geringste Abstand, in dem zwei getrennte Reizpunkte noch als solche
identifiziert werden können. Diese Schwelle ist auf der Zungenspitze
und an Fingerbeeren besonders gering (ungefähr 1-2 mm, hohes
Auflösungsvermögen) und im Bereich des Thorax besonders hoch ungefähr
45-70 mm, geringes Auflösungsvermögen). Mit zunehmendem Alter
nimmt die Fähigkeit der Zwei-Punkt-Diskrimination ab.
Abbildung und Tabelle unten): Es ist dies der
geringste Abstand, in dem zwei getrennte Reizpunkte noch als solche
identifiziert werden können. Diese Schwelle ist auf der Zungenspitze
und an Fingerbeeren besonders gering (ungefähr 1-2 mm, hohes
Auflösungsvermögen) und im Bereich des Thorax besonders hoch ungefähr
45-70 mm, geringes Auflösungsvermögen). Mit zunehmendem Alter
nimmt die Fähigkeit der Zwei-Punkt-Diskrimination ab.
Minimalabstand Zwei-Punkte-Diskrimination

Werte nach: Mörike KD, Betz E, Mergenthaler M: Biologie des Menschen,
Heidelberg 1991; und Weber M: Tastsinn und Gemeingefühl, Braunschweig
1981
|
Zungenspitze
|
1,1 mm
| Stirm |
22 mm |
Fingerspitze
|
2,3 mm
| Handrücken |
32 mm |
Lippenrot
|
4,5 mm
| Scheitel |
34 mm |
Nasenspitze
|
6,8 mm
| Unterarm, Unterschenkel |
40 mm |
Daumen, Zungenrand
|
9 mm
| Brustbeinbereich |
45 mm |
Wange, Handinnenfläche, Augenlid außen
|
11 mm
| Rücken, Oberarm, Oberschenkel |
68 mm |
Fingerrücken
|
16 mm
|
|
|
Das höchste taktile Auflösungsvermögen haben Zungenspitze und Fingerbeeren
|
Die Wahrnehmung von Außenreizen über den Körper wird weiters als Exterozeption bezeichnet. Mechano-, Thermo- und Schmerzsensibilität
werden mittels etwa 20 Arten von mehr oder weniger spezialisierten Rezeptoren aufgenommen.

Eine besondere Rolle spielen Rezeptoren in der Fußsohle ( Abbildung): Sie beteiligen sich an
Abbildung): Sie beteiligen sich an
 Balance im Stehen
Balance im Stehen

 Gangstabilisierung
Gangstabilisierung

 automatischen Korrekturen der Körperhaltung
automatischen Korrekturen der Körperhaltung

 Modulation der Motorik der oberen und unteren Extremitäten
Modulation der Motorik der oberen und unteren Extremitäten

 vestibulären Reflexen (Gleichgewicht)
vestibulären Reflexen (Gleichgewicht)
Thermosensibilität
Die Temperatur von "Wärme-" bzw. "Kältepunkten" im Gewebe wird
von Nervenzellen detektiert, die schon
auf Unterschiede von 0,01°C reagieren können. Kältepunkte sind
zahlreicher als
Wärmepunkte (um bis zu einer Größenordnung mehr). Die rezeptiven Felder
der Thermosensibilität sind sehr klein und überlappen sich nicht,
vielmehr gibt es zwischen ihnen große Hautflächen, die überhaupt nicht
thermosensibel sind. Die Zahl der
thermosensiblen Stellen ist je nach Hautareal unterschiedlich, z.B.
findet man in der Gesichtshaut 15-20 Kältepunkte / cm2, in der Haut der Handfläche nur 1-5 / cm2; hier
sind Kältefelder 5-10 mm voneinander entfernt, Wärmefelder ca. 15 mm;
an den Armen nehmen die Distanzen zwischen den thermosensitiven Punkten
zu. Dementsprechend gering ist die Zahl thermo-afferenter Fasern im
Rückenmark (nur einige tausend im tractus spinothalamicus).
 Abbildung: Temperaturabhängiges Ansprechverhalten von Kälte- und Wärmerezeptoren
Abbildung: Temperaturabhängiges Ansprechverhalten von Kälte- und Wärmerezeptoren
Nach einer Vorlage bei Guyton and Hall, Textbook of Medical Physiology, 15th ed. Elsevier 2026t
Kälte-,
Wärme- und Schmerzrezeptoren haben temperaturabhängiges
Empfindlichkeitsverhalten. Auf Temperaturen unter 10°C und über 46°C
sprechen nur noch Schmerzrezeptoren an; Kälterezeptoren reagiern am
stärksten auf Temperaturen um 25°C, Wärmerezeptoren sind auf
Temperaturen um 40°C am empfindlichsten

Die Empfindung ”heiß“ entspricht einer gleichzeitigen
Reizung von Wärme- und Kälte- bzw. Wärme- und Schmerzrezeptoren ( Abbildung).
Abbildung).
Die kutane Thermosensitivität des Menschen nutzt
 kälteempfindliche Aδ-Nervenfasern (Leitungsgeschwindigkeit 5-30 m/s). Diese sprechen auf Hauttemperaturen zwischen ~10°C und 40°C an und haben maximale Entladungsfrequenz bei ~25°C - und
kälteempfindliche Aδ-Nervenfasern (Leitungsgeschwindigkeit 5-30 m/s). Diese sprechen auf Hauttemperaturen zwischen ~10°C und 40°C an und haben maximale Entladungsfrequenz bei ~25°C - und
 wärme- und kälteempfindliche C-Fasern (Leitungsgeschwindigkeit 0,2-2 m/s). Wärmesensible Fasern sprechen auf Temperaturen über ~30°C an, maximal auf 40-45°.
wärme- und kälteempfindliche C-Fasern (Leitungsgeschwindigkeit 0,2-2 m/s). Wärmesensible Fasern sprechen auf Temperaturen über ~30°C an, maximal auf 40-45°.
Wie ein Neuron auf Temperatur anspricht, hängt von der Besetzung seiner Membran mit speziellen Rezeptormolekülen ab. Es sind dies TRP-Kanäle
mit unterschiedlicher Ansprechbarkeit durch Temperatur oder diverse
chemische Reize ( Abbildung): TRPA1 sprechen auf Temperaturen unter 16°C an, TRPM8 unter 28°C (und Menthol), TRPV4 über 26°C, TRPV3 über 31°C, TRPV1 über 43°C (und Capsaicin), TRPV2 über 52°C.
Abbildung): TRPA1 sprechen auf Temperaturen unter 16°C an, TRPM8 unter 28°C (und Menthol), TRPV4 über 26°C, TRPV3 über 31°C, TRPV1 über 43°C (und Capsaicin), TRPV2 über 52°C.
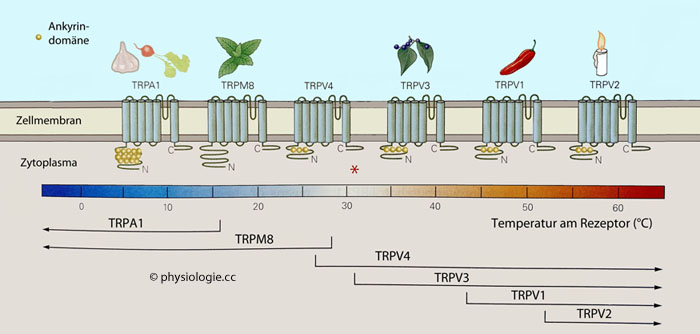
 A
Abbildung: TRP-Ionenkanäle
Nach einer Vorlage in Kandel / Koester / Mack / Siegelbaum (eds), Principles of Neural Sciences, 6th ed. 2021 (McGraw Hill)
Der
rote Stern deutet die normale Hauttemperatur von etwa 32°C an. Hier
sind nur TRPV4- und einige TRPV3- Rezeptoren aktiv (zu TRP-Kanälen s. dort).
Gezeigt sind die Temperaturbereiche, auf die
unterschiedliche TRP-Kanäle ansprechen. Bestimmte Neuronengruppen
exprimieren bestimmte TRP-Sensoren und erlangen dadurch Spezifität.
Bei 32°C sind nur TRPV4 (auch berührungsempfindlich) und einige TRPV3
aktiv. TRPA1 und TRPM8 feuern bei niedrigen Temperaturen; TRPA1
reagiert darüber hinaus auf Glykoside in Lauchpflanzen (Knoblauch,
Rettich), TRPM8 spricht auf niedrige Temperatur (unter 27°C) an, aber auch auf Menthol und Minze. Ähnliches gilt
für die "Warmrezeptoren" TRPV3 (Kampfer) und TRPV1 ("brennende"
Chemikalien, z.B. Capsaicin in Chili-Pfeffer). TRPV2 feuern bei
Hitzeeinwirkung (>50°C)
Diese thermosensitiven Strukturen sind
nichtselektive Ionenkanäle, sie lassen Na+, K+ und Ca++ durch die Membran passieren, die durch ihre Öffnung depolarisiert wird. Ein einzelnes thermosensitives Neuron exprimiert meist nur eine Art von TRP-Kanal - mit Ausnahme einiger Kaltsensoren, die auch auf Temperaturen über 43°C ansprechen (das kann zur Erklärung paradoxer Kaltempfindungen beitragen: Das Gehirn interpretiert alles, was über eine "Kaltfaser" gemeldet wird, als Kälte).
Die Durchblutung der Haut beeinflusst die subjektive Einschätzung der Außentemperatur.
Kommt es zur Erweiterung der Hautgefäße, dann wird die damit
einhergehende Erwärmung des Gewebes um die Rezeptoren als erhöhte
Umgebungstemperatur gedeutet (Wärmegefühl bei alkoholbedingter
Vasodilatation). Kommt es umgekehrt zu starker Vasokonstriktion (wie
beim Raynaud-Syndrom oder durch Gifteinwirkung - z.B. Tabak, Koffein), wird die Umgebungstemperatur als niedrig empfunden.
Längerfristige Temperaturreizung führt zu Adaptation der Sensoren. Diese erfolgt innerhalb von Sekunden, sowohl bei Kalt- als auch bei Warmrezeptoren. Warm- und Kaltrezeptoren verhalten sich als Proportional-Differental-Fühler.
Thermosensoren (kalt, warm) sind PD-Fühler
|
 Abbildung: Dreischalenversuch nach Eduard Weber
Abbildung: Dreischalenversuch nach Eduard Weber
Impulsfrequenzkurven nach einer Vorlage in Müller / Frings / Möhrlen, Tier- und Humanphysiologie, 6. Aufl. (Springer 2019)
Oben:
Versuchsdurchführung. Eine Hand wird in kaltes (z.B. 20°C), die andere
in warmes (z.B. 40°C) getaucht. Nach etwa einer Minute
(Adaptationszeit) werden beide Hände in eine Schale mit mittlerer
Temperatur (z.B. 30°C) getaucht.
Nach
Adaptation der Thermorezeptoren vermittelt der Wechsel in das
mittelwarme Wasser (z.B. 30°C) in der Hand, die im kalten (z.B. 20°C)
Wasser war, eine Warmempfindung. Umgekehrt ist es bei der anderen Hand:
Diese (an das wärmste Wasser, z.B. 40°C) adaptierte Hand empfindet das
Wasser in der mittleren Schale als kalt.
Unten: Erklärung. Taucht man
eine Hand in Wasser höherer Temperatur, nimmt die Entladungsfrequenz
der Afferenzen von den Wärmerezeptoren umso stärker zu, je höher die
Temperatur des Wassers ist. Umgekehrt ist es mit den Kälterezeptoren:
Je höher die Temperatur, desto mehr nimmt die Entladungsfrequenz
der Kälterezeptoren ab.
Der
Zeitverläuf der Aktionspotentialfrequenzen zeigt eine ausgeprägte
Differentialkomponente: Innerhalb von Sekunden nimmt der
Übergangseffekt wieder ab, die Impulsfrequenz stellt sich wieder auf
etwa den vorangegangenen Wert ein (Adaptationseffekt). Bei Abkühlung
(Wärmeentzug) ist die Wirkung auf den Zeitverlauf der
Entladungsfrequenzen entgegengesetzt.
Taucht
man die Hand anschließend in die Schale mit mittlerer Temperatur, kommt
es zu einem entgegengesetzten Effekt: Die an warmes Wasser adaptierte
Hand meldet einen Abkühlungseffekt (höhere Aktionspotentialfrequenz von
den Kälterezeptoren, verringerte von Wärmerezeptoren); bei der anderen
Hand ist es umgekehrt

Das zeigt sich beim Weberschen Dreischalenversuch
 (
( Abbildung): Taucht man z.B. die linke Hand in kaltes, die rechte in warmes
Wasser, und gibt beide Hände nach etwa einer Minute in lauwarmes Wasser,
so empfindet man dieses links als warm, rechts gleichzeitig als kühl.
Abbildung): Taucht man z.B. die linke Hand in kaltes, die rechte in warmes
Wasser, und gibt beide Hände nach etwa einer Minute in lauwarmes Wasser,
so empfindet man dieses links als warm, rechts gleichzeitig als kühl.
Ansprechverhalten: Kaltrezeptoren
sprechen auf plötzliche Abkühlung etwa 100-mal stärker an als auf
allmähliche Temperaturänderung - darin zeigt sich die starke
Differentialempfindlichkeit (und rasche Adaptation) des
Ansprechverhaltens dieser Fasern. Beispielsweise spürt man den
schwachen Luftzug, wenn eine Person (bei geschlossenem Raum mit
stehender Luft) hinter einem vorbeigeht.
Im Gegensatz dazu funktionieren Warmrezeptoren eher wie Thermometer: Sie reagieren zunächst proportional zur Temperatur, um anschließend allmählich zu adaptieren.
Die
Afferenzen der Thermosensibilität laufen analog zu denen des Schmerzempfindens - Kälteinformation wird durch Aδ- (hauptsächlich) sowie auch C-Fasern übertragen, Wärme nur
über C-Fasern. "Brennend heiß" wird über sowohl C- als auch Aδ-Fasern signalisiert.
 Über die Klassifizierung von Nervenfasern s. dort
Über die Klassifizierung von Nervenfasern s. dort
Kalt- und Warmimpulse gelangen zum Hinterhorn des
Rückenmarks und schalten dort auf ein zweites Neuron um, die
aufsteigende Leitung erfolgt über
den lateralen tractus spinothalamicus (Vorderseitenstrangbahn).
Die
zentrale Integrierung der
Temperaturinformation erfolgt in der Gehirnrinde (Insel, somatosensorische
Gebiete).
Thermosensibilität wird in Hinterhorn umgeschaltet und über die Vorderseitenstrangbahn zum Thalamus weitergeleitet
|
Änderungen der Umwelt- bzw. Hauttemperatur lösen regulative
Antworten aus mit dem Ziel, die Körpertemperatur zu stabilisieren und
Wohlbefinden zu sichern:
Juckreiz
Juckreiz (pruritus, itch) ist eine eigene Modalität im Rahmen der somatischen Sensibilität. Er
ist auf die Haut und einige anrenzende Schleimhäute (z.B. Conjunctiva)
begrenzt. Ausgelöst wird Juckreiz - der zu dem Verlangen führt, sich an
entsprechenden Stellen zu kratzen (Juckreflex) - üblicherweise durch
bestimmte Stoffe, die (nach ihrem Effekt) als Pruritogene zusammengefasst werden; Nervenfasern, welche Juckreize leiten, nennt man pruritozeptiv. Juckreiz kann endogen (z.B. durch Histamin), exogen (z.B. bestimmte pfanzliche Reize) oder medikamentös verursacht sein.
Jucken wurde für lange Zeit als eine Unterkategorie des Schmerzes
aufgefasst. Die
neurophysiologische Abgrenzung von Juckreiz zu Schmerz ist auf der
Basis von involvierten Übeträgerstoffen, Rezeptoren und Nervenfasern
schwierig, weil überlappend; so exprimieren z.B. die meisten Neurone
mit Histaminrezeptoren auch TRPV1. Juckreiz wird empfunden, wenn das
Muster
beteiligter Rezeptoren und Afferenzen anders ist als z.B. bei Wärme-
oder Schmerzreizen (z.B. wird "kalt" über Aktivierung von TRPA1 und
TRPM8 signalisiert - s. oben -, während "es juckt" empfunden wird, wenn nur TRPA1 feuern, nicht aber TRPM8.
Ein deutlicher Unterschied ist die
reflektorische Antwort:
 Schmerz (oberflächlich) löst Beugereflexe aus, welche die irritierte Zone vom Schmerzauslöser wegbewegen soll (withdrawal reflex)
Schmerz (oberflächlich) löst Beugereflexe aus, welche die irritierte Zone vom Schmerzauslöser wegbewegen soll (withdrawal reflex)
 Juckreiz löst Kratzbewegungen aus, die irritierende Objekte (z.B. Insekten) von der Reizzone entfernen sollen (scratch reflex)
Juckreiz löst Kratzbewegungen aus, die irritierende Objekte (z.B. Insekten) von der Reizzone entfernen sollen (scratch reflex)
Involvierte Neuronen sind langsam leitend (C-Fasern); "Prurizeptoren"
sind histaminempfindliche Fasern mit großem rezeptiven Feld und
geringem räumlichem Auflösungsvermögen (z.B. ~15 cm am Oberarm),
sprechen auf chemische, nicht aber mechanische Reize an (CMi: C-afferents, mechano-insensitive). Polymodale Schmerzfasern (CMH: C-fiber, mechano-heat-sensitive nociceptors) sprechen auf mechanische, Hitze- oder chemische Reize an, auf Histamin hingegen kaum
oder gar nicht; sie kommen in der Haut häufiger vor (Jugendliche
4-fach, ältere Personen 2-3-fach) als CMi-Fasern und tragen zum
Juckempfinden bei ( Abbildung).
Abbildung).
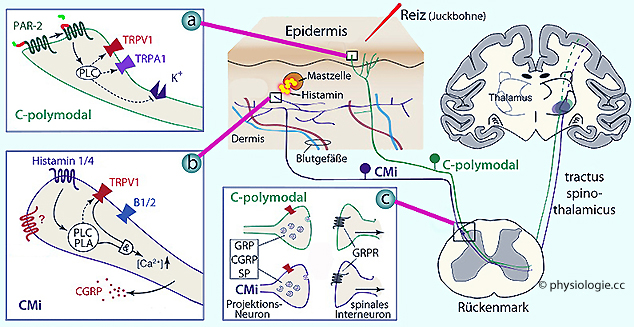
 Abbildung: Auslösung von Juckreiz
Nach Davidson S, Giesler GJ. The multiple pathways for itch and their interactions with pain. Trends Neurosci 2010; 33: 550-8
Abbildung: Auslösung von Juckreiz
Nach Davidson S, Giesler GJ. The multiple pathways for itch and their interactions with pain. Trends Neurosci 2010; 33: 550-8

Schmerzrezeptoren können proteaseaktivierte Rezeptoren, TRP-Rezeptoren (die auch nozizeptiv wirken) sowie Histaminrezeptoren sein. Diese sind auf polymodalen und CMi-Fasern unterschiedlich
verteilt. Beide Fasertypen setzen im Hinterhorn des Rückenmarks
Transmitterstoffe wie GRP, CGRP oder Substanz P frei ( Abbildung). Eine Neuronengruppe im Rückenmark exprimiert Rezeptoren für GRP (GRPR, gastrin-releasing peptide receptors), sie vermitteln selektiv reflektorisches Kratzen nach Reizung durch Pruritogene und prurizeptive Neurone.
Abbildung). Eine Neuronengruppe im Rückenmark exprimiert Rezeptoren für GRP (GRPR, gastrin-releasing peptide receptors), sie vermitteln selektiv reflektorisches Kratzen nach Reizung durch Pruritogene und prurizeptive Neurone.
Juckreiz leitende Fasern verwenden einen speziellen Neurotransmitter: Natriuretic polypeptide B (Nppb).
Dieser stimuliert Neurone im Hinterhorn. Kratzen der betreffenden
Hautstelle verringert die Aktivität dieser Neurone und führt zu
Linderung des empfundenen Juckreizes; in diesen Effekt ist NPY als Transmitter involviert.
Zentrale Projektionen des
Juckreizes aktivieren mehrere Hirnregionen: Thalamus, Kleinhirn,
motorische und prämotorische Rinde, Insel, gyrus cinguli. Das Muster
hängt u.a. davon ab, ob der Juckreiz mit Schmerz kombiniert ist oder
nicht, und ob das Jucken von Kratzbewegungen gefolgt ist - deren Effekt
seinerseits unterschiedlich eingestuft wird: Er kann unangenehm,
neutral oder "hedonisch" empfunden werden.
Außer durch Juckreiz auslösende Stoffe (z.B. Stoffe der Juckbohne,  Abbildung) und nachfolgende Ausschüttung von Transmittern (wie
Histamin) als physiologische Reaktion kann Jucken auch durch mehrere pathologische Zustände auftreten, z.B. neurogen, neuropathisch oder psychogen.
Abbildung) und nachfolgende Ausschüttung von Transmittern (wie
Histamin) als physiologische Reaktion kann Jucken auch durch mehrere pathologische Zustände auftreten, z.B. neurogen, neuropathisch oder psychogen.
Afferenzen und ihre Bedeutung
Mit
einer Hinterwurzel in das Rückenmark eintretende afferente
(sensorische) Nervenfasern treffen im Hinterhorn auf
verschiedene spezialisierte (nach Rexed benannte) Zonen (laminae I bis
VI) und bilden hier synaptische Verschaltungen ( Abbildung).
Abbildung).
 Wärme-,
Kälte-, Juck- und Schmerzsignale werden primär in die Zonen I und II
geleitet,
Wärme-,
Kälte-, Juck- und Schmerzsignale werden primär in die Zonen I und II
geleitet,
 mechanosensible in Zonen III bis V.
mechanosensible in Zonen III bis V.
Nachfolgende Projektionen erfolgen auf Hirnstamm und Thalamus
(aufsteigende Systeme).
 Abbildung: Somatosensorische Projektionen auf Hinterhornzellen und anterolaterales System
Nach einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Abbildung: Somatosensorische Projektionen auf Hinterhornzellen und anterolaterales System
Nach einer Vorlage in Augustine / Groh / Huettel / LaMantia / White (eds),
Neuroscience. Intl 7th ed. Oxford University Press 2024
Die graue Substanz der Hinter- und Seitensäule wird in Rexed-Zonen (laminae) unterteilt (vgl. dort).
Deren Neurone haben unterschiedliche Funktion: Solche in Zone I und II
(hellrot unterlegt) erhalten thermo- und nozizeptive Impulse (auch Juckreiz) über Aδ- und
C-Fasern. Neurone in lamina I korrespondieren mit kleinen rezeptiven Feldern in
jeweils einem Dermatom; solche in lamina II nehmen exzitatorische
und/oder inhibitorische Verbindung mit Nachbarzonen auf.
Mechanozeptive
Information (LTMR: low-threshold mechanoreceptors) projiziert in laminae III bis V (C-Fasern dorsal, Aδ-Fasern ventral). In lamina V finden sich multimodale Neurone (WDR-Neurone s. dort).
Die hier beispielhaft gezeigten synaptischen Verschaltungen werden
durch eine Vielzahl weiterer ergänzt, z.B. im Rahmen von Reflexmustern,
Koordination mehrerer Muskelgruppen und Extremitäten, oder absteigenden
(modifizierenden, schmerzhemmenden etc.) Bahnen.
Der tractus posterolateralis (Lissauer-Trakt  )
an der Spitze des Hinterhorns zieht durch das gesamte Rückenmark. Er
leitet über Aδ- (myelinisiert) und C-Fasern (unmyelinisiert)
Temperatur- und Schmerzimpulse jeweils über 1-2 auf- und absteigende
Segmente und endet dann in der substantia gelatinosa (Rexed Zone 2)
oder dem benachbarten nucleus proprius, von dem aus Projektionen in
tiefere Schichten des Rückenmarks erfolgen. Afferenzen ziehen über den
tractus anterolateralis zu Hirnstamm und Zwischenhirn (Hypothalamus und
VPLN, ventraler posterolateraler Thalamuskern)
)
an der Spitze des Hinterhorns zieht durch das gesamte Rückenmark. Er
leitet über Aδ- (myelinisiert) und C-Fasern (unmyelinisiert)
Temperatur- und Schmerzimpulse jeweils über 1-2 auf- und absteigende
Segmente und endet dann in der substantia gelatinosa (Rexed Zone 2)
oder dem benachbarten nucleus proprius, von dem aus Projektionen in
tiefere Schichten des Rückenmarks erfolgen. Afferenzen ziehen über den
tractus anterolateralis zu Hirnstamm und Zwischenhirn (Hypothalamus und
VPLN, ventraler posterolateraler Thalamuskern)

 Aktivierende Wirkung von Fußsohlenreizung auf das Gehirn:
Afferenzen von der Fußsohle haben aktivierende Effekte im ZNS
(auch z.B. bei Intensiv- oder neurologischen Patienten); längerer
Verlust mechanischer Stimulation der plantaren Haut trägt zu negativen
Folgen längerer Bettlägrigkeit bei ("Astronautensyndrom").
Aktivierende Wirkung von Fußsohlenreizung auf das Gehirn:
Afferenzen von der Fußsohle haben aktivierende Effekte im ZNS
(auch z.B. bei Intensiv- oder neurologischen Patienten); längerer
Verlust mechanischer Stimulation der plantaren Haut trägt zu negativen
Folgen längerer Bettlägrigkeit bei ("Astronautensyndrom").
Neben den intensiven
Kreislaufeffekten haben das Aufrichten zum Stehen und frühzeitige Mobilisierung auch diesbezüglich bedeutende stimulierende Wirkung.
Die Afferenz erfolgt über verschiedene Fasertypen (A-beta, A-delta, C). Werden Nervenfasern (insbesondere Typ C) in der Haut wiederholt schwach gereizt, entsteht Juckreiz; bei stärkerer Reizung und bewegtem Reiz Kitzeln.
Berührungsinformation von behaarter Haut
wird im Rückenmark nicht nur über die Hintersäulen vermittelt, sondern
auch über den tractus spinocervicalis, der im lateralen nucleus
cervicalis (C1-C3) endet und von dort in den kontralateralen Thalamus
projiziert. Ein Ziel einiger Vorderstrangaxone sind weiters die nuclei parabrachiales in der pons, welche via Projektionen auf Mandelkerne und Hypothalamus Reaktionen auf Schmerzreize steuern.
Finale "Abnehmer" der diversen Afferenzen aus dem Körper (Mechano-,
Thermo-, Schmerzempfinden) sind die entsprechenden Rindengebiete des
Großhirns (somatosensorische Gebiete, Insel usw). Ein sehr kleiner Teil
dieser Information wird bewusst erlebt, der Großteil ohne bewusste
Wahrnehmung automatisiert genutzt.
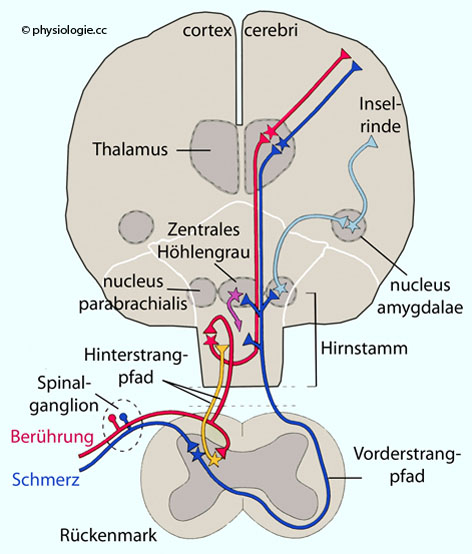
 Abbildung: Zentrale Leitungssysteme für Berührung und Schmerz
Abbildung: Zentrale Leitungssysteme für Berührung und Schmerz
Nach einer Vorlage in Liqun Luo, Principles of Neurobiology, 2nd ed. CRC Press 2021
Afferenzen
für Berührung rot, für Schmerz dunkelblau dargestellt. Das Schema gibt
eine vereinfachte Übersicht über die wichtigsten Bahnen. So melden
mehrere parallele Bahnen "Berührung" an das Gehirn. Die
Wahrnehmungsschwelle wird durch die jeweils sensitivsten sensorischen
Neurone definiert.
Sensorische Neuronen für Berührung (Aß-LTMRs - low threshold mechanoreceptors) senden Impulse zum
Hirnstamm - direkt sowie via Zwischenneurone (gelb) indirekt über den
Hinterstrang (dorsaler Pfad). Ein weiteres Neuron kreuzt im Hirnstamm
die Seite und projiziert auf den Thalamus, und dieser auf die
Großhirnrinde.
Schmerzafferenzen schalten im Hinterhorn auf ein zweites Neuron. Dieses
kreuzt die Seite und zieht (im Vorder-Seitenstrang) zu Hirnstamm und
Thalamus. Kollaterale zu den nuclei parabrachiales projizieren auf
Neurone im Mandelkern und diese auf die Insel (hellblau), was affektive
Aspekte der Schmerzwahrnehmung anregt. Im zentralen Höhlengrau werden
absteigende modulierende Neurone (lila) aktiviert
 Über das Kleinhirn s. dort
Über das Kleinhirn s. dort
 Über das Hinterhorn und dort stattfindende spinale Umschaltungen s. dort
Über das Hinterhorn und dort stattfindende spinale Umschaltungen s. dort
Die komplette Sinnesempfindung gelangt - nach Leitung über Rückenmark
und Umschaltung im Rückenmark oder Hirnstamm sowie im Thalamus - in die
hintere Zentralwindung. Hier entstehen aus Empfindungen subjektive Gesamtheiten (Wahrnehmungen).
Hautstellen mit großem Auflösungsvermögen (=Schärfe der
Unterscheidungsfähigkeit) weisen die größte Dichte an Mechanorezeptoren
auf. Die Lippen haben z.B. wesentlich kleinere und stark überlappende
rezeptive Felder als die Oberarme. Das bedeutet mehr zentrale Neurone
und große Projektionsflächen in der Großhirnrinde. So kommt dem Gesicht
in der Zentralwindung ein größeres Areal zu als dem Körperstamm (sensorischer Homunculus).
Lemniskales System
Die
neurale Leitung der Sinnesinformationen von der Körperoberfläche
erfolgt in spezialisierten Bahnen (Lemniskales System  ).
).
 Abbildung: Somatosensorische Afferenzen
Nach einer Vorlage bei R. TannerThies: Physiology - An Illustrated Review. Thieme 2011
Abbildung: Somatosensorische Afferenzen
Nach einer Vorlage bei R. TannerThies: Physiology - An Illustrated Review. Thieme 2011
Mechanosensible
Oberflächen- und Tiefensensibilität (2. Neuron in Hinterstrangkern)
projiziert über den Hinterstrang, Schmerz und Thermosensitivität (2.
Neuron im Hinterhorn) über den Vorder-Seiten-Strang. Das 3. Beuron
befindet sich im Thalamus. In der somatosensorischen Hirnrinde findet sich eine Organisation in kortikale Säulen,
ähnlich wie im visuellen Cortex: Hier reagieren die Neurone auf
bestimmte Reiztypen (wie Druck oder Temperatur). Der primäre und
sekundäre somatosensorische Cortex enthalten mehrere (vielleicht 10) Karten der Körperoberfläche.
Die Hinterstränge übertragen präzise
Berührungs- und kinästhetische Information, die Vorder-Seiten-Stränge
(tractus spinothalamici) unscharf lokalisierbare (wie Temperatur oder
Schmerz)
Afferente Impulse aus dem Gesichtsbereich gelangen über den N. trigeminus
(V) und seine Projektionen über den nucleus ventralis posterior medialis thalami ( Abbildung) in höhere Zentren.
Abbildung) in höhere Zentren.
Vom Rest der Körperoberfläche
(Hinterkopf, Hals, Rumpf, Extremitäten) wird die Information über zwei
große
Leitungsbahnen über das Rückenmark geleitet:

Für die Auflösung räumlich eng benachbarter Berührungsreize - also Präzision der taktilen Wahrnehmung (
epikritische Sensibilität: Leichte Berührung, Vibration, taktile Formerkennung, Zwei-Punkt-Diskriminierung) - und
Tiefensensibilität
- sind die
Hinterstränge verantwortlich.
Diese Bahn zieht nach Eintritt
über die Hinterwurzel auf der gleichen Seite bis zu den
Hinterstrangkernen (nucl. gracilis und cuneatus), dann wird die Seite
gekreuzt und der Thalamus erreicht.
 Für die protopathische
Sensibilität - rasche Leitung unscharfer Druckwahrnehmung, von Jucken,
Temperatur- und Schmerzwahrnehmung - kreuzen die Fasern die Seite und
ziehen im Vorderseitenstrang bis zum Thalamus; die Bearbeitung dieser Information erfolgt im lateralen nucleus ventralis posterior (
Für die protopathische
Sensibilität - rasche Leitung unscharfer Druckwahrnehmung, von Jucken,
Temperatur- und Schmerzwahrnehmung - kreuzen die Fasern die Seite und
ziehen im Vorderseitenstrang bis zum Thalamus; die Bearbeitung dieser Information erfolgt im lateralen nucleus ventralis posterior ( Abbildung).
Abbildung).
 Über Projektionen auf die Großhirnrinde und weitere Verarbeitungen der somatischen Sensibilität s. dort
Über Projektionen auf die Großhirnrinde und weitere Verarbeitungen der somatischen Sensibilität s. dort


 Abbildung: Aesthesiometer
Abbildung: Aesthesiometer  Nach einer Vorlage bei healthproductsforyou.com
Nach einer Vorlage bei healthproductsforyou.com
Geräte dieser oder ähnlicher Bauart werden zur
Bestimmung der Tastschwelle genutzt. Der Einfluss der Temperatur auf
die Auflösungsschwelle wird durch Verwendung von Kunststoff (geringe
Wärmeleitung) minimiert. Das Gerät erlaubt alternierende Bestimmungen der Ein- oder
Zwei-Punkt- Diskrimination (epikritische Sensibilität)
 Sensibilitätstestung: Die
Empfindlichkeit der Haut auf mechanische Reize wird als neurologisches
Kriterium gewertet. Eine solche Sensibilitätsprüfung erfolgt z.B. mit
einer Stimmgabel (Vibrationssinn), einem Ästhesiometer (2-Punkt-Diskrimination,
Sensibilitätstestung: Die
Empfindlichkeit der Haut auf mechanische Reize wird als neurologisches
Kriterium gewertet. Eine solche Sensibilitätsprüfung erfolgt z.B. mit
einer Stimmgabel (Vibrationssinn), einem Ästhesiometer (2-Punkt-Diskrimination,  Abbildung) oder einem Wattebausch (Berührungssinn).
Abbildung) oder einem Wattebausch (Berührungssinn).
Ein wichtiges Kriterium ist die Distanz, ab der zwei getrennte
Druckpunkte als solche erkannt werden können
(Zweipunkt-Diskrimination). Je besser das Auflösungsvermögen, desto
geringer ist diese Distanz. Diese ist auch altersabhängig - z.B. an der
Fingerspitze ~1 mm bei jungen, ~2 mm bei älteren Personen.
Die Prüfung des taktilen Auflösungsvermögens (Berührungstest, Ästhesiometer, haptische Technologie) gehört
zur diagnostischen Routine. Die Berührungssensibilität kann mit
normierten mechanischen Reizsystemen (Klassiker: Frey'sches Reizhaar  ) getestet werden.
) getestet werden.
Mangelnde Empfindlichkeit und
Auflösung kann bei Störungen auf allen Ebenen der Afferenz auftreten,
z.B. in den Hintersträngen des Rückenmarks. Störungen der Oberflächensensibilität können als Steigerung (Hyperästhesie), Abschwächung (Hypästhesie), völliges Fehlen (Anästhesie) oder Störung der Wahrnehmung (Parästhesie) imponieren. Letzteres kann u.a. auf Durchblutungs- (Ischämie) oder Stoffwechselstörungen (Diabetes) hinweisen.


 Somatische Sensibilität umfasst Oberflächensensibilität (Haut) und
Tiefensensibilität (Muskeln, Sehnen, Gelenke, Bänder).
Dehnungsempfindliche Ionenkanäle sensibler Fasern reagieren auf
mechanische Reizung mit Na+- und/oder Ca++-Einstrom, bei ausreichender Reduktion des Generatorpotentials treten Aktionspotentiale auf
Somatische Sensibilität umfasst Oberflächensensibilität (Haut) und
Tiefensensibilität (Muskeln, Sehnen, Gelenke, Bänder).
Dehnungsempfindliche Ionenkanäle sensibler Fasern reagieren auf
mechanische Reizung mit Na+- und/oder Ca++-Einstrom, bei ausreichender Reduktion des Generatorpotentials treten Aktionspotentiale auf
 Haarfollikelrezeptoren, Merkelzellen, Ruffini-Körperchen,
Meissner-Körperchen, Vater-Pacini-Vibrationsfühler sind mechanosensible
Organe und ermöglichen Druck-, Berührungs- und Vibrationswahrnehmung.
Mehrere hundert Millionen tastsensible Rezeptoren sind unterschiedlich
in der Haut verteilt. Haptik ist die Wahrnehmung berührter Gegenstände
nach Form,
Gewicht, Größe, Oberflächenbeschaffenheit
Haarfollikelrezeptoren, Merkelzellen, Ruffini-Körperchen,
Meissner-Körperchen, Vater-Pacini-Vibrationsfühler sind mechanosensible
Organe und ermöglichen Druck-, Berührungs- und Vibrationswahrnehmung.
Mehrere hundert Millionen tastsensible Rezeptoren sind unterschiedlich
in der Haut verteilt. Haptik ist die Wahrnehmung berührter Gegenstände
nach Form,
Gewicht, Größe, Oberflächenbeschaffenheit
 Muskeln, Sehnen, Gelenke und Bänder verfügen über Mechanorezeptoren für
die Tiefensensibilität (Kinästhesie: Kraft-, Lage- Stellungs-,
Bewegungssinn). Sie adaptieren kaum, melden Muskellänge
(Muskelspindeln) und Krafteinwirkung (Sehnenspindeln); in
Gelenkskapseln, Bändern, Menisci und Periost finden sich Ruffini-,
Vater-Pacini- und Golgi-Körperchen. Winkeländerungen werden in
proximalen Gelenken präziser wahrgenommen als in distalen Muskeln, Sehnen, Gelenke und Bänder verfügen über Mechanorezeptoren für
die Tiefensensibilität (Kinästhesie: Kraft-, Lage- Stellungs-,
Bewegungssinn). Sie adaptieren kaum, melden Muskellänge
(Muskelspindeln) und Krafteinwirkung (Sehnenspindeln); in
Gelenkskapseln, Bändern, Menisci und Periost finden sich Ruffini-,
Vater-Pacini- und Golgi-Körperchen. Winkeländerungen werden in
proximalen Gelenken präziser wahrgenommen als in distalen
 RA- sind rasch (z.B. Meissner'sche Tastkörperchen), SA- langsam (slowly)
adaptierende Rezeptoren (z.B. Ruffini-Körperchen). Die
Wahrnehmungsschwelle solcher Rezeptoren ist bei einer bestimmten
Reizfrequenz am niedrigsten (die Empfindlichkeit am höchsten). Beim
Ertasten von Oberflächendetails werden SA- und RA-Rezeptoren kombiniert erregt RA- sind rasch (z.B. Meissner'sche Tastkörperchen), SA- langsam (slowly)
adaptierende Rezeptoren (z.B. Ruffini-Körperchen). Die
Wahrnehmungsschwelle solcher Rezeptoren ist bei einer bestimmten
Reizfrequenz am niedrigsten (die Empfindlichkeit am höchsten). Beim
Ertasten von Oberflächendetails werden SA- und RA-Rezeptoren kombiniert erregt
 Das Auflösungsvermögen ist der geringste Abstand, in dem zwei getrennte
Reizpunkte noch als solche identifiziert werden können. Das höchste
taktile Auflösungsvermögen haben Zungenspitze und Fingerbeeren.
Mechanosensibilität der Fußsohlen ist notwendig für Gleichgewicht,
Gangstabilisierung, automatische Korrekturen der Körperhaltung und
Modulation der Extremitätenmotorik
Das Auflösungsvermögen ist der geringste Abstand, in dem zwei getrennte
Reizpunkte noch als solche identifiziert werden können. Das höchste
taktile Auflösungsvermögen haben Zungenspitze und Fingerbeeren.
Mechanosensibilität der Fußsohlen ist notwendig für Gleichgewicht,
Gangstabilisierung, automatische Korrekturen der Körperhaltung und
Modulation der Extremitätenmotorik
 Afferenzen aus dem Gesichtsbereich laufen über den N. trigeminus, vom
Rest der Körperoberfläche über Hinterstrang (epikritische und
Tiefensensibilität) und Vorderseitenstrang (protopathische Sensibilität)
Afferenzen aus dem Gesichtsbereich laufen über den N. trigeminus, vom
Rest der Körperoberfläche über Hinterstrang (epikritische und
Tiefensensibilität) und Vorderseitenstrang (protopathische Sensibilität)
 Thermosensitivität wird (ähnlich wie Schmerz) über Aδ-Fasern (Kälte)
und C-Fasern (Wärme und Kälte) geleitet. TRPV1- bis TRPV4-Kanäle
reagieren auf Wärme, TRPM8 auf Kälte. Thermosensoren haben
PD-Charakteristik; sie adaptieren innerhalb von Sekunden.
Thermosensibilität schaltet in Hinterhorn um und gelangt über die
Vorderseitenstrangbahn zum Thalamus
Thermosensitivität wird (ähnlich wie Schmerz) über Aδ-Fasern (Kälte)
und C-Fasern (Wärme und Kälte) geleitet. TRPV1- bis TRPV4-Kanäle
reagieren auf Wärme, TRPM8 auf Kälte. Thermosensoren haben
PD-Charakteristik; sie adaptieren innerhalb von Sekunden.
Thermosensibilität schaltet in Hinterhorn um und gelangt über die
Vorderseitenstrangbahn zum Thalamus
 Juckreiz wird durch mechanische, Hitze- oder chemische Reize angeregt
und über spezielle C-Fasern (Neurotransmitter: Natriuretic polypeptide B) geleitet. Zentrale Projektionen erfolgen auf Thalamus, Kleinhirn, motorische und prämotorische Rinde, Insel, gyrus cinguli
Juckreiz wird durch mechanische, Hitze- oder chemische Reize angeregt
und über spezielle C-Fasern (Neurotransmitter: Natriuretic polypeptide B) geleitet. Zentrale Projektionen erfolgen auf Thalamus, Kleinhirn, motorische und prämotorische Rinde, Insel, gyrus cinguli
|

 Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.
Die Informationen in dieser Website basieren auf verschiedenen Quellen:
Lehrbüchern, Reviews, Originalarbeiten u.a. Sie
sollen zur Auseinandersetzung mit physiologischen Fragen, Problemen und
Erkenntnissen anregen. Soferne Referenzbereiche angegeben sind, dienen diese zur Orientierung; die Grenzen sind aus biologischen, messmethodischen und statistischen Gründen nicht absolut. Wissenschaft fragt, vermutet und interpretiert; sie ist offen, dynamisch und evolutiv. Sie strebt nach Erkenntnis, erhebt aber nicht den Anspruch, im Besitz der "Wahrheit" zu sein.





 Oberflächensensibilität
Oberflächensensibilität  Thermosensibilität
Thermosensibilität  Juckreiz
Juckreiz  Afferenzen im Rückenmark
Afferenzen im Rückenmark  Lemniskales System, "epikritisch" vs. "protopathisch"
Lemniskales System, "epikritisch" vs. "protopathisch" Somatosensorik, Oberflächen- / Tiefensensibilität
Somatosensorik, Oberflächen- / Tiefensensibilität
 Core messages
Core messages
 Abbildung: Somatosensorische Achse des Nervernsystems
Abbildung: Somatosensorische Achse des Nervernsystems
 Sinnesmeldungen von der Körperoberfläche werden unter dem Begriff Oberflächensensibilität (kutane Sensibilität
- die Haut wird auch als das größte Sinnesorgan bezeichnet)
zusammengefasst, solche aus der Tiefe des Bewegungsapparates (Muskeln,
Sehnen, Gelenke etc) als Tiefensensibilität, beide zusammen als somatische Sensibilität oder Somatosensorik
Sinnesmeldungen von der Körperoberfläche werden unter dem Begriff Oberflächensensibilität (kutane Sensibilität
- die Haut wird auch als das größte Sinnesorgan bezeichnet)
zusammengefasst, solche aus der Tiefe des Bewegungsapparates (Muskeln,
Sehnen, Gelenke etc) als Tiefensensibilität, beide zusammen als somatische Sensibilität oder Somatosensorik .
.  Über Tiefensensibilität (Propriozeption, Muskel- und Sehnenspindeln, Lagesinn, Kraftsinnn, Bewegungssinn) s. dort
Über Tiefensensibilität (Propriozeption, Muskel- und Sehnenspindeln, Lagesinn, Kraftsinnn, Bewegungssinn) s. dort Über viszerale Sensibilität / Interozeption s. dort und dort
Über viszerale Sensibilität / Interozeption s. dort und dort
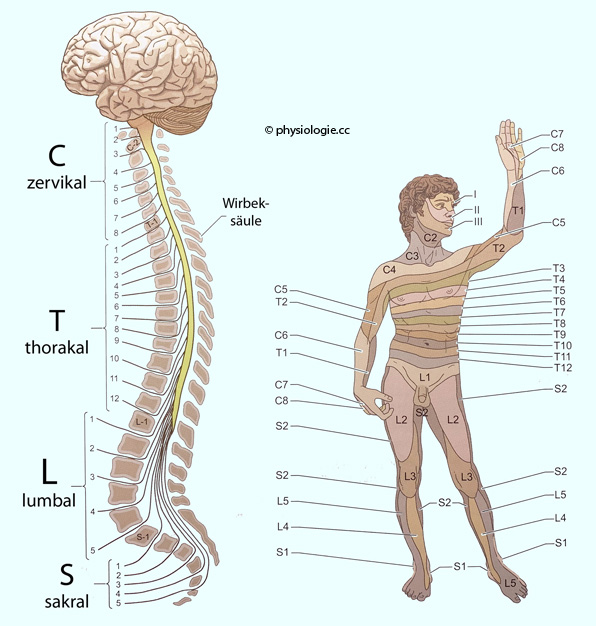
 Abbildung: Anatomie des Rückenmarks und Dermatome
Abbildung: Anatomie des Rückenmarks und Dermatome sind von jeweils einem Hirn- oder Spinalnerven sensibel innervierte
Hautareale. I = N. ophthalmicus, II = N. maxillaris, III = N.
mandibularis des N. trigeminus. Das Zervikalsegment C1 hat nur eine ventrale (motorische) Wurzel (kein Hinterhorn).
sind von jeweils einem Hirn- oder Spinalnerven sensibel innervierte
Hautareale. I = N. ophthalmicus, II = N. maxillaris, III = N.
mandibularis des N. trigeminus. Das Zervikalsegment C1 hat nur eine ventrale (motorische) Wurzel (kein Hinterhorn). Abbildung).
Abbildung). 
 Abbildung: Peripherie des somatosensorischen Systems
Abbildung: Peripherie des somatosensorischen Systems
 Abbildung oben),
Muskeln, Gelenkskapseln oder Eingeweide innervieren und über spezielle
Rezeptoren verfügen (Detektion mechanischer, thermischer, chemischer
Reize). Die zentralen Axonsegmente endigen im Rückenmark (Spinalnerven)
oder Hirnstamm (Hirnnerven). Der Körper des Neurons liegt jeweils in
einem Ganglion in der Nähe des ZNS.
Abbildung oben),
Muskeln, Gelenkskapseln oder Eingeweide innervieren und über spezielle
Rezeptoren verfügen (Detektion mechanischer, thermischer, chemischer
Reize). Die zentralen Axonsegmente endigen im Rückenmark (Spinalnerven)
oder Hirnstamm (Hirnnerven). Der Körper des Neurons liegt jeweils in
einem Ganglion in der Nähe des ZNS.  Rezeptive
Zone (verfügt über spezifische Rezeptoren und produziert
reizproportionale Rezeptorpotentiale, hat keine spannungsgesteuerten Na+- oder K+-Kanäle),
Rezeptive
Zone (verfügt über spezifische Rezeptoren und produziert
reizproportionale Rezeptorpotentiale, hat keine spannungsgesteuerten Na+- oder K+-Kanäle),
 Entstehungsort von Aktionspotentialen (spike generation site - mit spannungsgesteuerten Na+-Kanälen, üblicherweise unmittelbar vor der ersten Schwann-Zelle),
Entstehungsort von Aktionspotentialen (spike generation site - mit spannungsgesteuerten Na+-Kanälen, üblicherweise unmittelbar vor der ersten Schwann-Zelle),
 periphere Faser (leitet Aktionspotentiale zum ZNS),
periphere Faser (leitet Aktionspotentiale zum ZNS),  Zellkörper (exprimiert u.a. Rezeptorproteine),
Zellkörper (exprimiert u.a. Rezeptorproteine),  zentrale Faser in einem Spinal / Hirnnerv (mit
synaptischen Verschaltungen).
zentrale Faser in einem Spinal / Hirnnerv (mit
synaptischen Verschaltungen). 
 Abbildung: Piezo-Protein
Abbildung: Piezo-Protein
 Abbildung); TRP-Kanäle für Mechano-, Thermo- und Nozizeption. Im N. medianus finden sich z.B. 22 afferente und 8 efferente Fasertypen (zu Muskeln, Schweißdrüsen, Blutgefäßen).
Abbildung); TRP-Kanäle für Mechano-, Thermo- und Nozizeption. Im N. medianus finden sich z.B. 22 afferente und 8 efferente Fasertypen (zu Muskeln, Schweißdrüsen, Blutgefäßen).
 Abbildung: Ionenkanäle in mechanorezeptiver Nervenzellmembran (schematisch)
Abbildung: Ionenkanäle in mechanorezeptiver Nervenzellmembran (schematisch)
 Abbildung) - wie bei einigen Berührungsrezeptoren in der Haut oder Haarzellen im Innenohr.
Abbildung) - wie bei einigen Berührungsrezeptoren in der Haut oder Haarzellen im Innenohr. Haarfollikelrezeptoren (hair follicle nerve receptors; RA- sowie SA-Rezeptoren) ermöglichen die Wahrnehmung von Bewegung und Abwinkelung von Haaren
Haarfollikelrezeptoren (hair follicle nerve receptors; RA- sowie SA-Rezeptoren) ermöglichen die Wahrnehmung von Bewegung und Abwinkelung von Haaren Merkelzellen
Merkelzellen  sind spezialisierte Epithelzellen, die sich zu Merkel-Scheiben (Merkel's disks) zusammentun
und noradrenerg (ß-Rezeptoren) auf die angeschlossenen sensorischen
Nervenfaserm wirken. Es handelt sich um SA1-Rezeptoren;
in der gesamten Haut insgesamt ~60 Millionen (in der Hand des Menschen machen sie ~25% der mechanosensorischen Innervation aus). SA bedeutet langsame
Adaptation, d.h. die Sensoren generieren bei konstantem Druck beständig
Aktionspotentiale ("Proportional"-Ansprechverhalten). Die betreffenden
rezeptiven Felder sind relativ
klein, die Auflösung ist hoch, es können feine Merkmale ertastet
werden. Merkel-Scheiben bezeichnet man auch als SAI-LTMR (slow-adapting type I low-threshold mechanoreceptors)
sind spezialisierte Epithelzellen, die sich zu Merkel-Scheiben (Merkel's disks) zusammentun
und noradrenerg (ß-Rezeptoren) auf die angeschlossenen sensorischen
Nervenfaserm wirken. Es handelt sich um SA1-Rezeptoren;
in der gesamten Haut insgesamt ~60 Millionen (in der Hand des Menschen machen sie ~25% der mechanosensorischen Innervation aus). SA bedeutet langsame
Adaptation, d.h. die Sensoren generieren bei konstantem Druck beständig
Aktionspotentiale ("Proportional"-Ansprechverhalten). Die betreffenden
rezeptiven Felder sind relativ
klein, die Auflösung ist hoch, es können feine Merkmale ertastet
werden. Merkel-Scheiben bezeichnet man auch als SAI-LTMR (slow-adapting type I low-threshold mechanoreceptors) Ruffini-Körperchen
Ruffini-Körperchen  (bulbous corpuscles, Ruffini endings; SA2-Rezeptoren) - auch SAII-LTMR (slow-adapting type II low-threshold mechanoreceptors)
- tragen zur kinästhetischen Kontrolle bei (Fingerposition und
-bewegung; in der Hand des Menschen machen sie ~20% der mechanosensorischen Innervation aus). Sie liegen tiefer als Merkelzellen und registrieren hier
Änderungen der mechnischen Spannung, unter der Gewebestrukturen stehen
- ähnlich den Golgi-Sehnenrezeptoren.
(bulbous corpuscles, Ruffini endings; SA2-Rezeptoren) - auch SAII-LTMR (slow-adapting type II low-threshold mechanoreceptors)
- tragen zur kinästhetischen Kontrolle bei (Fingerposition und
-bewegung; in der Hand des Menschen machen sie ~20% der mechanosensorischen Innervation aus). Sie liegen tiefer als Merkelzellen und registrieren hier
Änderungen der mechnischen Spannung, unter der Gewebestrukturen stehen
- ähnlich den Golgi-Sehnenrezeptoren.  Meissner-Körperchen
Meissner-Körperchen  (Meissner's corpuscles; RA1-Rezeptoren, insgesamt etwa eine halbe Million) - auch RAI-LTMR (rapidly adapting type I low-threshold mechanoreceptors). In der Hand des Menschen machen sie ~40% der mechanosensorischen Innervation aus. Sie detektieren Bewegung der Haut, u.a. niedrigfrequente Vibration. RA bedeutet rasche Adaptation, d.h. die Sensoren feuern nur zu Beginn und nach Beendigung eines mechanischen Reizes ("Differenzial"-Ansprechverhalten)
(Meissner's corpuscles; RA1-Rezeptoren, insgesamt etwa eine halbe Million) - auch RAI-LTMR (rapidly adapting type I low-threshold mechanoreceptors). In der Hand des Menschen machen sie ~40% der mechanosensorischen Innervation aus. Sie detektieren Bewegung der Haut, u.a. niedrigfrequente Vibration. RA bedeutet rasche Adaptation, d.h. die Sensoren feuern nur zu Beginn und nach Beendigung eines mechanischen Reizes ("Differenzial"-Ansprechverhalten) Krause'sche-Endkolben
Krause'sche-Endkolben  (bulboid corpuscles, end-bulbs of Krause) innervieren Randzonen von Haut und Schleimhäuten, wie um die Lippen und äußeren Genitalien; vermutlich sind es RA-Rezeptoren.
(bulboid corpuscles, end-bulbs of Krause) innervieren Randzonen von Haut und Schleimhäuten, wie um die Lippen und äußeren Genitalien; vermutlich sind es RA-Rezeptoren. (Vater-) Pacini-Körperchen
(Vater-) Pacini-Körperchen  (Pacinian Corpuscle) - auch RAII-LTMR (rapidly adapting type II low-threshold mechanoreceptors)
- detektieren tiefen Druck. In der Hand des Menschen machen sie 10-15% der mechanosensorischen Innervation aus. Im Experiment reagieren sie empfindlich auf
Vibration - ein Reiztyp, der in der Natur so gut wie nicht vorkommt,
daher ist die Bezeichnung "Vibrationsrezeptor"
eigentlich irreführend. Plätzliche Lageveränderung eines Gegenstandes
wird von Pacini-Körperchen bereits detektiert, wenn sich die Position
um ca. 10 µm ändert. Das kann schon ausreichen, um beginnendes
"Rutschen" eines von Fingern gehaltenen Gegenstandes durch Erhöhung des
Griffdrucks rechtzeitig zu stoppen.
(Pacinian Corpuscle) - auch RAII-LTMR (rapidly adapting type II low-threshold mechanoreceptors)
- detektieren tiefen Druck. In der Hand des Menschen machen sie 10-15% der mechanosensorischen Innervation aus. Im Experiment reagieren sie empfindlich auf
Vibration - ein Reiztyp, der in der Natur so gut wie nicht vorkommt,
daher ist die Bezeichnung "Vibrationsrezeptor"
eigentlich irreführend. Plätzliche Lageveränderung eines Gegenstandes
wird von Pacini-Körperchen bereits detektiert, wenn sich die Position
um ca. 10 µm ändert. Das kann schon ausreichen, um beginnendes
"Rutschen" eines von Fingern gehaltenen Gegenstandes durch Erhöhung des
Griffdrucks rechtzeitig zu stoppen. 
 Abbildung: Rezeptoren in der Haut
Abbildung: Rezeptoren in der Haut
 Oberflächensensibilität
aus der Haut (
Oberflächensensibilität
aus der Haut ( Abbildung - Druck, Berührung, Vibration) - sie ermöglicht z.B. die
Ertastung auch kleinster Erhebungen an einer Oberfläche (wenige µm,
d.h. zwei Zehnerpotenzen weniger als gerade noch optisch wahrnehmbare
Strukturen) - und kann Schmerz vermitteln; und
Abbildung - Druck, Berührung, Vibration) - sie ermöglicht z.B. die
Ertastung auch kleinster Erhebungen an einer Oberfläche (wenige µm,
d.h. zwei Zehnerpotenzen weniger als gerade noch optisch wahrnehmbare
Strukturen) - und kann Schmerz vermitteln; und Tiefensensibilität in Muskeln, Sehnen, Gelenken und Bändern. Hier unterscheidet man Kraft-, Lage- (Stellungs-) und Bewegungssinn (Kinästhesie
Tiefensensibilität in Muskeln, Sehnen, Gelenken und Bändern. Hier unterscheidet man Kraft-, Lage- (Stellungs-) und Bewegungssinn (Kinästhesie  ).
).  Kräfte werden vor allem über Sehnenspindeln detektiert, die auf Dehnung ansprechen und langsam adaptierten (SA-Rezeptoren: slowly adapting, Proportionaldetektion).
Kräfte werden vor allem über Sehnenspindeln detektiert, die auf Dehnung ansprechen und langsam adaptierten (SA-Rezeptoren: slowly adapting, Proportionaldetektion).  Der Lage- bzw. Stellungssinn
informiert über die Winkelstellung der Gelenke und damit die Stellung
des Körpers in seiner Umgebung; er adaptiert kaum
(Proportionaldetektion). Gelenke
verfügen (wie die Haut) über mechanosensible Rezeptoren vom Typ
Ruffini, Vater-Pacini und Golgi; diese finden sich in Kapselgewebe,
Ligamenten, Menisci, Synovia, Fettgewebe und Periost. Knorpelgewebe ist
nicht innerviert, Hautrezeptoren spielen für den Stellungssinn so gut wie keine Rolle. Sollten in Gelenken Schmerzen auftreten, so entstehen diese durch Defekte (z.B. Einrisse) oder
Entzündungen (z.B. Osteoarthritis).
Der Lage- bzw. Stellungssinn
informiert über die Winkelstellung der Gelenke und damit die Stellung
des Körpers in seiner Umgebung; er adaptiert kaum
(Proportionaldetektion). Gelenke
verfügen (wie die Haut) über mechanosensible Rezeptoren vom Typ
Ruffini, Vater-Pacini und Golgi; diese finden sich in Kapselgewebe,
Ligamenten, Menisci, Synovia, Fettgewebe und Periost. Knorpelgewebe ist
nicht innerviert, Hautrezeptoren spielen für den Stellungssinn so gut wie keine Rolle. Sollten in Gelenken Schmerzen auftreten, so entstehen diese durch Defekte (z.B. Einrisse) oder
Entzündungen (z.B. Osteoarthritis). Die Bewegungswahrnehmung erfolgt im Wesentlichen über Muskelspindel- und Sehnenspindelrezeptoren.
Die Bewegungswahrnehmung erfolgt im Wesentlichen über Muskelspindel- und Sehnenspindelrezeptoren.  Abbildung unten: Rückenmarksquerschnitt).
Abbildung unten: Rückenmarksquerschnitt). (haptische Wahrnehmung) bezeichnet.
(haptische Wahrnehmung) bezeichnet.  Berührung ist nicht nur für Mechanorezeption, sondern auch für
die normale körperliche und seelische Entwicklung entscheidend (angenehme Berührungsreize führen zur Ausschüttung von Oxytocin).
Berührung ist nicht nur für Mechanorezeption, sondern auch für
die normale körperliche und seelische Entwicklung entscheidend (angenehme Berührungsreize führen zur Ausschüttung von Oxytocin). 
 Abbildung). Aktivitätsmuster der verschiedenen Afferenzen
von der Haut zum ZNS (Typ 1 von oberflächlich, Typ 2 von tiefer
gelegenen Mechanosensoren) lasssen sich mittels Mikroneurographie
separiert darstellen.
Abbildung). Aktivitätsmuster der verschiedenen Afferenzen
von der Haut zum ZNS (Typ 1 von oberflächlich, Typ 2 von tiefer
gelegenen Mechanosensoren) lasssen sich mittels Mikroneurographie
separiert darstellen.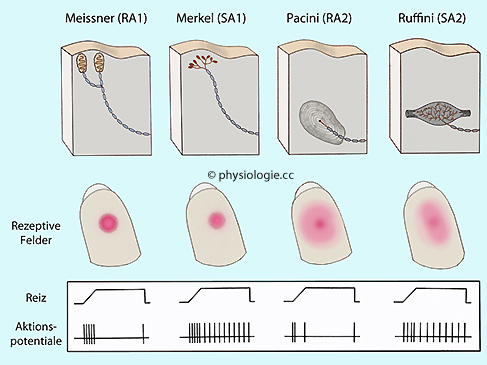
 Abbildung: Antwortverhalten von Mechanosensoren der Oberflächensensibilität
Abbildung: Antwortverhalten von Mechanosensoren der Oberflächensensibilität
 Die epithelähnlichen Merkel-Tastzellen
bilden mit den Endigungen sensibler Neuriten (Aß,
also relativ rasch leitend) synaptische Komplexe, die man in behaarter
Haut an der Grenze zwischen Epidermis und Dermis rund um Haarwurzeln
(als "Haarscheiben" bzw. "Berührungskuppeln" ausgeformt), in
unbehaarter Haut in der Mitte von Papillenkämmen findet (
Die epithelähnlichen Merkel-Tastzellen
bilden mit den Endigungen sensibler Neuriten (Aß,
also relativ rasch leitend) synaptische Komplexe, die man in behaarter
Haut an der Grenze zwischen Epidermis und Dermis rund um Haarwurzeln
(als "Haarscheiben" bzw. "Berührungskuppeln" ausgeformt), in
unbehaarter Haut in der Mitte von Papillenkämmen findet ( Abbildung
oben).
Abbildung
oben).  Auch Ruffini-Körperchen - in der inneren Handfläche ~20 / cm2 - adaptieren nur langsam und detektieren Dehnung der Haut (insbesondere
über Gelenken - damit tragen sie auch zur Tiefensensibilität bei),
wie sie z.B. bei Bewegung der Extremitäten auftritt. Man findet sie vor
allem über Finger- und Handwurzelgelenken, in der Nachbarschaft von
Fingernägeln, und entlang Hautfalten der Handflächen. Sie sind mit
bindegewebigen Fasern in ihrer Umgebung verankert. Sie werden vor allem
durch Dehnung der Haut in der Längsrichtung angeregt (
Auch Ruffini-Körperchen - in der inneren Handfläche ~20 / cm2 - adaptieren nur langsam und detektieren Dehnung der Haut (insbesondere
über Gelenken - damit tragen sie auch zur Tiefensensibilität bei),
wie sie z.B. bei Bewegung der Extremitäten auftritt. Man findet sie vor
allem über Finger- und Handwurzelgelenken, in der Nachbarschaft von
Fingernägeln, und entlang Hautfalten der Handflächen. Sie sind mit
bindegewebigen Fasern in ihrer Umgebung verankert. Sie werden vor allem
durch Dehnung der Haut in der Längsrichtung angeregt ( Abbildung
unten).
Abbildung
unten). Abbildung).
Ruffini-Körperchen adaptieren ebenfalls nur langsam und geben bei
beständiger Reizung für längere Perioden Aktionspotentialsalven ab
(SA-System).
Abbildung).
Ruffini-Körperchen adaptieren ebenfalls nur langsam und geben bei
beständiger Reizung für längere Perioden Aktionspotentialsalven ab
(SA-System). 
 Abbildung: Meissner'sches Tastkörperchen (RA1)
Abbildung: Meissner'sches Tastkörperchen (RA1)
 Meissner'sche Tastkörperchen (
Meissner'sche Tastkörperchen ( Abbildung; Durchmesser etwa 0,1 mm, Anzahl ~150 / cm2) bzw. Haarfollikelrezeptoren sind ausgeprägt differentialempfindlich: Bei konstantem Reiz nimmt ihre Entladungsfrequenz rasch ab. Haarfollikelrezeptoren
können Textur, Form und Festigkeit von Objekten signalisieren (sie
können rasch oder langsam adaptieren). Die
höchste Empfindlichkeit zeigen Meissner-Körperchen auf mechanische
Schwingungen mit einer Frequenz um ~50 Hz.
Abbildung; Durchmesser etwa 0,1 mm, Anzahl ~150 / cm2) bzw. Haarfollikelrezeptoren sind ausgeprägt differentialempfindlich: Bei konstantem Reiz nimmt ihre Entladungsfrequenz rasch ab. Haarfollikelrezeptoren
können Textur, Form und Festigkeit von Objekten signalisieren (sie
können rasch oder langsam adaptieren). Die
höchste Empfindlichkeit zeigen Meissner-Körperchen auf mechanische
Schwingungen mit einer Frequenz um ~50 Hz.  Noch rascher adaptieren die (~2 mm langen und ~1 mm dicken) (Vater-) Pacini-Körperchen (PC für Pacinian Corpuscle). Sie sind bis zu 1 mal 2
mm groß, aus bis zu 70 zwiebelschalenartig angeordneten bindegewebigen
Schichten - mit einer viskösen Flüssigkeit dazwischen - aufgebaut, die
um eine zentrale Nervenfaser angeordnet sind. Auf der Fläche einer Hand finden sich
>600, ~40.000 in der gesamten Haut - rund 20 / cm2.
Noch rascher adaptieren die (~2 mm langen und ~1 mm dicken) (Vater-) Pacini-Körperchen (PC für Pacinian Corpuscle). Sie sind bis zu 1 mal 2
mm groß, aus bis zu 70 zwiebelschalenartig angeordneten bindegewebigen
Schichten - mit einer viskösen Flüssigkeit dazwischen - aufgebaut, die
um eine zentrale Nervenfaser angeordnet sind. Auf der Fläche einer Hand finden sich
>600, ~40.000 in der gesamten Haut - rund 20 / cm2.



 Abbildung).
Abbildung). Umgekehrt reagieren Rezeptoren für Druckdetektion - Ruffini-Körperchen, Merkel-Tastscheiben
- stark proportionalempfindlich, d.h. sie adaptieren nur schwach (SA) und antworten ziemlich konstant auf die Stärke des mechanischen
Reizes.
Umgekehrt reagieren Rezeptoren für Druckdetektion - Ruffini-Körperchen, Merkel-Tastscheiben
- stark proportionalempfindlich, d.h. sie adaptieren nur schwach (SA) und antworten ziemlich konstant auf die Stärke des mechanischen
Reizes.  Über Schmerz s. dort, über Propriozeption s. dort
Über Schmerz s. dort, über Propriozeption s. dort
 Abbildung: Frequenzabhängige Empfindlichkeit stark adaptierender (RA)-Rezeptoren
Abbildung: Frequenzabhängige Empfindlichkeit stark adaptierender (RA)-Rezeptoren
 Abbildung: Pacini-Vibrationssensoren maximal bei ~250, Meissner- Körperchen bei ~50 Hz. Diese Rezeptoren bestimmen gemeinsam Wahrnehmungsschwelle und Frequenzabhängigkeit des menschlichen Vibrationssinns.
Abbildung: Pacini-Vibrationssensoren maximal bei ~250, Meissner- Körperchen bei ~50 Hz. Diese Rezeptoren bestimmen gemeinsam Wahrnehmungsschwelle und Frequenzabhängigkeit des menschlichen Vibrationssinns. gesetzten Buchstaben auftreten
(
gesetzten Buchstaben auftreten
( Abbildung):
Abbildung):
 Abbildung: Wie Tastrezeptoren auf Braille-Schrift reagieren
Abbildung: Wie Tastrezeptoren auf Braille-Schrift reagieren
 Merkel-Scheiben
(SA1) haben relativ kleine rezeptive Felder und feuern, solange die Haut
durch den jeweiligen Reizpunkt verformt ist, das Erregungsmuster
spiegelt die Schrift präzise wider.
Merkel-Scheiben
(SA1) haben relativ kleine rezeptive Felder und feuern, solange die Haut
durch den jeweiligen Reizpunkt verformt ist, das Erregungsmuster
spiegelt die Schrift präzise wider. Meissner-Körperchen (RA1) adaptieren ähnlich langsam, haben aber größere rezeptive Felder, und die Abbildung der Noppen ist weniger genau.
Meissner-Körperchen (RA1) adaptieren ähnlich langsam, haben aber größere rezeptive Felder, und die Abbildung der Noppen ist weniger genau. Ruffini-Endigungen (SA2) reagieren auf Dehnung der Haut, adaptieren ebenfalls langsam, geben aber ein ziemlich verwaschenes Bild der Reizmuster.
Ruffini-Endigungen (SA2) reagieren auf Dehnung der Haut, adaptieren ebenfalls langsam, geben aber ein ziemlich verwaschenes Bild der Reizmuster. Pacini-Körperchen
(RA2) adaptieren sehr rasch und haben große rezeptive Felder, sie ermitteln
vor allem die Textur des Papiers, nicht so sehr die Position der Braille-Punkte.
Pacini-Körperchen
(RA2) adaptieren sehr rasch und haben große rezeptive Felder, sie ermitteln
vor allem die Textur des Papiers, nicht so sehr die Position der Braille-Punkte. Abbildung):
Abbildung):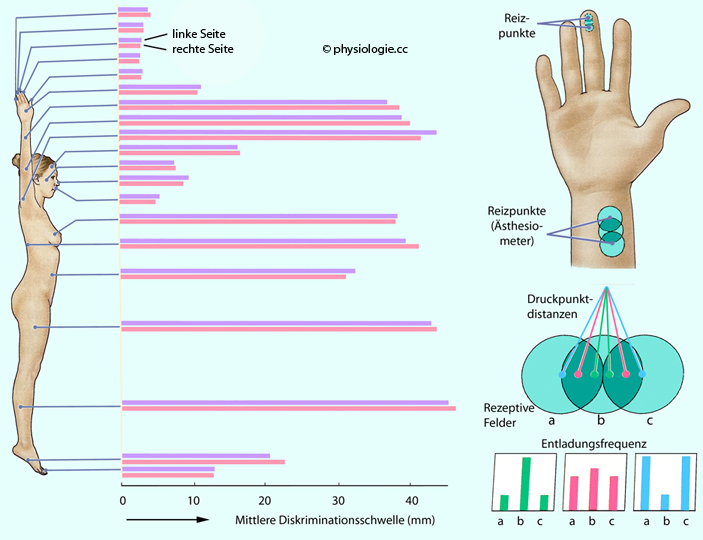
 Abbildung: Rezeptive Felder und Zwei-Punkt-Diskriminationsvermögen der Haut
Abbildung: Rezeptive Felder und Zwei-Punkt-Diskriminationsvermögen der Haut Ist der Reizabstand gering (grün), kommt aus Feld b (das beide Reize
empfängt) ein stärkeres Signal als aus den Feldern a und c. Dieses
Muster interpretiert das Gehirn als Reizung des rezeptiven Feldes b, es
wird nur ein Reizpunkt wahrgenommen.
Ist der Reizabstand gering (grün), kommt aus Feld b (das beide Reize
empfängt) ein stärkeres Signal als aus den Feldern a und c. Dieses
Muster interpretiert das Gehirn als Reizung des rezeptiven Feldes b, es
wird nur ein Reizpunkt wahrgenommen. Ist
der Reizabstand etwas größer (rot), kommt aus allen drei Feldern eine
etwa gleich starke Entladungsfrequenz des afferenten Neurons. Dieses
Muster interpretiert das Gehirn als gleich starke Reizung aller drei
rezeptiven Felder, es
wird ebenfalls nur ein (breiterer) Reizpunkt wahrgenommen.
Ist
der Reizabstand etwas größer (rot), kommt aus allen drei Feldern eine
etwa gleich starke Entladungsfrequenz des afferenten Neurons. Dieses
Muster interpretiert das Gehirn als gleich starke Reizung aller drei
rezeptiven Felder, es
wird ebenfalls nur ein (breiterer) Reizpunkt wahrgenommen. Ist
der Reizabstand so groß wie (oder größer als) der Durchmesser der
rezeptiven Felder (blau), kommt aus Feldern a und c (in deren Zentrum
die Reizpunkte liegen) ein stärkeres neuronales Signal als aus dem
mittigen Feld b. Diesen Kontrast interpretiert das Gehirn als Reizung
der rezeptiven Felder a und c, es werden (korrekterweise) zwei
Reizpunkte wahrgenommen.
Ist
der Reizabstand so groß wie (oder größer als) der Durchmesser der
rezeptiven Felder (blau), kommt aus Feldern a und c (in deren Zentrum
die Reizpunkte liegen) ein stärkeres neuronales Signal als aus dem
mittigen Feld b. Diesen Kontrast interpretiert das Gehirn als Reizung
der rezeptiven Felder a und c, es werden (korrekterweise) zwei
Reizpunkte wahrgenommen.
 Abbildung und Tabelle unten): Es ist dies der
geringste Abstand, in dem zwei getrennte Reizpunkte noch als solche
identifiziert werden können. Diese Schwelle ist auf der Zungenspitze
und an Fingerbeeren besonders gering (ungefähr 1-2 mm, hohes
Auflösungsvermögen) und im Bereich des Thorax besonders hoch ungefähr
45-70 mm, geringes Auflösungsvermögen). Mit zunehmendem Alter
nimmt die Fähigkeit der Zwei-Punkt-Diskrimination ab.
Abbildung und Tabelle unten): Es ist dies der
geringste Abstand, in dem zwei getrennte Reizpunkte noch als solche
identifiziert werden können. Diese Schwelle ist auf der Zungenspitze
und an Fingerbeeren besonders gering (ungefähr 1-2 mm, hohes
Auflösungsvermögen) und im Bereich des Thorax besonders hoch ungefähr
45-70 mm, geringes Auflösungsvermögen). Mit zunehmendem Alter
nimmt die Fähigkeit der Zwei-Punkt-Diskrimination ab.


 Abbildung: Rezeptive Felder in der Fußsohle
Abbildung: Rezeptive Felder in der Fußsohle SA, langsam adaptierend
SA, langsam adaptierend  Typ I, klein und scharf begrenzt
Typ I, klein und scharf begrenzt  Typ II, groß und unscharf begrenzt. Rechts: Summe aller Felder
Typ II, groß und unscharf begrenzt. Rechts: Summe aller Felder
 Abbildung): Sie beteiligen sich an
Abbildung): Sie beteiligen sich an Balance im Stehen
Balance im Stehen
 Gangstabilisierung
Gangstabilisierung
 automatischen Korrekturen der Körperhaltung
automatischen Korrekturen der Körperhaltung
 Modulation der Motorik der oberen und unteren Extremitäten
Modulation der Motorik der oberen und unteren Extremitäten
 vestibulären Reflexen (Gleichgewicht)
vestibulären Reflexen (Gleichgewicht)
 Abbildung: Temperaturabhängiges Ansprechverhalten von Kälte- und Wärmerezeptoren
Abbildung: Temperaturabhängiges Ansprechverhalten von Kälte- und Wärmerezeptoren
 Abbildung).
Abbildung).  kälteempfindliche Aδ-Nervenfasern (Leitungsgeschwindigkeit 5-30 m/s). Diese sprechen auf Hauttemperaturen zwischen ~10°C und 40°C an und haben maximale Entladungsfrequenz bei ~25°C - und
kälteempfindliche Aδ-Nervenfasern (Leitungsgeschwindigkeit 5-30 m/s). Diese sprechen auf Hauttemperaturen zwischen ~10°C und 40°C an und haben maximale Entladungsfrequenz bei ~25°C - und wärme- und kälteempfindliche C-Fasern (Leitungsgeschwindigkeit 0,2-2 m/s). Wärmesensible Fasern sprechen auf Temperaturen über ~30°C an, maximal auf 40-45°.
wärme- und kälteempfindliche C-Fasern (Leitungsgeschwindigkeit 0,2-2 m/s). Wärmesensible Fasern sprechen auf Temperaturen über ~30°C an, maximal auf 40-45°.  Abbildung): TRPA1 sprechen auf Temperaturen unter 16°C an, TRPM8 unter 28°C (und Menthol), TRPV4 über 26°C, TRPV3 über 31°C, TRPV1 über 43°C (und Capsaicin), TRPV2 über 52°C.
Abbildung): TRPA1 sprechen auf Temperaturen unter 16°C an, TRPM8 unter 28°C (und Menthol), TRPV4 über 26°C, TRPV3 über 31°C, TRPV1 über 43°C (und Capsaicin), TRPV2 über 52°C.
 Abbildung: TRP-Ionenkanäle
Abbildung: TRP-Ionenkanäle

 Abbildung: Dreischalenversuch nach Eduard Weber
Abbildung: Dreischalenversuch nach Eduard Weber
 (
( Abbildung): Taucht man z.B. die linke Hand in kaltes, die rechte in warmes
Wasser, und gibt beide Hände nach etwa einer Minute in lauwarmes Wasser,
so empfindet man dieses links als warm, rechts gleichzeitig als kühl.
Abbildung): Taucht man z.B. die linke Hand in kaltes, die rechte in warmes
Wasser, und gibt beide Hände nach etwa einer Minute in lauwarmes Wasser,
so empfindet man dieses links als warm, rechts gleichzeitig als kühl. Über die Klassifizierung von Nervenfasern s. dort
Über die Klassifizierung von Nervenfasern s. dort Autonom-nervöse Reaktionen (wie Vasodilatation / Vasokonstriktion, Schwitzen, Kältezittern)
Autonom-nervöse Reaktionen (wie Vasodilatation / Vasokonstriktion, Schwitzen, Kältezittern) Verhaltensänderungen (wie Aufsuchen kühler / warmer Orte, Wechsel der Kleidung).
Verhaltensänderungen (wie Aufsuchen kühler / warmer Orte, Wechsel der Kleidung). Schmerz (oberflächlich) löst Beugereflexe aus, welche die irritierte Zone vom Schmerzauslöser wegbewegen soll (withdrawal reflex)
Schmerz (oberflächlich) löst Beugereflexe aus, welche die irritierte Zone vom Schmerzauslöser wegbewegen soll (withdrawal reflex) Juckreiz löst Kratzbewegungen aus, die irritierende Objekte (z.B. Insekten) von der Reizzone entfernen sollen (scratch reflex)
Juckreiz löst Kratzbewegungen aus, die irritierende Objekte (z.B. Insekten) von der Reizzone entfernen sollen (scratch reflex) Abbildung).
Abbildung).
 Abbildung: Auslösung von Juckreiz
Abbildung: Auslösung von Juckreiz CMi = mechano-insensitiver Nozizeptor
CMi = mechano-insensitiver Nozizeptor  GRP(R) = Gastrin-releasing peptide (Rezeptor)
GRP(R) = Gastrin-releasing peptide (Rezeptor)  PAR = Protease-aktivierter Rezeptor
PAR = Protease-aktivierter Rezeptor  PLC = Phospholipase C
PLC = Phospholipase C  SP = Substanz P
SP = Substanz P  TRPA = transient receptor potential ankyrin
TRPA = transient receptor potential ankyrin  TRPV = transient receptor potential vanilloid
TRPV = transient receptor potential vanilloid

 Abbildung). Eine Neuronengruppe im Rückenmark exprimiert Rezeptoren für GRP (GRPR, gastrin-releasing peptide receptors), sie vermitteln selektiv reflektorisches Kratzen nach Reizung durch Pruritogene und prurizeptive Neurone.
Abbildung). Eine Neuronengruppe im Rückenmark exprimiert Rezeptoren für GRP (GRPR, gastrin-releasing peptide receptors), sie vermitteln selektiv reflektorisches Kratzen nach Reizung durch Pruritogene und prurizeptive Neurone.  Abbildung) und nachfolgende Ausschüttung von Transmittern (wie
Histamin) als physiologische Reaktion kann Jucken auch durch mehrere pathologische Zustände auftreten, z.B. neurogen, neuropathisch oder psychogen.
Abbildung) und nachfolgende Ausschüttung von Transmittern (wie
Histamin) als physiologische Reaktion kann Jucken auch durch mehrere pathologische Zustände auftreten, z.B. neurogen, neuropathisch oder psychogen. Abbildung).
Abbildung). Wärme-,
Kälte-, Juck- und Schmerzsignale werden primär in die Zonen I und II
geleitet,
Wärme-,
Kälte-, Juck- und Schmerzsignale werden primär in die Zonen I und II
geleitet,  mechanosensible in Zonen III bis V.
mechanosensible in Zonen III bis V. 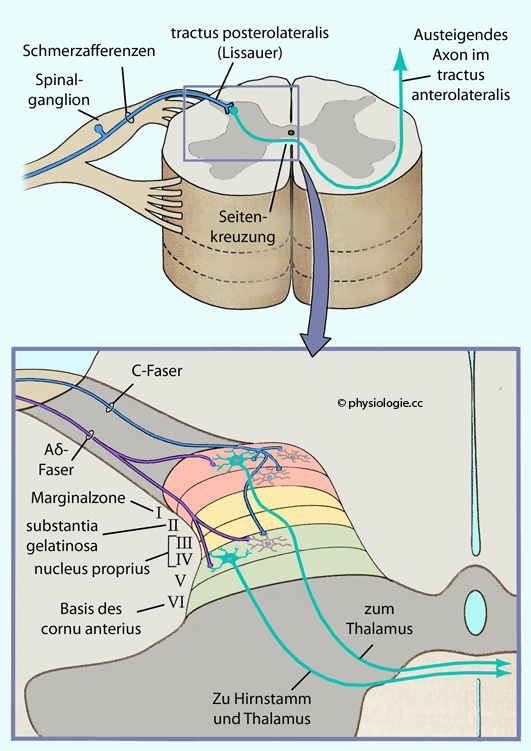
 Abbildung: Somatosensorische Projektionen auf Hinterhornzellen und anterolaterales System
Abbildung: Somatosensorische Projektionen auf Hinterhornzellen und anterolaterales System )
an der Spitze des Hinterhorns zieht durch das gesamte Rückenmark. Er
leitet über Aδ- (myelinisiert) und C-Fasern (unmyelinisiert)
Temperatur- und Schmerzimpulse jeweils über 1-2 auf- und absteigende
Segmente und endet dann in der substantia gelatinosa (Rexed Zone 2)
oder dem benachbarten nucleus proprius, von dem aus Projektionen in
tiefere Schichten des Rückenmarks erfolgen. Afferenzen ziehen über den
tractus anterolateralis zu Hirnstamm und Zwischenhirn (Hypothalamus und
VPLN, ventraler posterolateraler Thalamuskern)
)
an der Spitze des Hinterhorns zieht durch das gesamte Rückenmark. Er
leitet über Aδ- (myelinisiert) und C-Fasern (unmyelinisiert)
Temperatur- und Schmerzimpulse jeweils über 1-2 auf- und absteigende
Segmente und endet dann in der substantia gelatinosa (Rexed Zone 2)
oder dem benachbarten nucleus proprius, von dem aus Projektionen in
tiefere Schichten des Rückenmarks erfolgen. Afferenzen ziehen über den
tractus anterolateralis zu Hirnstamm und Zwischenhirn (Hypothalamus und
VPLN, ventraler posterolateraler Thalamuskern)
 Aktivierende Wirkung von Fußsohlenreizung auf das Gehirn:
Afferenzen von der Fußsohle haben aktivierende Effekte im ZNS
(auch z.B. bei Intensiv- oder neurologischen Patienten); längerer
Verlust mechanischer Stimulation der plantaren Haut trägt zu negativen
Folgen längerer Bettlägrigkeit bei ("Astronautensyndrom").
Aktivierende Wirkung von Fußsohlenreizung auf das Gehirn:
Afferenzen von der Fußsohle haben aktivierende Effekte im ZNS
(auch z.B. bei Intensiv- oder neurologischen Patienten); längerer
Verlust mechanischer Stimulation der plantaren Haut trägt zu negativen
Folgen längerer Bettlägrigkeit bei ("Astronautensyndrom"). 
 Abbildung: Zentrale Leitungssysteme für Berührung und Schmerz
Abbildung: Zentrale Leitungssysteme für Berührung und Schmerz ).
). 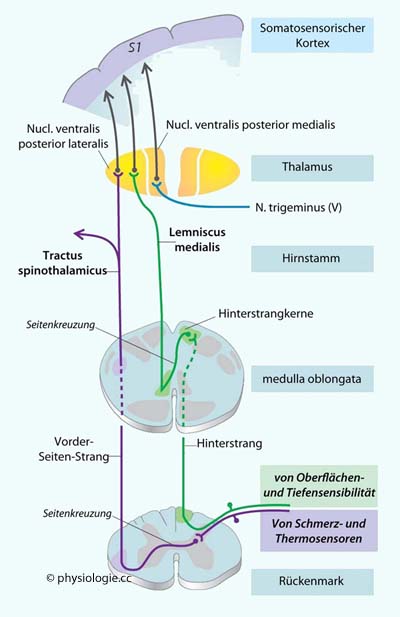
 Abbildung: Somatosensorische Afferenzen
Abbildung: Somatosensorische Afferenzen
 Abbildung) in höhere Zentren.
Abbildung) in höhere Zentren.  Für die Auflösung räumlich eng benachbarter Berührungsreize - also Präzision der taktilen Wahrnehmung (epikritische Sensibilität: Leichte Berührung, Vibration, taktile Formerkennung, Zwei-Punkt-Diskriminierung) - und Tiefensensibilität
- sind die Hinterstränge verantwortlich.
Für die Auflösung räumlich eng benachbarter Berührungsreize - also Präzision der taktilen Wahrnehmung (epikritische Sensibilität: Leichte Berührung, Vibration, taktile Formerkennung, Zwei-Punkt-Diskriminierung) - und Tiefensensibilität
- sind die Hinterstränge verantwortlich.  Für die protopathische
Sensibilität - rasche Leitung unscharfer Druckwahrnehmung, von Jucken,
Temperatur- und Schmerzwahrnehmung - kreuzen die Fasern die Seite und
ziehen im Vorderseitenstrang bis zum Thalamus; die Bearbeitung dieser Information erfolgt im lateralen nucleus ventralis posterior (
Für die protopathische
Sensibilität - rasche Leitung unscharfer Druckwahrnehmung, von Jucken,
Temperatur- und Schmerzwahrnehmung - kreuzen die Fasern die Seite und
ziehen im Vorderseitenstrang bis zum Thalamus; die Bearbeitung dieser Information erfolgt im lateralen nucleus ventralis posterior ( Abbildung).
Abbildung). Über Projektionen auf die Großhirnrinde und weitere Verarbeitungen der somatischen Sensibilität s. dort
Über Projektionen auf die Großhirnrinde und weitere Verarbeitungen der somatischen Sensibilität s. dort

 Abbildung: Aesthesiometer
Abbildung: Aesthesiometer 

 Sensibilitätstestung: Die
Empfindlichkeit der Haut auf mechanische Reize wird als neurologisches
Kriterium gewertet. Eine solche Sensibilitätsprüfung erfolgt z.B. mit
einer Stimmgabel (Vibrationssinn), einem Ästhesiometer (2-Punkt-Diskrimination,
Sensibilitätstestung: Die
Empfindlichkeit der Haut auf mechanische Reize wird als neurologisches
Kriterium gewertet. Eine solche Sensibilitätsprüfung erfolgt z.B. mit
einer Stimmgabel (Vibrationssinn), einem Ästhesiometer (2-Punkt-Diskrimination,  Abbildung) oder einem Wattebausch (Berührungssinn).
Abbildung) oder einem Wattebausch (Berührungssinn).  ) getestet werden.
) getestet werden.
 Somatische Sensibilität umfasst Oberflächensensibilität (Haut) und
Tiefensensibilität (Muskeln, Sehnen, Gelenke, Bänder).
Dehnungsempfindliche Ionenkanäle sensibler Fasern reagieren auf
mechanische Reizung mit Na+- und/oder Ca++-Einstrom, bei ausreichender Reduktion des Generatorpotentials treten Aktionspotentiale auf
Somatische Sensibilität umfasst Oberflächensensibilität (Haut) und
Tiefensensibilität (Muskeln, Sehnen, Gelenke, Bänder).
Dehnungsempfindliche Ionenkanäle sensibler Fasern reagieren auf
mechanische Reizung mit Na+- und/oder Ca++-Einstrom, bei ausreichender Reduktion des Generatorpotentials treten Aktionspotentiale auf Haarfollikelrezeptoren, Merkelzellen, Ruffini-Körperchen,
Meissner-Körperchen, Vater-Pacini-Vibrationsfühler sind mechanosensible
Organe und ermöglichen Druck-, Berührungs- und Vibrationswahrnehmung.
Mehrere hundert Millionen tastsensible Rezeptoren sind unterschiedlich
in der Haut verteilt. Haptik ist die Wahrnehmung berührter Gegenstände
nach Form,
Gewicht, Größe, Oberflächenbeschaffenheit
Haarfollikelrezeptoren, Merkelzellen, Ruffini-Körperchen,
Meissner-Körperchen, Vater-Pacini-Vibrationsfühler sind mechanosensible
Organe und ermöglichen Druck-, Berührungs- und Vibrationswahrnehmung.
Mehrere hundert Millionen tastsensible Rezeptoren sind unterschiedlich
in der Haut verteilt. Haptik ist die Wahrnehmung berührter Gegenstände
nach Form,
Gewicht, Größe, Oberflächenbeschaffenheit Muskeln, Sehnen, Gelenke und Bänder verfügen über Mechanorezeptoren für
die Tiefensensibilität (Kinästhesie: Kraft-, Lage- Stellungs-,
Bewegungssinn). Sie adaptieren kaum, melden Muskellänge
(Muskelspindeln) und Krafteinwirkung (Sehnenspindeln); in
Gelenkskapseln, Bändern, Menisci und Periost finden sich Ruffini-,
Vater-Pacini- und Golgi-Körperchen. Winkeländerungen werden in
proximalen Gelenken präziser wahrgenommen als in distalen
Muskeln, Sehnen, Gelenke und Bänder verfügen über Mechanorezeptoren für
die Tiefensensibilität (Kinästhesie: Kraft-, Lage- Stellungs-,
Bewegungssinn). Sie adaptieren kaum, melden Muskellänge
(Muskelspindeln) und Krafteinwirkung (Sehnenspindeln); in
Gelenkskapseln, Bändern, Menisci und Periost finden sich Ruffini-,
Vater-Pacini- und Golgi-Körperchen. Winkeländerungen werden in
proximalen Gelenken präziser wahrgenommen als in distalen  RA- sind rasch (z.B. Meissner'sche Tastkörperchen), SA- langsam (slowly)
adaptierende Rezeptoren (z.B. Ruffini-Körperchen). Die
Wahrnehmungsschwelle solcher Rezeptoren ist bei einer bestimmten
Reizfrequenz am niedrigsten (die Empfindlichkeit am höchsten). Beim
Ertasten von Oberflächendetails werden SA- und RA-Rezeptoren kombiniert erregt
RA- sind rasch (z.B. Meissner'sche Tastkörperchen), SA- langsam (slowly)
adaptierende Rezeptoren (z.B. Ruffini-Körperchen). Die
Wahrnehmungsschwelle solcher Rezeptoren ist bei einer bestimmten
Reizfrequenz am niedrigsten (die Empfindlichkeit am höchsten). Beim
Ertasten von Oberflächendetails werden SA- und RA-Rezeptoren kombiniert erregt Das Auflösungsvermögen ist der geringste Abstand, in dem zwei getrennte
Reizpunkte noch als solche identifiziert werden können. Das höchste
taktile Auflösungsvermögen haben Zungenspitze und Fingerbeeren.
Mechanosensibilität der Fußsohlen ist notwendig für Gleichgewicht,
Gangstabilisierung, automatische Korrekturen der Körperhaltung und
Modulation der Extremitätenmotorik
Das Auflösungsvermögen ist der geringste Abstand, in dem zwei getrennte
Reizpunkte noch als solche identifiziert werden können. Das höchste
taktile Auflösungsvermögen haben Zungenspitze und Fingerbeeren.
Mechanosensibilität der Fußsohlen ist notwendig für Gleichgewicht,
Gangstabilisierung, automatische Korrekturen der Körperhaltung und
Modulation der Extremitätenmotorik Afferenzen aus dem Gesichtsbereich laufen über den N. trigeminus, vom
Rest der Körperoberfläche über Hinterstrang (epikritische und
Tiefensensibilität) und Vorderseitenstrang (protopathische Sensibilität)
Afferenzen aus dem Gesichtsbereich laufen über den N. trigeminus, vom
Rest der Körperoberfläche über Hinterstrang (epikritische und
Tiefensensibilität) und Vorderseitenstrang (protopathische Sensibilität) Thermosensitivität wird (ähnlich wie Schmerz) über Aδ-Fasern (Kälte)
und C-Fasern (Wärme und Kälte) geleitet. TRPV1- bis TRPV4-Kanäle
reagieren auf Wärme, TRPM8 auf Kälte. Thermosensoren haben
PD-Charakteristik; sie adaptieren innerhalb von Sekunden.
Thermosensibilität schaltet in Hinterhorn um und gelangt über die
Vorderseitenstrangbahn zum Thalamus
Thermosensitivität wird (ähnlich wie Schmerz) über Aδ-Fasern (Kälte)
und C-Fasern (Wärme und Kälte) geleitet. TRPV1- bis TRPV4-Kanäle
reagieren auf Wärme, TRPM8 auf Kälte. Thermosensoren haben
PD-Charakteristik; sie adaptieren innerhalb von Sekunden.
Thermosensibilität schaltet in Hinterhorn um und gelangt über die
Vorderseitenstrangbahn zum Thalamus Juckreiz wird durch mechanische, Hitze- oder chemische Reize angeregt
und über spezielle C-Fasern (Neurotransmitter: Natriuretic polypeptide B) geleitet. Zentrale Projektionen erfolgen auf Thalamus, Kleinhirn, motorische und prämotorische Rinde, Insel, gyrus cinguli
Juckreiz wird durch mechanische, Hitze- oder chemische Reize angeregt
und über spezielle C-Fasern (Neurotransmitter: Natriuretic polypeptide B) geleitet. Zentrale Projektionen erfolgen auf Thalamus, Kleinhirn, motorische und prämotorische Rinde, Insel, gyrus cinguli